20.1: Hidrokaboni
- Page ID
- 175900
- Eleza umuhimu wa hidrokaboni na sababu ya utofauti wao
- Jina ulijaa na hidrokaboni isokefu, na molekuli inayotokana nao
- Eleza tabia ya athari za hidrokaboni zilizojaa na zisizohifadhiwa
- Kutambua isoma za miundo na kijiometri za hidrokaboni
Database kubwa 1 ya misombo ya kikaboni inaorodhesha kuhusu dutu milioni 10, ambazo ni pamoja na misombo inayotokana na viumbe hai na yale yaliyotengenezwa na maduka ya dawa. Idadi ya misombo ya kikaboni yenye uwezo imekadiriwa 2 kwa 10 60 —idadi kubwa ya astronomia. Kuwepo kwa molekuli nyingi za kikaboni ni matokeo ya uwezo wa atomi za kaboni kuunda hadi vifungo vinne vikali kwa atomi nyingine za kaboni, na kusababisha minyororo na pete za ukubwa tofauti, maumbo, na matatizo mbalimbali.
Misombo ya kikaboni rahisi zaidi ina vipengele tu vya kaboni na hidrojeni, na huitwa hidrokaboni. Japokuwa zinajumuisha aina mbili tu za atomi, kuna aina mbalimbali za hidrokaboni kwa sababu zinaweza kuwa na urefu tofauti wa minyororo, minyororo ya matawi, na pete za atomi za kaboni, au mchanganyiko wa miundo hii. Aidha, hidrokaboni inaweza kutofautiana katika aina za vifungo vya kaboni-kaboni zilizopo katika molekuli zao. Hidrokaboni nyingi hupatikana katika mimea, wanyama, na fossils zao; hidrokaboni nyingine zimeandaliwa katika maabara. Tunatumia hidrokaboni kila siku, hasa kama fueli, kama vile gesi asilia, asetilini, propane, butane, na sehemu kuu za petroli, mafuta ya dizeli, na mafuta ya kupokanzwa. Ya kawaida plastiki polyethilini, polypropylene, na polystyrene pia ni hidrokaboni Tunaweza kutofautisha aina kadhaa za hidrokaboni kwa tofauti katika kuunganishwa kati ya atomi za kaboni. Hii inasababisha tofauti katika jiometri na katika hybridization ya orbitals kaboni.
Alkanes
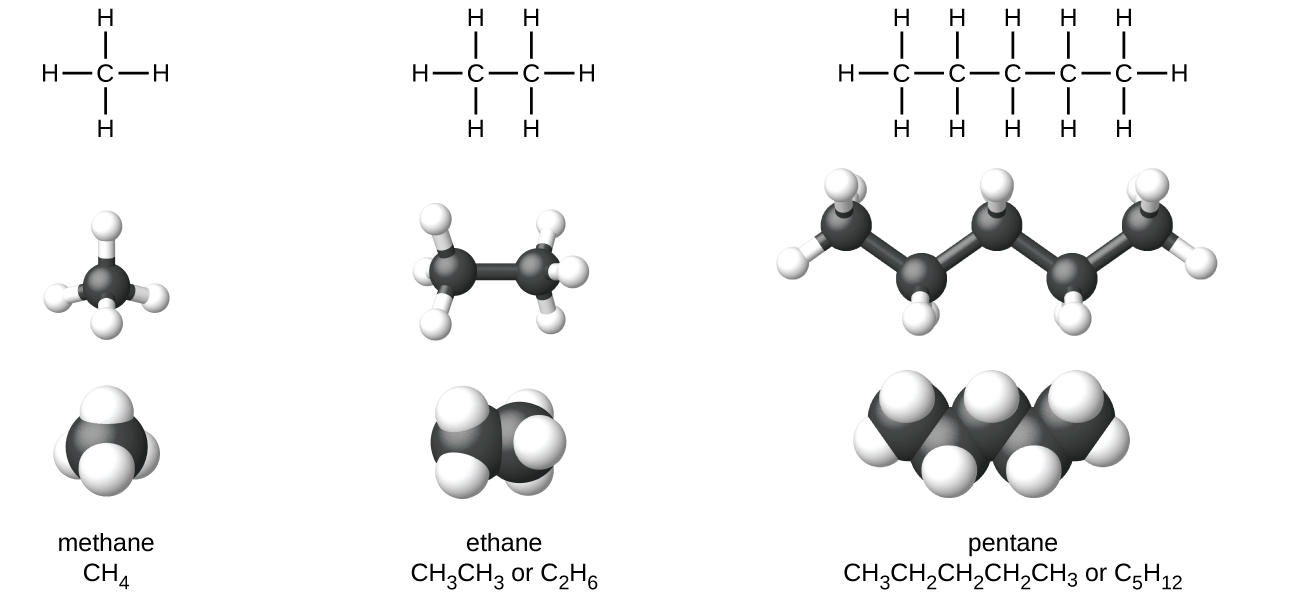
Alkanes, au hidrokaboni zilizojaa, zina vifungo moja tu vya covalent kati ya atomi za kaboni. Kila moja ya atomi za kaboni katika alkane ina orbitali za mseto wa sp 3 na huunganishwa na atomi nyingine nne, ambazo kila mmoja ni ama kaboni au hidrojeni. Miundo ya Lewis na mifano ya methane, ethane, na pentane zinaonyeshwa kwenye Kielelezo\(\PageIndex{1}\). Minyororo ya kaboni kwa kawaida hutolewa kama mistari ya moja kwa moja katika miundo ya Lewis, lakini mtu anapaswa kukumbuka kwamba miundo ya Lewis haikusudiwa kuonyesha jiometri ya molekuli. Kumbuka kwamba atomi za kaboni katika mifano ya kimuundo (mifano ya mpira-na-fimbo na nafasi ya kujaza) ya molekuli ya pentane haifai kwenye mstari wa moja kwa moja. Kwa sababu ya mahuluti ya sp 3, pembe za dhamana katika minyororo ya kaboni ni karibu na 109.5°, na kutoa minyororo hiyo katika alkane umbo la zigzag.
Miundo ya alkanes na molekuli nyingine za kikaboni zinaweza pia kuwakilishwa kwa njia isiyo ya kina na fomu za kimuundo zilizopunguzwa (au tu, fomu zilizopunguzwa). Badala ya muundo wa kawaida wa formula za kemikali ambazo kila ishara ya kipengele inaonekana mara moja tu, formula iliyosababishwa imeandikwa ili kupendekeza kuunganisha katika molekuli. Fomula hizi zina muonekano wa muundo wa Lewis ambao wengi au wote wa alama za dhamana zimeondolewa. Fomu za kimuundo za ethane na pentane zinaonyeshwa chini ya Kielelezo\(\PageIndex{1}\), na mifano kadhaa ya ziada hutolewa katika mazoezi mwishoni mwa sura hii.
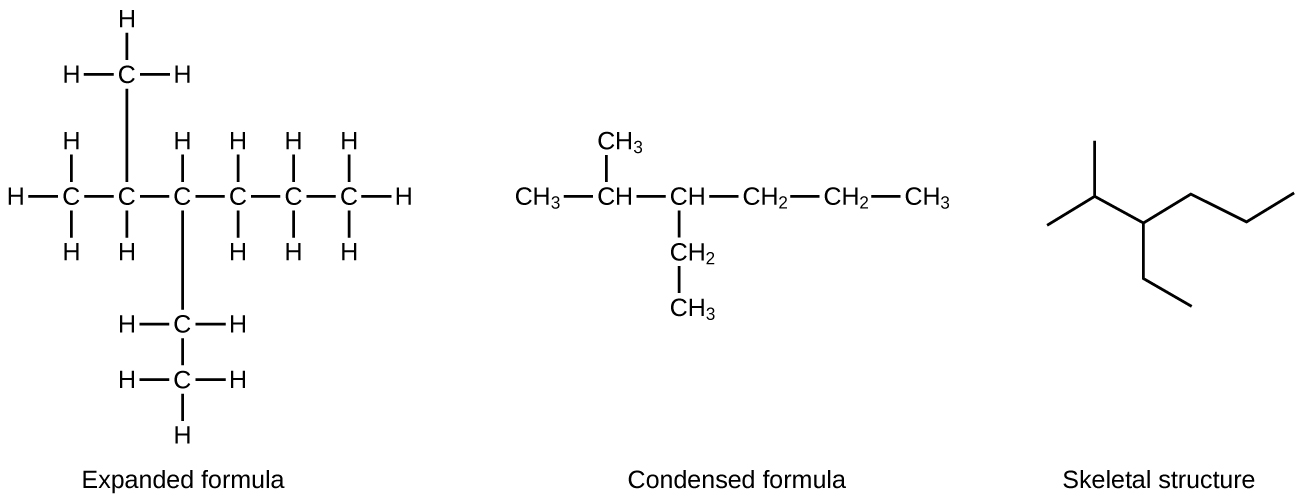
Njia ya kawaida inayotumiwa na wanakemia kikaboni ili kurahisisha michoro ya molekuli kubwa ni kutumia muundo wa mifupa (pia huitwa muundo wa mstari-angle). Katika aina hii ya muundo, atomi za kaboni hazionyeshwa na C, lakini zinawakilishwa na kila mwisho wa mstari au bend katika mstari. Atomi za hidrojeni hazipatikani kama zinaunganishwa na kaboni. Atomi nyingine badala ya kaboni na hidrojeni zinawakilishwa na alama zao za msingi. Kielelezo\(\PageIndex{2}\) kinaonyesha njia tatu tofauti za kuteka muundo huo.
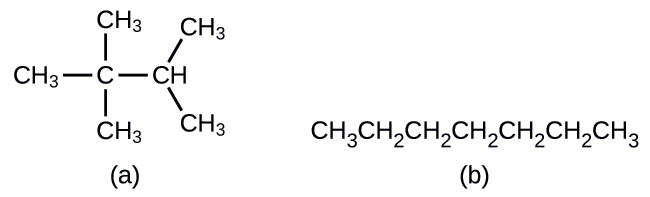
Kuchora Miundo ya Skeletal Chora miundo ya mifupa kwa molekuli hizi mbili:
Suluhisho
Kila atomu ya kaboni hubadilishwa kuwa mwisho wa mstari au mahali ambako mistari huingiliana. Atomi zote za hidrojeni zilizounganishwa na atomi za kaboni zimeachwa nje ya muundo (ingawa bado tunahitaji kutambua zipo):
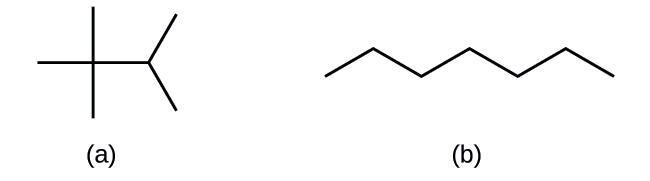
Chora miundo ya mifupa kwa molekuli hizi mbili:

- Jibu
-

Katika, hexagon yenye vertex hapo juu inavyoonyeshwa. Vertex tu kwa haki ina sehemu ya mstari masharti kwamba inaenea juu na kulia. Katika b, muundo wa zig zag unaonyeshwa ambapo makundi ya mstari yanaongezeka, kuanguka, kuongezeka, kuanguka, na kupanda kusonga kushoto kwenda kulia.
Kufafanua Miundo ya Skeletal Kutambua fomu ya kemikali ya molekuli iliyowakilishwa hapa:
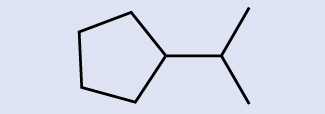
Suluhisho
Kuna sehemu nane ambako mistari huingiliana au kuishia, maana yake ni kwamba kuna atomi nane za kaboni katika molekuli. Kwa kuwa tunajua kwamba atomi za kaboni huwa na kufanya vifungo vinne, kila atomu ya kaboni itakuwa na idadi ya atomi za hidrojeni zinazohitajika kwa vifungo vinne. Kiwanja hiki kina atomi 16 za hidrojeni kwa formula ya Masi ya C 8 H 16.
Eneo la atomi za hidrojeni:
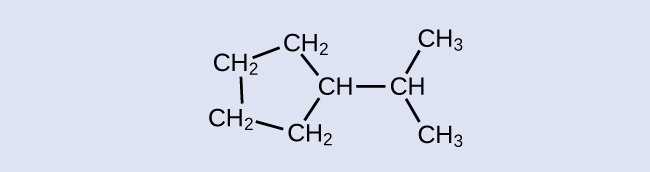
Tambua formula ya kemikali ya molekuli iliyowakilishwa hapa:
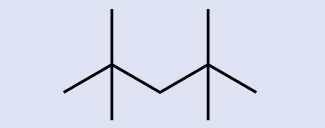
- Jibu
-
C 9 H 20
Alkanes zote zinajumuisha atomi za kaboni na hidrojeni, na zina vifungo, miundo, na formula sawa; alkanes zisizo za kawaida zote zina formula ya C n H 2n +2. Idadi ya atomi za kaboni zilizopo katika alkane haina kikomo. Idadi kubwa ya atomi katika molekuli itasababisha vivutio vya nguvu vya intermolecular (vikosi vya utawanyiko) na mali tofauti za kimwili za molekuli. Mali kama vile kiwango cha kuyeyuka na kiwango cha kuchemsha (Jedwali\(\PageIndex{1}\)) kwa kawaida hubadilika vizuri na kwa kutabiri kadiri idadi ya atomi za kaboni na hidrojeni katika molekuli inabadilika.
| Alkane | Mfumo wa Masi | Kiwango cha kuyeyuka (°C) | Kiwango cha kuchemsha (°C) | Awamu katika STP 4 | Idadi ya Isoma za Miundo |
|---|---|---|---|---|---|
| methani | CH 4 | —182.5 | —161.5 | gesi | 1 |
| ethani | C 2 H 6 | —183.3 | —88.6 | gesi | 1 |
| propane | C 3 H 8 | —187.7 | —42.1 | gesi | 1 |
| butane | C 4 H 10 | —138.3 | —0.5 | gesi | 2 |
| pentane | C 5 H 12 | —129.7 | 36.1 | kioevu | 3 |
| hexane | C 6 H 14 | —95.3 | 68.7 | kioevu | 5 |
| heptane | C 7 H 16 | —90.6 | 98.4 | kioevu | 9 |
| oktani | C 8 H 18 | —56.8 | 125.7 | kioevu | 18 |
| nonane | C 9 H 20 | —53.6 | 150.8 | kioevu | 35 |
| decane | C 10 H 22 | —29.7 | 174.0 | kioevu | 75 |
| tetradecane | C 14 H 30 | 5.9 | 253.5 | thabiti | 1858 |
| octadecane | C 18 H 38 | 28.2 | 316.1 | thabiti | 60,523 |
Hidrokaboni yenye formula sawa, ikiwa ni pamoja na alkanes, inaweza kuwa na miundo tofauti. Kwa mfano, alkanes mbili zina formula C 4 H 10: Wao huitwa n -butane na 2-methylpropane (au isobutane), na kuwa na miundo ya Lewis ifuatayo:
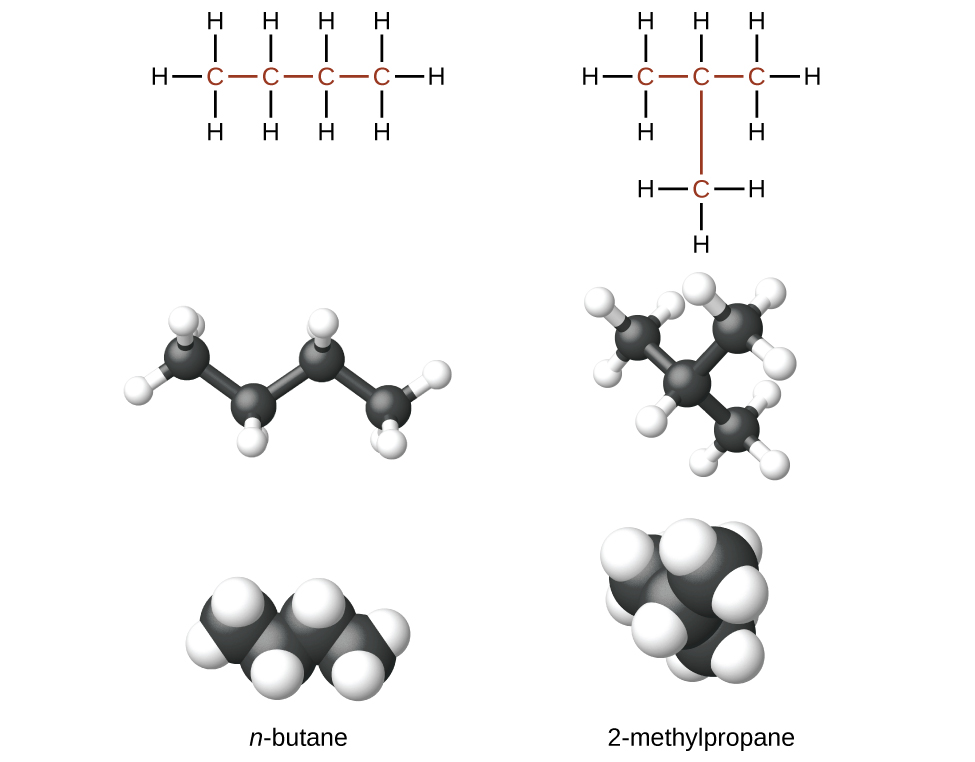
Misombo n -butane na 2-methylpropane ni isoma za kimuundo (neno isomers ya kikatiba pia hutumiwa kawaida). Isoma za kikatiba zina fomula sawa ya Masi lakini mipangilio tofauti ya anga ya atomi katika molekuli zao. Molekuli ya n -butane ina mnyororo usio na matawi, maana yake ni kwamba hakuna atomi ya kaboni inayounganishwa na zaidi ya atomi nyingine mbili za kaboni. Tunatumia neno kawaida, au kiambishi awali n, kutaja mlolongo wa atomi za kaboni bila matawi. Kiwanja 2—methylpropane kina mnyororo wa matawi (atomu ya kaboni katikati ya muundo wa Lewis imeunganishwa na atomi nyingine tatu za kaboni)
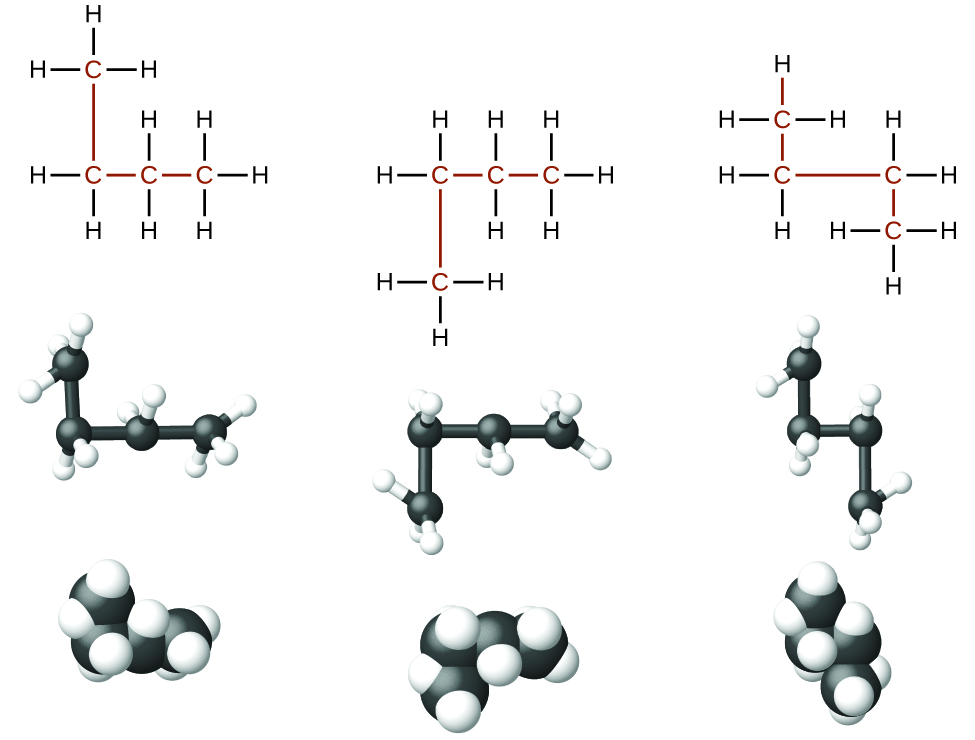
Kutambua isomers kutoka miundo Lewis si rahisi kama inaonekana. Lewis miundo kwamba kuangalia tofauti inaweza kweli kuwakilisha isoma sawa. Kwa mfano, miundo mitatu katika Kielelezo\(\PageIndex{3}\) zote zinawakilisha molekuli sawa, n -butane, na hivyo si isomers tofauti. Zinafanana kwa sababu kila mmoja ana mnyororo usio na matawi wa atomi nne za kaboni.
Misingi ya Majina ya Organic: Kutaja Alkanes
Umoja wa Kimataifa wa Kemia safi na Applied (IUPAC) umetengeneza mfumo wa nomenclature unaoanza na majina ya alkanes na inaweza kubadilishwa kutoka huko ili kuhesabu miundo ngumu zaidi. Nomenclature kwa alkanes inategemea sheria mbili:
- Ili kutaja alkane, kwanza kutambua mlolongo mrefu zaidi wa atomi za kaboni katika muundo wake. Mlolongo wa kaboni mbili huitwa ethane; mnyororo wa kaboni tatu, propane; na mnyororo wa kaboni nne, butani. Minyororo ndefu inaitwa kama ifuatavyo: pentane (mnyororo wa kaboni tano), hexane (6), heptane (7), octane (8), nonane (9), na decane (10). Viambishi hivi vinaweza kuonekana katika majina ya alkanes yaliyoelezwa katika Jedwali\(\PageIndex{1}\).
- Ongeza viambishi awali kwa jina la mlolongo mrefu zaidi ili kuonyesha nafasi na majina ya wasimamizi. Substituents ni matawi au makundi ya kazi ambayo hubadilisha atomi za hidrojeni kwenye mnyororo Msimamo wa mbadala au tawi hutambuliwa na idadi ya atomi ya kaboni inayounganishwa nayo katika mnyororo. Tunahesabu atomi za kaboni katika mlolongo kwa kuhesabu kutoka mwisho wa mnyororo karibu na mbadala. Wafanyabiashara wengi huitwa mmoja mmoja na kuwekwa kwa utaratibu wa alfabeti mbele ya jina.
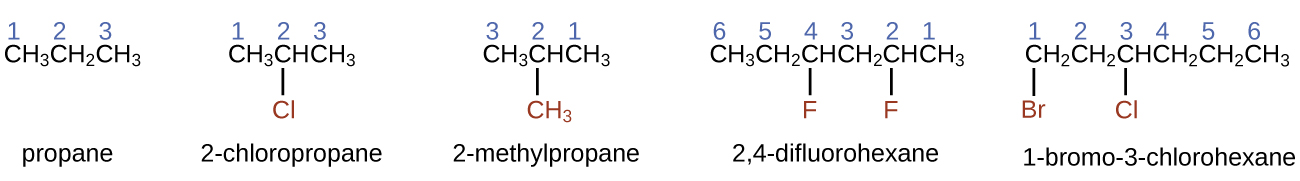
Wakati mbadala zaidi ya moja yapo, ama kwenye atomi moja ya kaboni au kwenye atomi tofauti za kaboni, wasimamizi huorodheshwa kialfabeti. Kwa sababu namba ya atomi ya kaboni inaanza mwishoni karibu zaidi na mbadala, mlolongo mrefu zaidi wa atomi za kaboni huhesabiwa kwa namna ya kuzalisha idadi ya chini kabisa kwa mbadala. Mwisho -o hubadilisha -ide mwishoni mwa jina la mbadala ya electronegative (katika misombo ya ionic, ion ya kushtakiwa vibaya inaisha na -ide kama kloridi; katika misombo ya kikaboni, atomi hizo zinatibiwa kama mbadala na mwisho -o hutumiwa). Idadi ya mbadala ya aina hiyo inaonyeshwa na viambishi awali di- (mbili), tri- (tatu), tetra- (nne), na kadhalika (kwa mfano, difluoro- inaonyesha mbadala mbili za fluoride).
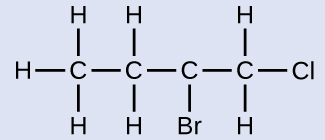
Jina la molekuli ambayo muundo wake umeonyeshwa hapa:
Suluhisho
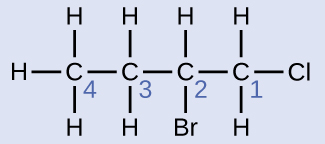
Mlolongo wa kaboni nne umehesabiwa kutoka mwisho na atomi ya klorini. Hii inaweka substituents juu ya nafasi 1 na 2 (kuhesabu kutoka upande mwingine bila kuweka substituents juu ya nafasi 3 na 4). Atomi nne za kaboni inamaanisha kuwa jina la msingi la kiwanja hiki litakuwa butane. Bromini katika nafasi ya 2 itaelezewa kwa kuongeza 2-bromo-; hii itakuja mwanzoni mwa jina, tangu bromo- inakuja kabla ya chloro- kialfabeti. Klorini katika nafasi ya 1 itaelezewa kwa kuongeza 1-chloro-, na kusababisha jina la molekuli kuwa 2-bromo-1-chlorobutane.
Jina la molekuli ifuatayo:
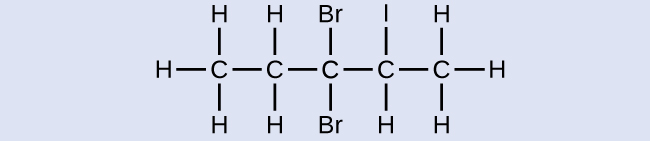
- Jibu
-
3,3-dibromo-2-iodopentane
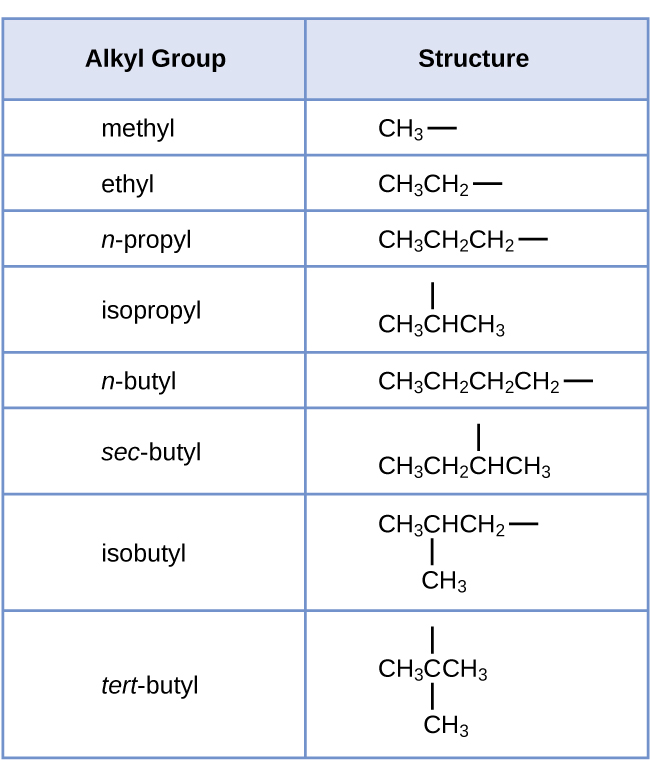
Tunaita mbadala ambayo ina hidrojeni moja chini kuliko alkane inayofanana na kundi la alkyl. Jina la kundi la alkyl linapatikana kwa kuacha suffix -ane ya jina la alkane na kuongeza -yl:
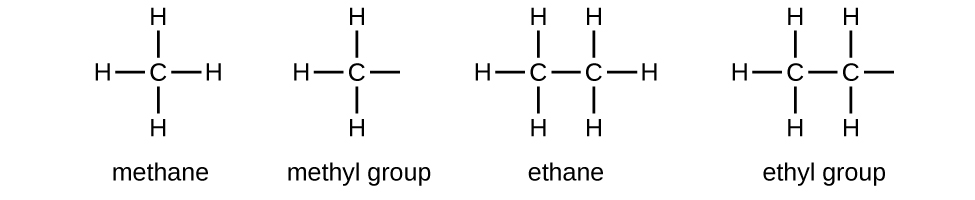
Vifungo vya wazi katika vikundi vya methyl na ethyl vinaonyesha kwamba makundi haya ya alkyl yanaunganishwa na atomi nyingine.
Jina la molekuli ambayo muundo wake umeonyeshwa hapa:
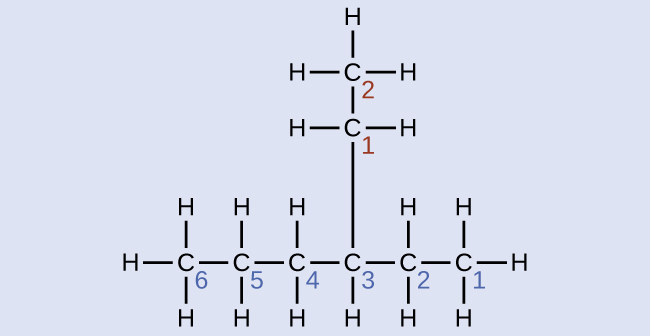
Suluhisho
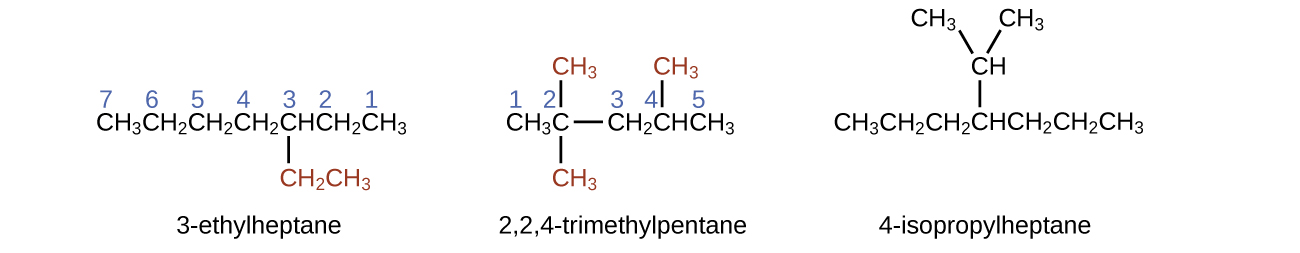
Mlolongo mrefu zaidi wa kaboni unaendesha usawa katika ukurasa na una atomi sita za kaboni (hii inafanya msingi wa jina hexane, lakini tutahitaji pia kuingiza jina la tawi). Katika kesi hiyo, tunataka idadi kutoka kulia kwenda kushoto (kama inavyoonekana kwa idadi ya bluu) hivyo tawi ni kushikamana na carbon 3 (kufikiria idadi kutoka kushoto kwenda kulia - hii ingekuwa kuweka tawi juu ya carbon 4, kukiuka sheria zetu). Tawi lililounganishwa na msimamo 3 wa mlolongo wetu lina atomi mbili za kaboni (zilizohesabiwa katika nyekundu) -hivyo tunachukua jina letu kwa kaboni mbili eth- na ambatanisha -yl mwishoni ili kuashiria tunaelezea tawi. Kuweka vipande vyote pamoja, molekuli hii ni 3-ethylhexane.
Jina la molekuli ifuatayo:

- Jibu
-
4-propyloctane
Baadhi ya hidrokaboni zinaweza kuunda zaidi ya aina moja ya kundi la alkili wakati atomi za hidrojeni ambazo zingeondolewa zina “mazingira” tofauti katika molekuli. Tofauti hii ya makundi ya alkili iwezekanavyo yanaweza kutambuliwa kwa njia ifuatayo: Atomi nne za hidrojeni katika molekuli ya methane ni sawa; zote zina mazingira sawa. Wao ni sawa kwa sababu kila mmoja huunganishwa na atomi ya kaboni (atomi moja ya kaboni) inayounganishwa na atomi tatu za hidrojeni. (Ni inaweza kuwa rahisi kuona equivalency katika mpira na fimbo mifano katika Kielelezo\(\PageIndex{3}\). Kuondolewa kwa moja yoyote ya atomi nne za hidrojeni kutoka methane huunda kundi la methyl. Vivyo hivyo, atomi sita za hidrojeni katika ethane ni sawa na kuondoa mojawapo ya atomi hizi za hidrojeni hutoa kundi la ethyl. Kila moja ya atomi sita za hidrojeni huunganishwa na atomi ya kaboni inayounganishwa na atomi nyingine mbili za hidrojeni na atomi ya kaboni. Hata hivyo, katika propane na 2—methylpropane, kuna atomi za hidrojeni katika mazingira mawili tofauti, zinajulikana kwa atomi zilizo karibu au vikundi vya atomi:
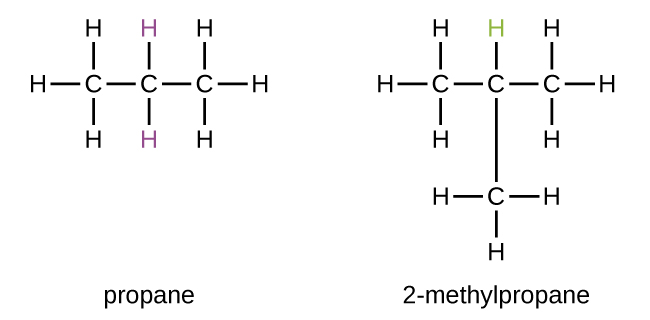
Kumbuka kwamba makundi ya alkyl haipo kama vyombo vya kujitegemea vilivyo imara. Wao daima ni sehemu ya molekuli kubwa. Eneo la kundi la alkyl kwenye mlolongo wa hydrocarbon linaonyeshwa kwa njia sawa na mbadala nyingine yoyote:
Alkanes ni molekuli thabiti kiasi, lakini joto au mwanga itaamsha athari zinazohusisha kuvunja C—H au C—C vifungo moja. Mwako ni moja ya majibu hayo:
\[\ce{CH4}(g)+\ce{2O2}(g)⟶\ce{CO2}(g)+\ce{2H2O}(g) \nonumber \]
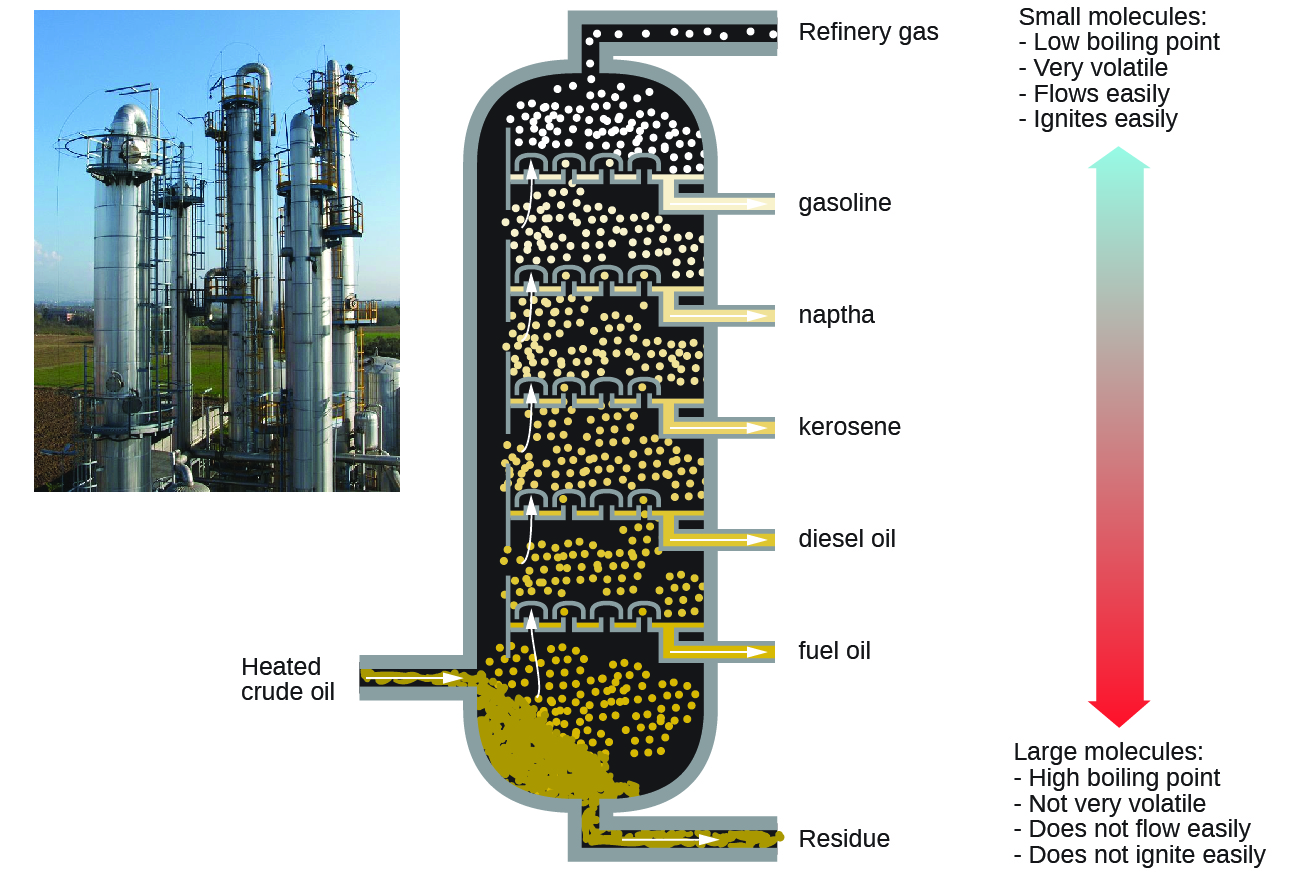
Alkanes huwaka mbele ya oksijeni, mmenyuko wa kupunguza oxidation yenye exothermic ambayo hutoa dioksidi kaboni na maji. Matokeo yake, alkanes ni mafuta bora. Kwa mfano, methane, CH 4, ni sehemu kuu ya gesi asilia. Butane, C 4 H 10, kutumika katika vituo vya kambi na nyepesi ni alkane. Petroli ni mchanganyiko wa kiowevu wa alkanes zinazoendelea- na matawi mnyororo, kila iliyo na atomi za kaboni tano hadi tisa, pamoja na viungio mbalimbali vya kuboresha utendaji wake kama mafuta. Mafuta ya mafuta, mafuta ya dizeli, na mafuta ya mafuta ni hasa mchanganyiko wa alkanes na raia wa juu wa Masi. Chanzo kikuu cha mafuta haya ya alkane ya kioevu ni mafuta yasiyosafishwa, mchanganyiko mgumu ambao hutenganishwa na kunereka kwa sehemu. Kunyoosha kwa sehemu inachukua faida ya tofauti katika pointi za kuchemsha za vipengele vya mchanganyiko (Kielelezo\(\PageIndex{5}\)). Unaweza kukumbuka kuwa kiwango cha kuchemsha ni kazi ya mwingiliano wa intermolecular, ambayo ilijadiliwa katika sura ya ufumbuzi na colloids.
Katika mmenyuko mbadala, mmenyuko mwingine wa kawaida wa alkanes, moja au zaidi ya atomi za hidrojeni za alkane hubadilishwa na atomi tofauti au kundi la atomi. Hakuna vifungo vya kaboni-kaboni vinavyovunjika katika athari hizi, na uharibifu wa atomi za kaboni haubadilika. Kwa mfano, mmenyuko kati ya ethane na klorini ya Masi iliyoonyeshwa hapa ni mmenyuko wa mbadala:
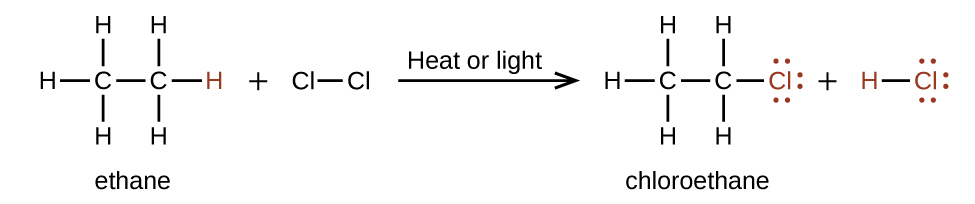
Sehemu ya C—Cl ya molekuli ya kloroethane ni mfano wa kundi la kazi, sehemu au moiety ya molekuli inayotoa reactivity maalum ya kemikali. Aina za makundi ya kazi zilizopo katika molekuli ya kikaboni ni vigezo vikubwa vya mali zake za kemikali na hutumiwa kama njia ya kuainisha misombo ya kikaboni kama kina katika sehemu zilizobaki za sura hii.
Alkenes
Misombo ya kikaboni ambayo yana vifungo moja au zaidi mara mbili au tatu kati ya atomi za kaboni huelezewa kama isokefu. Una uwezekano wa kusikia mafuta yasiyotumiwa. Hizi ni molekuli tata za kikaboni zenye minyororo mirefu ya atomi za kaboni, ambazo zina angalau dhamana moja mara mbili kati ya atomi za kaboni Molekuli zisizohifadhiwa za hidrokaboni zilizo na vifungo moja au zaidi mara mbili huitwa alkenes. Atomi za kaboni zilizounganishwa na dhamana mbili zimefungwa pamoja na vifungo viwili, dhamana moja σ na moja π dhamana. Vifungo viwili na vitatu vinatoa kupanda kwa jiometri tofauti karibu na atomu ya kaboni inayoshiriki ndani yake, na kusababisha tofauti muhimu katika umbo la Masi na mali. Jiometri tofauti huwajibika kwa mali tofauti za mafuta yasiyotokana na mafuta yaliyojaa.
Ethene, C 2 H 4, ni alkene rahisi. Kila atomu ya kaboni katika ethene, inayoitwa ethylene, ina muundo wa mpango wa trigonal. Mwanachama wa pili wa mfululizo ni propene (propylene) (Kielelezo\(\PageIndex{6}\)); isoma ya butene hufuata katika mfululizo. Atomi nne za kaboni katika mlolongo wa butene inaruhusu kuundwa kwa isomers kulingana na nafasi ya dhamana mbili, pamoja na aina mpya ya isomerism.
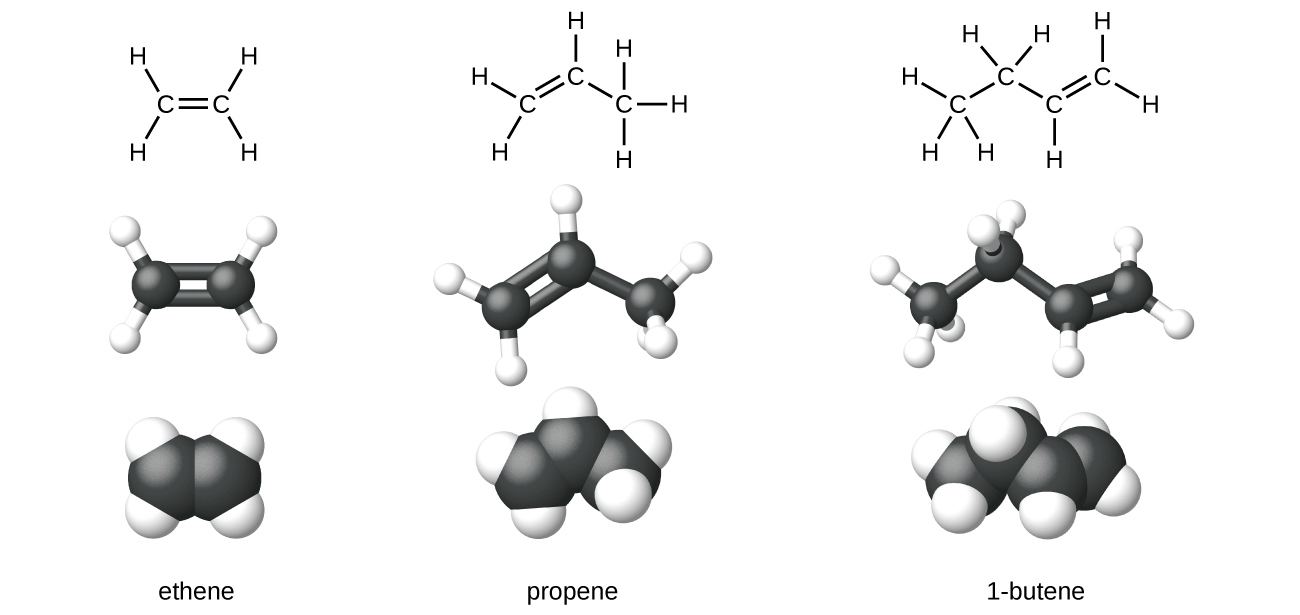
Ethylene (jina la kawaida la viwanda kwa ethene) ni malighafi ya msingi katika uzalishaji wa polyethilini na misombo mingine muhimu. Zaidi ya tani milioni 135 za ethylene zilizalishwa duniani kote mwaka 2010 kwa ajili ya matumizi katika viwanda vya polymer, petrochemical, na plastiki. Ethylene huzalishwa viwanda katika mchakato unaoitwa ngozi, ambapo minyororo ndefu ya hidrokaboni katika mchanganyiko wa mafuta ya petroli huvunjika kuwa molekuli ndogo.
Usafishaji wa plastiki
Polima (kutoka maneno ya Kigiriki aina nyingi inayomaanisha “wengi” na mer inayomaanisha “sehemu”) ni molekuli kubwa zinazoundwa na vitengo vya kurudia, zinajulikana kama monoma. Polima zinaweza kuwa za asili (wanga ni polymer ya mabaki ya sukari na protini ni polima za asidi amino) au synthetic [kama polyethilini, polyvinyl hidrojeni (PVC), na polystyrene]. Aina mbalimbali za miundo ya polima hutafsiriwa kuwa mali mbalimbali na matumizi ambayo huwafanya kuwa sehemu muhimu za maisha yetu ya kila siku. Kuongeza makundi ya kazi kwa muundo wa polymer inaweza kusababisha mali tofauti sana (angalia majadiliano kuhusu Kevlar baadaye katika sura hii).
Mfano wa mmenyuko wa upolimishaji unaonyeshwa kwenye Kielelezo\(\PageIndex{7}\). Monoma ethilini (C 2 H 4) ni gesi kwenye joto la kawaida, lakini inapopolimishwa, kwa kutumia kichocheo cha chuma cha mpito, inabadilishwa kuwa nyenzo imara iliyoundwa na minyororo mirefu ya —CH 2 — vitengo vinavyoitwa polyethilini. Polyethilini ni plastiki ya bidhaa inayotumiwa hasa kwa ajili ya ufungaji (mifuko na filamu).
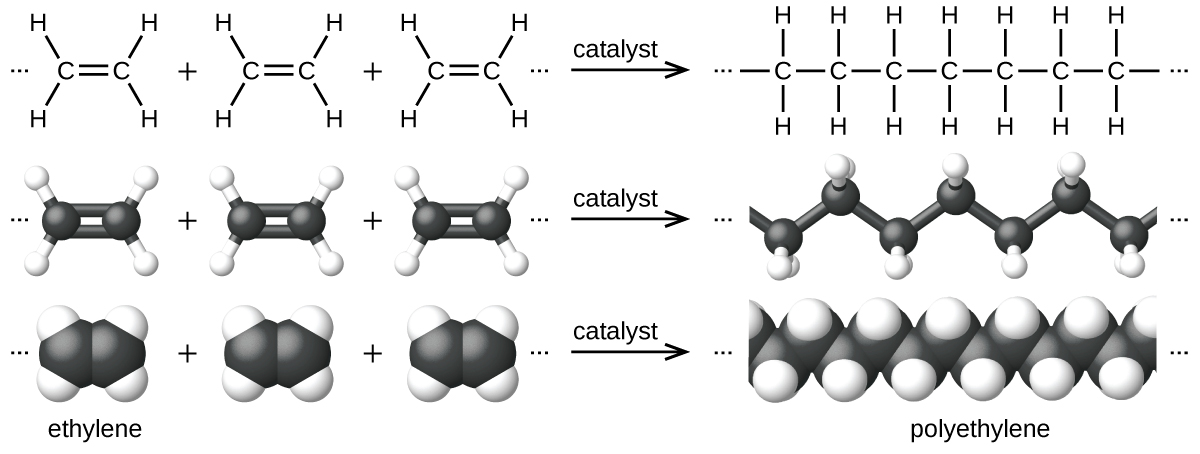
Polyethilini ni mwanachama wa subset moja ya polima za synthetic zilizowekwa kama plastiki. Plastiki ni solidi za kikaboni za synthetic ambazo zinaweza kuumbwa; kwa kawaida ni polima za kikaboni zilizo na raia Wengi wa monoma zinazoingia kwenye plastiki za kawaida (ethylene, propylene, kloridi ya vinyl, styrene, na ethylene terefalt) zinatokana na petrochemicals na hazibadiliki sana, na kuzifanya vifaa vya mgombea kwa kuchakata. Usafishaji wa plastiki husaidia kupunguza haja ya kutumia zaidi ya vifaa vya petrochemical na pia hupunguza uharibifu wa mazingira unaosababishwa na kutupa vifaa hivi visivyoweza kuharibika.
Usafishaji wa plastiki ni mchakato wa kurejesha taka, chakavu, au plastiki zilizotumiwa, na kurejesha nyenzo kuwa bidhaa muhimu. Kwa mfano, polyethilini terethilini (chupa za kunywa laini) zinaweza kuyeyuka chini na kutumika kwa samani za plastiki, katika mazulia, au kwa matumizi mengine. Plastiki nyingine, kama polyethilini (mifuko) na polypropen (vikombe, vyombo vya chakula vya plastiki), vinaweza kutengenezwa tena au kurekebishwa kutumiwa tena. Maeneo mengi ya nchi yana mipango ya kuchakata inayozingatia moja au zaidi ya plastiki za bidhaa ambazo zimepewa msimbo wa kuchakata (Kielelezo\(\PageIndex{8}\)). Shughuli hizi zimeanza kutumika tangu miaka ya 1970 na zimefanya uzalishaji wa baadhi ya plastiki kati ya shughuli za viwanda bora zaidi leo.
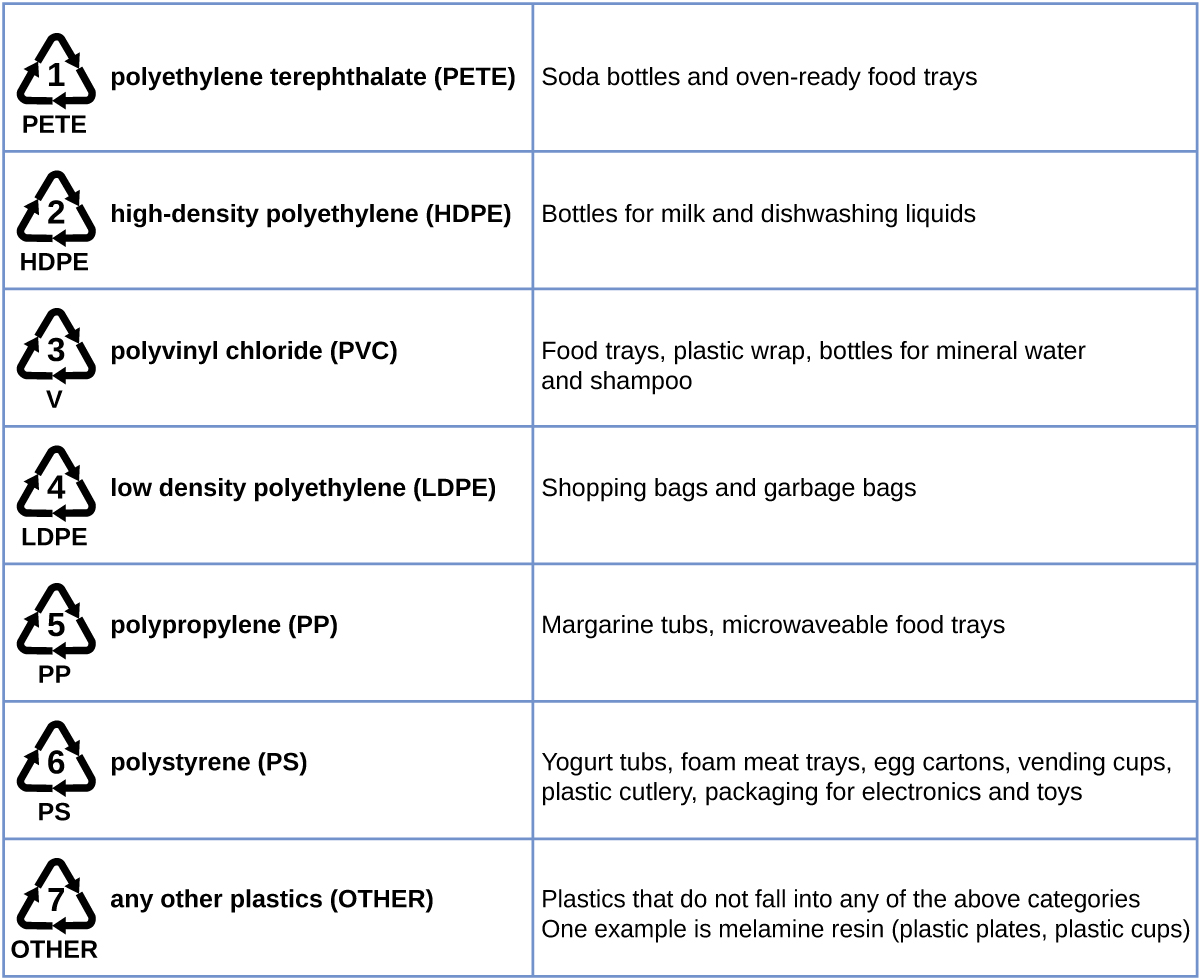
Jina la alkene limetokana na jina la alkane lenye idadi sawa ya atomi za kaboni. Uwepo wa dhamana mara mbili unaashiria kwa kuchukua nafasi ya suffix -ane na suffix -ene. Eneo la dhamana mara mbili hutambuliwa kwa kutaja ndogo ya idadi ya atomi za kaboni zinazoshiriki katika dhamana mbili:
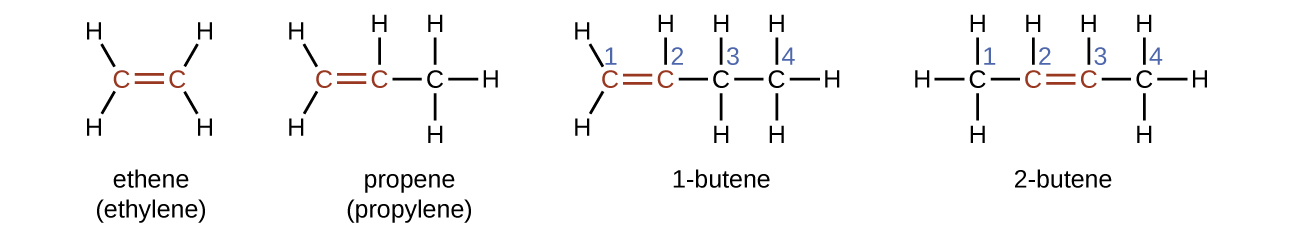
Isoma wa Alkenes
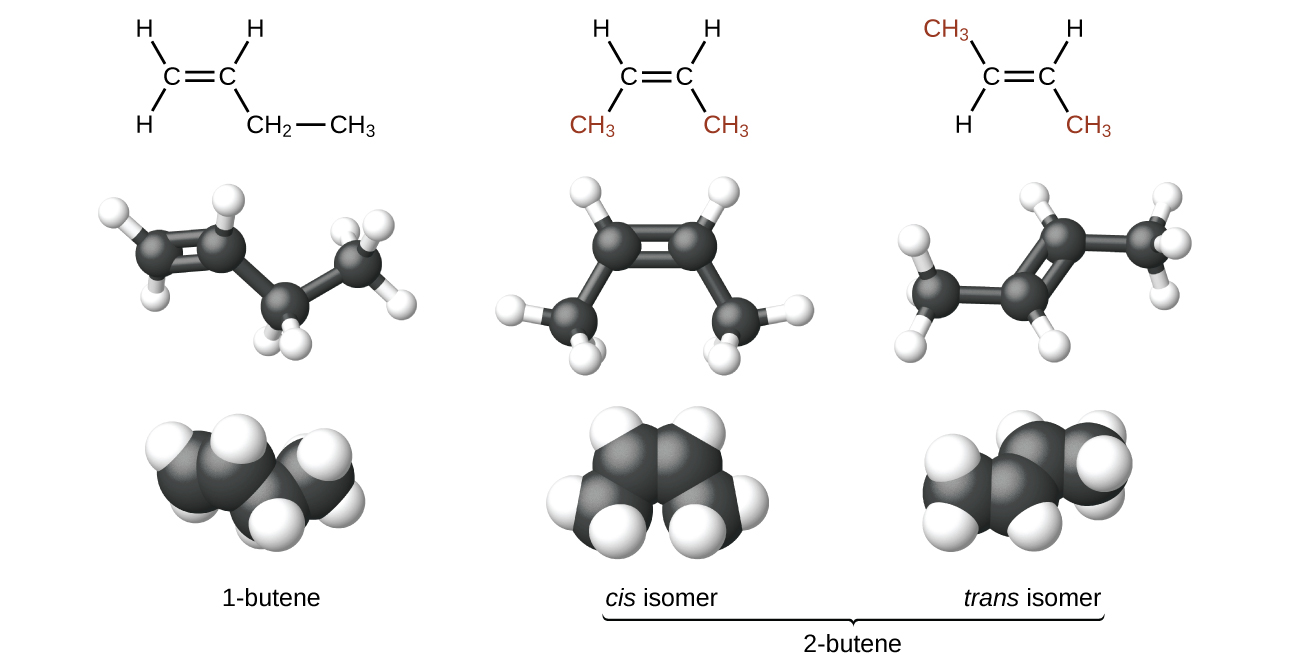
Molekuli ya 1-butene na 2-butene ni isoma za kimuundo; mpangilio wa atomi katika molekuli hizi mbili hutofautiana. Kama mfano wa tofauti za mpangilio, atomi ya kwanza ya kaboni katika 1-butene inaunganishwa na atomi mbili za hidrojeni; atomi ya kwanza ya kaboni katika 2-butene inaunganishwa na atomi tatu za hidrojeni.
Kiwanja 2-butene na alkeni nyingine pia huunda aina ya pili ya isoma inayoitwa isoma ya kijiometri. Katika seti ya isoma za kijiometri, aina hizo za atomi zinaunganishwa kwa utaratibu huo, lakini jiometri za molekuli mbili zinatofautiana. Isoma za kijiometri za alkenes zinatofautiana katika mwelekeo wa vikundi upande wowote wa\(\mathrm{C=C}\) dhamana.
Atomi za kaboni ni huru kuzunguka karibu na dhamana moja lakini si karibu na dhamana mbili; dhamana mara mbili ni rigid. Hii inafanya uwezekano wa kuwa na isoma mbili za 2-butene, moja na vikundi vyote viwili vya methyl upande mmoja wa dhamana mbili na moja na makundi ya methyl pande tofauti. Wakati miundo ya butene inayotolewa na pembe 120° dhamana karibu na atomi sp 2 -hybridized carbon kushiriki katika dhamana mara mbili, isoma ni dhahiri. Isoma ya 2-butene ambayo vikundi viwili vya methyl viko upande mmoja huitwa cis -isoma; moja ambayo vikundi viwili vya methyl viko pande tofauti huitwa trans -isoma (Kielelezo\(\PageIndex{9}\)). Jiometri tofauti huzalisha mali tofauti za kimwili, kama vile kiwango cha kuchemsha, ambacho kinaweza kufanya kujitenga kwa isoma iwezekanavyo:
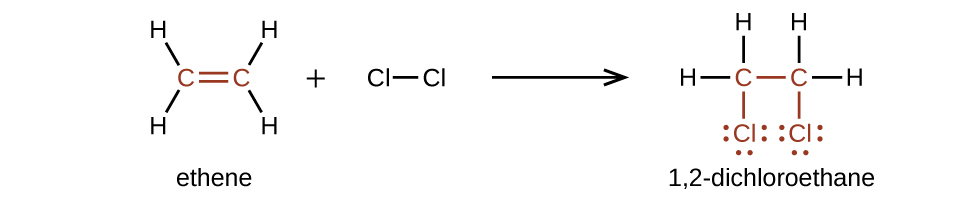
Alkenes ni tendaji zaidi kuliko alkanes kwa sababu\(\mathrm{C=C}\) moiety ni kundi tendaji kazi. Dhamana π, kuwa dhamana dhaifu, huvunjika kwa urahisi zaidi kuliko dhamana ya σ. Hivyo, alkenes hupata mmenyuko wa tabia ambayo dhamana ya π imevunjika na kubadilishwa na vifungo viwili vya σ. Tabia hii inaitwa mmenyuko wa kuongeza. Uchanganyiko wa atomi za kaboni katika dhamana mbili katika alkene hubadilika kutoka sp 2 hadi sp 3 wakati wa mmenyuko wa kuongeza. Kwa mfano, halojeni huongeza kwenye dhamana mara mbili katika alkene badala ya kuchukua nafasi ya hidrojeni, kama inatokea katika alkane:
Kutoa majina ya IUPAC kwa reactant na bidhaa ya mmenyuko halogenation inavyoonekana hapa:
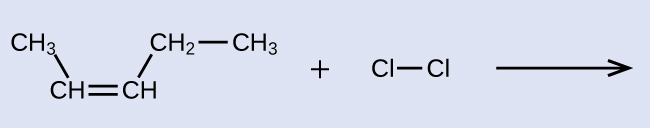
Suluhisho
Mtendaji ni mnyororo wa kaboni tano ambao una dhamana ya kaboni-kaboni mara mbili, hivyo jina la msingi litakuwa pentene. Tunaanza kuhesabu mwishoni mwa mlolongo karibu na mara mbili dhamana - katika kesi hii, kutoka kushoto-mara mbili dhamana spans carbon 2 na 3, hivyo jina inakuwa 2-pentene. Kwa kuwa kuna makundi mawili yaliyo na kaboni yaliyounganishwa na atomi mbili za kaboni katika dhamana ya mara mbili-na wako upande uleule wa kifungo mara mbili—molekuli hii ni isoma ya cis-, na kufanya jina la alkene kuanzia cis -2-pentene. Bidhaa ya mmenyuko wa halogenation itakuwa na atomi mbili za klorini zilizounganishwa na atomi za kaboni ambazo zilikuwa sehemu ya dhamana mbili ya kaboni-kaboni:
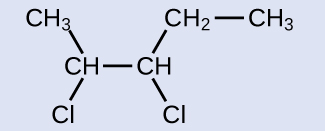
Molekuli hii sasa ni alkane iliyobadilishwa na itaitwa kama vile. Msingi wa jina utakuwa pentane. Tutahesabu kutoka mwisho kwamba namba atomi za kaboni ambapo atomi za klorini zimeunganishwa kama 2 na 3, na kufanya jina la bidhaa 2,3-dichloropentane.
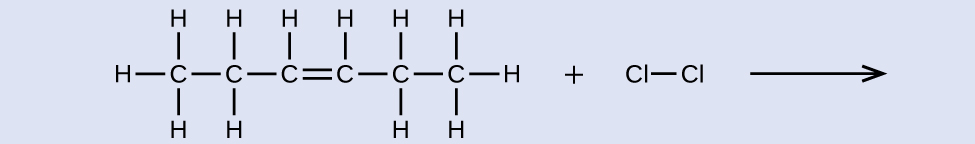
Kutoa majina kwa reactant na bidhaa ya mmenyuko umeonyeshwa:
- Jibu
-
reactant: cis-3-hexene, bidhaa: 3,4-dichlorohexane
Alkynes
Molekuli ya hidrokaboni yenye vifungo moja au zaidi mara tatu huitwa alkynes; hufanya mfululizo mwingine wa hidrokaboni zisizohifadhiwa. Atomi mbili za kaboni zilizounganishwa na dhamana tatu zimefungwa pamoja na dhamana moja σ na vifungo viwili π. Kaboni za sp -hybridized zinazohusika katika dhamana tatu zina pembe za dhamana za 180°, zikitoa aina hizi za vifungo umbo linear, kama fimbo.
Mwanachama rahisi zaidi wa mfululizo wa alkyne ni ethyne, C 2 H 2, inayoitwa asetilini. Muundo wa Lewis kwa ethyne, molekuli linear, ni:
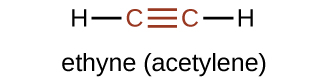
Nomenclature ya IUPAC kwa alkines ni sawa na ile kwa alkenes isipokuwa kwamba suffix -yne hutumiwa kuonyesha dhamana mara tatu katika mnyororo. Kwa mfano,\(\mathrm{CH_3CH_2C≡CH}\) inaitwa 1-butyne.
Eleza jiometri na mahuluti ya atomi za kaboni katika molekuli ifuatayo:
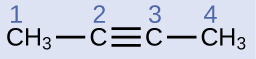
Suluhisho
Atomi za kaboni 1 na 4 zina vifungo vinne vya moja na hivyo ni tetrahedral na mahuluti ya sp 3. Atomi za kaboni 2 na 3 zinahusika katika dhamana ya mara tatu, hivyo zina jiometri linear na zingeainishwa kama mahuluti sp.
Kutambua hybridization na dhamana pembe katika atomi kaboni katika molekuli inavyoonekana:
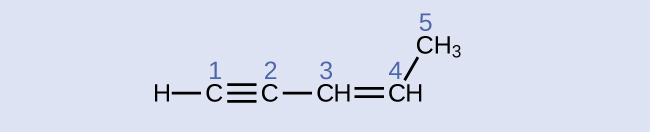
- Jibu
-
kaboni 1: sp, 180°; kaboni 2: sp, 180°; kaboni 3: sp 2, 120°; kaboni 4: sp 2, 120°; kaboni 5: sp 3, 109.5°
Kemikali, alkynes ni sawa na alkenes. Kwa kuwa kundi la\(\mathrm{C≡C}\) kazi lina vifungo viwili vya π, alkynes kawaida huguswa hata kwa urahisi zaidi, na huitikia na reagent mara mbili zaidi katika athari za kuongeza. Tabia ya asetilini na bromini ni mfano wa kawaida:
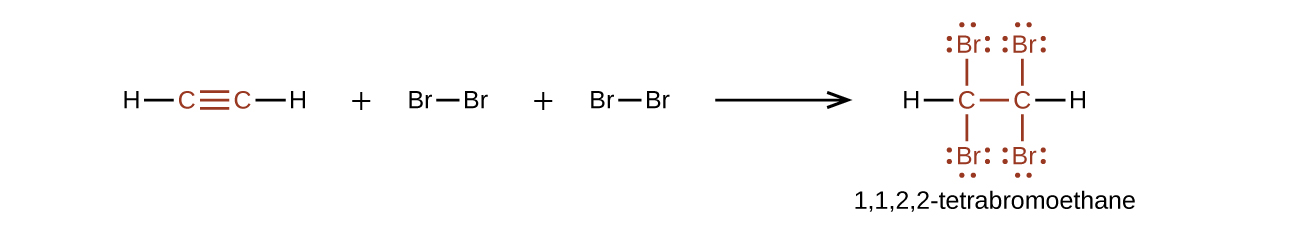
Asetilini na alkini nyingine pia huwaka kwa urahisi. Tochi ya asetilini inachukua faida ya joto kubwa la mwako kwa asetilini.
Hidrokaboni kunukia
Benzini, C 6 H 6, ni mwanachama rahisi zaidi wa familia kubwa ya hidrokaboni, inayoitwa hidrokaboni yenye kunukia. Misombo hii ina miundo pete na maonyesho bonding kwamba lazima ilivyoelezwa kwa kutumia resonance mseto dhana ya nadharia valence dhana dhamana au delanication dhana ya molekuli orbital nadharia. (Ili kupitia dhana hizi, rejea sura za awali juu ya kuunganisha kemikali). Miundo ya resonance ya benzini, C 6 H 6, ni:
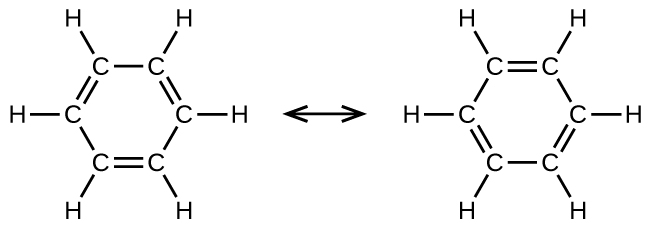

Kuna derivatives nyingi za benzini. Atomi za hidrojeni zinaweza kubadilishwa na mbadala nyingi tofauti. Misombo ya kunukia kwa urahisi zaidi kupitia athari badala ya athari za kuongeza; badala ya moja ya atomi za hidrojeni na mbadala mwingine utaondoka vifungo viwili vilivyowekwa ndani. Yafuatayo ni mifano ya kawaida ya derivatives ya benzini iliyobadilishwa:
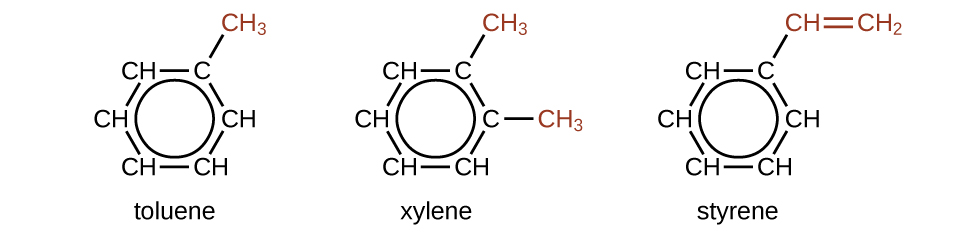
Toluene na xylene ni vimumunyisho muhimu na malighafi katika sekta ya kemikali. Styrene hutumiwa kuzalisha polystyrene ya polymer.
Isoma moja inayowezekana iliyoundwa na mmenyuko mbadala ambayo inachukua nafasi ya atomi ya hidrojeni iliyoambatana na pete yenye kunukia ya toluini yenye atomi ya klorini inavyoonyeshwa hapa. Chora isoma nyingine mbili zinazowezekana ambazo atomu ya klorini inachukua nafasi ya atomi tofauti ya hidrojeni iliyounganishwa na pete yenye kunukia:
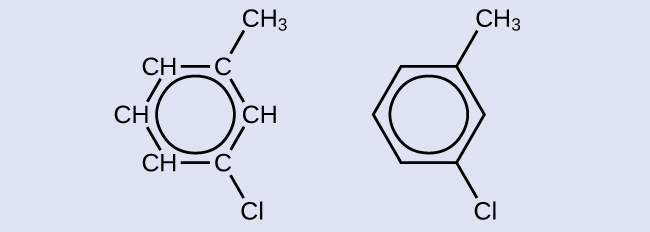
Suluhisho
Kwa kuwa pete ya kaboni sita na vifungo vya mara mbili ni muhimu kwa molekuli kuhesabiwa kama kunukia, isoma zinazofaa zinaweza kuzalishwa tu kwa kubadilisha nafasi za chloro-substituent jamaa na methyl-mbadala:
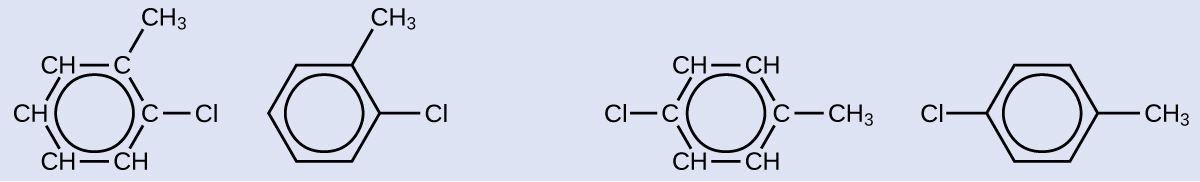
Chora isoma tatu za kiwanja cha pete cha kunukia cha sita kilichowekwa na bromini mbili.
- Jibu
-
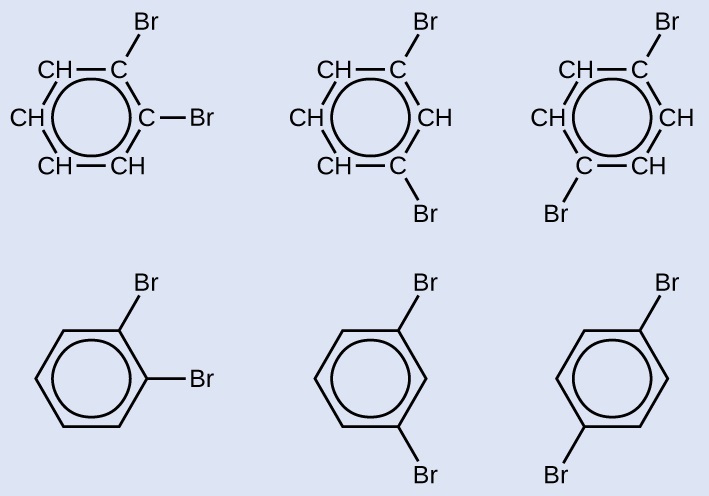
Jozi tatu za formula za kimuundo zinaonyeshwa. Ya kwanza ina pete sita ya hidrokaboni ya kaboni ambamo atomi nne za C kila mmoja huunganishwa na atomi moja tu ya H. Katika haki ya juu na kulia ya pete, mbili C atomi ambazo hazina Bonded H atomi na moja B r atomi bonded kila. Mduara ni katikati ya pete. Chini ya muundo huu, muundo sawa unaonyeshwa ambao una hexagon na mduara ndani. Kutoka kwa vipeo vya hexagon kwenye atomi za juu za kulia na za kulia za B r zimeunganishwa. Ya pili ina pete sita ya hidrokaboni ya kaboni ambamo atomi nne za C kila mmoja huunganishwa na atomi moja tu ya H. Katika haki ya juu na chini ya kulia ya pete, mbili C atomi ambazo hazina Bonded H atomi na moja B r atomi bonded kila. Mduara ni katikati ya pete. Chini ya muundo huu, muundo sawa unaonyeshwa ambao una hexagon na mduara ndani. Kutoka kwa vipeo vya hexagon kwenye atomi za juu za kulia na za chini za moja B r zimeunganishwa. Ya tatu ina pete sita ya hidrokaboni ya kaboni ambamo atomi nne za C kila mmoja huunganishwa na atomi moja tu ya H. Katika upande wa juu kulia na chini kushoto wa pete, mbili C atomi ambazo hazina Bonded H atomi na B r atomi Bonded. Mduara ni katikati ya pete. Chini ya muundo huu, muundo sawa unaonyeshwa ambao una hexagon na mduara ndani. Kutoka kwenye vipeo vya hexagon upande wa juu wa kushoto na wa chini, atomi moja ya B r ni masharti.
Muhtasari
Nguvu, imara vifungo kati ya atomi za kaboni huzalisha molekuli tata zenye minyororo, matawi, na pete. Kemia ya misombo hii inaitwa kemia ya kikaboni. Hidrokaboni ni misombo ya kikaboni yenye kaboni na hidrojeni tu. Alkanes ni hidrokaboni zilizojaa- yaani hidrokaboni ambazo zina vifungo moja tu. Alkenes zina vifungo moja au zaidi ya kaboni-kaboni mara mbili. Alkynes zina vifungo moja au zaidi ya kaboni-kaboni mara tatu. Hidrokaboni yenye kunukia huwa na miundo ya pete na mifumo ya elektroni iliyosafishwa π
maelezo ya chini
- Hii ni database ya Beilstein, sasa inapatikana kupitia tovuti ya Reaxys (www.elsevier.com/online-tools/reaxys).
- Peplow, Mark. “Organic awali: Robo-Kemia, "Nature 512 (2014): 20—2.
- Mali ya kimwili kwa C 4 H 10 na molekuli nzito ni yale ya isoma ya kawaida, n -butane, n -pentane, nk.
- STP inaonyesha halijoto ya 0 °C na shinikizo la atm 1.
faharasa
- majibu ya kuongeza
- majibu ambayo dhamana ya kaboni-kaboni mara mbili huunda dhamana moja ya kaboni-kaboni kwa kuongeza ya reactant. Tabia ya kawaida kwa alkene.
- alkane
- molekuli yenye atomi za kaboni na hidrojeni tu zilizounganishwa na vifungo moja (σ)
- alkene
- molekuli yenye kaboni na hidrojeni zenye angalau carbon-carbon mara mbili dhamana
- kundi la alkyl
- substituent, yenye alkane kukosa atomi moja hidrojeni, masharti ya muundo kubwa
- alkyne
- molekuli yenye kaboni na hidrojeni zenye angalau carbon-carbon mara tatu dhamana
- kunukia hidrokaboni
- mzunguko molekuli yenye kaboni na hidrojeni na delocalized alternating carbon-carbon moja na mbili vifungo, na kusababisha utulivu kuimarishwa
- kikundi cha kazi
- sehemu ya molekuli ya kikaboni ambayo inatoa reactivity maalum kemikali kwa molekuli
- kiwanja kikaboni
- asili au synthetic kiwanja ambayo ina kaboni
- hydrokaboni iliyojaa
- molekuli zenye kaboni na hidrojeni ambayo ina vifungo moja tu kati ya atomi za kaboni
- muundo wa mifupa
- njia ya shorthand ya kuchora molekuli za kikaboni ambazo atomi za kaboni zinawakilishwa na mwisho wa mistari na hupiga kati ya mistari, na atomi za hidrojeni zilizounganishwa na atomi za kaboni hazionyeshwa (lakini zinaeleweka kuwa sasa na muktadha wa muundo)
- mbadala
- tawi au kundi kazi kwamba nafasi ya atomi hidrojeni katika mnyororo kubwa hydrocarbon
- mmenyuko wa badala
- mmenyuko ambao atomu moja hubadilisha mwingine katika molekuli


