18.5: Vacinas
- Page ID
- 181433
Objetivos de
- Compare os vários tipos de imunidade artificial
- Diferenciar entre variolação e vacinação
- Descreva diferentes tipos de vacinas e explique suas respectivas vantagens e desvantagens
Para muitas doenças, a prevenção é a melhor forma de tratamento, e poucas estratégias de prevenção de doenças são tão eficazes quanto a vacinação. A vacinação é uma forma de imunidade artificial. Ao estimular artificialmente as defesas imunes adaptativas, uma vacina desencadeia a produção de células de memória semelhante à que ocorreria durante uma resposta primária. Ao fazer isso, o paciente é capaz de gerar uma forte resposta secundária após a exposição ao patógeno, mas sem ter que sofrer primeiro uma infecção inicial. Nesta seção, exploraremos vários tipos diferentes de imunidade artificial, juntamente com vários tipos de vacinas e os mecanismos pelos quais elas induzem a imunidade artificial.
Classificações da imunidade adaptativa
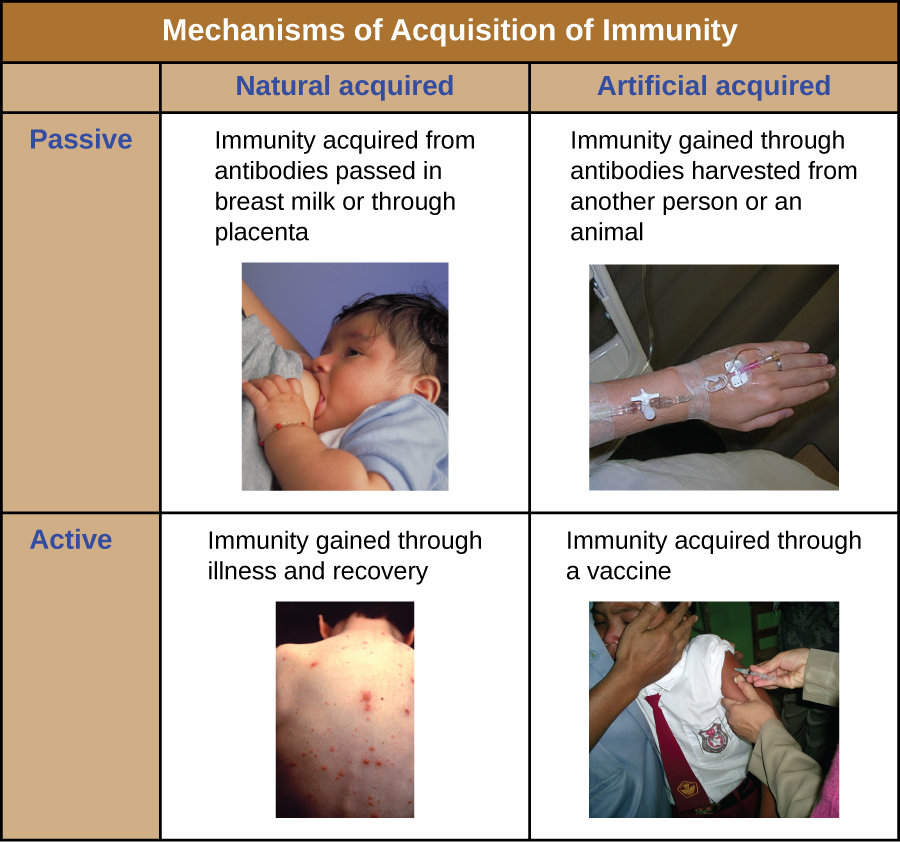
Todas as formas de imunidade adaptativa podem ser descritas como ativas ou passivas. A imunidade ativa se refere à ativação das defesas imunes adaptativas do próprio indivíduo, enquanto a imunidade passiva se refere à transferência de defesas imunes adaptativas de outro indivíduo ou animal. A imunidade ativa e passiva pode ser subdividida ainda mais com base no fato de a proteção ser adquirida natural ou artificialmente.
A imunidade ativa natural é a imunidade adaptativa que se desenvolve após a exposição natural a um patógeno (Figura\(\PageIndex{1}\)). Os exemplos incluem a imunidade vitalícia que se desenvolve após a recuperação de uma infecção por catapora ou sarampo (embora nem sempre seja necessária uma infecção aguda para ativar a imunidade adaptativa). O período de proteção de um indivíduo pode variar substancialmente, dependendo do patógeno e dos antígenos envolvidos. Por exemplo, a ativação da imunidade adaptativa por estruturas de pico de proteína durante uma infecção viral intracelular pode ativar a imunidade vitalícia, enquanto a ativação por antígenos da cápsula de carboidratos durante uma infecção bacteriana extracelular pode ativar a imunidade de curto prazo.
A imunidade passiva natural envolve a passagem natural de anticorpos da mãe para o filho antes e depois do nascimento. A IgG é a única classe de anticorpos que pode atravessar a placenta do sangue da mãe até o suprimento sanguíneo fetal. A transferência placentária de IgG é uma importante defesa imune passiva para o bebê, durando até seis meses após o nascimento. A IgA secretora também pode ser transferida da mãe para o bebê através do leite materno.
A imunidade passiva artificial se refere à transferência de anticorpos produzidos por um doador (humano ou animal) para outro indivíduo. Essa transferência de anticorpos pode ser feita como uma medida profilática (ou seja, para prevenir doenças após a exposição a um patógeno) ou como uma estratégia para tratar uma infecção ativa. Por exemplo, a imunidade passiva artificial é comumente usada para profilaxia pós-exposição contra raiva, hepatite A, hepatite B e varicela (em indivíduos de alto risco). As infecções ativas tratadas pela imunidade passiva artificial incluem infecções por citomegalovírus em pacientes imunocomprometidos e infecções pelo vírus Ebola. Em 1995, oito pacientes na República Democrática do Congo com infecções ativas por Ebola foram tratados com transfusões de sangue de pacientes que estavam se recuperando do Ebola. Apenas um dos oito pacientes morreu (uma taxa de mortalidade de 12,5%), o que foi muito menor do que a taxa de mortalidade esperada de 80% para o Ebola em pacientes não tratados. 1 A imunidade passiva artificial também é usada para o tratamento de doenças causadas por toxinas bacterianas, incluindo tétano, botulismo e difteria.
A imunidade ativa artificial é a base para a vacinação. Envolve a ativação da imunidade adaptativa por meio da exposição deliberada de um indivíduo a patógenos enfraquecidos ou inativados, ou preparações que consistem em antígenos patogênicos essenciais.
Exercício\(\PageIndex{1}\)
- Qual a diferença entre imunidade ativa e passiva?
- Que tipo de imunidade é conferida por uma vacina?
Imunidade de rebanho
Os quatro tipos de imunidade que acabamos de descrever resultam do sistema imunológico adaptativo de um indivíduo. Para qualquer doença, um indivíduo pode ser considerado imune ou suscetível, dependendo de sua capacidade de gerar uma resposta imune eficaz após a exposição. Assim, é provável que qualquer população tenha alguns indivíduos imunes e outros suscetíveis. Se uma população tiver muito poucos indivíduos suscetíveis, mesmo esses indivíduos serão protegidos por um fenômeno chamado imunidade coletiva. A imunidade coletiva não tem nada a ver com a capacidade do indivíduo de criar uma resposta imune eficaz; ao contrário, ocorre porque há poucos indivíduos suscetíveis em uma população para que a doença se espalhe de forma eficaz.
Os programas de vacinação criam imunidade coletiva ao reduzir consideravelmente o número de indivíduos suscetíveis em uma população. Mesmo que alguns indivíduos da população não sejam vacinados, desde que uma certa porcentagem esteja imune (natural ou artificialmente), é improvável que os poucos indivíduos suscetíveis sejam expostos ao patógeno. No entanto, como novos indivíduos estão constantemente entrando nas populações (por exemplo, por meio do nascimento ou da realocação), programas de vacinação são necessários para manter a imunidade do rebanho.
Vacinação: obrigação ou escolha
Um número crescente de pais está optando por não vacinar seus filhos. Eles são apelidados de “antivaxxers” e a maioria deles acredita que as vacinas são a causa do autismo (ou de outras doenças), uma ligação que agora foi totalmente refutada. Outros se opõem às vacinas por motivos religiosos ou morais (por exemplo, o argumento de que a vacinação com Gardasil contra o HPV pode promover a promiscuidade sexual), por motivos éticos pessoais (por exemplo, uma objeção de consciência a qualquer intervenção médica) ou por motivos políticos (por exemplo, a noção de que as vacinações obrigatórias são violação das liberdades individuais). 2
Acredita-se que esse número crescente de indivíduos não vacinados tenha levado a novos surtos de coqueluche e sarampo. Esperaríamos que a imunidade coletiva protegesse aqueles não vacinados em nossa população, mas a imunidade do rebanho só pode ser mantida se um número suficiente de indivíduos estiver sendo vacinado.
A vacinação é claramente benéfica para a saúde pública. Mas, do ponto de vista individual dos pais, a visão pode ser mais obscura. As vacinas, como todas as intervenções médicas, têm riscos associados e, embora os riscos da vacinação possam ser extremamente baixos em comparação com os riscos de infecção, os pais nem sempre entendem ou aceitam o consenso da comunidade médica. Esses pais têm o direito de reter a vacinação de seus filhos? Eles deveriam ter permissão para colocar seus filhos — e a sociedade em geral — em risco?
Muitos governos insistem na vacinação infantil como condição para ingressar na escola pública, mas tornou-se fácil na maioria dos estados optar por não cumprir a exigência ou manter as crianças fora do sistema público. Desde a década de 1970, a Virgínia Ocidental e o Mississippi estabeleceram uma exigência rigorosa de vacinação infantil, sem exceções, e nenhum estado teve um caso de sarampo desde o início da década de 1990. Os legisladores da Califórnia aprovaram recentemente uma lei semelhante em resposta a um surto de sarampo em 2015, tornando muito mais difícil para os pais optarem por não receber vacinas se seus filhos frequentarem escolas públicas. Dado esse histórico e os esforços legislativos renovados, outros estados deveriam adotar requisitos igualmente rígidos?
Que papel os profissionais de saúde devem desempenhar na promoção ou aplicação da vacinação universal? Estudos mostraram que a mente de muitos pais pode mudar em resposta às informações fornecidas pelos profissionais de saúde, mas cabe aos profissionais de saúde tentar persuadir os pais a vacinarem seus filhos? Alguns profissionais de saúde estão compreensivelmente relutantes em tratar pacientes não vacinados. Eles têm o direito de recusar o atendimento a pacientes que recusam vacinas? As seguradoras têm o direito de negar cobertura aos antivaxxers? Todas essas são questões éticas que os formuladores de políticas podem ser forçados a abordar à medida que mais pais contornam as normas de vacinação.
Variolação e vacinação
Milhares de anos atrás, foi reconhecido pela primeira vez que indivíduos que sobreviveram a uma infecção por varíola estavam imunes a infecções subsequentes. A prática de inocular indivíduos para protegê-los ativamente da varíola parece ter se originado no século 10 na China, quando a prática da variolação foi descrita (Figura\(\PageIndex{2}\)). A variolação se refere à inoculação deliberada de indivíduos com material infeccioso de crostas ou pústulas de vítimas de varíola. Os materiais infecciosos foram injetados na pele ou introduzidos pela via nasal. A infecção que se desenvolveu foi geralmente mais leve do que a varíola adquirida naturalmente, e a recuperação da infecção mais leve forneceu proteção contra a doença mais grave.
Embora a maioria dos indivíduos tratados por variolação tenha desenvolvido apenas infecções leves, a prática não foi isenta de riscos. Ocorreram infecções mais graves e às vezes fatais e, como a varíola era contagiosa, infecções resultantes da variolação poderiam levar a epidemias. Mesmo assim, a prática da variolação para prevenção da varíola se espalhou para outras regiões, incluindo Índia, África e Europa.

Embora a variolação tenha sido praticada há séculos, o médico inglês Edward Jenner (1749—1823) é geralmente creditado por ter desenvolvido o processo moderno de vacinação. Jenner observou que as leiteiras que desenvolveram a varíola bovina, uma doença semelhante à varíola, mas mais leve, eram imunes à varíola mais grave. Isso levou Jenner a hipotetizar que a exposição a um patógeno menos virulento poderia fornecer proteção imune contra um patógeno mais virulento, fornecendo uma alternativa mais segura à variolação. Em 1796, Jenner testou sua hipótese obtendo amostras infecciosas da lesão ativa da varíola bovina de uma leiteira e injetando os materiais em um menino (Figura\(\PageIndex{3}\)). O menino desenvolveu uma infecção leve que incluiu febre baixa, desconforto nas axilas (axilas) e perda de apetite. Quando o menino foi posteriormente infectado com amostras infecciosas de lesões de varíola, ele não contraiu varíola. 3 Essa nova abordagem foi denominada vacinação, um nome derivado do uso da varíola bovina (latim vacca que significa “vaca”) para proteção contra a varíola. Hoje, sabemos que a vacina de Jenner funcionou porque o vírus da varíola bovina está geneticamente e antigenicamente relacionado aos vírus Varíola que causaram a varíola. A exposição a antígenos da varíola bovina resultou em uma resposta primária e na produção de células de memória que são epítopos idênticos ou relacionados do vírus Varíola após uma exposição posterior à varíola.
O sucesso da vacinação contra varíola de Jenner levou outros cientistas a desenvolverem vacinas para outras doenças. Talvez o mais notável tenha sido Louis Pasteur, que desenvolveu vacinas para raiva, cólera e antraz. Durante os séculos XX e XXI, vacinas eficazes foram desenvolvidas para prevenir uma ampla gama de doenças causadas por vírus (por exemplo, varicela e herpes zoster, hepatite, sarampo, caxumba, poliomielite e febre amarela) e bactérias (por exemplo, difteria, pneumonia pneumocócica, tétano e coqueluche tosse,).
Exercício\(\PageIndex{2}\)
- Qual é a diferença entre variolação e vacinação contra a varíola?
- Explique por que a vacinação é menos arriscada do que a variolação.
Classes de vacinas
Para que uma vacina forneça proteção contra uma doença, ela deve expor um indivíduo a antígenos específicos do patógeno que estimularão uma resposta imune adaptativa protetora. Por sua própria natureza, isso acarreta algum risco. Como acontece com qualquer medicamento farmacêutico, as vacinas têm o potencial de causar efeitos adversos. No entanto, a vacina ideal não causa efeitos adversos graves e não apresenta risco de contrair a doença que se destina a prevenir. Vários tipos de vacinas foram desenvolvidos com esses objetivos em mente. Essas diferentes classes de vacinas são descritas na próxima seção e resumidas na Tabela\(\PageIndex{1}\).
Vacinas vivas atenuadas
Vacinas vivas atenuadas expõem o indivíduo a uma cepa enfraquecida de um patógeno com o objetivo de estabelecer uma infecção subclínica que ativará as defesas imunológicas adaptativas. Os patógenos são atenuados para diminuir sua virulência usando métodos como manipulação genética (para eliminar os principais fatores de virulência) ou cultivo de longo prazo em um hospedeiro ou ambiente não natural (para promover mutações e diminuir a virulência).
Ao estabelecer uma infecção ativa, as vacinas vivas atenuadas estimulam uma resposta imune mais abrangente do que alguns outros tipos de vacinas. As vacinas vivas atenuadas ativam a imunidade celular e humoral e estimulam o desenvolvimento da memória para uma imunidade duradoura. Em alguns casos, a vacinação de um indivíduo com um patógeno vivo atenuado pode até levar à transmissão natural do patógeno atenuado para outros indivíduos. Isso pode fazer com que os outros indivíduos também desenvolvam uma infecção subclínica ativa que ativa suas defesas imunes adaptativas.
As desvantagens associadas às vacinas vivas atenuadas incluem os desafios associados ao armazenamento e transporte a longo prazo, bem como o potencial de um paciente desenvolver sinais e sintomas da doença durante a infecção ativa (particularmente em pacientes imunocomprometidos). Também existe o risco de o patógeno atenuado voltar à virulência total. A tabela\(\PageIndex{1}\) lista exemplos de vacinas vivas atenuadas.
Vacinas inativadas
As vacinas inativadas contêm patógenos inteiros que foram mortos ou inativados com calor, produtos químicos ou radiação. Para que as vacinas inativadas sejam eficazes, o processo de inativação não deve afetar a estrutura dos antígenos essenciais do patógeno.
Como o patógeno é morto ou inativo, as vacinas inativadas não produzem uma infecção ativa e a resposta imune resultante é mais fraca e menos abrangente do que a provocada por uma vacina viva atenuada. Normalmente, a resposta envolve apenas imunidade humoral e o patógeno não pode ser transmitido a outros indivíduos. Além disso, as vacinas inativadas geralmente requerem doses mais altas e vários reforços, possivelmente causando reações inflamatórias no local da injeção.
Apesar dessas desvantagens, as vacinas inativadas têm as vantagens de estabilidade de armazenamento a longo prazo e facilidade de transporte. Além disso, não há risco de causar infecções ativas graves. No entanto, as vacinas inativadas têm seus efeitos colaterais. A tabela\(\PageIndex{1}\) lista exemplos de vacinas inativadas.
Vacinas de subunidade
Enquanto as vacinas vivas atenuadas e inativas expõem um indivíduo a um patógeno enfraquecido ou morto, as vacinas de subunidade expõem o paciente apenas aos antígenos essenciais de um patógeno — não a células inteiras ou vírus. As vacinas de subunidade podem ser produzidas degradando quimicamente um patógeno e isolando seus antígenos principais ou produzindo os antígenos por meio da engenharia genética. Como essas vacinas contêm apenas os antígenos essenciais de um patógeno, o risco de efeitos colaterais é relativamente baixo. A tabela\(\PageIndex{1}\) lista exemplos de vacinas de subunidade.
Vacinas contra toxóides
Como as vacinas de subunidade, as vacinas contra toxóides não introduzem um patógeno completo no paciente; elas contêm toxinas bacterianas inativadas, chamadas toxóides. As vacinas contra toxóides são usadas para prevenir doenças nas quais as toxinas bacterianas desempenham um papel importante na patogênese. Essas vacinas ativam a imunidade humoral que neutraliza as toxinas. A tabela\(\PageIndex{1}\) lista exemplos de vacinas contra toxóides.
Vacinas conjugadas
Uma vacina conjugada é um tipo de vacina de subunidade que consiste em uma proteína conjugada a um polissacarídeo em cápsula. As vacinas conjugadas foram desenvolvidas para aumentar a eficácia das vacinas de subunidade contra patógenos que possuem cápsulas protetoras de polissacarídeos que os ajudam a evitar a fagocitose, causando infecções invasivas que podem levar à meningite e outras condições graves. As vacinas de subunidade contra esses patógenos introduzem antígenos polissacarídeos capsulares independentes de T que resultam na produção de anticorpos que podem opsonizar a cápsula e, assim, combater a infecção; no entanto, crianças menores de dois anos não respondem efetivamente a essas vacinas. As crianças respondem de forma eficaz quando vacinadas com a vacina conjugada, na qual uma proteína com antígenos dependentes de T é conjugada ao polissacarídeo em cápsula. O antígeno proteína-polissacarídeo conjugado estimula a produção de anticorpos contra a proteína e o polissacarídeo em cápsula. A tabela\(\PageIndex{1}\) lista exemplos de vacinas conjugadas.
| Classe | Descrição | Vantagens | Desvantagens | Exemplos |
|---|---|---|---|---|
| Ao vivo atenuado | Estirpe enfraquecida de todo o patógeno | Imunidade celular e humoral | Difícil de armazenar e transportar | Varicela, sarampo alemão, sarampo, caxumba, tuberculose, febre tifóide, febre amarela |
| Imunidade duradoura | Risco de infecção em pacientes imunocomprometidos | |||
| Transmissão para contatos | Risco de reversão | |||
| Inativado | Patógeno inteiro morto ou inativado com calor, produtos químicos ou radiação | Facilidade de armazenamento e transporte | Imunidade mais fraca (somente humoral) | Cólera, hepatite A, gripe, peste, raiva |
| Sem risco de infecção ativa grave | São necessárias doses mais altas e mais reforços | |||
| Subunidade | Antígenos imunogênicos | Menor risco de efeitos colaterais | Longevidade limitada | Antraz, hepatite B, gripe, meningite, papilomavírus, pneumonia pneumocócica, coqueluche |
| Várias doses necessárias | ||||
| Sem proteção contra variação antigênica | ||||
| Toxóide | Toxina bacteriana inativada | Imunidade humoral para neutralizar a toxina | Não previne a infecção | Botulismo, difteria, coqueluche, tétano |
| Conjugar | Polissacárido em cápsula conjugado com proteína | Resposta dependente de T à cápsula | Caro de produzir |
Meningite (Haemophilus influenzae, Streptococcus pneumoniae, Neisseria meningitides) |
| Sem proteção contra variação antigênica | ||||
| Melhor resposta em crianças pequenas | Pode interferir com outras vacinas |
Exercício\(\PageIndex{3}\)
- Qual é o risco associado a uma vacina viva atenuada?
- Por que uma vacina conjugada é necessária em alguns casos?
As vacinas de DNA representam uma abordagem relativamente nova e promissora da vacinação. Uma vacina de DNA é produzida pela incorporação de genes para antígenos em uma vacina de plasmídeo recombinante. A introdução da vacina de DNA em um paciente leva à captação do plasmídeo recombinante por algumas células do paciente, seguida pela transcrição e tradução de antígenos e apresentação desses antígenos com MHC I para ativar a imunidade adaptativa. Isso resulta na estimulação da imunidade humoral e celular sem o risco de doença ativa associada a vacinas vivas atenuadas.
Embora a maioria das vacinas de DNA para humanos ainda esteja em desenvolvimento, é provável que elas se tornem mais prevalentes em um futuro próximo, à medida que os pesquisadores estão trabalhando na engenharia de vacinas de DNA que ativarão a imunidade adaptativa contra vários patógenos diferentes ao mesmo tempo. As vacinas de DNA de primeira geração testadas na década de 1990 pareciam promissoras em modelos animais, mas foram decepcionantes quando testadas em humanos. A baixa absorção celular dos plasmídeos de DNA foi um dos principais problemas que afetaram sua eficácia. Os testes de vacinas de DNA de segunda geração têm sido mais promissores graças às novas técnicas para melhorar a absorção celular e otimizar antígenos. Vacinas de DNA para vários tipos de câncer e patógenos virais, como HIV, HPV e hepatite B e C, estão atualmente em desenvolvimento.
Algumas vacinas de DNA já estão em uso. Em 2005, uma vacina de DNA contra o vírus do Nilo Ocidental foi aprovada para uso em cavalos nos Estados Unidos. O Canadá também aprovou uma vacina de DNA para proteger os peixes do vírus da necrose hematopoiética infecciosa. 4 Uma vacina de DNA contra o vírus da encefalite japonesa foi aprovada para uso em humanos em 2010 na Austrália.
Foco clínico: Resolução
Com base nos sintomas de Olivia, seu médico fez um diagnóstico preliminar de meningite bacteriana sem esperar pela identificação positiva das amostras de sangue e LCR enviadas ao laboratório. Olivia foi internada no hospital e tratada com antibióticos intravenosos de amplo espectro e terapia de reidratação. Nos dias seguintes, sua condição começou a melhorar, e novas amostras de sangue e amostras de punção lombar mostraram ausência de micróbios no sangue e no líquido cefalorraquidiano, com níveis de glóbulos brancos voltando ao normal. Durante esse período, o laboratório produziu uma identificação positiva de Neisseria meningitidis, o agente causador da meningite meningocócica, em sua amostra original de LCR.
N. meningitidis produz uma cápsula de polissacarídeo que serve como fator de virulência. N. meningitidis tende a afetar bebês depois que eles começam a perder a imunidade passiva natural fornecida pelos anticorpos maternos. Com um ano de idade, os anticorpos IgG maternos de Olivia teriam desaparecido e ela não teria desenvolvido células de memória capazes de reconhecer antígenos associados à cápsula polissacarídica do N. meningitidis. Como resultado, seu sistema imunológico adaptativo foi incapaz de produzir anticorpos protetores para combater a infecção e, sem antibióticos, ela pode não ter sobrevivido. A infecção de Olivia provavelmente teria sido completamente evitada se ela tivesse sido vacinada. Uma vacina conjugada para prevenir a meningite meningocócica está disponível e aprovada para bebês a partir dos dois meses de idade. No entanto, os esquemas de vacinação atuais nos Estados Unidos recomendam que a vacina seja administrada aos 11 a 12 anos com um reforço aos 16 anos.
Em países com sistemas de saúde pública desenvolvidos, muitas vacinas são administradas rotineiramente a crianças e adultos. Os cronogramas de vacinas são alterados periodicamente, com base em novas informações e resultados de pesquisas coletados pelas agências de saúde pública. Nos Estados Unidos, o CDC publica cronogramas e outras informações atualizadas sobre vacinas.
Conceitos principais e resumo
- A imunidade adaptativa pode ser dividida em quatro classificações distintas: imunidade ativa natural, imunidade passiva natural, imunidade passiva artificial e imunidade ativa artificial.
- A imunidade ativa artificial é a base para a vacinação e o desenvolvimento de vacinas. Os programas de vacinação não apenas conferem imunidade artificial aos indivíduos, mas também promovem a imunidade de rebanho nas populações.
- A variolação contra a varíola teve origem no século 10 na China, mas o procedimento era arriscado porque poderia causar a doença que pretendia prevenir. A vacinação moderna foi desenvolvida por Edward Jenner, que desenvolveu a prática de inocular pacientes com materiais infecciosos de lesões de varíola bovina para prevenir a varíola.
- As vacinas vivas atenuadas e inativadas contêm patógenos inteiros que são fracos, mortos ou inativados. Vacinas de subunidades, vacinas contra toxóides e vacinas conjugadas contêm componentes acelulares com antígenos que estimulam uma resposta imune.
Notas de pé
- 1 K. Mupapa, M. Massamba, K. Kibadi, Kivula, A. Bwaka, M. Kipasa, R. Colebunders, J. J. Muyembe-Tamfum. “Tratamento da febre hemorrágica do Ebola com transfusões de sangue de pacientes convalescentes”. Jornal de Doenças Infecciosas 179 Suppl. (1999): S18—S23.
- 2 Elizabeth Yale. “Por que os movimentos antivacinação nunca podem ser domesticados.” Religion & Politics, 22 de julho de 2014. religionandpolitics.org/2014/... never be domed.
- 3 N. J. Willis. “Edward Jenner e a erradicação da varíola.” Jornal Médico Escocês 42 (1997): 118—121.
- 4 M. Alonso e J. C. Leong. “Vacinas de DNA licenciadas contra o vírus da necrose hematopoiética infecciosa (IHNV).” Patentes recentes sobre sequências de DNA e genes (descontinuadas) 7 no. 1 (2013): 62—65, issn 1872-2156/2212-3431. doi 10.2174/1872215611307010009.
- 5 S.B. Halstead e S. J. Thomas. “Novas vacinas contra encefalite japonesa: alternativas à produção no cérebro de camundongos.” Análise especializada de vacinas 10 no. 3 (2011): 355—64.


