13.1: Controlando o crescimento microbiano
- Page ID
- 181129
Objetivos de
- Compare desinfetantes, antissépticos e esterilizantes
- Descreva os princípios de controle da presença de microrganismos por meio de esterilização e desinfecção
- Diferencie entre microrganismos de vários níveis de segurança biológica e explique os métodos usados para lidar com micróbios em cada nível
Foco clínico: Parte 1
Roberta é uma corretora imobiliária de 46 anos que foi submetida recentemente a uma colecistectomia (cirurgia para remover cálculos biliares dolorosos). A cirurgia foi realizada de forma laparoscópica com o auxílio de um duodenoscópio, um endoscópio especializado que permite aos cirurgiões enxergar o interior do corpo com o auxílio de uma pequena câmera. Ao voltar para casa do hospital, Roberta desenvolveu dor abdominal e febre alta. Ela também sentiu uma sensação de queimação ao urinar e notou sangue na urina. Ela notificou seu cirurgião sobre esses sintomas, de acordo com suas instruções pós-operatórias.
Exercício\(\PageIndex{1}\)
Quais são algumas das possíveis causas dos sintomas de Roberta?
Para evitar a propagação de doenças humanas, é necessário controlar o crescimento e a abundância de micróbios em ou sobre vários itens frequentemente usados por humanos. Itens inanimados, como maçanetas, brinquedos ou toalhas, que podem abrigar micróbios e ajudar na transmissão de doenças, são chamados de fômites. Dois fatores influenciam fortemente o nível de limpeza necessário para um determinado fômito e, portanto, o protocolo escolhido para atingir esse nível. O primeiro fator é a aplicação para a qual o item será usado. Por exemplo, aplicações invasivas que exigem inserção no corpo humano exigem um nível de limpeza muito maior do que aplicações que não exigem. O segundo fator é o nível de resistência ao tratamento antimicrobiano por possíveis patógenos. Por exemplo, alimentos conservados em conservas geralmente ficam contaminados com a bactéria Clostridium botulinum, que produz a neurotoxina que causa o botulismo. Como a C. botulinum pode produzir endosporos capazes de sobreviver a condições adversas, temperaturas e pressões extremas devem ser usadas para eliminar os endosporos. Outros organismos podem não exigir medidas tão extremas e podem ser controlados por um procedimento, como lavar roupas em uma lavadora de roupas.
Níveis de segurança biológica de
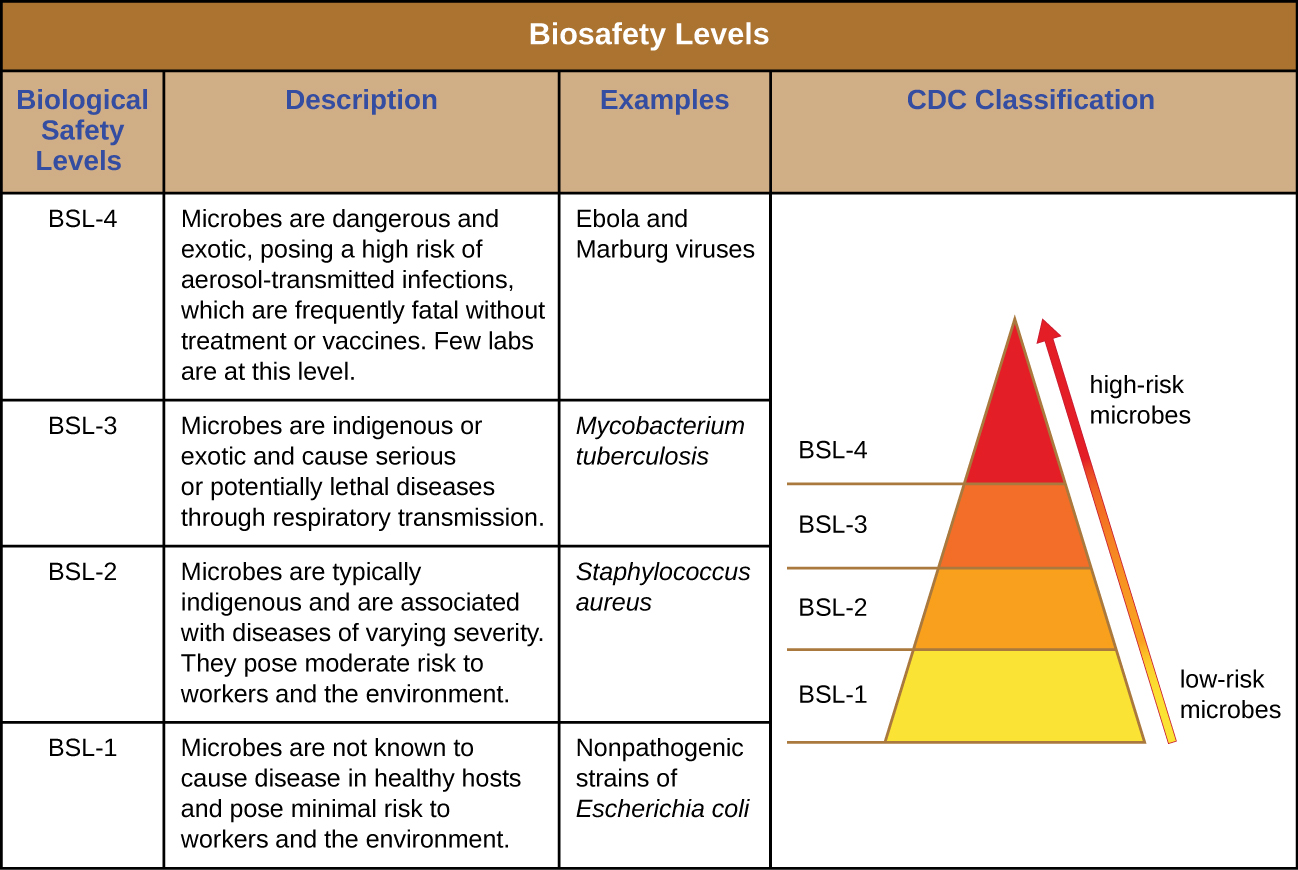
Para pesquisadores ou funcionários de laboratório que trabalham com patógenos, os riscos associados a patógenos específicos determinam os níveis de limpeza e controle necessários. Os Centros de Controle e Prevenção de Doenças (CDC) e os Institutos Nacionais de Saúde (NIH) estabeleceram quatro níveis de classificação, chamados de “níveis de segurança biológica” (BSLs). Várias organizações em todo o mundo, incluindo a Organização Mundial da Saúde (OMS) e a União Europeia (UE), usam um esquema de classificação semelhante. De acordo com o CDC, o BSL é determinado pela infectividade do agente, facilidade de transmissão e potencial gravidade da doença, bem como pelo tipo de trabalho que está sendo realizado com o agente. 1
Cada BSL requer um nível diferente de biocontenção para evitar a contaminação e a disseminação de agentes infecciosos para o pessoal do laboratório e, finalmente, para a comunidade. Por exemplo, o BSL mais baixo, o BSL-1, requer o menor número de precauções porque se aplica a situações com o menor risco de infecção microbiana.
Os agentes BSL-1 são aqueles que geralmente não causam infecção em adultos humanos saudáveis. Isso inclui bactérias não infecciosas, como cepas não patogênicas de Escherichia coli e Bacillus subtilis, e vírus conhecidos por infectar animais que não sejam humanos, como baculovírus (vírus de insetos). Como trabalhar com agentes BSL-1 representa muito pouco risco, poucas precauções são necessárias. Os trabalhadores do laboratório usam a técnica asséptica padrão e podem trabalhar com esses agentes em uma bancada ou mesa de laboratório aberta, usando equipamento de proteção individual (EPI), como jaleco, óculos e luvas, conforme necessário. Além de uma pia para lavar as mãos e portas para separar o laboratório do resto do prédio, nenhuma modificação adicional é necessária.
Os agentes classificados como BSL-2 incluem aqueles que representam risco moderado para os trabalhadores do laboratório e para a comunidade, e são tipicamente “indígenas”, o que significa que são comumente encontrados nessa área geográfica. Isso inclui bactérias como Staphylococcus aureus e Salmonella spp., e vírus como hepatite, caxumba e vírus do sarampo. Os laboratórios da BSL-2 exigem precauções adicionais além das da BSL-1, incluindo acesso restrito; EPI necessários, incluindo um protetor facial em algumas circunstâncias; e o uso de gabinetes de segurança biológica para procedimentos que podem dispersar agentes pelo ar (chamados de “aerossolização”). Os laboratórios BSL-2 são equipados com portas de fechamento automático, uma estação de lavagem de olhos e uma autoclave, que é um dispositivo especializado para esterilizar materiais com vapor pressurizado antes do uso ou descarte. Os laboratórios BSL-1 também podem ter uma autoclave.
Os agentes BSL-3 têm o potencial de causar infecções letais por inalação. Eles podem ser indígenas ou “exóticos”, o que significa que são derivados de um local estrangeiro e incluem patógenos como Mycobacterium tuberculosis, Bacillus anthracis, vírus do Nilo Ocidental e vírus da imunodeficiência humana (HIV). Devido à natureza grave das infecções causadas pelos agentes BSL-3, os laboratórios que trabalham com eles exigem acesso restrito. Os trabalhadores do laboratório estão sob vigilância médica, possivelmente recebendo vacinas para os micróbios com os quais trabalham. Além do EPI padrão já mencionado, o pessoal do laboratório nos laboratórios BSL-3 também deve usar um respirador e trabalhar com micróbios e agentes infecciosos em um gabinete de segurança biológica o tempo todo. Os laboratórios BSL-3 exigem uma pia sem usar as mãos, uma estação de lavagem de olhos perto da saída e dois conjuntos de portas com fecho automático e trava na entrada. Esses laboratórios são equipados com fluxo de ar direcional, o que significa que o ar limpo é puxado pelo laboratório de áreas limpas para áreas potencialmente contaminadas. Esse ar não pode ser recirculado, portanto, é necessário um suprimento constante de ar limpo.
Os agentes BSL-4 são os mais perigosos e muitas vezes fatais. Esses micróbios são tipicamente exóticos, são facilmente transmitidos por inalação e causam infecções para as quais não há tratamentos ou vacinas. Os exemplos incluem o vírus Ebola e o vírus Marburg, ambos causadores de febre hemorrágica, e o vírus da varíola. Há apenas um pequeno número de laboratórios nos Estados Unidos e em todo o mundo devidamente equipados para trabalhar com esses agentes. Além das precauções da BSL-3, os trabalhadores de laboratório nas instalações da BSL-4 também devem trocar de roupa ao entrar no laboratório, tomar banho ao sair e descontaminar todo o material ao sair. Enquanto trabalham no laboratório, eles devem usar um traje de proteção de corpo inteiro com um suprimento de ar designado ou realizar todo o trabalho dentro de um gabinete de segurança biológica com um suprimento de ar particulado de alta eficiência (HEPA) e um escapamento duplamente filtrado por HEPA. Se estiver usando um traje, a pressão do ar dentro do traje deve ser maior do que a do lado de fora do traje, de modo que, se ocorrer um vazamento no traje, o ar do laboratório que possa estar contaminado não possa ser aspirado para dentro do traje (Figura\(\PageIndex{1}\)). O laboratório em si deve estar localizado em um prédio separado ou em uma parte isolada de um prédio e ter seu próprio sistema de suprimento de ar e exaustão, bem como seu próprio sistema de descontaminação. Os BSLs estão resumidos na Figura\(\PageIndex{2}\).

Para saber mais sobre os quatro BSLs, visite o site do CDC.
Exercício\(\PageIndex{2}\)
Quais são alguns fatores usados para determinar o BSL necessário para trabalhar com um patógeno específico?
Esterilização
Os protocolos mais extremos de controle microbiano visam alcançar a esterilização: a remoção completa ou eliminação de todas as células vegetativas, endosporos e vírus do item ou ambiente alvo. Os protocolos de esterilização geralmente são reservados para ambientes laboratoriais, médicos, de manufatura e da indústria alimentícia, onde pode ser imperativo que certos itens estejam completamente livres de agentes potencialmente infecciosos. A esterilização pode ser realizada por meios físicos, como exposição a altas temperaturas, pressão ou filtração por meio de um filtro apropriado, ou por meios químicos. Os produtos químicos que podem ser usados para obter a esterilização são chamados de esterilizantes. Os esterilizantes matam efetivamente todos os micróbios e vírus e, com o tempo de exposição adequado, também podem matar os endosporos.
Para muitos propósitos clínicos, a técnica asséptica é necessária para evitar a contaminação de superfícies estéreis. A técnica asséptica envolve uma combinação de protocolos que mantêm coletivamente a esterilidade, ou assepsia, evitando assim a contaminação do paciente com micróbios e agentes infecciosos. A falha na prática da técnica asséptica durante muitos tipos de procedimentos clínicos pode introduzir micróbios no corpo do paciente e colocá-lo em risco de sepse, uma resposta inflamatória sistêmica a uma infecção que resulta em febre alta, aumento da frequência cardíaca e respiratória, choque e, possivelmente, morte. Os procedimentos médicos que apresentam risco de contaminação devem ser realizados em um campo estéril, uma área designada que é mantida livre de todos os micróbios vegetativos, endosporos e vírus. Os campos estéreis são criados de acordo com protocolos que exigem o uso de materiais esterilizados, como embalagens e cortinas, e procedimentos rigorosos de lavagem e aplicação de esterilizantes. Outros protocolos são seguidos para manter o campo estéril enquanto o procedimento médico está sendo realizado.
Um protocolo de esterilização de alimentos, a esterilização comercial, usa calor a uma temperatura baixa o suficiente para preservar a qualidade dos alimentos, mas alta o suficiente para destruir patógenos comuns responsáveis por intoxicações alimentares, como C. botulinum. Como C. botulinum e seus endosporos são comumente encontrados no solo, eles podem facilmente contaminar as plantações durante a colheita, e esses endosporos podem germinar posteriormente no ambiente anaeróbico quando os alimentos são enlatados. Latas de metal com alimentos contaminados com C. botulinum ficarão inchadas devido à produção de gases pelo micróbio; frascos de alimentos contaminados normalmente incham na tampa de metal. Para eliminar o risco de contaminação por C. botulinum, os protocolos comerciais de enlatamento de alimentos são projetados com uma grande margem de erro. Eles assumem uma população incrivelmente grande de endosporos (10 12 por lata) e visam reduzir essa população para 1 endosporo por lata para garantir a segurança dos alimentos enlatados. Por exemplo, alimentos com baixa e média acidez são aquecidos a 121 °C por um mínimo de 2,52 minutos, que é o tempo necessário para reduzir uma população de 10 12 endosporos por lata para 1 endosporo nessa temperatura. Mesmo assim, a esterilização comercial não elimina a presença de todos os micróbios; em vez disso, ela tem como alvo os patógenos que causam deterioração e doenças transmitidas por alimentos, ao mesmo tempo em que permite que muitos organismos não patogênicos sobrevivam. Portanto, “esterilização” é um pouco impróprio nesse contexto, e a esterilização comercial pode ser descrita com mais precisão como “quase esterilização”.
Exercício\(\PageIndex{3}\)
Qual a diferença entre esterilização e técnica asséptica?
A Association of Surgical Technologists publica padrões para técnicas assépticas, incluindo a criação e manutenção de um campo estéril.
Outros métodos de controle
Os protocolos de esterilização exigem procedimentos que não são práticos ou necessários em muitos ambientes. Vários outros métodos são usados em ambientes clínicos e não clínicos para reduzir a carga microbiana nos itens. Embora os termos para esses métodos sejam frequentemente usados de forma intercambiável, existem distinções importantes (Figura\(\PageIndex{3}\)).
O processo de desinfecção inativa a maioria dos micróbios na superfície de uma fômite usando produtos químicos antimicrobianos ou calor. Como alguns micróbios permanecem, o item desinfetado não é considerado estéril. Idealmente, os desinfetantes devem ser de ação rápida, estáveis, fáceis de preparar, baratos e fáceis de usar. Um exemplo de desinfetante natural é o vinagre; sua acidez mata a maioria dos micróbios. Desinfetantes químicos, como alvejante à base de cloro ou produtos que contêm cloro, são usados para limpar superfícies não vivas, como bancos de laboratório, superfícies clínicas e pias de banheiro. A desinfecção típica não leva à esterilização porque os endosporos tendem a sobreviver mesmo quando todas as células vegetativas foram mortas.
Ao contrário dos desinfetantes, os antissépticos são produtos químicos antimicrobianos seguros para uso em pele ou tecidos vivos. Exemplos de antissépticos incluem peróxido de hidrogênio e álcool isopropílico. O processo de aplicação de um antisséptico é chamado de antissepsia. Além das características de um bom desinfetante, os antissépticos também devem ser seletivamente eficazes contra microrganismos e capazes de penetrar profundamente no tecido sem causar danos aos tecidos.
O tipo de protocolo necessário para atingir o nível de limpeza desejado depende do item específico a ser limpo. Por exemplo, aqueles usados clinicamente são categorizados como críticos, semicríticos e não críticos. Os itens essenciais devem ser estéreis porque serão usados dentro do corpo, geralmente penetrando nos tecidos estéreis ou na corrente sanguínea; exemplos de itens críticos incluem instrumentos cirúrgicos, cateteres e fluidos intravenosos. Endoscópios gastrointestinais e vários tipos de equipamentos para terapia respiratória são exemplos de itens semicríticos; eles podem entrar em contato com membranas mucosas ou com a pele não intacta, mas não penetram nos tecidos. Itens semicríticos normalmente não precisam ser esterilizados, mas requerem um alto nível de desinfecção. Itens que podem entrar em contato, mas não penetrar na pele intacta, são itens não críticos; exemplos são roupas de cama, móveis, muletas, estetoscópios e manguitos de pressão arterial. Esses artigos precisam estar limpos, mas não altamente desinfetados.
O ato de lavar as mãos é um exemplo de degermação, em que os números microbianos são significativamente reduzidos esfregando suavemente os tecidos vivos, mais comumente a pele, com uma substância química leve (por exemplo, sabão) para evitar a transmissão de micróbios patogênicos. Limpar a pele com uma compressa embebida em álcool no local da injeção é outro exemplo de degerminação. Esses métodos de degerminação removem a maioria (mas não todos) dos micróbios da superfície da pele.
O termo higienização se refere à limpeza de fômites para remover micróbios suficientes para atingir níveis considerados seguros para a saúde pública. Por exemplo, as máquinas de lavar louça comerciais usadas na indústria de food service geralmente usam água e ar muito quentes para lavar e secar; as altas temperaturas matam a maioria dos micróbios, higienizando a louça. As superfícies dos quartos dos hospitais são geralmente higienizadas usando um desinfetante químico para evitar a transmissão de doenças entre pacientes. A figura\(\PageIndex{3}\) resume protocolos, definições, aplicações e agentes comuns usados para controlar o crescimento microbiano.

Exercício\(\PageIndex{4}\)
- Qual a diferença entre um desinfetante e um antisséptico?
- O que é mais eficaz na remoção de micróbios de um produto: higienização, degerminação ou esterilização? Explique.
Foco clínico: Parte 2
O médico de Roberta suspeitou que uma infecção bacteriana fosse responsável por seu início repentino de febre alta, dor abdominal e urina com sangue. Com base nesses sintomas, o médico diagnosticou uma infecção do trato urinário (ITU). Uma grande variedade de bactérias pode causar ITUs, que normalmente ocorrem quando bactérias do trato gastrointestinal inferior são introduzidas no trato urinário. No entanto, a recente cirurgia de cálculos biliares de Roberta fez com que o médico suspeitasse que ela havia contraído uma infecção hospitalar (adquirida no hospital) durante a cirurgia. O médico coletou uma amostra de urina e solicitou uma cultura de urina para verificar a presença de glóbulos brancos, glóbulos vermelhos e bactérias. Os resultados desse teste ajudariam a determinar a causa da infecção. O médico também prescreveu um tratamento com o antibiótico ciprofloxacina, confiante de que isso eliminaria a infecção de Roberta.
Exercício\(\PageIndex{5}\)
Quais são algumas das possíveis maneiras pelas quais bactérias poderiam ter sido introduzidas no trato urinário de Roberta durante sua cirurgia?
Medindo o controle microbiano
Os métodos físicos e químicos de controle microbiano que matam o microrganismo alvo são identificados pelo sufixo -cide (ou -cida). O prefixo indica o tipo de micróbio ou agente infeccioso morto pelo método de tratamento: bactericidas matam bactérias, viricidas matam ou inativam vírus e fungicidas matam fungos. Outros métodos não matam organismos, mas, em vez disso, impedem seu crescimento, tornando sua população estática; esses métodos são identificados pelo sufixo -stat (ou -static). Por exemplo, os tratamentos bacteriostáticos inibem o crescimento de bactérias, enquanto os tratamentos fungistáticos inibem o crescimento de fungos. Os fatores que determinam se um tratamento específico é -cida ou estático incluem os tipos de microrganismos visados, a concentração do produto químico usado e a natureza do tratamento aplicado.
Embora os tratamentos estáticos não matem realmente agentes infecciosos, eles geralmente são menos tóxicos para humanos e outros animais e também podem preservar melhor a integridade do item tratado. Esses tratamentos geralmente são suficientes para manter a população microbiana de um item sob controle. A toxicidade reduzida de alguns desses produtos químicos estáticos também permite que eles sejam impregnados com segurança em plásticos para evitar o crescimento de micróbios nessas superfícies. Esses plásticos são usados em produtos como brinquedos para crianças e tábuas de corte para preparação de alimentos. Quando usados para tratar uma infecção, os tratamentos estáticos geralmente são suficientes em um indivíduo saudável, impedindo que o patógeno se multiplique, permitindo que o sistema imunológico do indivíduo elimine a infecção.
O grau de controle microbiano pode ser avaliado usando uma curva de morte microbiana para descrever o progresso e a eficácia de um protocolo específico. Quando exposto a um protocolo específico de controle microbiano, uma porcentagem fixa dos micróbios da população morrerá. Como a taxa de morte permanece constante mesmo quando o tamanho da população varia, a porcentagem de mortos é uma informação mais útil do que o número absoluto de micróbios mortos. As curvas de morte são frequentemente traçadas como gráficos de semilog, assim como as curvas de crescimento microbiano, porque a redução de microrganismos é tipicamente logarítmica (Figura\(\PageIndex{4}\)). A quantidade de tempo que um protocolo específico leva para produzir uma diminuição de uma ordem de magnitude no número de organismos, ou a morte de 90% da população, é chamada de tempo de redução decimal (DRT) ou valor D.
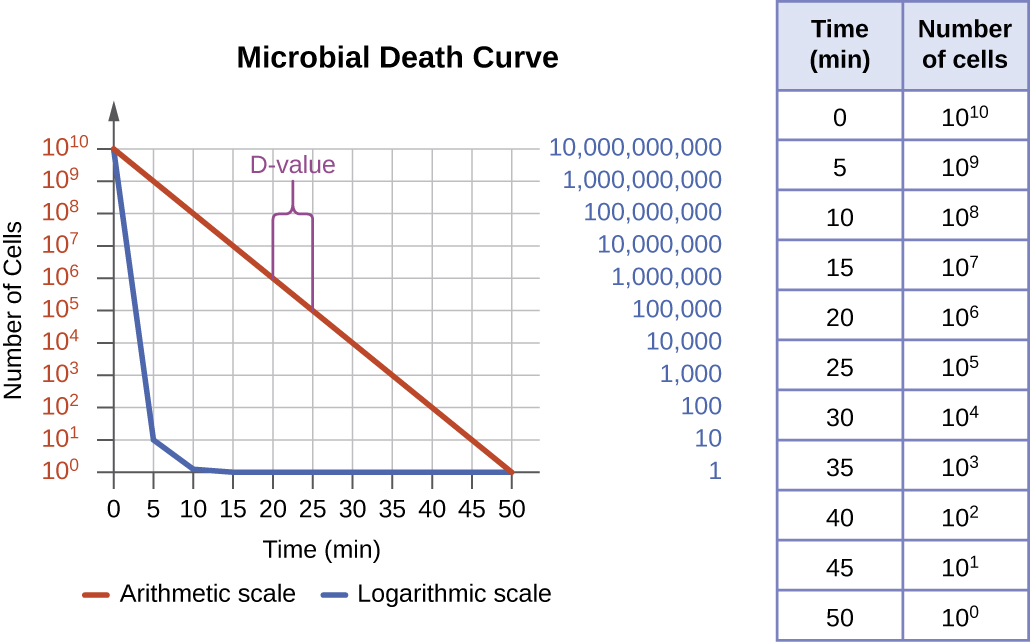
Vários fatores contribuem para a eficácia de um agente desinfetante ou protocolo de controle microbiano. Primeiro, conforme demonstrado na Figura\(\PageIndex{4}\), o tempo de exposição é importante. Tempos de exposição mais longos matam mais micróbios. Como a morte microbiana de uma população exposta a um protocolo específico é logarítmica, leva mais tempo para eliminar uma carga populacional alta do que uma carga populacional baixa exposta ao mesmo protocolo. É necessário um tempo de tratamento mais curto (medido em múltiplos do valor D) ao iniciar com um número menor de organismos. A eficácia também depende da suscetibilidade do agente a esse agente ou protocolo desinfetante. A concentração do agente desinfetante ou a intensidade da exposição também são importantes. Por exemplo, temperaturas mais altas e concentrações mais altas de desinfetantes matam micróbios de forma mais rápida e eficaz. Condições que limitam o contato entre o agente e as células-alvo — por exemplo, a presença de fluidos corporais, tecidos, detritos orgânicos (por exemplo, lama ou fezes) ou biofilmes nas superfícies — aumentam o tempo de limpeza ou a intensidade do protocolo de controle microbiano necessário para alcançar o nível de limpeza desejado . Todos esses fatores devem ser considerados ao escolher o protocolo apropriado para controlar o crescimento microbiano em uma determinada situação.
Exercício\(\PageIndex{6}\)
- Quais são as duas razões possíveis para escolher um tratamento bacteriostático em vez de um bactericida?
- Cite pelo menos dois fatores que podem comprometer a eficácia de um agente desinfetante.
Conceitos principais e resumo
- Itens inanimados que podem abrigar micróbios e auxiliar em sua transmissão são chamados de fômites. O nível de limpeza necessário para uma fômite depende tanto do uso do item quanto do agente infeccioso com o qual o item pode estar contaminado.
- O CDC e o NIH estabeleceram quatro níveis de segurança biológica (BSLs) para laboratórios que realizam pesquisas sobre agentes infecciosos. Cada nível é projetado para proteger o pessoal do laboratório e a comunidade. Esses BSLs são determinados pela infectividade do agente, facilidade de transmissão e potencial gravidade da doença, bem como pelo tipo de trabalho que está sendo realizado com o agente.
- A desinfecção remove possíveis patógenos de um fômite, enquanto a antissepsia usa produtos químicos antimicrobianos seguros o suficiente para os tecidos; em ambos os casos, a carga microbiana é reduzida, mas os micróbios podem permanecer, a menos que o produto químico usado seja forte o suficiente para ser um esterilizante.
- A quantidade de limpeza (esterilização versus desinfecção de alto nível versus limpeza geral) necessária para itens usados clinicamente depende se o item entrará em contato com tecidos estéreis (item crítico), membranas mucosas (item semicrítico) ou intacto pele (item não crítico).
- Procedimentos médicos com risco de contaminação devem ser realizados em um campo estéril mantido por técnica asséptica adequada para prevenir a sepse.
- A esterilização é necessária para algumas aplicações médicas, bem como na indústria alimentícia, onde os endosporos de Clostridium botulinum são eliminados por meio de protocolos comerciais de esterilização.
- Os métodos físicos ou químicos para controlar o crescimento microbiano que resultam na morte do micróbio são indicados pelos sufixos -cida ou -cida (por exemplo, como com bactericidas, viricidas e fungicidas), enquanto aqueles que inibem o crescimento microbiano são indicado pelos sufixos -stat ou -static (por exemplo, bacteriostático, fungistático).
- As curvas de morte microbiana mostram o declínio logarítmico de micróbios vivos expostos a um método de controle microbiano. O tempo necessário para que um protocolo produza uma redução de 1 log (90%) na população microbiana é o tempo de redução decimal, ou valor D.
- Ao escolher um protocolo de controle microbiano, os fatores a serem considerados incluem a duração do tempo de exposição, o tipo de micróbio alvo, sua suscetibilidade ao protocolo, a intensidade do tratamento, a presença de orgânicos que podem interferir no protocolo e as condições ambientais que podem alterar o eficácia do protocolo.
Notas de pé
- 1 Centros dos EUA para Controle e Prevenção de Doenças. “Reconhecendo os níveis de biossegurança”. http://www.cdc.gov/training/quicklearns/biosafety/. Acessado em 7 de junho de 2016.


