6.1: Vírus
- Page ID
- 181189
Objetivos de
- Descreva as características gerais dos vírus como patógenos
- Descreva genomas virais
- Descreva as características gerais dos ciclos de vida virais
- Diferencie entre bacteriófagos, vírus vegetais e vírus animais
- Descreva as características usadas para identificar vírus como parasitas intracelulares obrigatórios
Foco clínico: Parte 1
David, jornalista de 45 anos, acaba de voltar para os EUA de viagens pela Rússia, China e África. Ele não está se sentindo bem, então vai ao clínico geral reclamando de fraqueza nos braços e pernas, febre, dor de cabeça, agitação perceptível e pequeno desconforto. Ele acha que isso pode estar relacionado a uma mordida de cachorro que ele sofreu ao entrevistar um fazendeiro chinês. Ele está sentindo algumas sensações de formigamento e coceira no local da picada, mas diz ao médico que o cachorro parecia saudável e que ele não estava preocupado até agora. O médico solicitou um teste de cultura e sensibilidade para descartar a infecção bacteriana da ferida, e os resultados deram negativo para qualquer possível bactéria patogênica.
Exercício\(\PageIndex{1}\)
- Com base nessas informações, quais exames adicionais devem ser realizados no paciente?
- Que tipo de tratamento o médico deve recomendar?
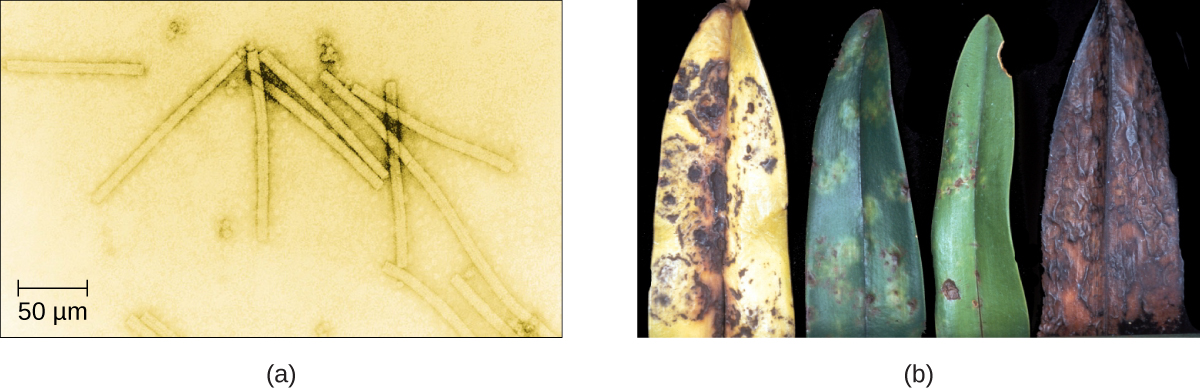
Apesar de seu tamanho pequeno, que os impedia de serem vistos com microscópios de luz, a descoberta de um componente filtrável menor do que uma bactéria que causa a doença do mosaico do tabaco (TMD) remonta a 1892. 1 Naquela época, Dmitri Ivanovski, um botânico russo, descobriu a origem da TMD usando um dispositivo de filtragem de porcelana inventado pela primeira vez por Charles Chamberland e Louis Pasteur em Paris em 1884. Os filtros Porcelain Chamberland têm um tamanho de poro de 0,1 µm, que é pequeno o suficiente para remover todas as bactérias ≥0,2 µm de qualquer líquido que passe pelo dispositivo. Um extrato obtido de plantas de tabaco infectadas com TMD foi feito para determinar a causa da doença. Inicialmente, acreditava-se que a origem da doença fosse bacteriana. Foi surpreendente para todos quando Ivanovski, usando um filtro Chamberland, descobriu que a causa da DTM não foi removida após passar o extrato pelo filtro de porcelana. Então, se uma bactéria não fosse a causa da DTM, o que poderia estar causando a doença? Ivanovski concluiu que a causa da DTM deve ser uma bactéria ou esporo bacteriano extremamente pequeno. Outros cientistas, incluindo Martinus Beijerinck, continuaram investigando a causa da DTM. Foi Beijerinck, em 1899, que finalmente concluiu que o agente causador não era uma bactéria, mas, em vez disso, possivelmente uma substância química, como um veneno biológico que descreveríamos hoje como uma toxina. Como resultado, a palavra vírus, em latim para veneno, foi usada para descrever a causa da DTM alguns anos após a descoberta inicial de Ivanovski. Embora não tenha conseguido ver o vírus que causou a DTM e não tenha percebido que a causa não era uma bactéria, Ivanovski é considerado o descobridor original dos vírus e fundador do campo da virologia.
Hoje, podemos ver vírus usando microscópios eletrônicos (Figura\(\PageIndex{1}\)) e sabemos muito mais sobre eles. Os vírus são entidades biológicas distintas; no entanto, sua origem evolutiva ainda é uma questão de especulação. Em termos de taxonomia, eles não estão incluídos na árvore da vida porque são acelulares (não consistem em células). Para sobreviver e se reproduzir, os vírus devem infectar um hospedeiro celular, tornando-os obrigatórios para parasitas intracelulares. O genoma de um vírus entra na célula hospedeira e direciona a produção dos componentes virais, proteínas e ácidos nucléicos, necessários para formar novas partículas virais chamadas viriões. Novos viriões são produzidos na célula hospedeira por meio da montagem de componentes virais. Os novos viriões transportam o genoma viral para outra célula hospedeira para realizar outra rodada de infecção. A tabela\(\PageIndex{1}\) resume as propriedades dos vírus.
| Características dos vírus |
|---|
| Patógenos infecciosos e acelulares |
| Parasitas intracelulares obrigatórios com especificidade do hospedeiro e do tipo celular |
| Genoma de DNA ou RNA (nunca ambos) |
| O genoma é cercado por um capsídeo proteico e, em alguns casos, uma membrana fosfolipídica repleta de glicoproteínas virais |
| Faltam genes para muitos produtos necessários para uma reprodução bem-sucedida, exigindo a exploração dos genomas da célula hospedeira para se reproduzir |
Exercício\(\PageIndex{2}\)
Por que o primeiro vírus investigado foi confundido com uma toxina?
Hospedeiros e transmissão viral
Os vírus podem infectar todos os tipos de células hospedeiras, incluindo plantas, animais, fungos, protistas, bactérias e arquéias. A maioria dos vírus só será capaz de infectar as células de uma ou algumas espécies de organismos. Isso é chamado de intervalo do host. No entanto, ter uma ampla variedade de hospedeiros não é comum e os vírus normalmente infectam apenas hospedeiros específicos e apenas tipos de células específicos dentro desses hospedeiros. Os vírus que infectam as bactérias são chamados de bacteriófagos, ou simplesmente fagos. A palavra fago vem da palavra grega para devorar. Outros vírus são apenas identificados pelo grupo hospedeiro, como vírus animais ou vegetais. Quando uma célula é infectada, os efeitos do vírus podem variar dependendo do tipo de vírus. Os vírus podem causar crescimento anormal da célula ou morte celular, alterar o genoma da célula ou causar pouco efeito perceptível na célula.
Os vírus podem ser transmitidos por contato direto, contato indireto com fômites ou por meio de um vetor: um animal que transmite um patógeno de um hospedeiro para outro. Artrópodes, como mosquitos, carrapatos e moscas, são vetores típicos de doenças virais e podem atuar como vetores mecânicos ou biológicos. A transmissão mecânica ocorre quando o artrópode carrega um patógeno viral na parte externa do corpo e o transmite para um novo hospedeiro por contato físico. A transmissão biológica ocorre quando o artrópode carrega o patógeno viral para dentro de seu corpo e o transmite ao novo hospedeiro por meio da picada.
Em humanos, uma grande variedade de vírus é capaz de causar várias infecções e doenças. Alguns dos patógenos emergentes mais mortais em humanos são os vírus, mas temos poucos tratamentos ou medicamentos para lidar com infecções virais, dificultando sua erradicação.
Vírus que podem ser transmitidos de um hospedeiro animal para um hospedeiro humano podem causar zoonoses. Por exemplo, o vírus da gripe aviária tem origem em aves, mas pode causar doenças em humanos. As zoonoses reversas são causadas pela infecção de um animal por um vírus que se originou em um ser humano.
Combatendo bactérias com vírus
O surgimento de superbactérias, ou bactérias multirresistentes, tornou-se um grande desafio para as empresas farmacêuticas e um sério problema de saúde. De acordo com um relatório de 2013 do Centro de Controle e Prevenção de Doenças (CDC) dos EUA, mais de 2 milhões de pessoas são infectadas com bactérias resistentes a medicamentos nos EUA anualmente, resultando em pelo menos 23.000 mortes. 2 O uso contínuo e o uso excessivo de antibióticos provavelmente levarão à evolução de cepas ainda mais resistentes aos medicamentos.
Uma solução potencial é o uso da terapia com fagos, um procedimento que usa vírus que matam bactérias (bacteriófagos) para tratar infecções bacterianas. A terapia fágica não é uma ideia nova. A descoberta dos bacteriófagos remonta ao início do século XX, e a terapia com fagos foi usada pela primeira vez na Europa em 1915 pelo bacteriologista inglês Frederick Twort. 3 No entanto, a descoberta subsequente da penicilina e de outros antibióticos levou ao quase abandono dessa forma de terapia, exceto na antiga União Soviética e em alguns países da Europa Oriental. O interesse pela fagoterapia fora dos países da antiga União Soviética só recentemente ressurgiu devido ao aumento de bactérias resistentes a antibióticos. 4
A fagoterapia tem algumas vantagens sobre os antibióticos, pois os fagos matam apenas uma bactéria específica, enquanto os antibióticos matam não apenas o patógeno, mas também as bactérias benéficas da microbiota normal. O desenvolvimento de novos antibióticos também é caro para empresas farmacêuticas e pacientes, especialmente para aqueles que vivem em países com altas taxas de pobreza.
Os fagos também têm sido usados para evitar a deterioração dos alimentos. Em 2006, a Food and Drug Administration dos EUA aprovou o uso de uma solução contendo seis bacteriófagos que podem ser pulverizados em carnes de almoço, como mortadela, presunto e perú, para matar a Listeria monocytogenes, uma bactéria responsável pela listeriose, uma forma de intoxicação alimentar. No entanto, alguns consumidores se preocupam com o uso de fagos em alimentos, especialmente devido à crescente popularidade dos produtos orgânicos. Os alimentos que foram tratados com fagos devem declarar “preparação de bacteriófagos” na lista de ingredientes ou incluir um rótulo declarando que a carne foi “tratada com solução antimicrobiana para reduzir microorganismos”. 5
Exercício\(\PageIndex{3}\)
- Por que os humanos não precisam se preocupar com a presença de bacteriófagos em seus alimentos?
- Quais são as três maneiras pelas quais os vírus podem ser transmitidos entre hospedeiros?
Estruturas virais
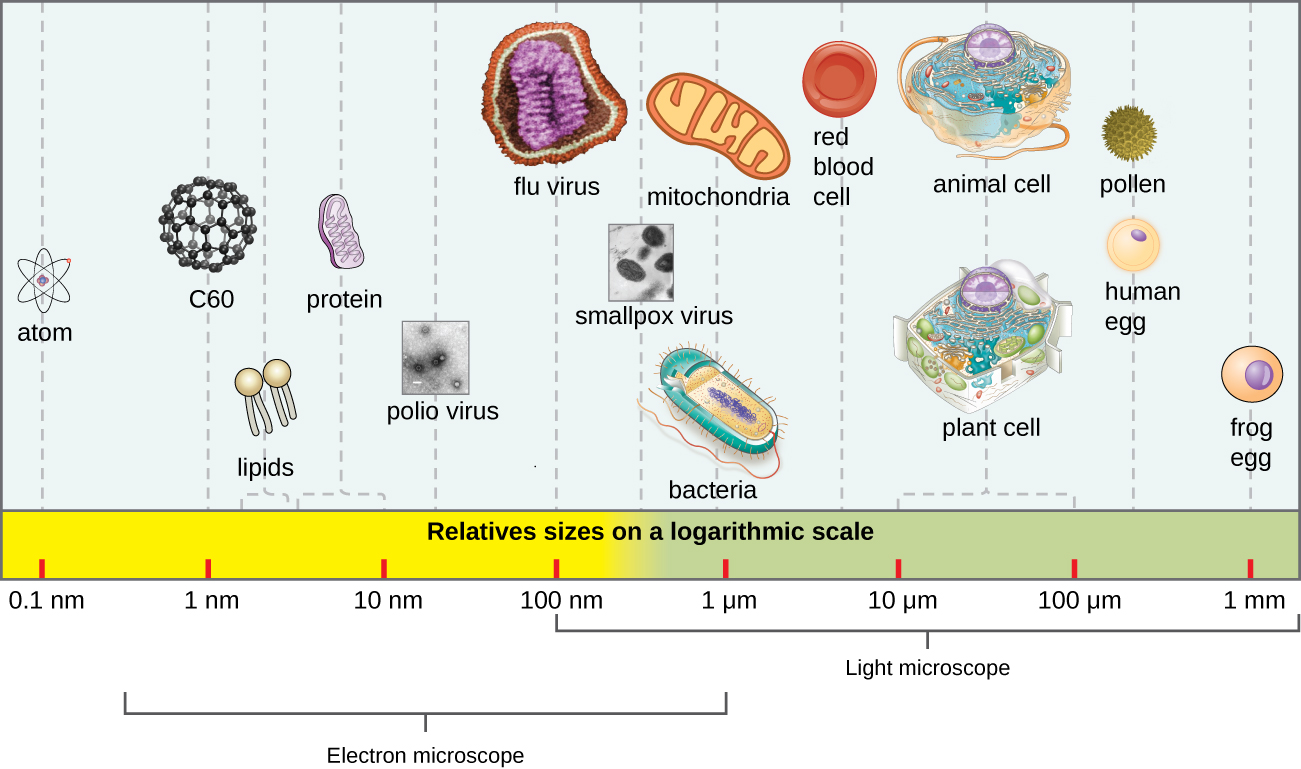
Em geral, os viriões (partículas virais) são pequenos e não podem ser observados usando um microscópio de luz comum. Eles são muito menores do que as células procarióticas e eucarióticas; essa é uma adaptação que permite que os vírus infectem essas células maiores (veja a Figura\(\PageIndex{2}\)). O tamanho de um virião pode variar de 20 nm para vírus pequenos até 900 nm para vírus grandes e típicos (veja a Figura\(\PageIndex{3}\)). Descobertas recentes, no entanto, identificaram novas espécies virais gigantes, como Pandoravirus salinus e Pithovirus sibericum, com tamanhos próximos aos de uma célula bacteriana. 6

Em 1935, após o desenvolvimento do microscópio eletrônico, Wendell Stanley foi o primeiro cientista a cristalizar a estrutura do vírus do mosaico do tabaco e descobriu que ele é composto de RNA e proteína. Em 1943, ele isolou o vírus Influenza B, que contribuiu para o desenvolvimento de uma vacina contra influenza (gripe). As descobertas de Stanley revelaram o mistério da natureza dos vírus que intrigavam os cientistas há mais de 40 anos e suas contribuições ao campo da virologia o levaram a receber o Prêmio Nobel em 1946.
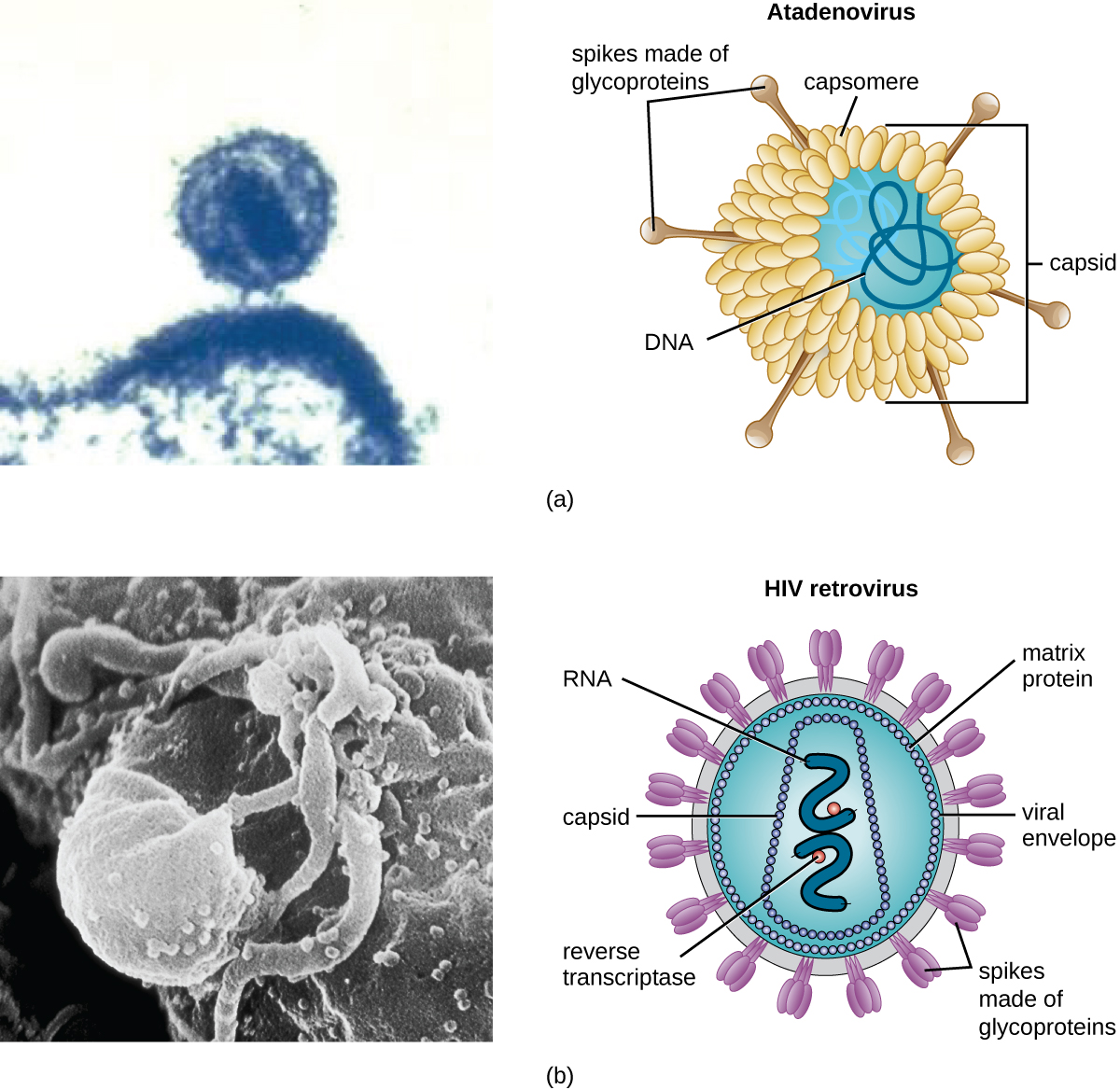
Como resultado de pesquisas contínuas sobre a natureza dos vírus, agora sabemos que eles consistem em um ácido nucléico (RNA ou DNA, mas nunca ambos) cercado por uma camada proteica chamada capsídeo (veja a Figura\(\PageIndex{4}\)). O interior do capsídeo não é preenchido com citosol, como em uma célula, mas contém as necessidades básicas em termos de genoma e enzimas necessárias para direcionar a síntese de novos viriões. Cada capsídeo é composto por subunidades proteicas chamadas capsómeros feitos de um ou mais tipos diferentes de proteínas capsômeros que se interligam para formar o capsídeo compactado.
Existem duas categorias de vírus com base na composição geral. Os vírus formados apenas por um ácido nucléico e um capsídeo são chamados de vírus nus ou vírus não envelopados. Os vírus formados com um capsídeo repleto de ácido nucleico cercado por uma camada lipídica são chamados de vírus envelopados (veja a Figura\(\PageIndex{4}\)). O envelope viral é uma pequena porção da membrana fosfolipídica obtida como gemas viriônicas de uma célula hospedeira. O envelope viral pode ser de origem intracelular ou citoplasmática.
Estendendo-se para fora e para longe do capsídeo em alguns vírus nus e vírus envelopados, existem estruturas proteicas chamadas espinhos. Nas pontas desses picos estão estruturas que permitem que o vírus se conecte e entre em uma célula, como os picos de hemaglutinina do vírus influenza (H) ou enzimas como os picos do vírus da influenza neuraminidase (N), que permitem que o vírus se separe da superfície celular durante a liberação de novos viriões. Os vírus da gripe são frequentemente identificados por seus picos de H e N. Por exemplo, os vírus da gripe H1N1 foram responsáveis pelas pandemias em 1918 e 2009, 7 H2N2 pela pandemia em 1957 e H3N2 pela pandemia em 1968.
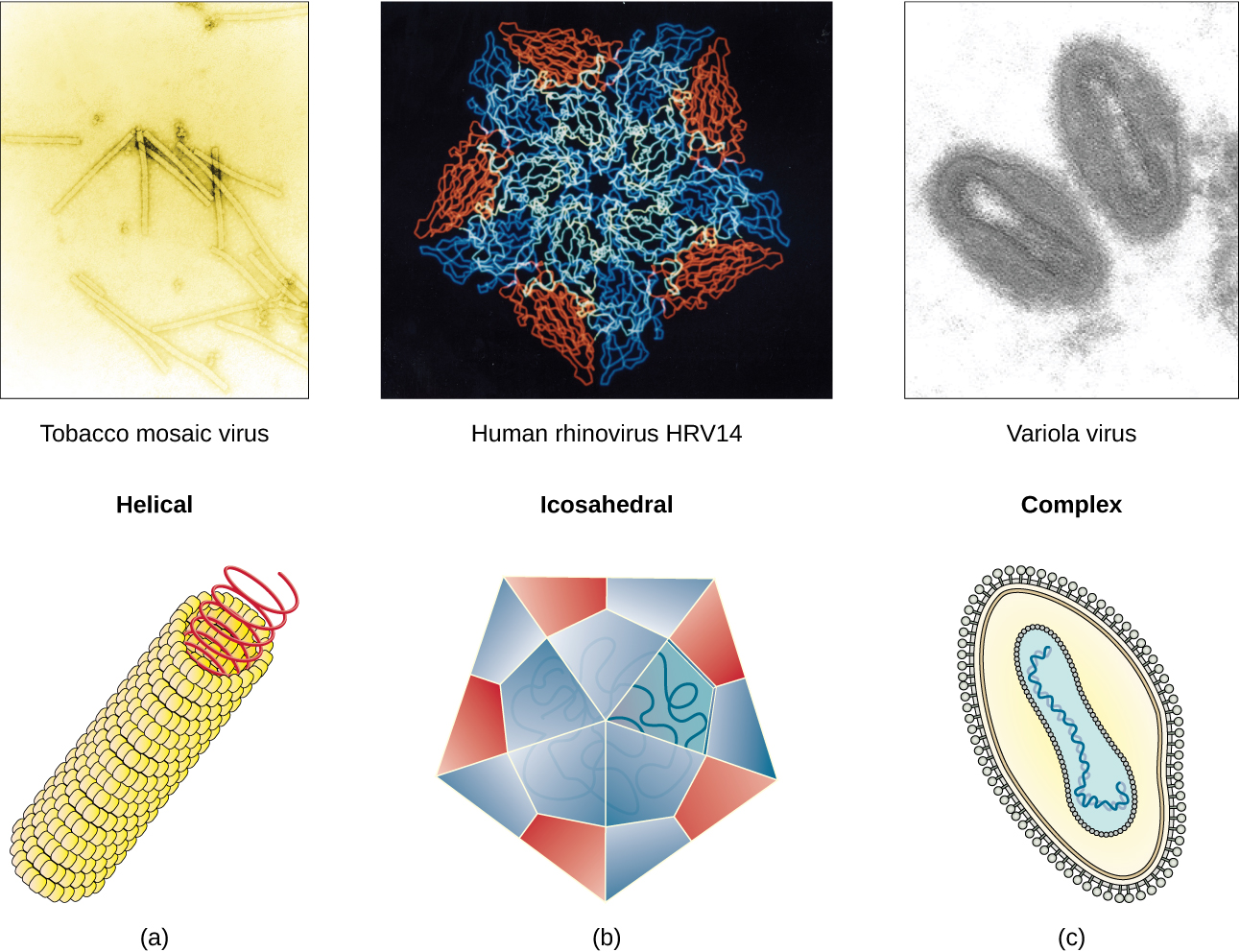
Os vírus variam na forma de seus capsídeos, que podem ser helicoidais, poliédricos ou complexos. Um capsídeo helicoidal forma o vírus do mosaico do tabaco (TMV), um vírus helicoidal nu, e o vírus Ebola, um vírus helicoidal envelopado. O capsídeo é cilíndrico ou em forma de bastonete, com o genoma encaixado dentro do comprimento do capsídeo. Os capsídeos poliédricos formam as formas do poliovírus e do rinovírus e consistem em um ácido nucléico cercado por um capsídeo poliédrico (de vários lados) na forma de um icosaedro. Um capsídeo icosaédrico é uma estrutura tridimensional de 20 lados com 12 vértices. Esses capsídeos lembram um pouco uma bola de futebol. Tanto os vírus helicoidais quanto os poliédricos podem ter envelopes. As formas virais observadas em certos tipos de bacteriófagos, como o fago T4 e os vírus da varíola, como o vírus da vacina, podem ter características de vírus poliédricos e helicoidais, por isso são descritas como uma forma viral complexa (veja a Figura\(\PageIndex{5}\)). Na forma do complexo bacteriófago, o genoma está localizado dentro da cabeça poliédrica e a bainha conecta a cabeça às fibras da cauda e aos pinos da cauda que ajudam o vírus a se conectar aos receptores na superfície da célula hospedeira. Os poxvírus que têm formas complexas geralmente são em forma de tijolo, com características de superfície intrincadas não vistas nas outras categorias de capsídeo.
Exercício\(\PageIndex{4}\)
Quais tipos de vírus têm picos?
Classificação e taxonomia de vírus
Embora os vírus não sejam classificados nos três domínios da vida, seus números são grandes o suficiente para exigir classificação. Desde 1971, a Divisão de Virologia da União Internacional das Sociedades Microbiológicas atribuiu a tarefa de desenvolver, refinar e manter uma taxonomia universal de vírus ao Comitê Internacional de Taxonomia de Vírus (ICTV). Como os vírus podem sofrer mutações tão rapidamente, pode ser difícil classificá-los em um gênero e um epíteto de espécie usando o sistema de nomenclatura binomial. Assim, o sistema de nomenclatura viral do ICTV classifica os vírus em famílias e gêneros com base na genética viral, química, morfologia e mecanismo de multiplicação. Até o momento, o ICTV classificou os vírus conhecidos em sete ordens, 96 famílias e 350 gêneros. Os nomes das famílias virais terminam em - viridae (por exemplo, Parvoviridae) e os nomes dos gêneros terminam em −vírus (por exemplo, Parvovírus). Os nomes das ordens virais, famílias e gêneros estão todos em itálico. Quando nos referimos a uma espécie viral, costumamos usar um epíteto de gênero e espécie, como Pandoravirus dulcis ou Pandoravirus salinus.
O sistema de classificação de Baltimore é uma alternativa à nomenclatura ICTV. O sistema de Baltimore classifica os vírus de acordo com seus genomas (DNA ou RNA, fita simples versus fita dupla e modo de replicação). Esse sistema cria, portanto, sete grupos de vírus que têm genética e biologia comuns.
Explore a taxonomia de vírus mais recente no site do ICTV.
Além dos sistemas formais de nomenclatura, os vírus geralmente são agrupados informalmente em categorias com base na química, morfologia ou outras características que eles compartilham em comum. As categorias podem incluir estrutura nua ou envelopada, DNA de fita simples (ss) ou dupla (ds) ou genomas de RNA ss ou ds, genomas segmentados ou não segmentados e RNA de fita positiva (+) ou de fita negativa (−). Por exemplo, os vírus do herpes podem ser classificados como um vírus envelopado de dsDNA; o vírus da imunodeficiência humana (HIV) é um vírus envelopado com +ssRNA e o vírus do mosaico do tabaco é um vírus +ssRNA. Outras características, como especificidade do hospedeiro, especificidade do tecido, formato do capsídeo e genes ou enzimas especiais, também podem ser usadas para descrever grupos de vírus semelhantes. A tabela\(\PageIndex{2}\) lista alguns dos vírus mais comuns que são patógenos humanos por tipo de genoma.
| Genoma | Família | Exemplo de vírus | Características clínicas |
|---|---|---|---|
| dsDNA, envelopado | Poxviridae | Orthopoxvirus | Pápulas cutâneas, pústulas, lesões |
| Poxviridae | Parapoxvírus | Lesões cutâneas | |
| Herpesviridae | Vírus Simplex | Herpes labial, herpes genital, doenças sexualmente transmissíveis | |
| DsDNA, nu | Adenoviridae | Atadenovírus | Infecção respiratória (resfriado comum) |
| Papillomaviridae | Papilomavírus | Verrugas genitais, câncer cervical, vulvar ou vaginal | |
| Reoviridae | Reovírus | Gastroenterite, diarreia grave (gripe estomacal) | |
| SSDNA, nu | Parvoviridae | Dependoparvovírus A adeno-associado | Infecção do trato respiratório |
| Parvoviridae | Dependdoparvovírus B adeno-associado | Infecção do trato respiratório | |
| Srna, nua | Reoviridae | Rotavírus | Gastroenterite |
| + sRNA, nu | Picornaviridae | Enterovírus C | Poliomielite |
| Picornaviridae | Rinovírus | Infecção do trato respiratório superior (resfriado comum) | |
| Picornaviridae | Hepatovírus | Hepatite | |
| + sSRNA, envelopado | Togaviridae | Alphavirus | Encefalite, febre hemorrágica |
| Togaviridae | Rubivírus | Rubéola | |
| Retroviridae | Lentivírus | Síndrome da imunodeficiência adquirida (AIDS) | |
| −ssRNA, envelopado | Filoviridae | Ebolavírus do Zaire | Febre hemorrágica |
| Orthomyxoviridae | Vírus da gripe A, B, C | Gripe | |
| Rhabdoviridae | Lyssavirus | Raiva |
Exercício\(\PageIndex{5}\)
Quais são os tipos de genomas de vírus?
Classificação das doenças virais
Embora o ICTV tenha sido encarregado da classificação biológica dos vírus, ele também desempenhou um papel importante na classificação das doenças causadas por vírus. Para facilitar o rastreamento de doenças humanas relacionadas a vírus, o ICTV criou classificações vinculadas à Classificação Internacional de Doenças (ICD), a taxonomia padrão de doenças mantida e atualizada pela Organização Mundial da Saúde (OMS). O ICD atribui um código alfanumérico de até seis caracteres a cada tipo de infecção viral, bem como a todos os outros tipos de doenças, condições médicas e causas de morte. Esse código ICD é usado em conjunto com dois outros sistemas de codificação (a Terminologia Procedural Atual e o Sistema de Codificação de Procedimentos Comuns de Saúde) para categorizar as condições do paciente para tratamento e reembolso do seguro.
Por exemplo, quando um paciente procura tratamento para uma infecção viral, os códigos ICD são usados rotineiramente pelos médicos para solicitar exames laboratoriais e prescrever tratamentos específicos para o vírus suspeito de causar a doença. Esse código ICD é então usado pelos laboratórios médicos para identificar os testes que devem ser realizados para confirmar o diagnóstico. O código ICD é usado pelo sistema de gerenciamento de saúde para verificar se todos os tratamentos e trabalhos de laboratório realizados são apropriados para o vírus em questão. Os codificadores médicos usam códigos ICD para atribuir o código adequado aos procedimentos realizados, e os cobradores médicos, por sua vez, usam essas informações para processar pedidos de reembolso pelas seguradoras. Os detentores de registros vitais usam códigos ICD para registrar a causa da morte nas certidões de óbito, e epidemiologistas usaram códigos ICD para calcular estatísticas de morbidade e mortalidade.
Exercício\(\PageIndex{6}\)
Identifique dois locais onde você provavelmente encontraria um código ICD.
Foco clínico: Parte 2
O médico de David estava preocupado com o fato de seus sintomas incluírem formigamento e coceira no local da picada do cachorro; essas sensações podem ser sintomas precoces da raiva. Vários testes estão disponíveis para diagnosticar a raiva em pacientes vivos, mas nenhum teste antemortem é adequado. O médico decidiu coletar amostras do sangue, saliva e pele de David para testes. A amostra de pele foi retirada da nuca (lado posterior do pescoço próximo à linha do cabelo). Tinha cerca de 6 mm de comprimento e continha pelo menos 10 folículos pilosos, incluindo o nervo cutâneo superficial. Uma técnica de coloração imunofluorescente foi usada na amostra de biópsia da pele para detectar anticorpos contra a raiva nos nervos cutâneos na base dos folículos pilosos. Um teste também foi realizado em uma amostra de soro do sangue de David para determinar se algum anticorpo para o vírus da raiva havia sido produzido.
Enquanto isso, a amostra de saliva foi usada para análise da reação em cadeia da polimerase por transcriptase reversa (RT-PCR), um teste que pode detectar a presença de ácido nucléico viral (RNA). Os exames de sangue deram positivo para a presença do antígeno do vírus da raiva, levando o médico de David a prescrever tratamento profilático. David recebe uma série de injeções intramusculares de imunoglobulina humana contra a raiva, juntamente com uma série de vacinas contra a raiva.
Exercício\(\PageIndex{7}\)
- Por que a técnica imunofluorescente procura anticorpos contra a raiva em vez do próprio vírus da raiva?
- Se David contraiu raiva, qual é o prognóstico dele?
Resumo
- Os vírus geralmente são ultramicroscópicos, normalmente de 20 nm a 900 nm de comprimento. Alguns vírus grandes foram encontrados.
- Os viriões são acelulares e consistem em um ácido nucléico, DNA ou RNA, mas não ambos, cercados por um capsídeo proteico. Também pode haver uma membrana fosfolipídica ao redor do capsídeo.
- Os vírus são parasitas intracelulares obrigatórios.
- Sabe-se que os vírus infectam vários tipos de células encontradas em plantas, animais, fungos, protistas, bactérias e arquéias. Os vírus geralmente têm um alcance limitado de hospedeiros e infectam tipos específicos de células.
- Os vírus podem ter formas helicoidais, poliédricas ou complexas.
- A classificação dos vírus é baseada na morfologia, tipo de ácido nucléico, alcance do hospedeiro, especificidade celular e enzimas transportadas dentro do virião.
- Como outras doenças, as doenças virais são classificadas usando códigos ICD.
Notas de pé
- 1 H. Lecoq. “[Descoberta do primeiro vírus, o vírus do mosaico do tabaco: 1892 ou 1898?].” Comptes Rendus de l'Academie des Sciences — Série III — Sciences de la Vie 324, nº 10 (2001): 929—933.
- 2 Departamento de Saúde e Serviços Humanos dos EUA, Centros de Controle e Prevenção de Doenças. “Ameaças de resistência a antibióticos nos Estados Unidos, 2013.” www.cdc.gov/drugresistance/pd... s-2013-508.pdf (acessado em 22 de setembro de 2015).
- 3 M. Clokie et al. “Fagos na natureza”. Bacteriófago 1, nº 1 (2011): 31—45.
- 4 A. Sulakvelidze et al. “Terapia de bacteriófagos”. Agentes antimicrobianos e quimioterapia 45, no. 3 (2001): 649—659.
- 5 Administração de Alimentos e Medicamentos dos EUA. “Aprovação da FDA da preparação de bacteriófagos específicos da Listeria em produtos de carne e aves prontos para comer (RTE).” www.fda.gov/food/ingredientsp... /ucm083572.htm (acessado em 22 de setembro de 2015).
- 6 N. Philippe et al. “Pandoravírus: vírus de ameba com genomas de até 2,5 Mb atingindo os de eucariotos parasitas.” Science 341, nº 6143 (2013): 281—286.
- 7 J. Cohen. “O que há de velho é novo: o vírus de 1918 corresponde à cepa H1N1 de 2009. Ciência 327, nº 5973 (2010): 1563—1564.


