26.3 : Maladies pathogènes acellulaires du système nerveux
- Page ID
- 187870
Objectifs d'apprentissage
- Identifier les agents pathogènes acellulaires les plus courants pouvant provoquer des infections du système nerveux
- Comparez les principales caractéristiques de maladies virales spécifiques affectant le système nerveux
Un certain nombre de virus et de particules subvirales peuvent provoquer des maladies affectant le système nerveux. Les maladies virales ont tendance à être plus fréquentes que les infections bactériennes du système nerveux aujourd'hui. Heureusement, les infections virales sont généralement plus bénignes que leurs homologues bactériennes et disparaissent souvent spontanément. Certains des agents pathogènes acellulaires les plus importants du système nerveux sont décrits dans cette section.
Méningite virale
Bien qu'elle soit beaucoup plus courante que la méningite bactérienne, la méningite virale est généralement moins grave. De nombreux virus peuvent provoquer une méningite en tant que séquelle de l'infection primaire, y compris ceux qui causent l'herpès, la grippe, la rougeole et les oreillons. La plupart des cas de méningite virale disparaissent spontanément, mais des cas graves surviennent.
Encéphalite arbovirale
Plusieurs types de virus transmis par les insectes peuvent provoquer une encéphalite. Collectivement, ces virus sont appelés arbovirus (parce qu'ils sont des arthropodes) et les maladies qu'ils provoquent sont décrites sous le nom d'encéphalite arbovirale. La plupart des arbovirus sont endémiques à des régions géographiques spécifiques. Les encéphalites arborvirales présentes aux États-Unis comprennent l'encéphalite équine de l'Est (EEE), l'encéphalite équine occidentale (WEE), l'encéphalite de Saint-Louis et l'encéphalite du Nil occidental (WNE). L'expansion des arbovirus au-delà de leurs régions endémiques se produit parfois, généralement à la suite de changements environnementaux favorables au virus ou à son vecteur. L'augmentation des déplacements d'humains, d'animaux ou de vecteurs infectés a également permis aux arbovirus de se propager dans de nouvelles régions.
Dans la plupart des cas, les infections arbovirales sont asymptomatiques ou entraînent une maladie bénigne. Cependant, lorsque des symptômes apparaissent, ils incluent une forte fièvre, des frissons, des maux de tête, des vomissements, de la diarrhée et de l'agitation. Chez les patients âgés, une encéphalite arbovirale sévère peut rapidement entraîner des convulsions, un coma et la mort.
Les moustiques sont les vecteurs biologiques les plus courants des arbovirus, qui sont généralement des virus à ARNss enveloppés. Ainsi, la meilleure façon de prévenir les infections arbovirales est d'éviter les moustiques, en utilisant un insectifuge, en portant des pantalons et des manches longs, en dormant dans des pièces bien grillagées, en utilisant des moustiquaires, etc.
Le diagnostic de l'encéphalite arbovirale repose sur les symptômes cliniques et les tests sérologiques du sérum ou du LCR. Comme il n'existe aucun médicament antiviral pour traiter ces maladies arbovirales, le traitement consiste en des soins de soutien et en une prise en charge des symptômes.
L'encéphalite équine de l'Est (EEE) est causée par le virus de l'encéphalite équine orientale (EEEV), qui peut provoquer de graves maladies chez les chevaux et les humains. Les oiseaux sont des réservoirs d'EEEV transmis accidentellement aux chevaux et aux humains par les espèces de moustiques Aedes, Coquillettidia et Culex. Ni les chevaux ni les humains ne servent de réservoirs. L'EEE est plus répandu dans les États américains de la côte du Golfe et de l'Atlantique. L'EEE est l'une des maladies transmises par les moustiques les plus graves aux États-Unis, mais heureusement, il s'agit d'une maladie très rare aux États-Unis (Figure\(\PageIndex{1}\)). 1 2
L'encéphalite équine occidentale (WEE) est causée par le virus de l'encéphalite équine occidentale (WEEV). Le WEEV est généralement transmis aux chevaux et aux humains par les moustiques Culex tarsalis et, au cours de la dernière décennie, a causé très peu de cas d'encéphalite chez l'homme aux États-Unis. Chez l'homme, les symptômes du WEE sont moins graves que ceux de l'EEE et incluent de la fièvre, des frissons et des vomissements, avec un taux de mortalité de 3 à 4 %. Comme l'EEEV, les oiseaux constituent le réservoir naturel du WEEV. Périodiquement, pour des raisons indéterminées, des épidémies de cas humains se sont produites en Amérique du Nord par le passé. Le plus important jamais enregistré remonte à 1941, avec plus de 3 400 cas. 3
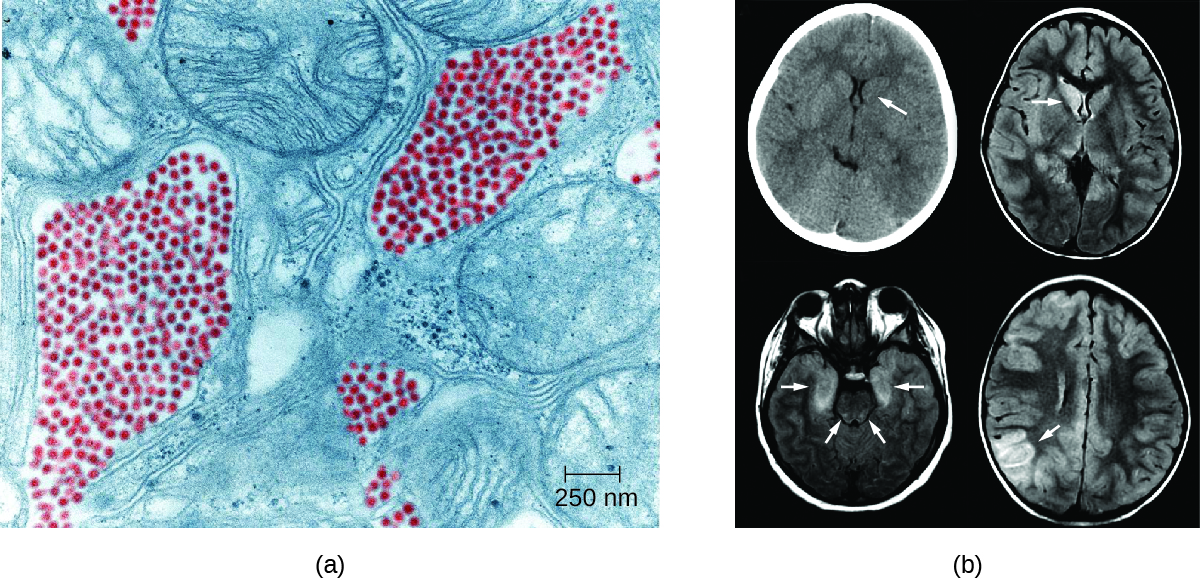
L'encéphalite de Saint-Louis (LES), causée par le virus de l'encéphalite de Saint-Louis (SLEV), est une forme rare d'encéphalite dont les symptômes se manifestent chez moins de 1 % des patients infectés. Les réservoirs naturels du SLEV sont des oiseaux. Le SLEV se trouve le plus souvent dans le bassin du fleuve Ohio et Mississippi, dans le centre des États-Unis, et a été nommé d'après une grave épidémie survenue au Missouri en 1934. La pire épidémie d'encéphalite de Saint-Louis s'est produite en 1975, avec plus de 2 000 cas signalés. 4 Les humains sont infectés lorsqu'ils sont mordus par des moustiques C. tarsalis, C. quinquefasciatus ou C. pipiens porteurs du SLEV. La plupart des patients sont asymptomatiques, mais chez un petit nombre de personnes, les symptômes vont de syndromes grippaux légers à une encéphalite fatale. Le taux de mortalité global des patients symptomatiques est de 5 à 15 %. 5
L'encéphalite japonaise, causée par le virus de l'encéphalite japonaise (JEV), est la principale cause d'encéphalite évitable par la vaccination chez l'homme et est endémique dans certains des pays les plus peuplés du monde, notamment la Chine, l'Inde, le Japon et toute l'Asie du Sud-Est. Le JEV est transmis à l'homme par les moustiques Culex, généralement de l'espèce C. tritaeniorhynchus. Les réservoirs biologiques du JEV comprennent des cochons et des échassiers. La plupart des patients infectés par le JEV sont asymptomatiques, les symptômes se produisant chez moins de 1 % des personnes infectées. Cependant, environ 25 % des personnes qui développent une encéphalite décèdent et, parmi celles qui se rétablissent, 30 à 50 % souffrent de troubles psychiatriques, neurologiques ou cognitifs. 6 Heureusement, il existe un vaccin efficace qui peut prévenir l'infection par le JEV. Le CDC recommande ce vaccin aux voyageurs qui prévoient de passer plus d'un mois dans des zones d'endémie.
Comme leur nom l'indique, le virus du Nil occidental (VNO) et la maladie associée, l'encéphalite du Nil occidental (WNE), ne sont pas originaires d'Amérique du Nord. Jusqu'en 1999, le virus était endémique au Moyen-Orient, en Afrique et en Asie ; toutefois, les premiers cas américains ont été identifiés à New York en 1999 et, en 2004, le virus s'était propagé sur l'ensemble de la zone continentale des États-Unis. Plus de 35 000 cas, dont 1 400 décès, ont été confirmés au cours de la période de cinq ans comprise entre 1999 et 2004. L'infection par le virus du Nil occidental doit toujours être signalée aux CDC.
Le VNO est transmis aux humains par les moustiques Culex à partir de leur réservoir naturel, les oiseaux infectés, et 70 à 80 % des patients infectés ne présentent aucun symptôme. La plupart des cas symptomatiques ne présentent que des symptômes légers semblables à ceux de la grippe, mais moins de 1 % des personnes infectées développent une encéphalite ou une méningite grave et parfois fatale. Le taux de mortalité chez les patients atteints du VNO qui développent une maladie neurologique est d'environ 10 %. Pour en savoir plus sur le virus du Nil occidental, consultez la section Modes de transmission de la maladie.
Cette carte interactive identifie les cas de plusieurs maladies arbovirales chez les humains et les espèces réservoirs par État et par année aux États-Unis.
Exercice\(\PageIndex{1}\)
- Pourquoi est-il peu probable que les virus de l'encéphalite arbovirale soient éradiqués à l'avenir ?
- Quelle est la forme d'encéphalite virale la plus répandue aux États-Unis ?
Orientation clinique : partie 2
La lévofloxacine est un antibiotique quinolone souvent prescrit pour traiter les infections bactériennes des voies respiratoires, notamment la pneumonie et la bronchite. Mais après avoir pris le médicament pendant une semaine, David est retourné chez son médecin plus malade qu'auparavant. Il a affirmé que l'antibiotique n'avait eu aucun effet sur ses premiers symptômes. De plus, il souffrait maintenant de maux de tête, d'une raideur de la nuque et de la difficulté à se concentrer au travail. Il a également montré au médecin une éruption cutanée qui s'était développée sur ses bras au cours de la semaine écoulée. Son médecin, plus inquiet maintenant, a commencé à poser des questions sur les activités de David au cours des deux dernières semaines.
David a expliqué qu'il avait récemment travaillé sur un projet visant à démonter une ancienne grange. Son médecin a prélevé des échantillons de crachats et des raclures sur l'éruption cutanée de David pour les cultures. Une ponction lombaire a également été réalisée pour examiner le LCR de David. L'examen microscopique de son LCR a révélé des cellules de levure encapsulées. Sur la base de ce résultat, le médecin a prescrit un nouveau traitement antimicrobien utilisant l'amphotéricine B et la flucytosine.
Exercice\(\PageIndex{2}\)
- Pourquoi le traitement initial était-il inefficace ?
- Pourquoi la présence d'une gélule est-elle cliniquement importante ?
Infection par le virus Zika
L'infection par le virus Zika est une maladie arbovirale émergente associée à des maladies humaines en Afrique, en Asie du Sud-Est, en Amérique du Sud et en Amérique centrale ; toutefois, son aire de répartition s'étend en raison de la vaste gamme de son moustique vecteur. Les premiers cas provenant des États-Unis ont été signalés en 2016. Le virus Zika a été initialement décrit en 1947 chez des singes de la forêt Zika en Ouganda par le biais d'un réseau de surveillance de la fièvre jaune. Il n'était pas considéré comme un agent pathogène humain grave avant les premières épidémies de grande ampleur en Micronésie en 20077 ; cependant, le virus a gagné en notoriété au cours de la dernière décennie, car il est devenu la cause de symptômes similaires à ceux d'autres infections arbovirales, notamment de la fièvre, des éruptions cutanées, conjonctivite, douleurs musculaires et articulaires, malaise et maux de tête. Les moustiques du genre Aedes en sont les principaux vecteurs, bien que le virus puisse également être transmis sexuellement, de la mère à l'enfant pendant la grossesse, ou par transfusion sanguine.
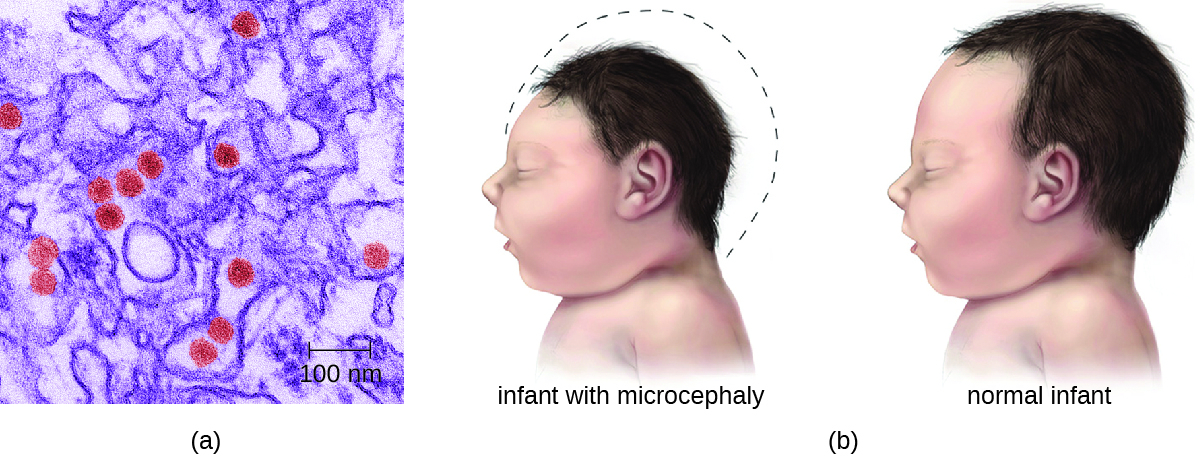
La plupart des infections par le virus Zika se traduisent par des symptômes bénins tels que de la fièvre, une légère éruption cutanée ou une conjonctivite. Cependant, les infections chez les femmes enceintes peuvent nuire au développement du fœtus. Des rapports publiés en 2015 indiquent que les infections foetales peuvent entraîner des lésions cérébrales, notamment une grave anomalie congénitale appelée microcéphalie, dans laquelle le nourrisson naît avec une tête anormalement petite (Figure\(\PageIndex{2}\)). 8
Le diagnostic du virus Zika repose principalement sur les symptômes cliniques. Cependant, la FDA a récemment autorisé l'utilisation d'un test d'ARN du virus Zika, du Trioplex RT-PCR et du Zika MAC-ELISA pour tester le sang et l'urine des patients afin de confirmer la présence du virus Zika. Il n'existe actuellement aucun traitement antiviral ni vaccin contre le virus Zika, et le traitement se limite aux soins de soutien.
Exercice\(\PageIndex{3}\)
- Quels sont les signes et symptômes de l'infection par le virus Zika chez les adultes ?
- Pourquoi l'infection par le virus Zika est-elle considérée comme une grave menace pour la santé publique ?
La rage
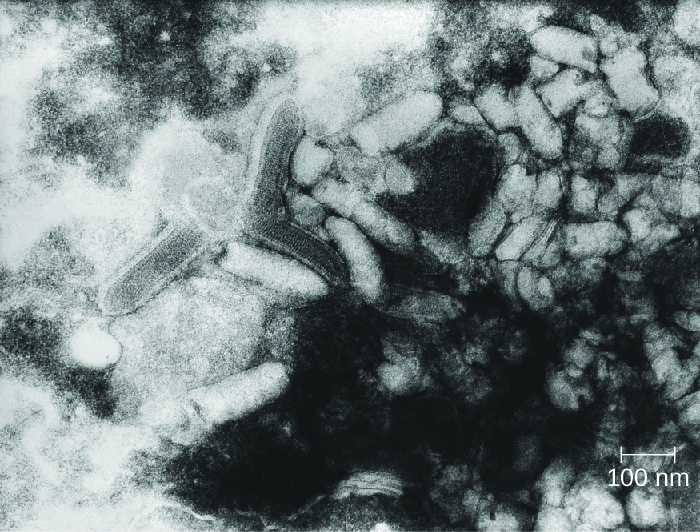
La rage est une zoonose mortelle connue depuis l'Antiquité. La maladie est causée par le virus de la rage (RV), un membre de la famille des Rhabdoviridae, et se transmet principalement par la morsure d'un mammifère infecté. Les rhabdoviridae sont des virus à ARN enveloppés qui ont une forme de balle caractéristique (Figure\(\PageIndex{3}\)) ; ils ont d'abord été étudiés par Louis Pasteur, qui a obtenu le virus de la rage chez des chiens enragés et l'a cultivé chez des lapins. Il a préparé avec succès un vaccin antirabique à partir de tissus nerveux séchés provenant d'animaux infectés. Ce vaccin a été utilisé pour la première fois pour traiter un humain infecté en 1885.
Les réservoirs les plus courants aux États-Unis sont des animaux sauvages tels que les ratons laveurs (30,2 % de tous les cas animaux en 2014), les chauves-souris (29,1 %), les mouffettes (26,3 %) et les renards (4,1 %) ; collectivement, ces animaux étaient responsables d'un total de 92,6 % des cas de rage animale aux États-Unis en 2014. Les 7,4 % restants de cas cette année-là concernaient des animaux domestiques tels que des chiens, des chats, des chevaux, des mulets, des moutons, des chèvres et des lamas. 9 Bien qu'il n'y ait généralement qu'un ou deux cas humains par an aux États-Unis, la rage cause toujours des dizaines de milliers de décès humains par an dans le monde, principalement en Asie et en Afrique.
La faible incidence de la rage aux États-Unis est principalement due à la vaccination généralisée des chiens et des chats. Un vaccin oral est également utilisé pour protéger les animaux sauvages, tels que les ratons laveurs et les renards, contre les infections. Les programmes de vaccination orale ont tendance à se concentrer sur les zones géographiques où la rage est endémique. 10 Le vaccin oral est généralement administré dans un paquet d'appâts qui est largué par avion, bien que l'appâtage dans les zones urbaines soit effectué à la main pour optimiser la sécurité. 11 De nombreux pays exigent une quarantaine ou une preuve de vaccination antirabique pour les animaux domestiques introduits dans le pays. Ces procédures sont particulièrement strictes dans les pays insulaires où la rage n'est pas encore présente, comme l'Australie.
La période d'incubation de la rage peut être longue, allant de plusieurs semaines ou mois à plus d'un an. Au fur et à mesure que le virus se reproduit, il se déplace du site de la morsure vers les axones moteurs et sensoriels des nerfs périphériques et se propage d'un nerf à l'autre selon un processus appelé transport rétrograde, pour finalement atteindre le SNC en passant par les ganglions spinaux. Une fois que le virus de la rage atteint le cerveau, l'infection entraîne une encéphalite causée par la perturbation du fonctionnement normal des neurotransmetteurs, ce qui entraîne les symptômes associés à la rage. Les virions agissent dans les espaces synaptiques en tant que concurrents de divers neurotransmetteurs pour les récepteurs de l'acétylcholine, du GABA et de la glycine. Ainsi, l'action du virus de la rage est neurotoxique plutôt que cytotoxique. Une fois que le virus de la rage a infecté le cerveau, il peut continuer à se propager par d'autres voies neuronales, sortant du SNC vers des tissus tels que les glandes salivaires, où le virus peut être libéré. Par conséquent, à mesure que la maladie progresse, le virus peut être présent dans de nombreux autres tissus, notamment les glandes salivaires, les papilles gustatives, les fosses nasales et les larmes.
Les premiers symptômes de la rage incluent une gêne au site de la morsure, de la fièvre et des maux de tête. Une fois que le virus atteint le cerveau et que les symptômes ultérieurs apparaissent, la maladie est toujours fatale. Les cas de rage en phase terminale peuvent se terminer de deux manières : rage furieuse ou rage paralytique. Les personnes atteintes d'une rage furieuse deviennent très agitées et hyperactives. L'hydrophobie (peur de l'eau) est courante chez les patients atteints de rage furieuse, causée par des spasmes musculaires de la gorge lorsqu'ils avalent de l'eau ou pensent à boire. Un excès de salivation et une envie de mordre peuvent provoquer une formation de mousse dans la bouche. Ces comportements contribuent à augmenter le risque de transmission virale, bien que le contact avec des sécrétions infectées telles que la salive ou les larmes soit suffisant à lui seul pour provoquer l'infection. La maladie culmine au bout de quelques jours dans la terreur et la confusion, suivies d'un arrêt cardiovasculaire et respiratoire. En revanche, les personnes atteintes de rage paralytique suivent généralement une évolution plus longue de la maladie. Les muscles du site de l'infection deviennent paralysés. Au fil du temps, la paralysie se propage lentement dans tout le corps. Cette forme de maladie paralytique aboutit au coma et à la mort.
Avant que les méthodes diagnostiques actuelles ne soient disponibles, le diagnostic de la rage était posé à l'aide des antécédents cliniques et d'un examen histopathologique des tissus de biopsie ou d'autopsie, afin de détecter la présence de corps de Negri. Nous savons maintenant que ces changements histologiques ne peuvent pas être utilisés pour confirmer un diagnostic de rage. Aucun test ne permet de détecter le virus de la rage chez les humains au moment de la morsure ou peu de temps après. Une fois que le virus a commencé à se répliquer (mais avant l'apparition des symptômes cliniques), il peut être détecté à l'aide d'un test d'immunofluorescence sur les nerfs cutanés situés à la base des follicules pileux. La salive peut également être testée pour détecter le matériel génétique viral par transcription inverse suivie d'une réaction en chaîne par polymérase (RT-PCR). Même lorsque ces tests sont effectués, la plupart des infections suspectées sont considérées comme positives en l'absence de preuves contraires. Il est préférable que les patients suivent un traitement inutile en raison d'un résultat faussement positif, plutôt que de mourir à la suite d'un résultat faussement négatif.
Les infections rabiques chez l'humain sont traitées par immunisation à l'aide de doses multiples d'un vaccin atténué afin de développer une immunité active chez le patient (voir la rubrique « Orientation clinique » dans le chapitre sur les agents pathogènes acellulaires). La vaccination d'une personne déjà infectée peut être efficace en raison de la lenteur de la progression de la maladie, ce qui laisse le temps au système immunitaire du patient de développer des anticorps contre le virus. Les patients peuvent également être traités avec des immunoglobulines antirabiques humaines (anticorps dirigés contre le virus de la rage) afin de favoriser une immunité passive. Ces anticorps neutraliseront toutes les particules virales libres. Bien que l'infection par la rage progresse lentement dans les tissus périphériques, les patients ne sont normalement pas en mesure de développer eux-mêmes une réponse immunitaire protectrice.
Exercice\(\PageIndex{4}\)
- Comment la morsure d'un animal infecté transmet-elle la rage ?
- Quel est l'objectif des programmes de vaccination de la faune contre la rage ?
- Comment traite-t-on la rage chez l'homme ?
Poliomyélite
La poliomyélite (poliomyélite), causée par le poliovirus, est une maladie essentiellement intestinale qui, dans un faible pourcentage des cas, atteint le système nerveux, provoquant la paralysie et, potentiellement, la mort. Le poliovirus est très contagieux et se transmet par voie fécale-orale, par aérosol ou par gouttelettes. Environ 72 % de toutes les infections par le poliovirus sont asymptomatiques ; 25 % ne provoquent que des maladies intestinales bénignes, provoquant nausées, fièvre et maux de tête. 12 Cependant, même en l'absence de symptômes, les patients infectés par le virus peuvent l'excréter dans les matières fécales et les sécrétions orales, ce qui peut transmettre le virus à d'autres personnes. Dans environ un cas sur 200, le poliovirus affecte les cellules du système nerveux central. 13
Après son entrée par la bouche, la réplication initiale du poliovirus se produit au site d'implantation dans le pharynx et le tractus gastro-intestinal. À mesure que l'infection progresse, le poliovirus est généralement présent dans la gorge et dans les selles avant l'apparition des symptômes. Une semaine après l'apparition des symptômes, il y a moins de poliovirus dans la gorge, mais pendant plusieurs semaines, le poliovirus continue d'être excrété dans les selles. Le poliovirus envahit les tissus lymphoïdes locaux, pénètre dans la circulation sanguine et peut ensuite infecter les cellules du SNC. La réplication du poliovirus dans les motoneurones des cellules de la corne antérieure de la moelle épinière, du tronc cérébral ou du cortex moteur entraîne la destruction des cellules et une paralysie flasque. Dans les cas graves, cela peut impliquer le système respiratoire et entraîner la mort. Les patients présentant une insuffisance respiratoire sont traités à l'aide de systèmes de ventilation à pression positive. Dans le passé, les patients étaient parfois confinés dans des respirateurs Emerson, également appelés poumons en fer (Figure\(\PageIndex{4}\)).
La détection directe du poliovirus dans la gorge ou les matières fécales peut être réalisée par PCR par transcriptase inverse (RT-PCR) ou par séquençage génomique afin d'identifier le génotype du poliovirus infectant le patient. Des tests sérologiques peuvent être utilisés pour déterminer si le patient a déjà été vacciné. Il n'existe aucune mesure thérapeutique contre la poliomyélite ; le traitement se limite à diverses mesures de soutien. Il s'agit notamment des analgésiques, du repos, de la thermothérapie pour soulager les spasmes musculaires, de la physiothérapie et des appareils orthopédiques correcteurs si nécessaire pour faciliter la marche, et de la ventilation mécanique pour aider à respirer si nécessaire.

Deux vaccins différents ont été introduits dans les années 1950 et ont entraîné une baisse spectaculaire de la poliomyélite dans le monde (Figure\(\PageIndex{5}\)). Le vaccin Salk est un poliovirus inactivé qui a été introduit pour la première fois en 1955. Ce vaccin est administré par injection intramusculaire. Le vaccin Sabin est un vaccin antipoliomyélitique oral qui contient un virus atténué ; son utilisation a été homologuée en 1962. Il existe trois sérotypes de poliovirus qui causent des maladies chez l'homme ; les vaccins Salk et Sabin sont tous deux efficaces contre les trois.
Les virus atténués issus du vaccin Sabin sont excrétés dans les matières fécales des personnes vaccinées et peuvent donc infecter les personnes non vaccinées. À la fin des années 1990, les quelques cas de poliomyélite originaires des États-Unis pouvaient être attribués au vaccin Sabin. Dans ces cas, les mutations du virus atténué à la suite de la vaccination ont probablement permis au microbe de revenir à une forme virulente. Pour cette raison, les États-Unis sont passés exclusivement au vaccin Salk en 2000. Comme le vaccin Salk contient un virus inactivé, il n'y a aucun risque de transmission à d'autres personnes (voir Vaccins). Actuellement, quatre doses du vaccin sont recommandées pour les enfants : à l'âge de 2, 4 et 6 à 18 mois, et à l'âge de 4 à 6 ans.
En 1988, l'OMS a lancé l'Initiative mondiale pour l'éradication de la poliomyélite dans le but d'éradiquer la polio dans le monde grâce à la vaccination Cet objectif est maintenant sur le point d'être atteint. La poliomyélite n'est désormais endémique que dans quelques pays, dont l'Afghanistan, le Pakistan et le Nigéria, où les efforts de vaccination ont été perturbés par des conflits militaires ou par l'instabilité politique.

La terreur de la polio
Dans les années qui ont suivi la Seconde Guerre mondiale, les États-Unis et l'Union soviétique sont entrés dans une période connue sous le nom de guerre froide. Bien qu'il n'y ait pas eu de conflit armé, les deux superpuissances étaient isolées l'une de l'autre du point de vue diplomatique et économique, comme le montre ce que l'on appelle le rideau de fer entre l'Union soviétique et le reste du monde. Après 1950, il était extrêmement difficile de migrer ou de voyager en dehors de l'Union soviétique, et il était tout aussi difficile pour les étrangers d'entrer en Union soviétique. Les États-Unis ont également imposé des limites strictes à l'entrée des Soviétiques dans le pays. Sous l'administration Eisenhower, seuls 20 étudiants des cycles supérieurs de l'Union soviétique étaient autorisés à venir étudier aux États-Unis par an.
Pourtant, même le rideau de fer n'était pas à la hauteur de la polio. Le vaccin Salk est devenu largement disponible dans l'Ouest en 1955, et lorsque le vaccin Sabin a été prêt pour les essais cliniques, la plupart de la population sensible aux États-Unis et au Canada avait déjà été vaccinée contre la polio. Sabin avait besoin de chercher des participants à l'étude ailleurs. Au plus fort de la guerre froide, Mikhaïl Chumakov a été autorisé à venir aux États-Unis pour étudier l'œuvre de Sabin. De même, Sabin, un microbiologiste américain, a été autorisé à se rendre en Union soviétique pour commencer des essais cliniques. Chumakov a organisé la production basée en Union soviétique et a géré les essais expérimentaux pour tester le nouveau vaccin en Union soviétique. En 1959, plus de dix millions d'enfants soviétiques avaient été traités en toute sécurité avec le vaccin de Sabin.
À la suite d'une campagne mondiale de vaccination avec le vaccin Sabin, l'incidence globale de la poliomyélite a chuté de façon spectaculaire. Aujourd'hui, la poliomyélite a été presque éliminée dans le monde et n'est que rarement observée aux États-Unis. Peut-être qu'un jour, la poliomyélite deviendra la troisième maladie microbienne à être éradiquée de la population générale [la variole et la peste bovine (cause de la peste bovine) étant les deux premières].
Exercice\(\PageIndex{5}\)
- Comment se transmet le poliovirus ?
- Comparez les avantages et les inconvénients de chacun des deux vaccins antipoliomyélitiques.
Encéphalopathies spongiformes transmissibles
Les agents infectieux acellulaires appelés prions sont responsables d'un groupe de maladies connexes appelées encéphalopathies spongiformes transmissibles (EST) qui touchent les humains et d'autres animaux (voir Viroïdes, Virusoïdes et Prions). Toutes les EST sont des maladies neurologiques dégénératives mortelles qui surviennent lorsque le tissu cérébral est infecté par des prions. Ces maladies se manifestent lentement ; les symptômes peuvent ne se manifester qu'après une période d'incubation de plusieurs années, voire des décennies, mais la mort survient généralement quelques mois ou quelques années après l'apparition des premiers symptômes.
Les EST chez les animaux incluent la tremblante du mouton, une maladie connue depuis les années 1700, et l'émaciation chronique, une maladie touchant les cerfs et les wapitis aux États-Unis et au Canada. La maladie de la vache folle est observée chez les bovins et peut être transmise à l'homme par la consommation de tissus nerveux infectés. Les maladies à prions chez l'homme incluent la maladie de Creutzfeldt-Jakob et le kuru, une maladie rare endémique en Papouasie-Nouvelle-Guinée.
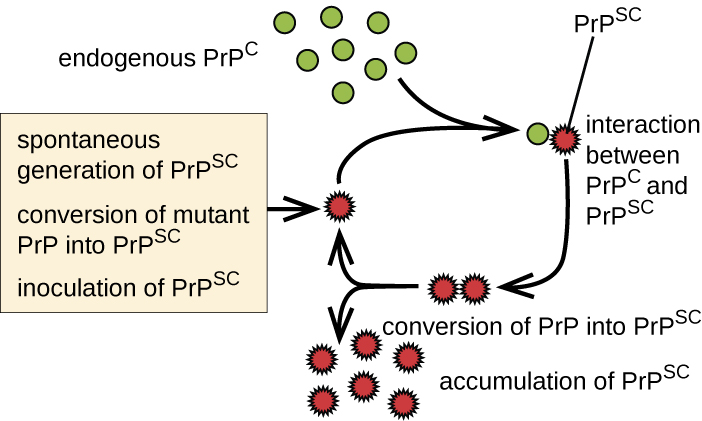
Les prions sont des particules protéiques infectieuses qui ne sont pas des virus et ne contiennent pas d'acide nucléique. Ils sont généralement transmis par exposition et ingestion de tissus infectés du système nerveux, par des greffes de tissus, par des transfusions sanguines ou par des vecteurs de contamination. Les protéines prion se trouvent normalement dans un tissu cérébral sain sous une forme appelée PrP C. Cependant, si cette protéine est mal repliée sous une forme dénaturée (PrP Sc), elle peut provoquer des maladies. Bien que la fonction exacte de la PrP C ne soit pas connue actuellement, la protéine se replie principalement en hélices alpha et se lie au cuivre. La protéine voyous, quant à elle, se replie principalement en feuilles bêta-plissées et résiste à la protéolyse. De plus, la PrP Sc peut provoquer un mauvais repliement de la PrP C et produire davantage de protéines indésirables (Figure\(\PageIndex{6}\)).
À mesure que la PrP Sc s'accumule, elle s'agrège et forme des fibrilles dans les cellules nerveuses. Ces complexes protéiques finissent par provoquer la mort des cellules. En conséquence, les tissus cérébraux des personnes infectées forment des masses d'enchevêtrements neurofibrillaires et de plaques amyloïdes qui donnent au cerveau un aspect spongieux. C'est pourquoi ces maladies sont appelées encéphalopathie spongiforme (Figure 6.4.3). Les dommages aux tissus cérébraux entraînent divers symptômes neurologiques. Le plus souvent, les personnes touchées souffrent de pertes de mémoire, de changements de personnalité, d'une vision floue, de mouvements non coordonnés et d'insomnie. Ces symptômes s'aggravent progressivement avec le temps et aboutissent au coma et à la mort.
La référence absolue pour le diagnostic des EST est l'examen histologique des biopsies cérébrales pour détecter la présence de plaques amyloïdes, de vacuoles et de protéines prions caractéristiques. Les cliniciens doivent être très prudents lorsqu'ils manipulent des matières soupçonnées d'être infectées par des prions afin d'éviter de s'infecter eux-mêmes. D'autres essais tissulaires visent à détecter la présence de la protéine 14-3-3, un marqueur de maladies à prions comme la maladie de Creutzfeldt-Jakob. De nouveaux tests, tels que le RT-Quic (conversion induite par le tremblement de terre en temps réel), offrent de nouveaux espoirs de détecter efficacement les protéines prions anormales dans les tissus plus tôt au cours de l'infection. Les maladies à prions ne peuvent être soignées. Cependant, certains médicaments peuvent aider à ralentir leur progression. Le soutien médical vise à maintenir les patients aussi confortables que possible malgré des symptômes évolutifs et débilitants.
Les matériaux contaminés par les prions étant des sources potentielles d'infection pour les cliniciens et les médecins, l'Organisation mondiale de la santé et les CDC fournissent des informations pour informer, éduquer et minimiser le risque d'infections dues aux prions.
Exercice\(\PageIndex{6}\)
- Les prions se reproduisent-ils au sens classique du terme ?
- Quel est le lien entre les prions et l'élimination des sous-produits animaux de la nourriture des animaux de ferme ?
Infections acellulaires du système nerveux
Les graves conséquences sont le dénominateur commun de ces maladies neurologiques. Plusieurs d'entre elles provoquent une paralysie invalidante et certaines, comme la maladie de Creutzfeldt-Jakob et la rage, sont toujours ou presque toujours mortelles. Étant donné que peu de médicaments sont disponibles pour combattre ces infections, la lutte antivectorielle et la vaccination sont essentielles pour la prévention et l'endiguement. La figure\(\PageIndex{7}\) résume certaines infections virales et à prions importantes du système nerveux.
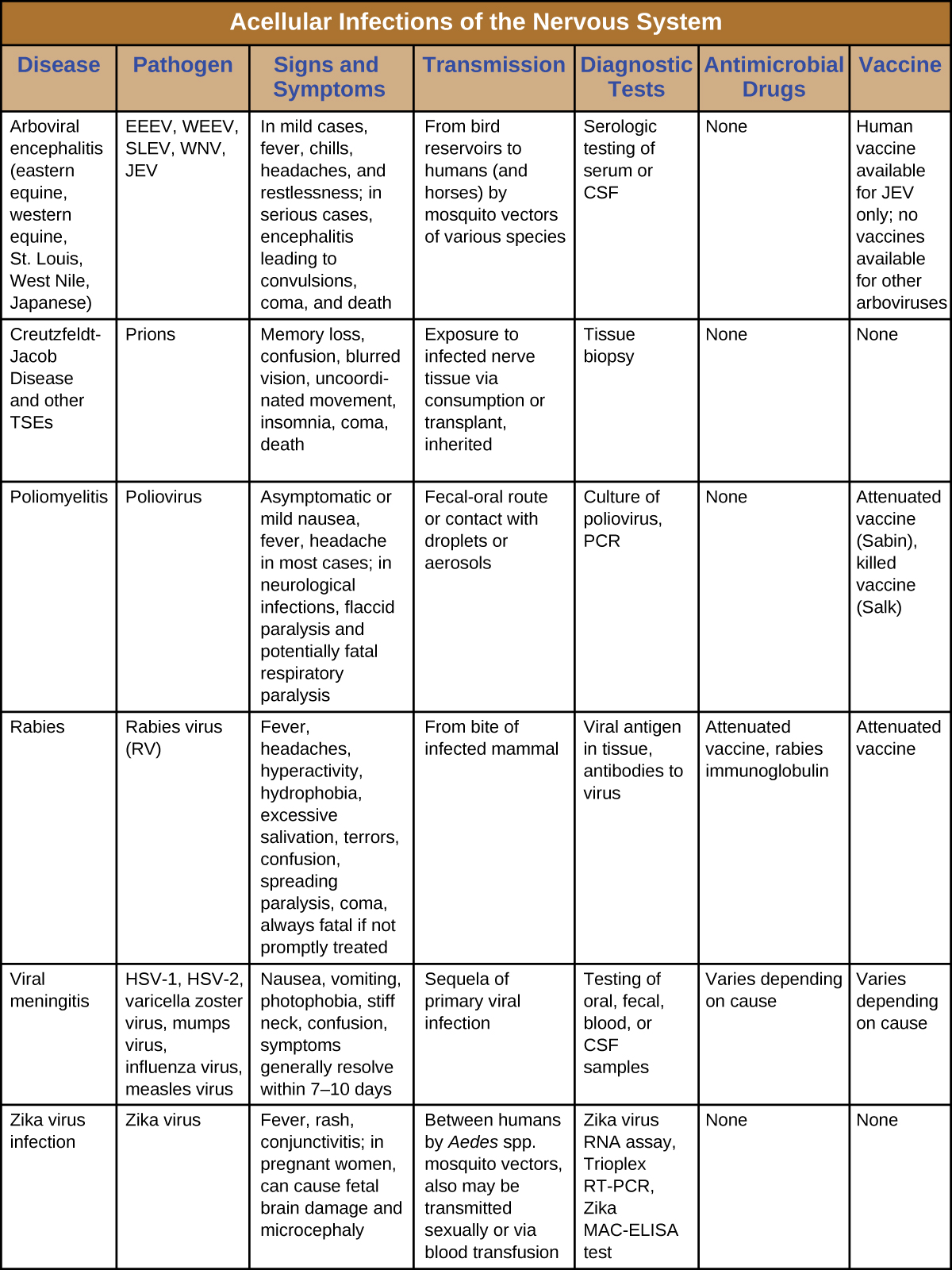
Concepts clés et résumé
- La méningite virale est plus fréquente et généralement moins grave que la méningite bactérienne. Elle peut résulter des séquelles secondaires de nombreux virus ou être causée par des infections par des arbovirus.
- Différents types d'encéphalite arbovirale sont concentrés dans des zones géographiques particulières à travers le monde. Ces infections virales du système nerveux transmises par les moustiques sont généralement bénignes, mais elles peuvent mettre la vie en danger dans certains cas.
- Le virus Zika est une infection arbovirale émergente dont les symptômes sont généralement bénins chez la plupart des personnes, mais les infections des femmes enceintes peuvent provoquer la microcéphalie d'une malformation congénitale.
- La poliomyélite est généralement une infection intestinale bénigne, mais elle peut être dommageable ou mortelle si elle évolue vers une maladie neurologique.
- La rage est presque toujours mortelle lorsqu'elle n'est pas traitée et demeure un problème important dans le monde entier.
- Les encéphalopathies spongiformes transmissibles telles que la maladie de Creutzfeldt-Jakob et le kuru sont causées par des prions. Ces maladies sont incurables et, en fin de compte, mortelles. Des maladies à prions similaires sont présentes chez les animaux.
Notes
- 1 Centers for Disease Control and Prevention des États-Unis, « Cas et décès liés à la maladie du virus de l'encéphalite équine orientale signalés aux CDC par année et présentation clinique, 2004—2013 », 2014. www.CDC.gov/EasterneQuineence... _2004-2013.pdf.
- 2 Centres américains pour le contrôle et la prévention des maladies, « Encéphalite équine orientale, symptômes et traitement, 2016 », consulté le 29 juin 2016. https://www.cdc.gov/easternequineenc... /symptoms.html.
- 3 Centres américains pour le contrôle et la prévention des maladies, « Western Equine Encephalitis—United States and Canada, 1987 », Morbidity and Mortality Weekly Report 36, n° 39 (1987) : 655.
- 4 Centres américains pour le contrôle et la prévention des maladies, « Saint Louis encéphalite, épidémiologie et distribution géographique », consulté le 30 juin 2016. http://www.cdc.gov/sle/technical/epi.html.
- 5 Centres américains pour le contrôle et la prévention des maladies, « Saint Louis encéphalite, symptômes et traitement », consulté le 30 juin 2016. http://www.cdc.gov/sle/technical/symptoms.html.
- 6 Centres américains pour le contrôle et la prévention des maladies, « Encéphalite japonaise, symptômes et traitement », consulté le 30 juin 2016. www.cdc.gov/japaneseencephali... oms/index.html.
- 7 Sikka, Veronica, Vijay Kumar Chattu, Raaj K. Popli, Sagar C. Galwankar, Dhanashree Kelkar, Stanley G. Sawicki, Stanislaw P. Stawicki et Thomas J. Papadimos, « L'émergence du virus Zika en tant que menace pour la sécurité sanitaire mondiale : examen et déclaration consensuelle du groupe de travail conjoint (JWG) de l'INDUSEM », Journal des maladies infectieuses mondiales 8, n° 1 (2016) : 3.
- 8 Mlakar, Jernej, Misa Korva, Nataša Tul, Mara Popović, Mateja Poljšak-Prijatelj, Jerica Mraz, Marko Kolenc et al., « Le virus Zika associé à la microcéphalie », New England Journal of Medicine 374, n° 10 (2016) : 951-8.
- 9 Centres américains pour le contrôle et la prévention des maladies, « Rabies, animaux sauvages », 2016. Consulté le 13 septembre 2016. www.cdc.gov/rabies/location/u... d_animals.html.
- 10 Slate, Dennis, Charles E. Rupprecht, Jane A. Rooney, Dennis Donovan, Donald H. Lein et Richard B. Chipman, « État de la vaccination orale contre la rage chez les carnivores sauvages aux États-Unis », Virus Research 111, no 1 (2005) : 68-76.
- 11 Finnegan, Christopher J., Sharon M. Brookes, Nicholas Johnson, Jemma Smith, Karen L. Mansfield, Victoria L. Keene, Lorraine M. McElhinney et Anthony R. Fooks, « La rage en Amérique du Nord et en Europe », Journal de la Royal Society of Medicine 95, no 1 (2002) : 9-13. www.ncbi.nlm.nih.gov/PMC/articles/PMC1279140/.
- 12 Centres américains pour le contrôle et la prévention des maladies, « Santé mondiale — Polio », 2014. Consulté le 30 juin 2016. http://www.cdc.gov/polio/about/index.htm.
- 13 Centres américains pour le contrôle et la prévention des maladies, « Santé mondiale — Polio », 2014. Consulté le 30 juin 2016. http://www.cdc.gov/polio/about/index.htm.


