21.5 : Infections oculaires à protozoaires et helminthiques
- Page ID
- 187736
Objectifs d'apprentissage
- Identifiez deux parasites qui causent fréquemment des infections de la peau et des yeux
- Identifier les principales caractéristiques de maladies parasitaires spécifiques affectant la peau et les yeux
De nombreux protozoaires et helminthes parasites utilisent la peau ou les yeux comme porte d'entrée. Certains peuvent s'enfouir physiquement dans la peau ou les muqueuses de l'œil ; d'autres peuvent percer la barrière cutanée à la suite d'une piqûre d'insecte. D'autres encore profitent d'une blessure pour contourner la barrière cutanée et pénétrer dans l'organisme, tout comme les autres agents pathogènes opportunistes. Bien que de nombreux parasites pénètrent dans l'organisme par la peau, nous limiterons dans ce chapitre à ceux dont la peau ou les yeux sont le principal site d'infection. Les parasites qui pénètrent par la peau mais se déplacent vers un site d'infection différent seront abordés dans d'autres chapitres. De plus, nous limiterons notre discussion aux infections parasitaires microscopiques de la peau et des yeux. Les parasites macroscopiques tels que les poux, la gale, les acariens et les tiques sortent du cadre de ce texte.
Infections à acanthamoeba
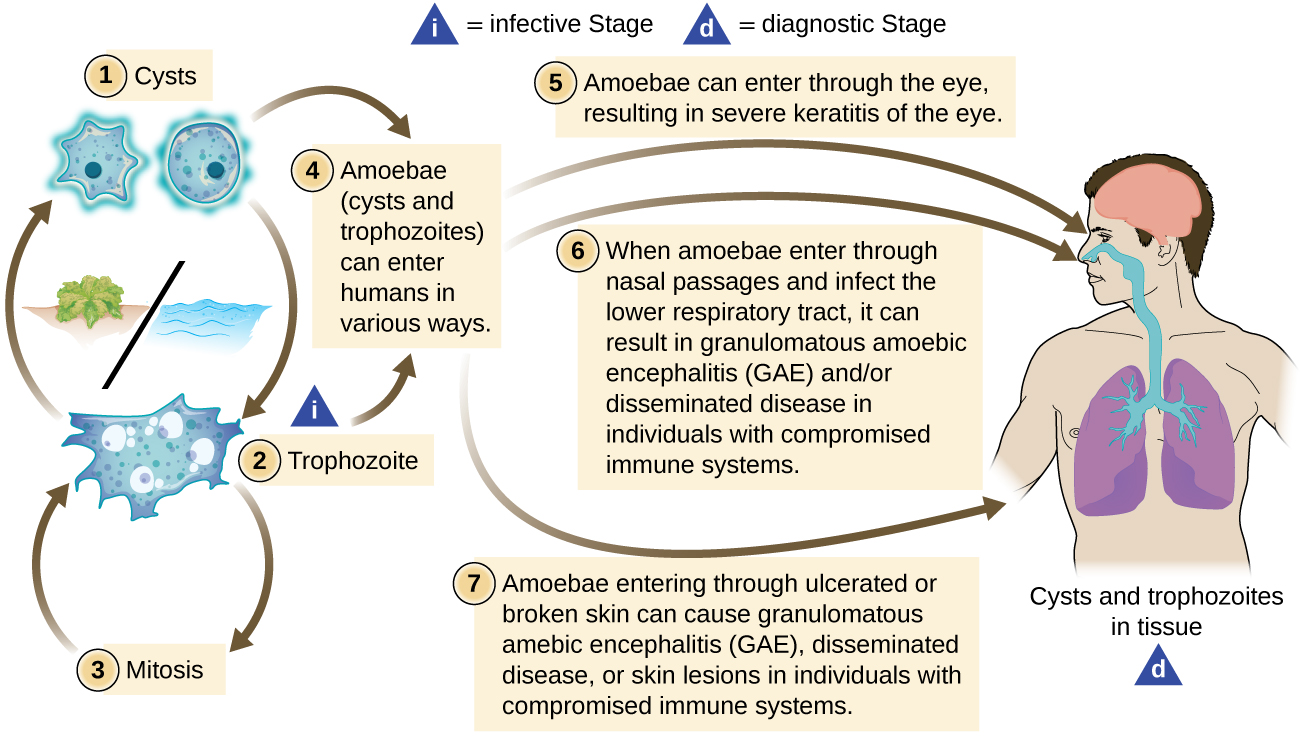
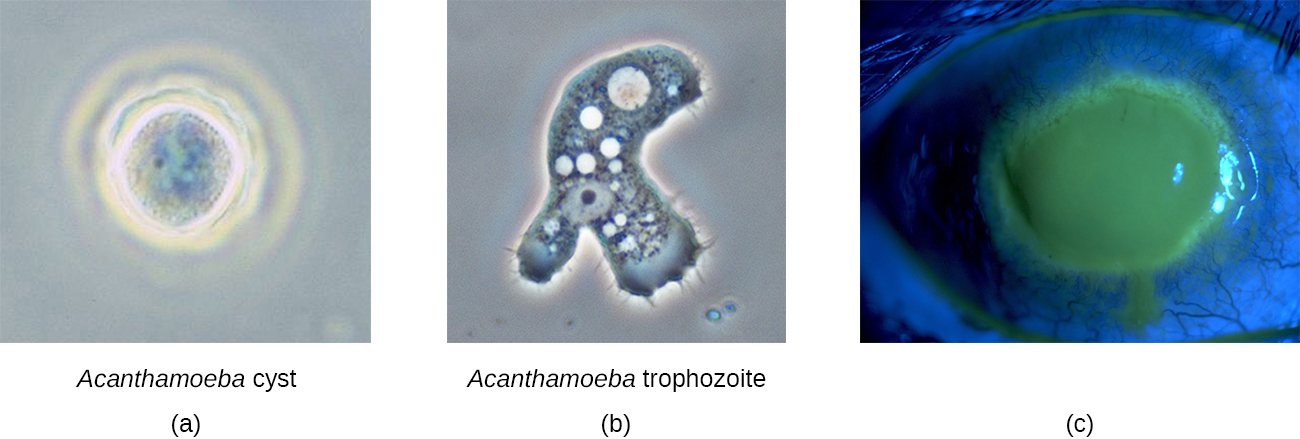
L'acanthamoeba est un genre d'amibes protozoaires libres qui sont communes dans les sols et les plans d'eau douce non chlorés. (C'est l'une des raisons pour lesquelles certaines piscines sont traitées au chlore.) Le genre contient quelques espèces parasitaires, dont certaines peuvent provoquer des infections des yeux, de la peau et du système nerveux. Ces infections peuvent parfois se propager et affecter d'autres systèmes corporels. Les infections cutanées peuvent se manifester par des abcès, des ulcères et des nodules. Lorsque les acanthamoebes infectent l'œil et provoquent une inflammation de la cornée, on parle de kératite à acanthamoeba. La figure\(\PageIndex{1}\) illustre le cycle de vie de l'acanthamoeba et les différents modes d'infection.
Bien que la kératite à acanthamoeba soit initialement légère, elle peut entraîner de graves lésions cornéennes, des troubles de la vision ou même la cécité si elle n'est pas traitée. À l'instar des infections oculaires impliquant P. aeruginosa, l'acanthamoeba présente un risque beaucoup plus élevé pour les porteurs de lentilles de contact, car l'amibe peut se développer dans l'espace situé entre les lentilles de contact et la cornée. La prévention par un entretien approprié des lentilles de contact est importante. Les lentilles doivent toujours être correctement désinfectées avant utilisation et ne doivent jamais être portées lorsque vous nagez ou que vous utilisez un bain à remous.
L'acanthamoeba peut également pénétrer dans l'organisme par d'autres voies, notamment par des blessures cutanées et par les voies respiratoires. Elle ne cause généralement pas de maladie, sauf chez les personnes immunodéprimées ; toutefois, dans de rares cas, l'infection peut se propager au système nerveux, entraînant une affection généralement fatale appelée encéphalite amibienne granulomateuse (EAG) (voir Maladies fongiques et parasitaires du système nerveux). Les infections disséminées, les lésions et la kératite à acanthamoeba peuvent être diagnostiquées en observant les symptômes et en examinant les échantillons des patients au microscope pour observer le parasite. Des biopsies cutanées peuvent être utilisées.
La kératite à acanthamoeba est difficile à traiter et un traitement rapide est nécessaire pour empêcher la progression de la maladie. La maladie nécessite généralement de trois à quatre semaines de traitement intensif pour se résoudre. Les traitements courants incluent les antiseptiques topiques (par exemple, le polyhexaméthylène biguanide, la chlorhexidine ou les deux), parfois avec des analgésiques ou des corticostéroïdes (bien que ces derniers soient controversés car ils inhibent le système immunitaire, ce qui peut aggraver l'infection). Des azoles sont également parfois prescrits. Les cas avancés de kératite peuvent nécessiter une greffe de cornée pour prévenir la cécité.
Exercice\(\PageIndex{1}\)
Comment sont contractées les infections à l'acanthamoeba ?
Loiase
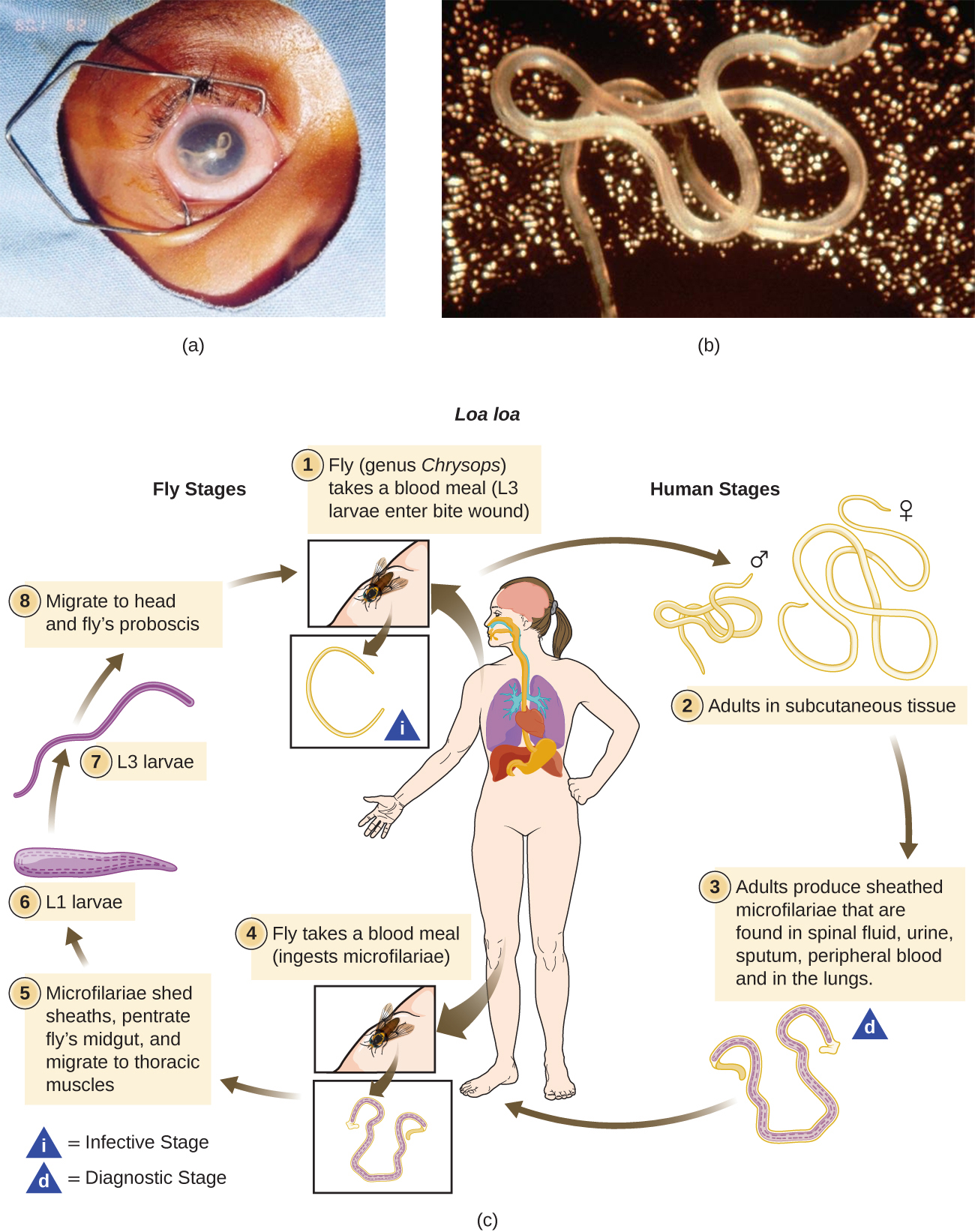
L'helminthe Loa loa, également connu sous le nom de ver oculaire africain, est un nématode qui peut provoquer la loase, une maladie endémique en Afrique de l'Ouest et du Centre (Figure\(\PageIndex{3}\)). La maladie ne survient pas en dehors de cette région, sauf lorsqu'elle est transportée par des voyageurs. Il est prouvé que les différences génétiques individuelles influent sur la susceptibilité au développement d'une loase après une infection par le ver Loa loa. Même dans les zones où les vers Loa loa sont courants, la maladie touche généralement moins de 30 % de la population. 1 Il a été suggéré que les voyageurs qui séjournent dans la région sont un peu plus susceptibles de développer des symptômes que la population autochtone, et que la présentation de l'infection peut différer. 2
Le parasite est transmis par les chevreuils (genre Chrysops), qui peuvent ingérer les larves d'un être humain infecté par un repas de sang (Figure\(\PageIndex{3}\)). Lorsque le cerf mord d'autres humains, il dépose les larves dans leur circulation sanguine. Après environ cinq mois dans le corps humain, certaines larves se transforment en vers adultes, qui peuvent atteindre plusieurs centimètres de long et vivre des années dans le tissu sous-cutané de l'hôte.
Le nom « ver oculaire » fait allusion à la migration visible des vers à travers la conjonctive de l'œil. Les vers adultes vivent dans les tissus sous-cutanés et peuvent se déplacer à une vitesse d'environ 1 cm par heure. Ils peuvent souvent être observés lors de la migration par l'œil, et parfois sous la peau ; en fait, c'est généralement ainsi que la maladie est diagnostiquée. Il est également possible de tester la présence d'anticorps, mais la présence d'anticorps n'indique pas nécessairement une infection en cours ; cela signifie simplement que la personne a été exposée à un moment donné. Certains patients sont asymptomatiques, mais chez d'autres, les vers migrateurs peuvent provoquer de la fièvre et des zones d'inflammation allergique appelées gonflements du calabar. Les vers qui migrent à travers la conjonctive peuvent provoquer des douleurs oculaires et des démangeaisons temporaires, mais il n'y a généralement pas de lésions oculaires durables. Certains patients présentent toute une série d'autres symptômes, tels que des démangeaisons généralisées, de l'urticaire et des douleurs articulaires et musculaires.
Les vers peuvent être retirés chirurgicalement de l'œil ou de la peau, mais ce traitement ne fait que soulager l'inconfort ; il ne guérit pas l'infection, qui implique de nombreux vers. Le traitement préféré est la diéthylcarbamazine, mais ce médicament provoque des effets secondaires graves chez certaines personnes, tels qu'une inflammation du cerveau et la mort possible chez les patients atteints d'infections graves. L'albendazole est également parfois utilisé si la diéthylcarbamazine n'est pas appropriée ou n'est pas efficace. Si elle n'est pas traitée pendant de nombreuses années, la loase peut endommager les reins, le cœur et les poumons, bien que ces symptômes soient rares.
Exercice\(\PageIndex{2}\)
Décrivez la méthode la plus courante pour diagnostiquer la loase.
Regardez une vidéo d'une microfilaire de Loa loa en direct au microscope.
Infections parasitaires de la peau et des yeux
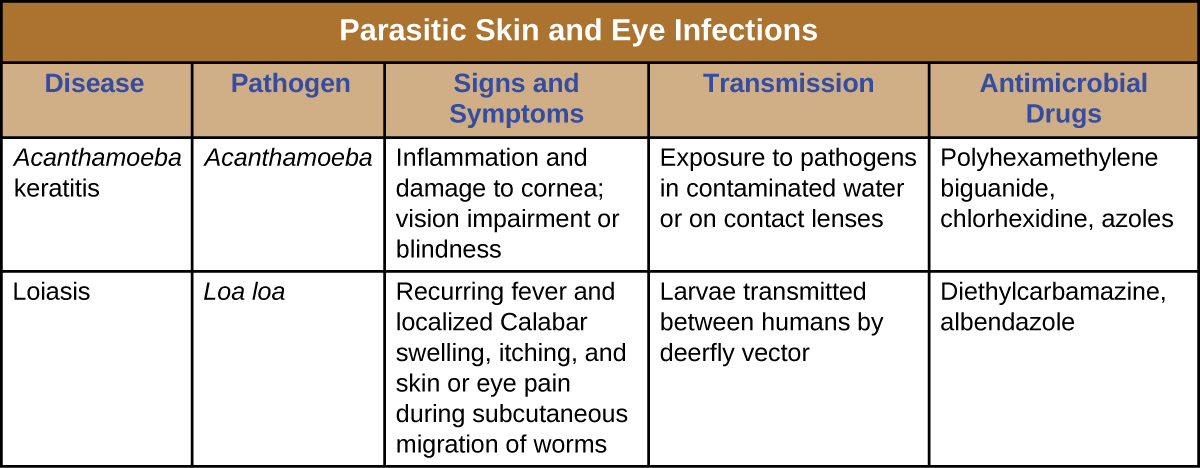
Le protozoaire Acanthamoeba et l'helminthe Loa loa sont deux parasites capables de provoquer des infections de la peau et des yeux. La figure\(\PageIndex{4}\) résume les caractéristiques de certaines infections fongiques courantes de la peau.
Concepts clés et résumé
Le protozoaire Acanthamoeba et l'helminthe Loa loa sont deux parasites qui peuvent percer la barrière cutanée et provoquer des infections de la peau et des yeux. La kératite à acanthamoeba est une infection parasitaire de l'œil qui résulte souvent d'une mauvaise désinfection des lentilles de contact ou d'une baignade pendant le port de lentilles de contact. La loiase, ou ver oculaire, est une maladie endémique en Afrique causée par des vers parasites qui infectent les tissus sous-cutanés de la peau et des yeux. Il est transmis par des vecteurs de mouches à chevreuil.
Notes
- 1 Garcia, A. et coll. « Épidémiologie génétique de la microfilarémie prédisposition à l'hôte dans la loiase humaine. » Médecine tropicale et santé internationale 4 (1999) 8:565 —74. http://www.ncbi.nlm.nih.gov/pubmed/10499080. Consulté le 14 septembre 2016.
- 2 Spinello, A., et coll. « Filariose de Loa loa importée : trois cas et examen des cas signalés dans des pays non endémiques au cours des 25 dernières années. » Journal international des maladies infectieuses 16 (2012) 9 : e649—e662. DOI : http://dx.doi.org/10.1016/j.ijid.2012.05.1023.


