28.7 : Modèles d'héritage
- Page ID
- 194952
Objectifs d'apprentissage
- Différencier le génotype du phénotype
- Décrire comment les allèles déterminent les traits d'une personne
- Résumez les expériences de Mendel et associez-les à la génétique humaine
- Expliquer l'hérédité des maladies génétiques autosomiques dominantes, récessives et liées au sexe
Nous avons discuté des événements qui ont conduit au développement d'un nouveau-né. Mais qu'est-ce qui rend chaque nouveau-né unique ? La réponse réside, bien entendu, dans l'ADN du sperme et de l'ovocyte qui se sont combinés pour produire la première cellule diploïde, le zygote humain.
Du génotype au phénotype
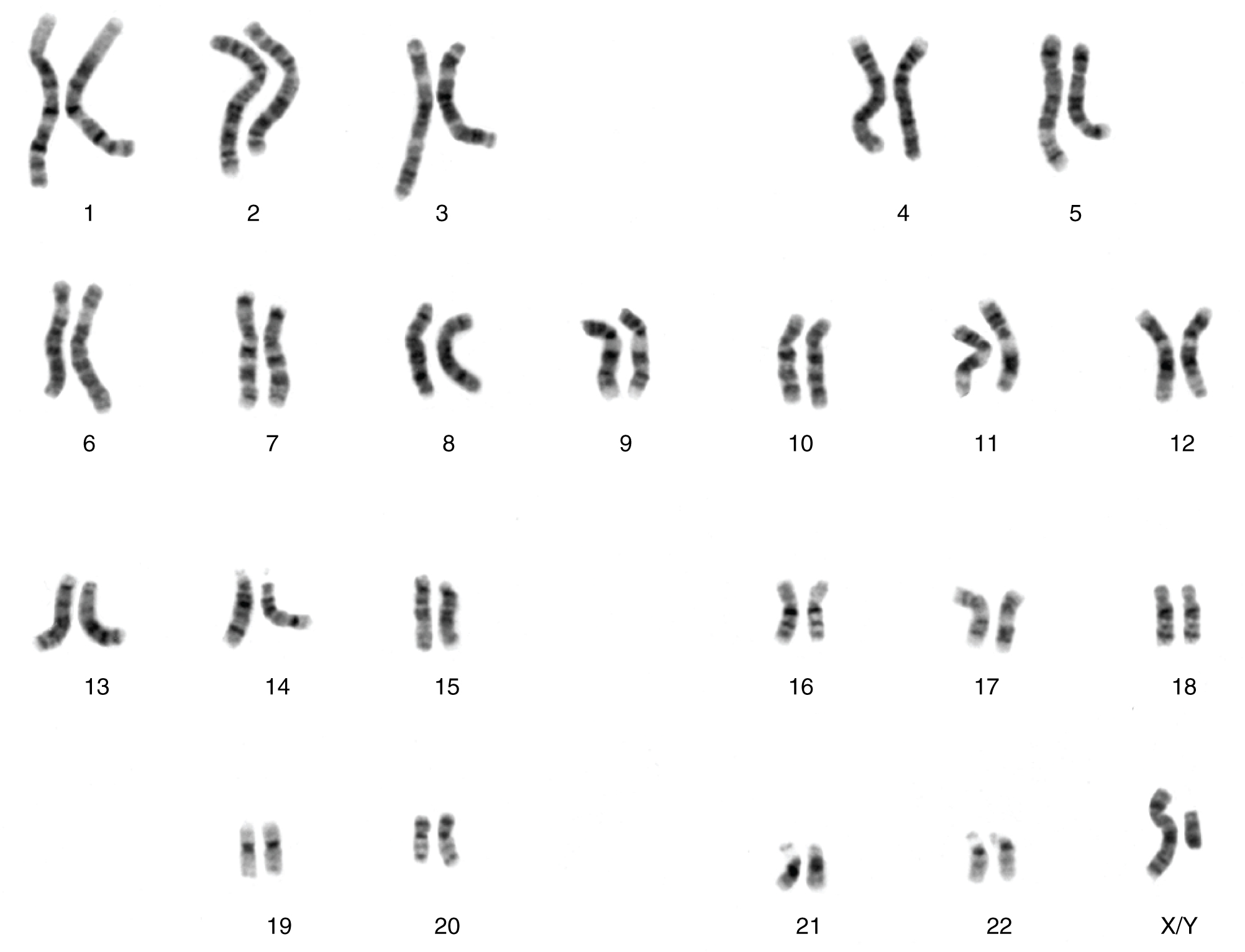
Chaque cellule du corps humain possède un ensemble complet d'ADN stocké dans 23 paires de chromosomes. La figure\(\PageIndex{1}\) montre les paires dans un arrangement systématique appelé caryotype. Parmi ceux-ci se trouve une paire de chromosomes, appelés chromosomes sexuels, qui détermine le sexe de l'individu (XX chez les femmes, XY chez les hommes). Les 22 paires de chromosomes restantes sont appelées chromosomes autosomiques. Chacun de ces chromosomes est porteur de centaines, voire de milliers de gènes, dont chacun code pour l'assemblage d'une protéine particulière, c'est-à-dire que les gènes sont « exprimés » sous forme de protéines. La constitution génétique complète d'un individu est appelée génotype. Les caractéristiques exprimées par les gènes, qu'elles soient physiques, comportementales ou biochimiques, sont le phénotype d'une personne.
Vous héritez d'un chromosome par paire, soit un complément complet de 23, de chaque parent. Cela se produit lorsque le sperme et l'ovocyte se combinent au moment de la conception. Les chromosomes homologues, c'est-à-dire ceux qui forment une paire complémentaire, possèdent des gènes ayant les mêmes caractéristiques au même endroit sur le chromosome. Comme une copie d'un gène, un allèle, est héritée de chaque parent, les allèles de ces paires complémentaires peuvent varier. Prenons par exemple un allèle qui code pour les fossettes. Un enfant peut hériter de l'allèle codant pour les fossettes du chromosome du père et de l'allèle codant pour une peau lisse (sans fossettes) sur le chromosome de la mère.
Bien qu'une personne puisse avoir deux allèles identiques pour un seul gène (état homozygote), il est également possible qu'une personne ait deux allèles différents (état hétérozygote). Les deux allèles peuvent interagir de différentes manières. L'expression d'un allèle peut être dominante, l'activité de ce gène masquant l'expression d'un allèle non dominant, ou récessif. Parfois, la domination est complète ; d'autres fois, elle est incomplète. Dans certains cas, les deux allèles sont exprimés en même temps sous une forme d'expression appelée codominance.
Dans le scénario le plus simple, une seule paire de gènes déterminera une seule caractéristique héréditaire. Cependant, il est assez fréquent que plusieurs gènes interagissent pour conférer une caractéristique. Par exemple, huit gènes ou plus, chacun ayant ses propres allèles, déterminent la couleur des yeux chez l'homme. De plus, bien qu'une personne ne puisse avoir que deux allèles correspondant à un gène donné, il existe généralement plus de deux allèles dans une population. Ce phénomène est appelé allèles multiples. Par exemple, trois allèles différents codent pour le groupe sanguin ABO ; ils sont désignés I A, I B et i.
Plus de 100 ans d'études génétiques théoriques et expérimentales, ainsi que le séquençage et l'annotation plus récents du génome humain, ont aidé les scientifiques à mieux comprendre comment le génotype d'un individu est exprimé sous forme de phénotype. Cet ensemble de connaissances peut aider les scientifiques et les professionnels de la santé à prédire, ou du moins à estimer, certaines des caractéristiques dont héritera une progéniture en examinant les génotypes ou les phénotypes des parents. L'une des applications importantes de ces connaissances consiste à identifier le risque d'une personne de développer certaines maladies génétiques héréditaires. Cependant, la plupart des maladies ont un mode de transmission multigénique et peuvent également être affectées par l'environnement. Par conséquent, l'examen des génotypes ou des phénotypes des parents d'une personne ne fournira que des informations limitées sur le risque d'hériter d'une maladie. Ce n'est que pour une poignée de maladies monogéniques que les tests génétiques permettent aux cliniciens de calculer la probabilité qu'un enfant né des deux parents testés hérite d'une maladie spécifique.
La théorie de l'héritage de Mendel
Notre compréhension contemporaine de la génétique repose sur les travaux d'un moine du XIXe siècle. En travaillant au milieu des années 1800, bien avant que quiconque ne connaisse les gènes ou les chromosomes, Gregor Mendel a découvert que les pois de jardin transmettaient leurs caractéristiques physiques aux générations suivantes de manière discrète et prévisible. Lorsqu'il a accouplé ou croisé deux plants de pois reproducteurs purs qui se distinguaient par une certaine caractéristique, la progéniture de première génération ressemblait tous à l'un des parents. Par exemple, lorsqu'il a croisé des plants de pois grands et nains reproducteurs purs, tous les descendants étaient grands. Mendel a qualifié la taille de dominante parce qu'elle s'exprimait chez la progéniture lorsqu'elle était présente chez un parent de race pure. Il a qualifié le nanisme de récessif parce qu'il était masqué chez la progéniture si l'un des parents de race pure possédait la caractéristique dominante. Notez que la taille et le nanisme sont des variations de la caractéristique de la hauteur. Mendel a qualifié cette variation de trait. Nous savons maintenant que ces traits sont l'expression de différents allèles du gène codant pour la hauteur.
Mendel a réalisé des milliers de croisements sur des plants de pois présentant des caractères différents pour une variété de caractéristiques. Et il est arrivé à plusieurs reprises aux mêmes résultats : parmi les traits qu'il a étudiés, l'un était toujours dominant et l'autre était toujours récessif. (Souvenez-vous toutefois que cette relation dominante—récessive entre allèles n'est pas toujours le cas ; certains allèles sont codominants et parfois la dominance est incomplète.)
À l'aide de sa compréhension des traits dominants et récessifs, Mendel a vérifié si un trait récessif pouvait être complètement perdu dans une lignée de pois ou s'il réapparaîtrait au cours d'une génération ultérieure. En croisant entre eux les descendants de parents de race pure de deuxième génération, il a démontré que cette dernière était vraie : des caractères récessifs sont réapparus chez les plantes de troisième génération dans un rapport de 3:1 (trois descendants ayant le caractère dominant et un ayant le caractère récessif). Mendel a ensuite proposé que des caractéristiques telles que la taille soient déterminées par des « facteurs » héréditaires transmis, un par chaque parent, et hérités par paires par la progéniture.
Dans le langage de la génétique, la théorie de Mendel appliquée aux humains indique que si un individu reçoit deux allèles dominants, un de chaque parent, le phénotype de l'individu exprimera le trait dominant. Si un individu reçoit deux allèles récessifs, le trait récessif sera exprimé dans le phénotype. Les individus qui possèdent deux allèles identiques pour un gène donné, qu'il soit dominant ou récessif, sont considérés comme homozygotes pour ce gène (homo- = « identique »). À l'inverse, un individu qui possède un allèle dominant et un allèle récessif est considéré comme hétérozygote pour ce gène (hétéro- = « différent » ou « autre »). Dans ce cas, le trait dominant sera exprimé et l'individu sera phénotypiquement identique à un individu qui possède deux allèles dominants pour le trait.
En génétique, il est courant d'utiliser des lettres majuscules et minuscules pour représenter les allèles dominants et récessifs. Si l'on prend les plants de pois de Mendel comme exemple, si un plant de pois de grande taille est homozygote, il possédera deux grands allèles (TT). Un plant de pois nain doit être homozygote car son nanisme ne peut s'exprimer que lorsque deux allèles récessifs sont présents (tt). Un plant de pois hétérozygote (Tt) serait grand et phénotypiquement impossible à distinguer d'un plant de pois homozygote de grande taille en raison du grand allèle dominant. Mendel a déduit qu'un ratio de 3:1 entre les plantes dominantes et récessives serait produit par la ségrégation aléatoire de facteurs héréditaires (gènes) lors du croisement de deux plants de pois hétérozygotes. En d'autres termes, pour tout gène donné, les parents sont également susceptibles de transmettre l'un ou l'autre de leurs allèles à leur progéniture par un gamète haploïde, et le résultat sera exprimé selon un schéma dominant—récessif si les deux parents sont hétérozygotes pour ce trait.
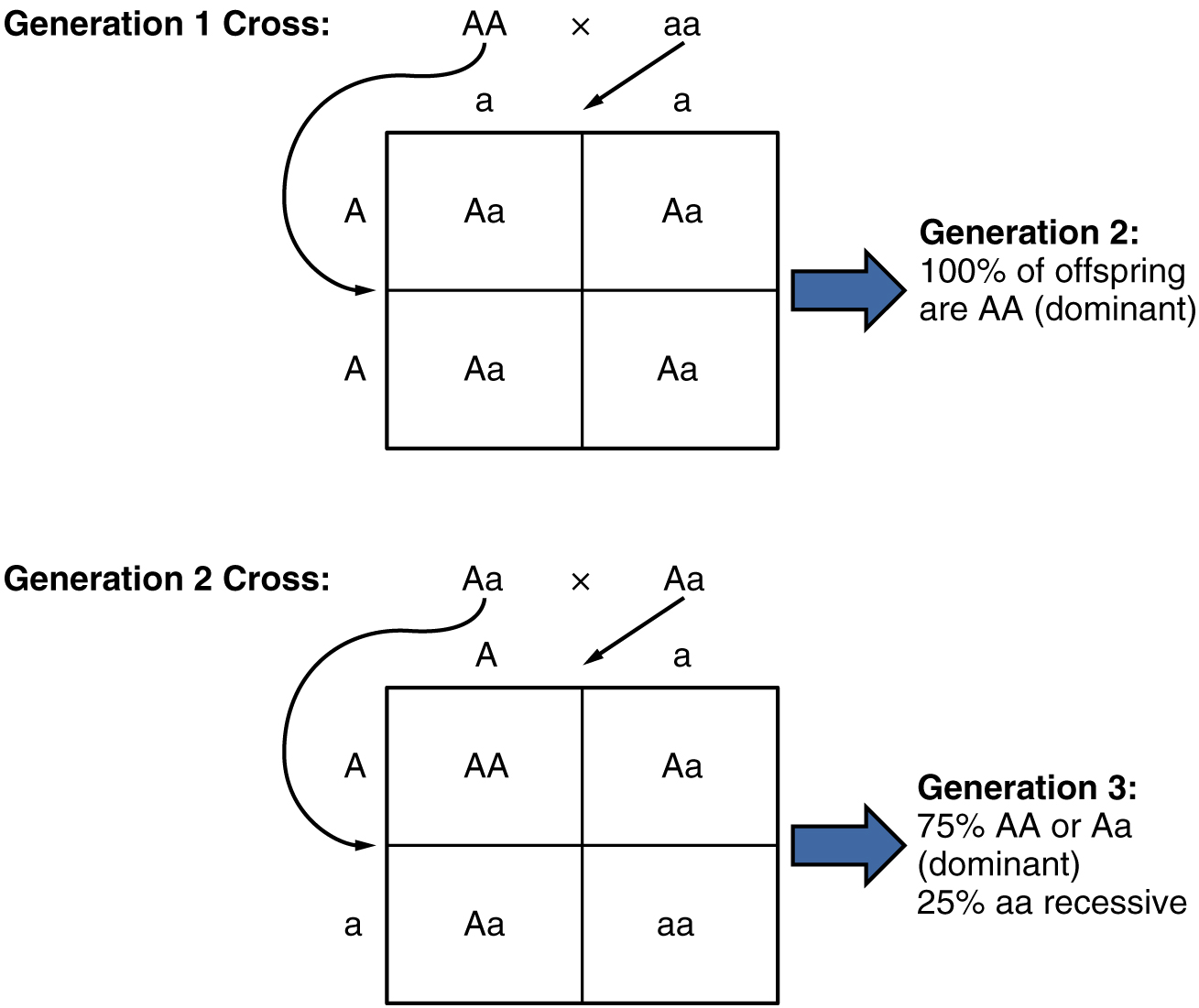
En raison de la ségrégation aléatoire des gamètes, les lois du hasard et de la probabilité entrent en jeu lorsqu'il s'agit de prédire la probabilité d'un phénotype donné. Considérons un croisement entre un individu possédant deux allèles dominants pour un trait (AA) et un individu possédant deux allèles récessifs pour le même trait (aa). Tous les gamètes parentaux de l'individu dominant seraient A, et tous les gamètes parentaux de l'individu récessif seraient A (Figure\(\PageIndex{2}\)). Tous les descendants de cette deuxième génération, héritant d'un allèle de chaque parent, porteraient le génotype Aa, et la probabilité d'exprimer le phénotype de l'allèle dominant serait de 4 sur 4, soit 100 pour cent.
Cela semble assez simple, mais le modèle d'héritage devient intéressant lorsque les individus Aa de deuxième génération sont croisés. Dans cette génération, 50 pour cent des gamètes de chaque parent sont A et les 50 pour cent restants sont a. Selon le principe de ségrégation aléatoire de Mendel, les combinaisons possibles de gamètes que la progéniture peut recevoir sont AA, Aa, aA (qui est identique à Aa) et aa. Comme la ségrégation et la fécondation sont aléatoires, chaque progéniture a 25 pour cent de chances de recevoir l'une de ces combinaisons. Par conséquent, si un croisement Aa × Aa était réalisé 1000 fois, environ 250 (25 pour cent) de la progéniture seraient AA ; 500 (50 pour cent) seraient Aa (c'est-à-dire Aa plus aA) ; et 250 (25 pour cent) seraient aa. Le ratio génotypique pour ce modèle de transmission est de 1:2:1. Cependant, nous avons déjà établi que les individus AA et Aa (et aA) expriment tous le trait dominant (c'est-à-dire qu'ils partagent le même phénotype) et peuvent donc être combinés en un seul groupe. Le résultat est un ratio phénotypique de 3 pour 1 de Mendel sur la troisième génération.
L'observation des plants de pois par Mendel comprenait également de nombreux croisements impliquant de multiples traits, ce qui l'a incité à formuler le principe d'un assortiment indépendant. La loi stipule que les membres d'une paire de gènes (allèles) d'un parent seront triés indépendamment des autres paires de gènes lors de la formation des gamètes. Appliqué aux plants de pois, cela signifie que les allèles associés aux différents traits de la plante, tels que la couleur, la hauteur ou le type de graine, seront triés indépendamment les uns des autres. Cela est vrai, sauf lorsque deux allèles se trouvent à proximité l'un de l'autre sur le même chromosome. Un assortiment indépendant offre une grande diversité de progéniture.
La génétique mendélienne représente les fondamentaux de l'hérédité, mais il y a deux qualificatifs importants à prendre en compte lors de l'application des résultats de Mendel à des études sur l'héritage chez l'homme. Tout d'abord, comme nous l'avons déjà noté, tous les gènes ne sont pas hérités selon un schéma dominant—récessif. Bien que tous les individus diploïdes possèdent deux allèles pour chaque gène, les paires d'allèles peuvent interagir pour créer plusieurs types de modèles héréditaires, y compris une dominance et une codominance incomplètes.
Ensuite, Mendel a réalisé ses études en utilisant des milliers de plants de pois. Il a pu identifier un ratio phénotypique de 3:1 chez les enfants de deuxième génération parce que la grande taille de son échantillon a surmonté l'influence de la variabilité due au hasard. En revanche, aucun couple humain n'a jamais eu de milliers d'enfants. Si nous savions qu'un homme et une femme sont tous deux hétérozygotes pour une maladie génétique récessive, nous pouvons prédire qu'un enfant sur quatre serait atteint de cette maladie. Dans la vie réelle, cependant, l'influence du hasard pourrait modifier ce ratio de manière significative. Par exemple, si un homme et une femme sont tous deux hétérozygotes pour la mucoviscidose, une maladie génétique récessive qui ne se manifeste que lorsque la personne présente deux allèles défectueux, on peut s'attendre à ce qu'un enfant sur quatre soit atteint de mucoviscidose. Cependant, il est tout à fait possible qu'ils aient sept enfants, dont aucun n'est atteint, ou qu'ils aient deux enfants, tous deux atteints. Pour chaque enfant, la présence ou l'absence d'un trouble génétique unique dépend des allèles que l'enfant hérite de ses parents.
Héritage autosomique dominant
Dans le cas de la mucoviscidose, le trouble est récessif par rapport au phénotype normal. Cependant, une anomalie génétique peut dominer le phénotype normal. Lorsque l'allèle dominant est situé sur l'une des 22 paires d'autosomes (chromosomes non sexuels), nous appelons son modèle héréditaire autosomique dominant. La neurofibromatose de type I est un exemple de trouble autosomique dominant, une maladie qui provoque la formation de tumeurs dans le système nerveux et entraîne des malformations de la peau et du squelette. Prenons un couple dans lequel l'un des parents est hétérozygote pour ce trouble (et qui est donc atteint de neurofibromatose), Nn, et l'un des parents est homozygote pour le gène normal, nn. Le parent hétérozygote aurait 50 pour cent de chances de transmettre l'allèle dominant de ce trouble à sa progéniture, et le parent homozygote transmettrait toujours l'allèle normal. Par conséquent, quatre génotypes possibles de descendance sont également susceptibles d'apparaître : Nn, Nn, nn et nn. C'est-à-dire que chaque enfant de ce couple aurait 50 pour cent de chances d'hériter d'une neurofibromatose. Ce modèle d'héritage est illustré sur la figure\(\PageIndex{3}\), sous une forme appelée carré de Punnett, du nom de son créateur, le généticien britannique Reginald Punnett.
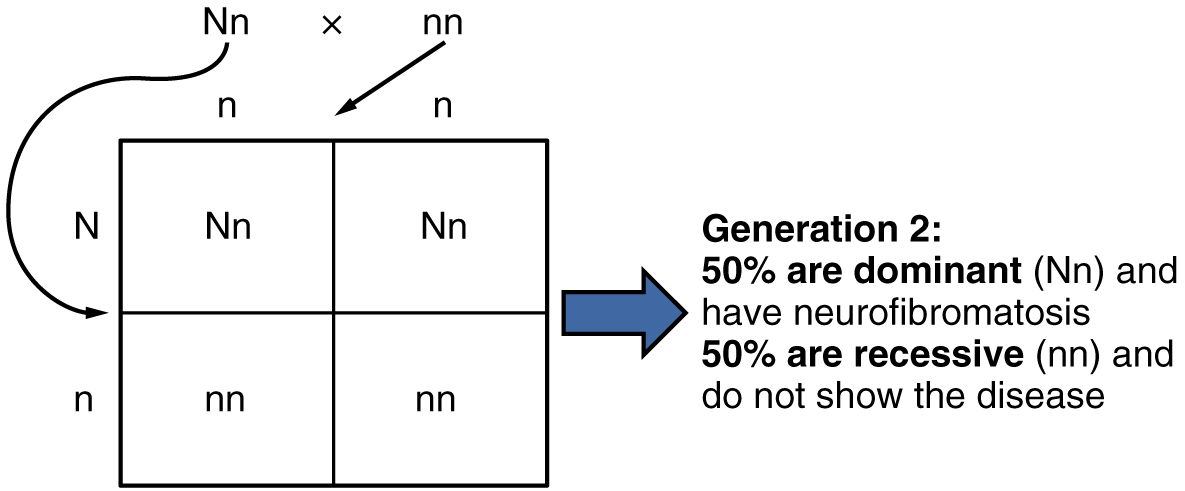
Les autres maladies génétiques héritées selon ce schéma sont le nanisme achondroplasique, le syndrome de Marfan et la maladie de Huntington. Comme les troubles autosomiques dominants se traduisent par la présence d'un seul gène, une personne atteinte de cette maladie saura qu'elle possède au moins un gène défectueux. L'expression de la maladie peut se manifester plus tard dans la vie, après les années de procréation, ce qui est le cas de la maladie de Huntington (abordée plus en détail plus loin dans cette section).
Héritage autosomique récessif
Lorsqu'un trouble génétique est hérité selon un schéma autosomique récessif, le trouble correspond au phénotype récessif. Les personnes hétérozygotes ne présenteront pas de symptômes de ce trouble, car leur gène non affecté compensera. Un tel individu s'appelle un transporteur. Les porteurs d'un trouble autosomique récessif peuvent ne jamais connaître leur génotype à moins d'avoir un enfant atteint de ce trouble.
La fibrose kystique (CF), que nous avons introduite plus tôt, est un exemple de trouble autosomique récessif. La mucoviscidose se caractérise par l'accumulation chronique d'un mucus épais et tenace dans les poumons et le tube digestif. Il y a des décennies, les enfants atteints de mucoviscidose vivaient rarement jusqu'à l' Grâce aux progrès de la technologie médicale, la durée de vie moyenne dans les pays développés a augmenté jusqu'au milieu de l'âge adulte. La mucoviscidose est un trouble relativement courant qui touche environ 1 Caucasien sur 2 000. Un enfant né de deux personnes porteuses de la mucoviscidose aurait 25 pour cent de chances d'hériter de la maladie. C'est le même ratio dominant:récessif de 3:1 que Mendel a observé chez ses plants de pois qui s'appliquerait ici. Le schéma est illustré dans la figure\(\PageIndex{4}\), à l'aide d'un diagramme qui suit l'incidence probable d'un trouble autosomique récessif sur la base des génotypes parentaux.
D'autre part, un enfant né d'une personne porteuse de mucoviscidose et d'une personne présentant deux allèles non affectés aurait une probabilité de 0 pour cent d'hériter de la mucoviscidose, mais aurait 50 pour cent de chances d'en être porteur. D'autres exemples de maladies génétiques récessives autosomiques incluent la drépanocytose, un trouble neurologique mortel, la maladie de Tay—Sachs, et le trouble métabolique phénylcétonurie.

Héritage dominant ou récessif lié à l'X
Un schéma de transmission lié à l'X implique des gènes situés sur le chromosome X de la 23e paire (Figure\(\PageIndex{5}\)). Rappelons qu'un homme possède un chromosome X et un chromosome Y. Lorsqu'un père transmet un chromosome Y, l'enfant est un homme, et lorsqu'il transmet un chromosome X, l'enfant est une femme. Une mère ne peut transmettre qu'un chromosome X, car ses deux chromosomes sexuels sont des chromosomes X.
Lorsqu'un allèle anormal d'un gène présent sur le chromosome X est dominant par rapport à l'allèle normal, le schéma est décrit comme dominant lié à l'X. C'est le cas du rachitisme résistant à la vitamine D : un père atteint transmettrait le gène de la maladie à toutes ses filles, mais à aucun de ses fils, car il ne donne que le chromosome Y à ses fils (voir Figure 28.7.5.a). Si c'est la mère qui est atteinte, tous ses enfants, hommes ou femmes, auraient 50 % de chances d'hériter du trouble, car elle ne peut transmettre le chromosome X qu'à ses enfants (voir Figure\(\PageIndex{5}\) .b). Pour une femme atteinte, le profil héréditaire serait identique à celui d'un modèle de transmission autosomique dominant dans lequel l'un des parents est hétérozygote et l'autre est homozygote pour le gène normal.
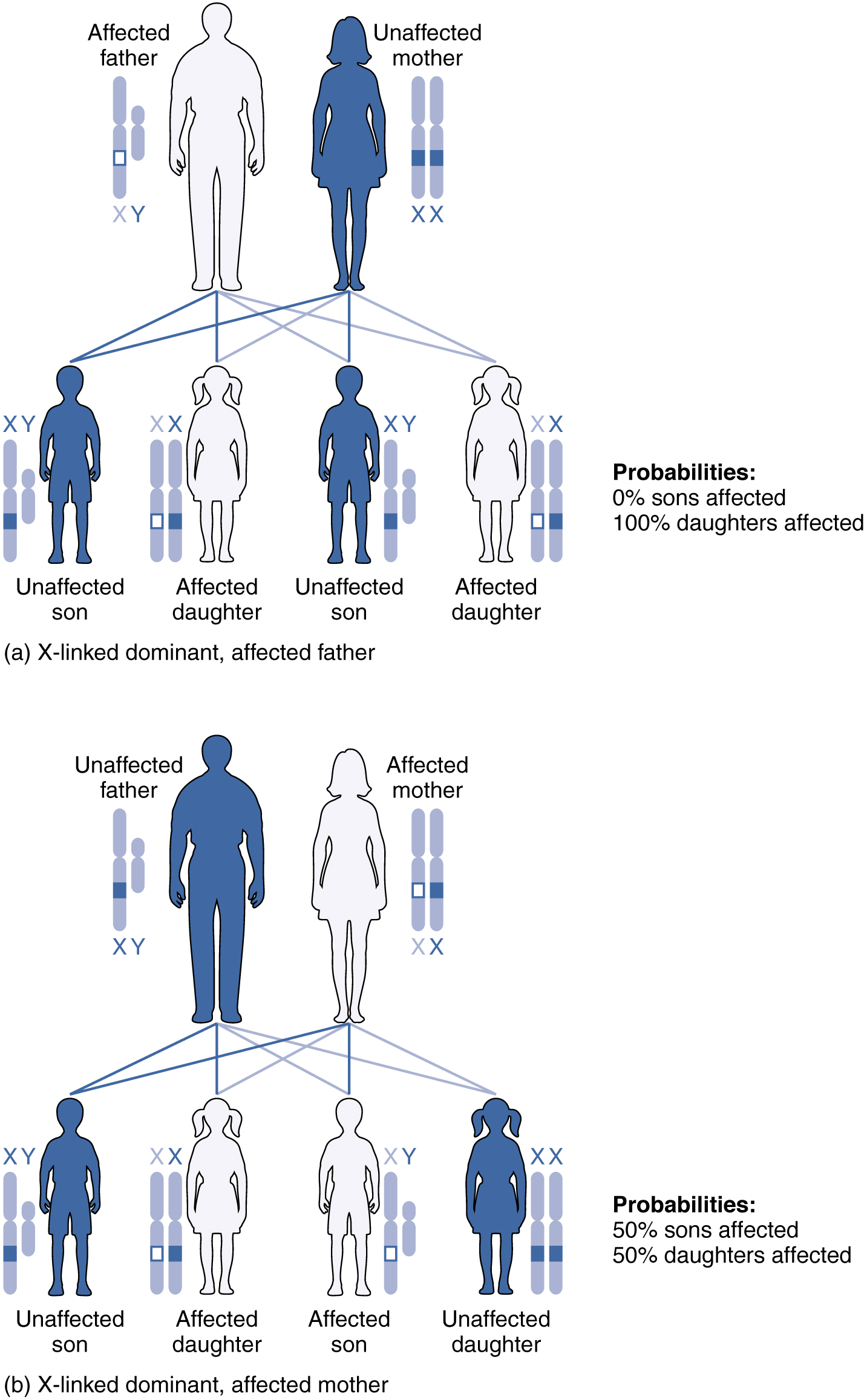
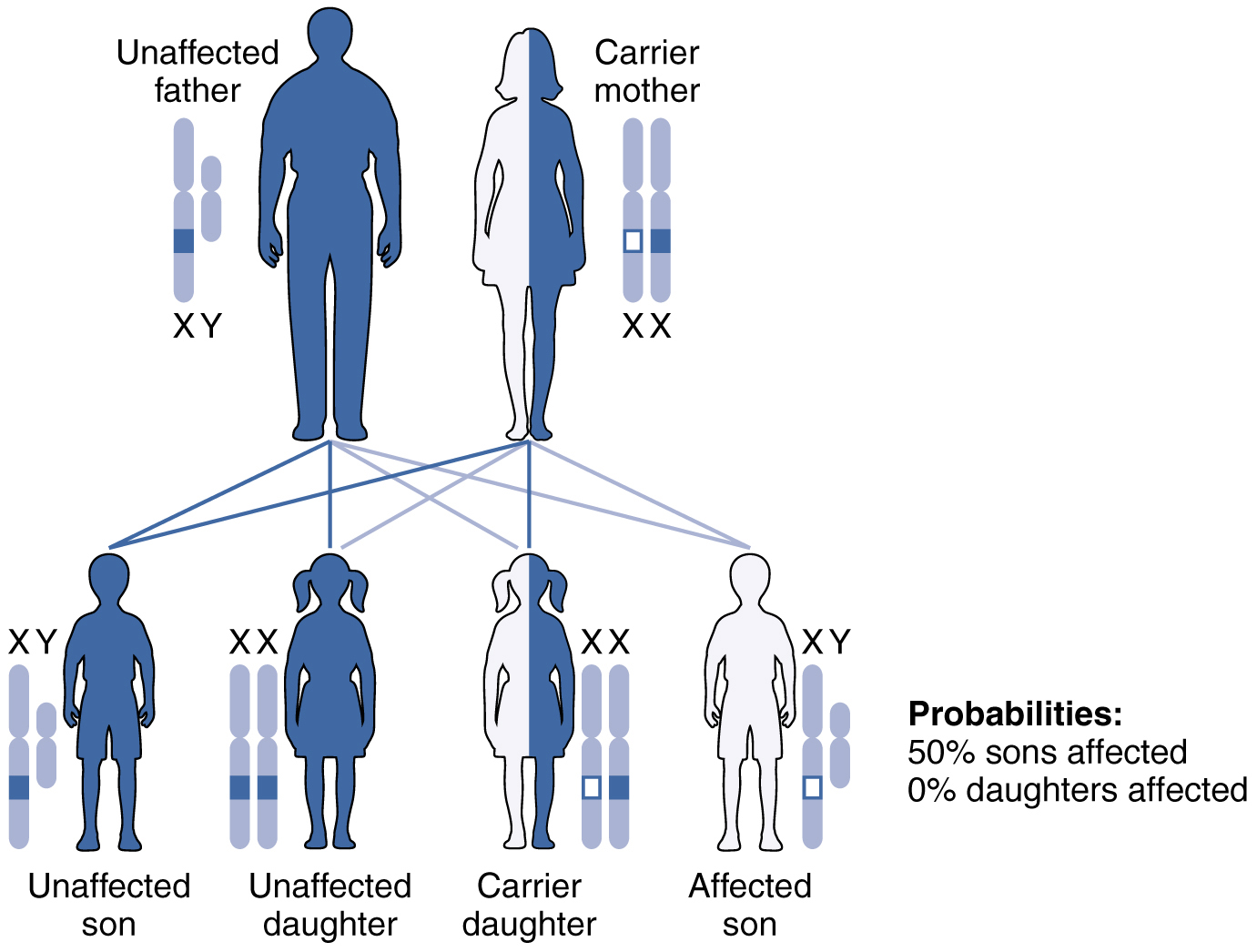
L'hérédité récessive liée à l'X est beaucoup plus fréquente car les femmes peuvent être porteuses de la maladie tout en ayant un phénotype normal. Les maladies transmises par transmission récessive liée à l'X incluent le daltonisme, le trouble de la coagulation sanguine, l'hémophilie et certaines formes de dystrophie musculaire. Pour un exemple d'héritage récessif lié à l'X, considérez les parents dont la mère n'est pas atteinte et le père est normal. Aucune des filles ne serait atteinte de la maladie parce qu'elles reçoivent un gène normal de leur père. Cependant, ils ont 50 pour cent de chances de recevoir le gène de la maladie de leur mère et d'en devenir porteurs. En revanche, 50 pour cent des fils seraient touchés (Figure\(\PageIndex{6}\)).
Dans le cas des maladies récessives liées à l'X, les hommes sont atteints de la maladie ou sont génotypiquement normaux ; ils ne peuvent pas être porteurs. Les femmes peuvent toutefois être génotypiquement normales, porteuses d'un phénotype normal ou atteintes de la maladie. Une fille peut hériter du gène d'une maladie récessive liée à l'X lorsque sa mère est porteuse ou atteinte, ou que son père est atteint. La fille ne sera affectée par la maladie que si elle hérite d'un gène récessif lié à l'X des deux parents. Comme vous pouvez l'imaginer, les troubles récessifs liés à l'X touchent beaucoup plus d'hommes que de femmes. Par exemple, le daltonisme touche au moins 1 homme sur 20, mais seulement environ 1 femme sur 400.
Autres modèles d'hérédité : dominance incomplète, codominance et allèles létaux
Les maladies génétiques ne sont pas toutes héréditaires selon un schéma dominant—récessif. En cas de dominance incomplète, les descendants expriment un phénotype hétérozygote intermédiaire entre le trait dominant homozygote d'un parent et le trait récessif homozygote de l'autre parent. On peut en voir un exemple chez les mufliers lorsque des plantes à fleurs rouges et des plantes à fleurs blanches sont croisées pour produire des plantes à fleurs roses. Chez l'homme, une dominance incomplète se produit avec l'un des gènes responsables de la texture des cheveux. Lorsque l'un des parents transmet un allèle des cheveux bouclés (l'allèle incomplètement dominant) et que l'autre parent transmet un allèle des cheveux raides, l'effet sur la progéniture sera intermédiaire, ce qui donnera des cheveux ondulés.
La codominance se caractérise par l'expression égale, distincte et simultanée des différents allèles des deux parents. Ce schéma diffère des caractéristiques mixtes intermédiaires observées dans une dominance incomplète. Un exemple classique de codominance chez l'homme est le groupe sanguin ABO. Les personnes sont du groupe sanguin A si elles possèdent un allèle d'une enzyme qui facilite la production d'antigène de surface A sur leurs érythrocytes. Cet allèle est désigné I A. De la même manière, les personnes sont du groupe sanguin B si elles expriment une enzyme pour la production d'antigène de surface B. Les personnes qui possèdent des allèles pour les deux enzymes (I A et I B) produisent les deux antigènes de surface A et B. Elles appartiennent donc au groupe sanguin AB. Comme l'effet des deux allèles (ou enzymes) est observé, nous disons que les allèles I A et I B sont codominants. Il existe également un troisième allèle qui détermine le groupe sanguin. Cet allèle (i) produit une enzyme non fonctionnelle. Les personnes qui ont deux allèles i ne produisent pas d'antigènes de surface A ou B : elles ont du sang de type O. Si une personne possède les allèles I A et i, elle aura le groupe sanguin A. Notez que peu importe qu'une personne possède deux allèles I A ou un allèle I A et un allèle i. Dans les deux cas, la personne est du groupe sanguin A. Comme I A masque i, on dit que I A est dominant par rapport à i. \(\PageIndex{1}\)Le tableau résume l'expression du groupe sanguin.
Tableau\(\PageIndex{1}\)
| Expression des groupes sanguins | ||
|---|---|---|
| Groupe sanguin | Génotype | Modèle d'héritage |
| UN | I A I A ou I A i | I A est dominant par rapport à i |
| B | I B I B ou I B i | I B est dominant par rapport à i |
| ABDO | JE SUIS I B | I A est co-dominant à I B |
| O | ii | Deux allèles récessifs |
Certaines combinaisons d'allèles peuvent être mortelles, c'est-à-dire qu'elles empêchent l'individu de se développer in utero ou qu'elles raccourcissent la durée de vie. Dans le cas d'une transmission létale récessive, un enfant né de deux parents hétérozygotes (porteurs) et ayant hérité de l'allèle défectueux des deux ne survivrait pas. Tay-Sachs, une maladie mortelle du système nerveux, en est un exemple. Dans ce trouble, les parents qui possèdent une copie de l'allèle du trouble sont porteurs. S'ils transmettent tous deux leur allèle anormal, leur progéniture développera la maladie et mourra dans l'enfance, généralement avant l'âge de 5 ans.
Les modèles d'hérédité létale dominants sont beaucoup plus rares car ni les hétérozygotes ni les homozygotes ne survivent. Bien entendu, les allèles létaux dominants qui apparaissent naturellement par mutation et provoquent des fausses couches ou des mortinaissances ne sont jamais transmis aux générations suivantes. Cependant, certains allèles létaux dominants, tels que l'allèle de la maladie de Huntington, réduisent l'espérance de vie mais peuvent ne pas être identifiés avant que la personne atteigne l'âge de procréer et ait eu des enfants. La maladie de Huntington provoque une dégénérescence irréversible des cellules nerveuses et la mort chez 100 % des personnes atteintes, mais elle peut ne pas s'exprimer avant que la personne atteigne l'âge mûr. De cette manière, les allèles létaux dominants peuvent être maintenus dans la population humaine. Les personnes ayant des antécédents familiaux de maladie de Huntington se voient généralement proposer des conseils génétiques, qui peuvent les aider à décider si elles souhaitent ou non subir un test de dépistage du gène défectueux.
Des mutations
Une mutation est une modification de la séquence des nucléotides de l'ADN qui peut ou non affecter le phénotype d'une personne. Les mutations peuvent survenir spontanément à la suite d'erreurs lors de la réplication de l'ADN, ou elles peuvent résulter d'agressions environnementales telles que les radiations, certains virus ou l'exposition à la fumée de tabac ou à d'autres produits chimiques toxiques. Comme les gènes codent pour l'assemblage des protéines, une mutation de la séquence nucléotidique d'un gène peut modifier la séquence d'acides aminés et, par conséquent, la structure et la fonction d'une protéine. On pense que les mutations spontanées survenant au cours de la méiose sont à l'origine de nombreux avortements spontanés (fausses couches).
Troubles chromosomiques
Parfois, une maladie génétique n'est pas causée par une mutation d'un gène, mais par la présence d'un nombre incorrect de chromosomes. Par exemple, le syndrome de Down est causé par la présence de trois copies du chromosome 21. C'est ce que l'on appelle la trisomie 21. La cause la plus fréquente de trisomie 21 est la non-disjonction chromosomique au cours de la méiose. La fréquence des événements sans disjonction semble augmenter avec l'âge, de sorte que la fréquence des grossesses d'un enfant atteint du syndrome de Down augmente chez les femmes de plus de 36 ans. L'âge du père importe moins, car la non-disjonction est beaucoup moins susceptible de se produire dans un spermatozoïde que dans un ovule.
Alors que le syndrome de Down est causé par la possession de trois copies d'un chromosome, le syndrome de Turner est causé par la possession d'une seule copie du chromosome X. C'est ce que l'on appelle la monosomie. L'enfant atteint est toujours une femme. Les femmes atteintes du syndrome de Turner sont stériles parce que leurs organes sexuels ne mûrissent pas.
LIENS PROFESSIONNELS
Conseiller en génétique
Compte tenu de l'orchestration complexe de l'expression génique, de la migration cellulaire et de la différenciation cellulaire au cours du développement prénatal, il est étonnant de constater que la grande majorité des nouveau-nés sont en bonne santé et exempts de malformations congénitales majeures. Lorsqu'une femme de plus de 35 ans est enceinte ou a l'intention de le devenir, ou que son partenaire a plus de 55 ans, ou s'il existe des antécédents familiaux de maladie génétique, elle et son partenaire voudront peut-être parler à un conseiller en génétique pour discuter de la probabilité que leur enfant soit atteint d'un trouble génétique ou chromosomique. Un conseiller génétique peut interpréter les antécédents familiaux d'un couple et estimer les risques pour leurs futurs enfants.
Pour de nombreuses maladies génétiques, un test ADN permet de déterminer si une personne est porteuse. Par exemple, le statut de porteur de l'X fragile, un trouble lié à l'X associé à un retard mental, ou de la mucoviscidose, peut être déterminé par une simple prise de sang pour obtenir de l'ADN à des fins de test. Un conseiller génétique peut renseigner un couple sur les implications d'un tel test et les aider à décider s'ils souhaitent se soumettre à un test. Pour les troubles chromosomiques, les options de dépistage disponibles incluent une prise de sang, une amniocentèse (dans laquelle le liquide amniotique est testé) et un prélèvement de villosités choriales (dans lequel les tissus du placenta sont testés). Chacune d'entre elles présente des avantages et des inconvénients. Un conseiller génétique peut également aider un couple à faire face à la nouvelle selon laquelle l'un des partenaires ou les deux sont porteurs d'une maladie génétique, ou que leur enfant à naître a reçu un diagnostic de trouble chromosomique ou d'une autre anomalie congénitale.
Pour devenir conseiller en génétique, il faut suivre un programme de premier cycle de quatre ans, puis obtenir une maîtrise en conseil génétique auprès d'une université accréditée. La certification du Conseil est obtenue après avoir réussi les examens de l'American Board of Genetic Counseling. Les conseillers génétiques sont des professionnels essentiels dans de nombreuses branches de la médecine, mais il existe une demande particulière de conseillers en génétique préconceptionnelle et prénatale.

Visitez le site Web de la National Society of Genetic Counselors pour plus d'informations sur les conseillers en génétique.

Visitez le site Web de l'American Board of Genetic Counselors, Inc., pour plus d'informations sur les conseillers en génétique.
Révision du chapitre
La constitution génétique d'une personne comporte deux aspects. Leur génotype fait référence à la constitution génétique des chromosomes présents dans toutes leurs cellules et des allèles transmis par leurs parents. Leur phénotype est l'expression de ce génotype, en fonction de l'interaction des allèles appariés, ainsi que de la façon dont les conditions environnementales affectent cette expression.
En travaillant sur des plants de pois, Mendel a découvert que les facteurs qui expliquent les différentes caractéristiques des parents sont transmis discrètement à la progéniture par paires, une par parent. Il a articulé les principes de la ségrégation aléatoire et de l'assortiment indépendant pour tenir compte des modèles d'héritage qu'il a observés. Les facteurs de Mendel sont des gènes, différents variants étant appelés allèles et ces allèles étant dominants ou récessifs dans leur expression. Chaque parent transmet un allèle pour chaque gène à sa progéniture, et la progéniture est également susceptible d'hériter de toute combinaison de paires d'allèles. Lorsque Mendel a croisé des individus hétérozygotes, il a trouvé à plusieurs reprises un ratio dominant—récessif de 3:1. Il a postulé à juste titre que l'expression du caractère récessif était masquée chez les hétérozygotes mais qu'elle réapparaîtrait chez leurs descendants de manière prévisible.
La génétique humaine vise à identifier les différents allèles et à comprendre comment ils s'expriment. Les chercheurs en médecine s'intéressent particulièrement à l'identification des modèles de transmission des maladies génétiques, qui permettent d'estimer le risque que la progéniture d'un couple donné hérite d'une maladie ou d'un trouble génétique. Les modèles d'hérédité chez les humains incluent la dominance et la récessivité autosomiques, la dominance et la récessivité liées à l'X, la dominance incomplète, la codominance et la létalité. Une modification de la séquence nucléotidique de l'ADN, qui peut se manifester ou non dans un phénotype, est appelée mutation.
Questions de révision
Le syndrome de Q. Marfan est héréditaire selon un schéma autosomique dominant. Lequel des énoncés suivants est vrai ?
R. Les femelles sont plus susceptibles d'être porteuses de la maladie.
B. Les enfants mâles sont plus susceptibles d'hériter de la maladie.
C. Les enfants mâles et femelles ont la même probabilité d'hériter de la maladie.
D. Les femelles sont plus susceptibles d'hériter de la maladie.
Réponse : C
Q. Outre la codominance, les antigènes du groupe sanguin ABO sont également un exemple de ________.
A. domination incomplète
B. Hérédité récessive liée à l'X
C. allèles multiples
D. héritage létal récessif
Réponse : C
Q. Zoé est atteinte de mucoviscidose. Laquelle des explications suivantes est la plus probable ?
R. Zoé a probablement hérité d'un allèle défectueux de son père, qui est porteur, et d'un allèle normal de sa mère.
B. Zoé a probablement hérité d'un allèle défectueux de sa mère, qui doit également être atteinte de mucoviscidose, et d'un allèle normal de son père.
C. Zoé doit avoir hérité d'allèles défectueux de ses deux parents, qui doivent tous deux être également atteints de mucoviscidose.
D. Zoé doit avoir hérité d'allèles défectueux de ses deux parents, tous deux porteurs.
Réponse : D
Questions sur la pensée critique
Q. Expliquez pourquoi il était essentiel que Mendel effectue ses croisements en utilisant un échantillon de grande taille ?
R. En utilisant des échantillons de grande taille, Mendel a minimisé l'effet de la variabilité aléatoire résultant du hasard. Cela lui a permis d'identifier les vrais ratios correspondant à l'héritage dominant—récessif.
Q. Comment une femme porteuse d'un trouble récessif lié à l'X peut-elle avoir une fille atteinte ?
R. La seule façon pour qu'une fille atteinte puisse naître est que la femelle porteuse s'accouple avec un mâle atteint. Dans ce cas, 50 pour cent des filles seraient touchées. Sinon, mais c'est extrêmement improbable, la fille pourrait être atteinte d'une mutation spontanée.
Lexique
- allèle
- formes alternatives d'un gène qui occupent un locus spécifique sur un gène spécifique
- chromosome autosomique
- chez l'homme, les 22 paires de chromosomes qui ne sont pas les chromosomes sexuels (XX ou XY)
- autosomique dominant
- schéma d'hérédité dominante qui correspond à un gène présent sur l'un des 22 chromosomes autosomiques
- autosomique récessif
- schéma d'hérédité récessif qui correspond à un gène présent sur l'un des 22 chromosomes autosomiques
- transporteur
- personne hétérozygote qui ne présente pas les symptômes d'un trouble génétique récessif mais qui peut transmettre le trouble à sa progéniture
- codominance
- modèle d'hérédité qui correspond à l'expression égale, distincte et simultanée de deux allèles différents
- dominant
- décrit un trait exprimé à la fois sous forme homozygote et hétérozygote
- létal dominant
- schéma héréditaire dans lequel les individus porteurs d'une ou deux copies d'un allèle létal ne survivent pas in utero ou ont une durée de vie raccourcie
- génotype
- constitution génétique complète d'un individu
- hétérozygote
- ayant deux allèles différents pour un gène donné
- homozygote
- ayant deux allèles identiques pour un gène donné
- domination incomplète
- schéma héréditaire dans lequel un génotype hétérozygote exprime un phénotype intermédiaire entre les phénotypes dominants et récessifs
- caryotype
- arrangement systématique des images des chromosomes en paires homologues
- mutation
- modification de la séquence nucléotidique de l'ADN
- phénotype
- manifestation physique ou biochimique du génotype ; expression des allèles
- Carré Punnett
- grille utilisée pour afficher toutes les combinaisons possibles d'allèles transmis par les parents à leur progéniture et prédire la probabilité mathématique que la progéniture hérite d'un génotype donné
- récessive
- décrit un trait qui n'est exprimé que sous forme homozygote et qui est masqué sous forme hétérozygote
- létal récessif
- schéma héréditaire dans lequel les individus porteurs de deux copies d'un allèle létal ne survivent pas in utero ou ont une durée de vie plus courte
- chromosomes sexuels
- paire de chromosomes impliqués dans la détermination du sexe ; chez les hommes, les chromosomes XY ; chez les femmes, les chromosomes XX
- trait
- variation d'une caractéristique exprimée
- Lié à X
- modèle d'hérédité dans lequel un allèle est porté sur le chromosome X de la 23e paire
- Dominante liée au X
- schéma d'hérédité dominante qui correspond à un gène du chromosome X de la 23e paire
- récessif lié à l'X
- schéma d'hérédité récessif qui correspond à un gène du chromosome X de la 23e paire


