11.5: 突变
- Page ID
- 200140
学习目标
- 比较点突变和移帧突变
- 描述错义突变、废话突变和沉默突变之间的区别
- 描述浅色修复和深色修复的区别
- 解释不同的诱变剂是如何起作用的
- 解释为什么艾姆斯测试可以用来检测致癌物
- 分析 DNA 序列并识别突变类型的示例
突变是生物体DNA序列中可遗传的变化。 由此产生的生物称为突变体,与野生型相比,其表型可能有明显的变化,野生型是自然界中最常观察到的表型。 DNA序列的变化通过转录赋予mRNA,并可能导致翻译时蛋白质中氨基酸序列的改变。 由于蛋白质具有绝大多数细胞功能,因此蛋白质中氨基酸序列的变化可能导致细胞和生物体表型的改变。
突变对 DNA 序列的影响
有几种类型的突变是根据DNA分子的改变方式进行分类的。 一种称为点突变的类型会影响单个基数,最常见的是当一个碱基被另一个碱基取代或取代时。 突变还源于添加一个或多个碱基(称为插入)或移除一个或多个碱基(称为缺失)。
练习\(\PageIndex{1}\)
当一个基因的序列中少了两个核苷酸时,会发生什么类型的突变?
突变对蛋白质结构和功能的影响
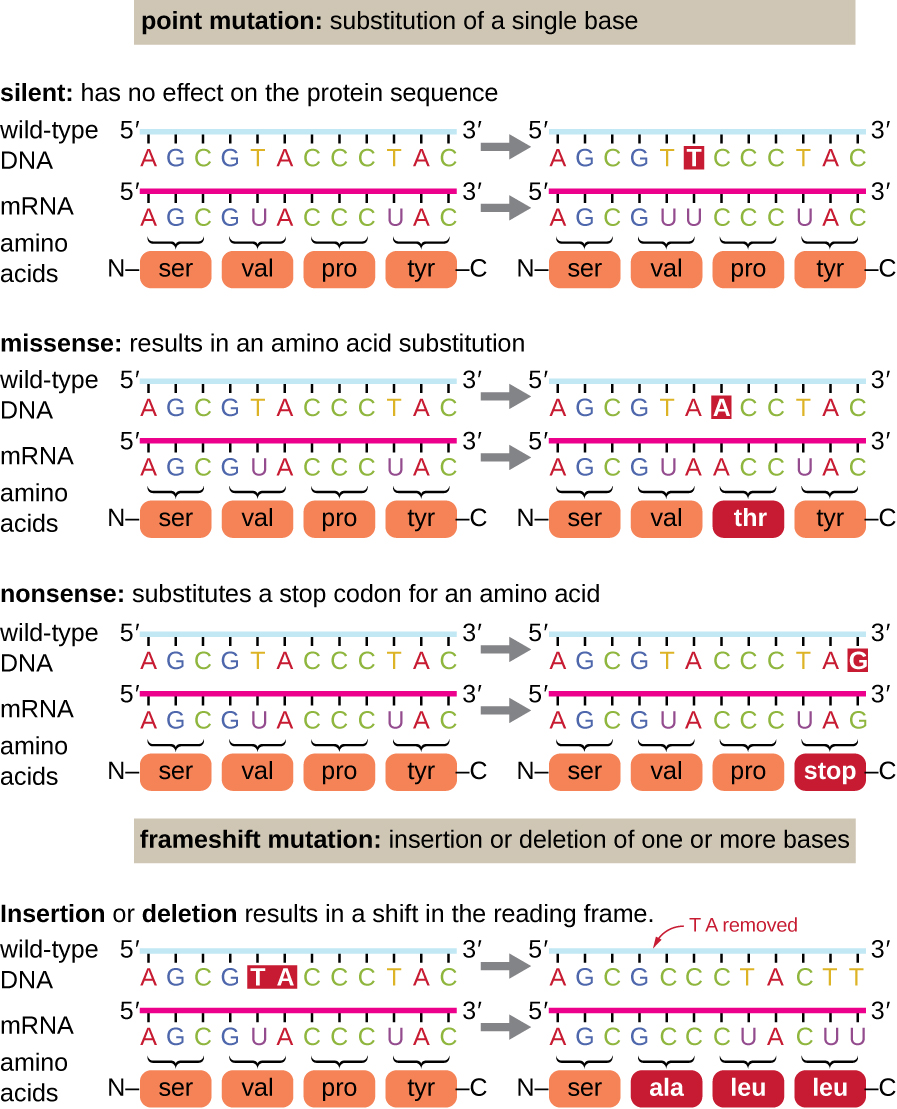
点突变可能对蛋白质功能产生广泛影响(图\(\PageIndex{1}\))。 由于遗传密码的退化,尽管序列发生变化,点突变通常会导致相同的氨基酸被掺入生成的多肽中。 这种变化不会影响蛋白质的结构,因此被称为无声突变。 错义突变会导致不同的氨基酸被掺入生成的多肽中。 错义突变的影响取决于新氨基酸与野生型氨基酸的化学差异。 改变后的氨基酸在蛋白质中的位置也很重要。 例如,如果改变后的氨基酸是酶活性位点的一部分,那么错义突变的影响可能很明显。 许多错义突变导致蛋白质仍然起作用,至少在某种程度上是如此。 有时,错义突变的影响可能只有在某些环境条件下才会显现出来;这种错义突变被称为条件突变。 在极少数情况下,错义突变可能是有益的。 在适当的环境条件下,这种类型的突变可能会给藏有它的生物带来选择性优势。 还有另一种类型的点突变,称为废话突变,它将编码氨基酸(感官密码子)的密码子转化为停止密码子(废话密码子)。 胡说八道的突变会导致蛋白质的合成比野生型短,而且通常不起作用。
删除和插入也会造成各种影响。 由于密码子是核苷酸的三联体,因此以三个核苷酸为一组的插入或缺失可能导致一种或多种氨基酸的插入或缺失,并且可能不会对所得蛋白质的功能造成显著影响。 但是,由于许多不是三倍的核苷酸的插入或缺失引起的移帧突变非常成问题,因为读取框架会发生变化(图\(\PageIndex{1}\))。 由于核糖体读取三重密码子中的 mRNA,因此移帧突变可以在突变点之后改变所有氨基酸。 新的读取帧还可以在编码序列结束之前包括停止密码子。 因此,由含有 frameshift 突变的基因制成的蛋白质几乎总是不起作用的。
练习\(\PageIndex{2}\)
- 蛋白质基因的核苷酸变化可能对该基因的表型没有任何影响的原因是什么?
- 在蛋白质编码基因中的第五个核苷酸之后插入三个核苷酸可以产生比正常短的蛋白质吗? 怎么或怎么不是?
有益的突变
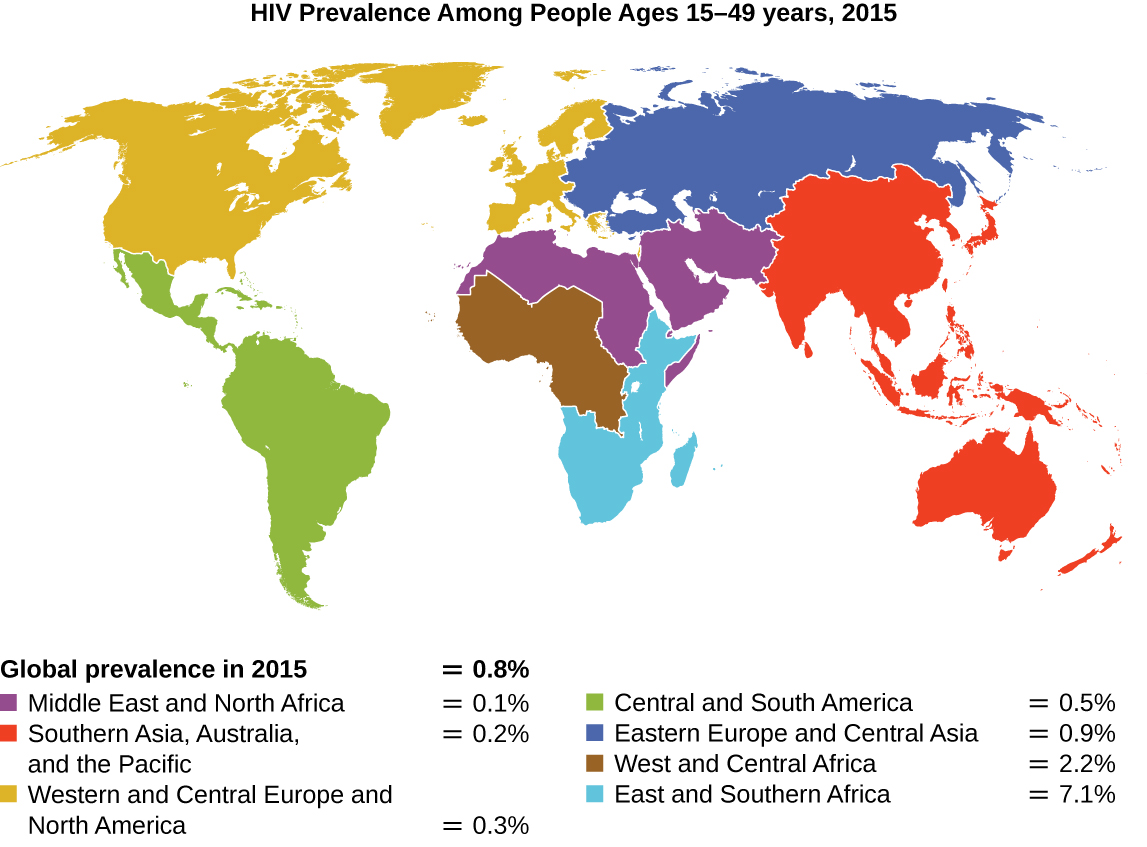
自1981年报告第一例人类免疫缺陷病毒(HIV)感染病例以来,已有近4000万人死于HIV感染,1 这种病毒导致获得性免疫缺陷综合症(AIDS)。 该病毒靶向辅助性T细胞,这些细胞在桥接先天和适应性免疫反应、感染和杀死通常参与人体感染反应的细胞方面起着关键作用。 目前尚无治愈HIV感染的方法,但是已经开发出许多药物来减缓或阻断病毒的发展。 尽管世界各地的人可能被感染,但15-49岁人群中感染率最高的是撒哈拉以南非洲,那里将近20人中就有一人被感染,占全球感染人数的70%以上 2(图\(\PageIndex{2}\))。 不幸的是,这也是世界上最缺乏预防战略和治疗感染药物的地区。
近年来,发现了几个来自北欧的人对艾滋病毒感染具有抗药性,这激起了科学界的兴趣。 1998年,美国国立卫生研究院(NIH)的美国遗传学家斯蒂芬·奥布赖恩及其同事公布了他们对4,000多人的遗传分析结果。 这些结果表明,许多欧亚血统的人(在某些族裔群体中高达14%)在编码CCR5的基因中存在一种称为CCR5-delta 32的缺失突变。 CCR5 是存在于 T 细胞表面的辅助受体,是许多病毒株进入宿主细胞所必需的。 这种突变导致产生HIV无法有效结合的受体,从而阻断病毒的进入。 这种突变纯合子的人大大降低了感染HIV的易感性,而那些杂合子的人也有一定的免受感染的保护。
目前尚不清楚为什么北欧血统的人会携带这种突变,但其流行率似乎在北欧最高,并且随着人们向南移动,其发病率稳步下降。 研究表明,该突变自HIV出现之前就已经存在,可能是由于接触鼠疫或天花而在欧洲人群中被选中的。 这种突变可以保护个人免受鼠疫(由鼠疫耶尔森氏菌引起)和天花(由天花病毒引起)的侵害,因为这种受体也可能与这些疾病有关。 这种突变的年龄尚有争议,但据估计,它出现在1875年至225年前,可能是通过维京人的入侵从北欧传播的。
这一激动人心的发现为HIV研究开辟了新的途径,包括寻找药物来阻断缺乏突变的人的CCR5与HIV的结合。 尽管可以进行DNA测试以确定哪些人携带CCR5-Delta 32突变,但有记录的个体因感染HIV的突变而纯合的案例。 出于这个原因,公共卫生官员并未广泛建议对该突变进行DNA检测,以免鼓励携带该突变的人采取危险行为。 尽管如此,抑制HIV与CCR5的结合仍然是为HIV感染者开发药物疗法的有效策略。
突变的原因
DNA 复制过程中的错误可能导致自发突变的发生。 DNA聚合酶的错误率是每复制十亿个碱基对中就有一个不正确的碱基。 暴露于诱变剂会导致诱发突变,即各种类型的化学制剂或辐射(表\(\PageIndex{1}\))。 暴露于诱变剂可以使突变率提高1000倍以上。 诱变剂通常也是致癌物质,是导致癌症的药物。 但是,尽管几乎所有致癌物质都具有致突变性,但并非所有诱变剂都一定是致癌物。
化学诱变剂
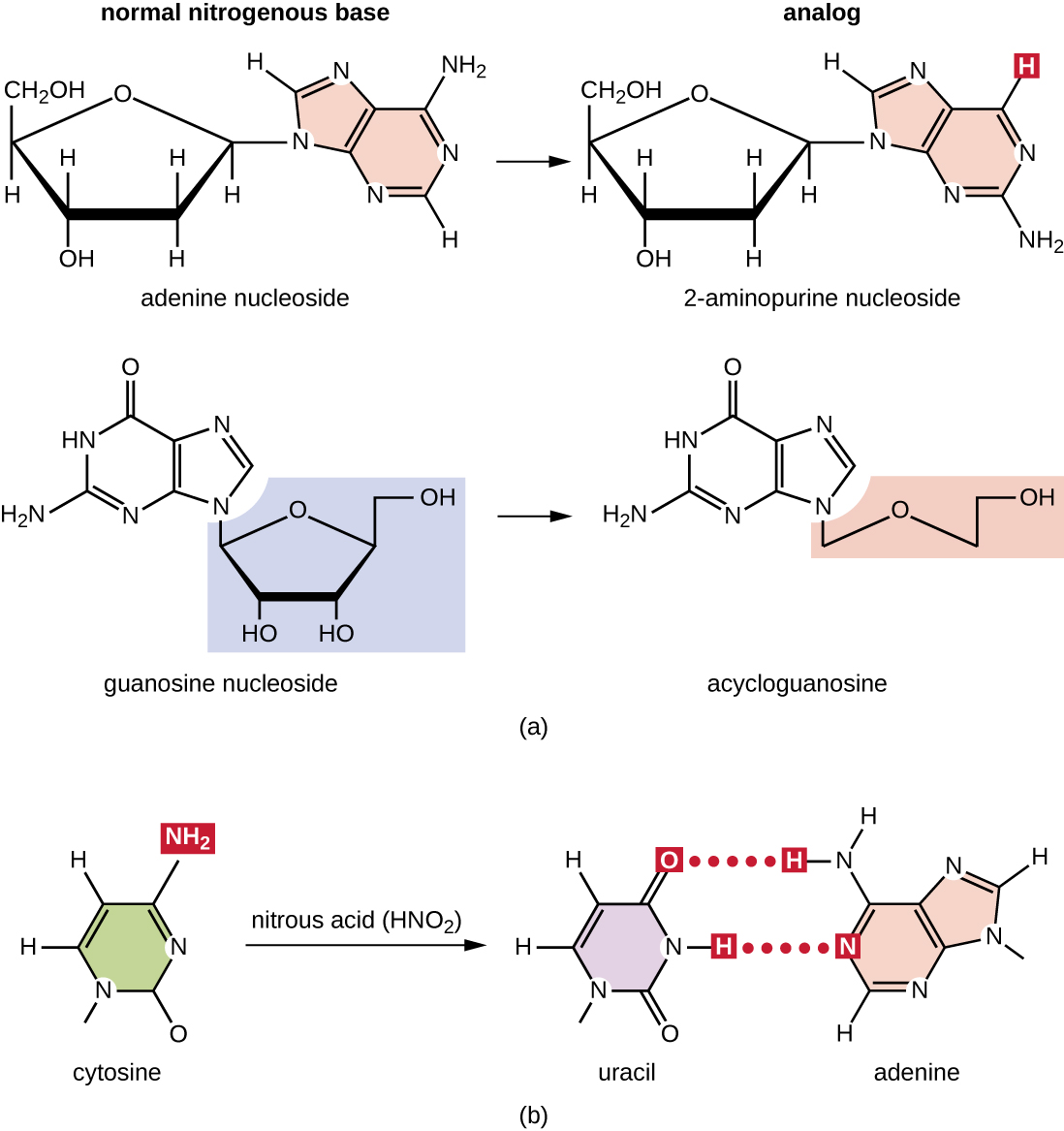
各种类型的化学诱变剂通过充当核苷类似物或通过修饰核苷碱基直接与DNA相互作用。 称为核苷类似物的化学物质在结构上与正常的核苷酸碱基相似,可以在复制过程中掺入到DNA中(图\(\PageIndex{3}\))。 这些碱基类似物会诱发突变,因为它们的碱基配对规则通常与它们所取代的碱基不同。 其他化学诱变剂可以修改正常的DNA碱基,从而产生不同的碱基配对规则。 例如,亚硝酸使胞嘧啶脱氨并将其转化为尿嘧啶。 然后,尿嘧啶在随后的一轮复制中与腺嘌呤配对,导致 GC 碱基对转化为 AT 碱基对。 亚硝酸还将腺嘌呤脱氨为次黄嘌呤,后者碱基与胞嘧啶而不是胸腺嘧啶配对,导致 TA 碱基对转化为 CG 碱基对。
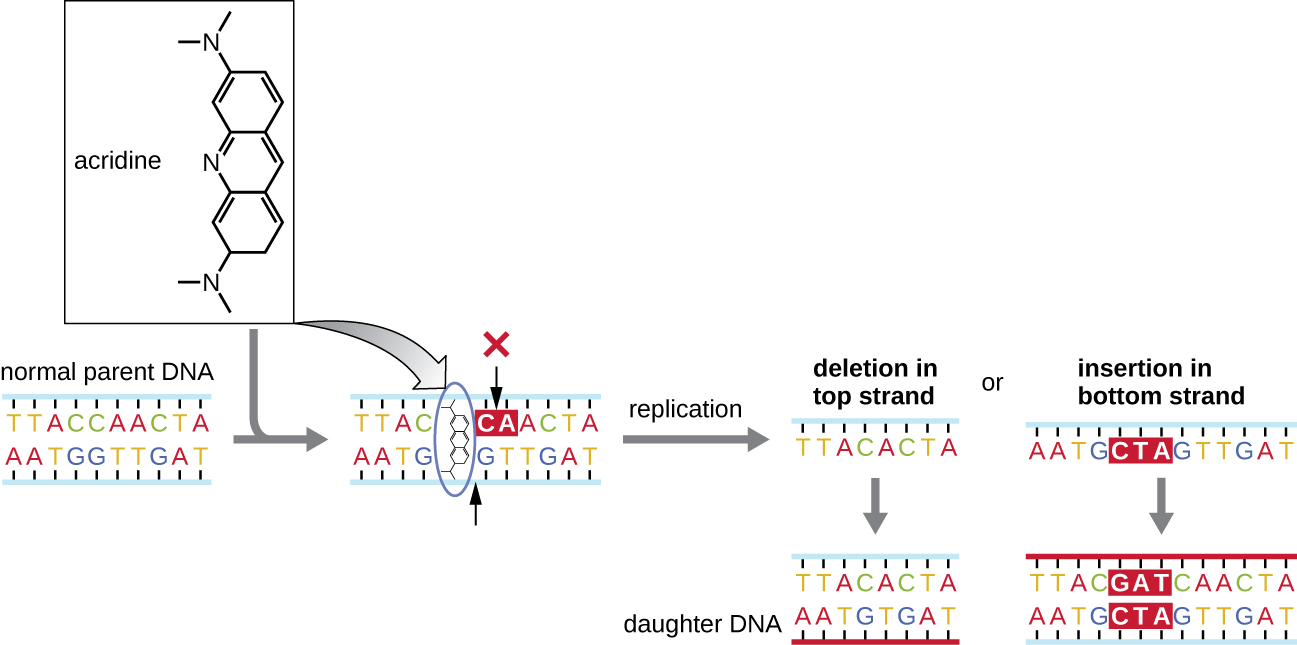
被称为插层剂的化学诱变剂的作用方式不同。 这些分子在 DNA 双螺旋堆叠的含氮碱基之间滑动,扭曲分子,并在核苷酸碱基对之间形成非典型间距(图\(\PageIndex{4}\))。 因此,在DNA复制过程中,DNA聚合酶要么跳过复制多个核苷酸(产生缺失),要么插入额外的核苷酸(产生插入物)。 无论哪种结果都可能导致移帧突变。 诸如多环芳烃之类的燃烧产物是特别危险的插层剂,可能导致突变引起的癌症。 插层剂溴化乙铵和阿司啶橙在实验室中通常用于染色 DNA 以进行可视化,它们是潜在的诱变剂。
辐射
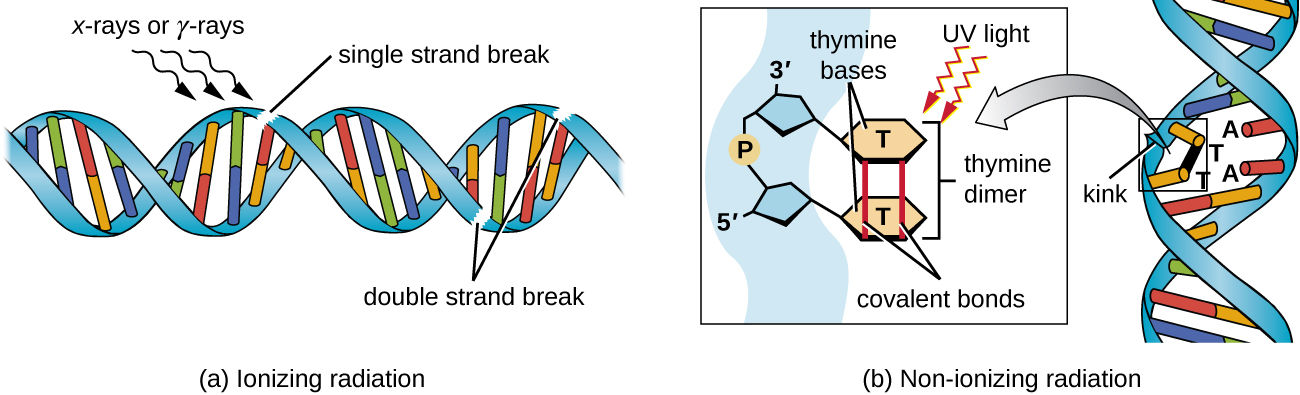
尽管机制不同,但暴露于电离或非电离辐射都可能诱发DNA突变。 X 射线和伽玛射线等强电离辐射可通过在辐射暴露时形成羟基自由基,导致 DNA 骨干的单链和双链断裂(图\(\PageIndex{5}\))。 电离辐射还可以改变碱基;例如,胞嘧啶脱氨化为尿嘧啶,类似于亚硝酸的作用。 3 电离辐射暴露用于杀死微生物,对医疗器械和食物进行消毒,因为它在破坏 DNA、蛋白质和其他细胞成分方面具有显著的非特异性作用(参见使用物理方法控制微生物)。
像紫外线这样的非电离辐射的能量不足以引发这些类型的化学变化。 但是,非电离辐射可以在核苷酸链内诱导两个相邻的嘧啶碱基(通常是两个胸腺嘧啶)之间形成二聚体。 在胸腺嘧啶二聚体形成过程中,两个相邻的胸腺嘧啶共价连接,如果不修复,此时DNA复制和转录都将停滞不前。 DNA 聚合酶可能会继续进行并错误地复制二聚体,从而可能导致帧移或点突变。
| 诱变剂 | 行动模式 | 对 DNA 的影响 | 由此产生的突变类型 |
|---|---|---|---|
| 核苷类似物 | |||
| 2-氨基嘌呤 | 代替 A 插入,但以 C 为碱基对 | 将 AT 转换为 GC 碱基对 | 点 |
| 5-溴尿嘧啶 | 代替 T 插入,但以 G 为碱基对 | 将 AT 转换为 GC 碱基对 | 点 |
| 核苷酸修饰剂 | |||
| 一氧化二氮 | 将 C 分解为 U | 将 GC 转换为 AT 碱基对 | 点 |
| 插层剂 | |||
| 嘧啶橙、溴化乙钠、多环芳烃 | 扭曲双螺旋,在核苷酸之间产生不寻常的间距 | 引入少量删除和插入内容 | Frameshift |
| 电离辐射 | |||
| X 射线、γ射线 | 形成羟基自由基 | 导致单链和双链 DNA 断裂 | 修复机制可能会引入突变 |
| X 射线、γ射线 | 修改碱基(例如,将 C 脱氨为 U) | 将 GC 转换为 AT 碱基对 | 点 |
| 非电离辐射 | |||
| 紫外线 | 形成嘧啶(通常是胸腺嘧啶)二聚体 | 导致 DNA 复制错误 | Frameshift 或 point |
练习\(\PageIndex{3}\)
- 基本模拟如何引入突变?
- 插层剂是如何引入突变的?
- 什么类型的诱变剂会导致胸腺嘧啶二聚体?
DNA 修复
DNA复制过程非常准确,但错误可能是自发发生的,也可能是由诱变剂引起的。 未纠正的错误会对表型造成严重后果。 细胞已经开发出多种修复机制,以最大限度地减少持续存在的突变数量。
校对
大多数 DNA 聚合酶通过一种称为校对的功能迅速纠正了 DNA 复制过程中引入的大多数错误。 在校对中,DNA聚合酶读取新添加的碱基,确保在添加下一个碱基之前,它与模板链中的相应碱基互补。 如果添加了错误的碱基,则该酶会切开以释放错误的核苷酸,然后添加新的碱基。
不匹配修复
复制过程中出现的一些错误将在复制机制移动后不久得到纠正。 这种机制称为不匹配修复。 这种机制所涉及的酶可以识别错误添加的核苷酸,将其切除,然后用正确的碱基代替。 一个例子是大肠杆菌中的甲基定向失配修复。 DNA 被半甲基化了。 这意味着亲链是甲基化的,而新合成的子链不是。 新链需要几分钟才能被甲基化。 蛋白质 mutS、mutL 和 muth 与发现错误核苷酸的半甲基化位点结合。 Muth 切割非甲基化链(新链)。 外切核酸酶去除部分链(包括不正确的核苷酸)。 然后,形成的间隙由 DNA pol III 和连接酶填充。
胸腺嘧啶二聚体的修复
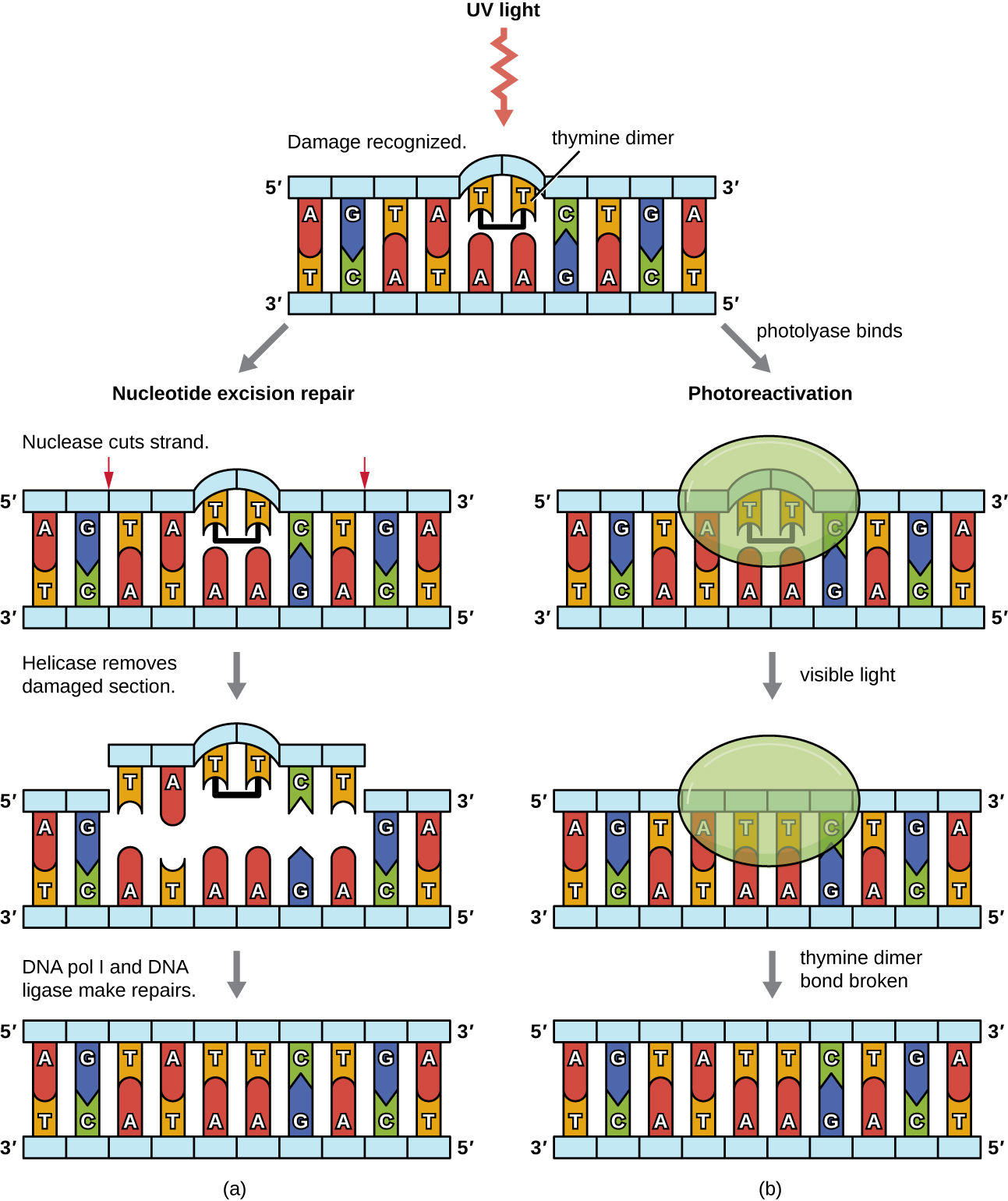
由于胸腺嘧啶二聚体的产生很常见(许多生物无法避开紫外线),因此修复这些病变的机制已经形成。 在核苷酸切除修复(也称为暗色修复)中,酶会去除嘧啶二聚体,然后用正确的核苷酸代替它(图\(\PageIndex{6}\))。 在大肠杆菌中,DNA由酶复合物扫描。 如果发现嘧啶二聚体引入的双螺旋变形,则酶复合物将糖磷酸骨干切开二聚体上游和下游的几个碱基,然后用酶法去除这两个切口之间的DNA片段。 DNA pol I 用正确的核苷酸代替缺失的核苷酸,DNA 连接酶封住了糖磷酸骨干中的空隙。
胸腺嘧啶二聚体的直接修复(也称为光修复)是通过在可见光存在下的光再激活过程进行的。 一种叫做光解酶的酶可识别胸腺嘧啶二聚体引起的 DNA 螺旋失真并与二聚体结合。 然后,在可见光存在的情况下,光解酶会改变构象并分解胸腺嘧啶二聚体,从而使胸腺嘧啶再次与互补链上的腺嘌呤正确碱基配对。 光再激活似乎存在于所有生物体中,但胎盘哺乳动物(包括人类)除外。 光再激活对于长期暴露于紫外线辐射的生物(如植物、光合细菌、藻类和珊瑚)尤其重要,可以防止胸腺嘧啶二聚体形成引起的突变积累。
练习\(\PageIndex{4}\)
- 在失配修复过程中,酶如何识别哪条是新链,哪条是旧链?
- 光解酶能修复哪种类型的突变?
识别细菌突变体
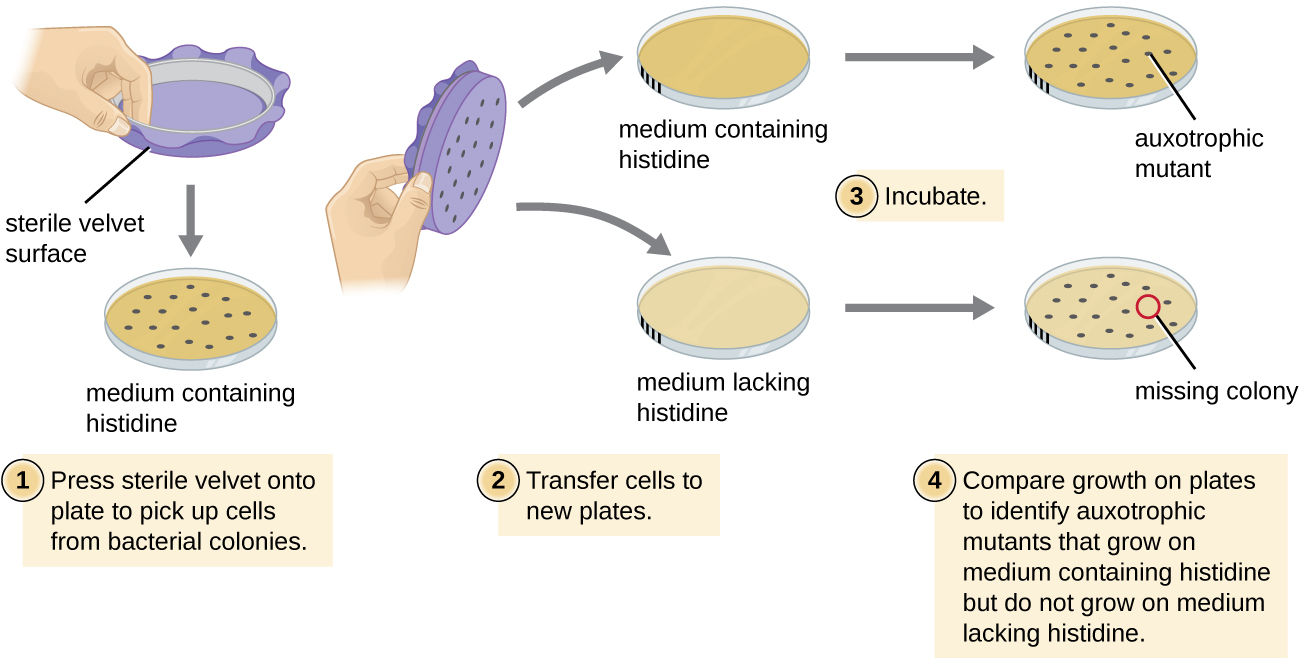
用于识别细菌突变体的一种常用技术称为复制品电镀。 该技术用于检测称为auxotrophs的营养突变体,这些突变体在编码特定营养素(例如氨基酸)的生物合成途径中的酶的基因中存在突变。 因此,尽管野生型细胞保留了在缺乏特定营养素的培养基上正常生长的能力,但auxotrophs无法在这样的培养基上生长。 在复制品镀层过程中(图\(\PageIndex{7}\)),一群细菌细胞被诱变,然后作为单个细胞镀在营养完整的复杂板上,然后长成菌落。 来自这些菌落的细胞通常使用无菌天鹅绒从该母板中移除。 然后,这种含有细胞的天鹅绒以相同的方向被压在各种培养基的板上。 至少还应有一盘营养完整,以确保细胞在板之间正确转移。 其他板块缺乏特定的营养素,这使研究人员能够发现各种无法产生特定营养素的营养缺陷突变体。 来自营养完整板上相应菌落的细胞可用于回收突变体以供进一步研究。
练习\(\PageIndex{5}\)
在寻找突变体时,为什么除了营养不足的板外,还要将细胞镀在营养完整的板上?
艾姆斯测试
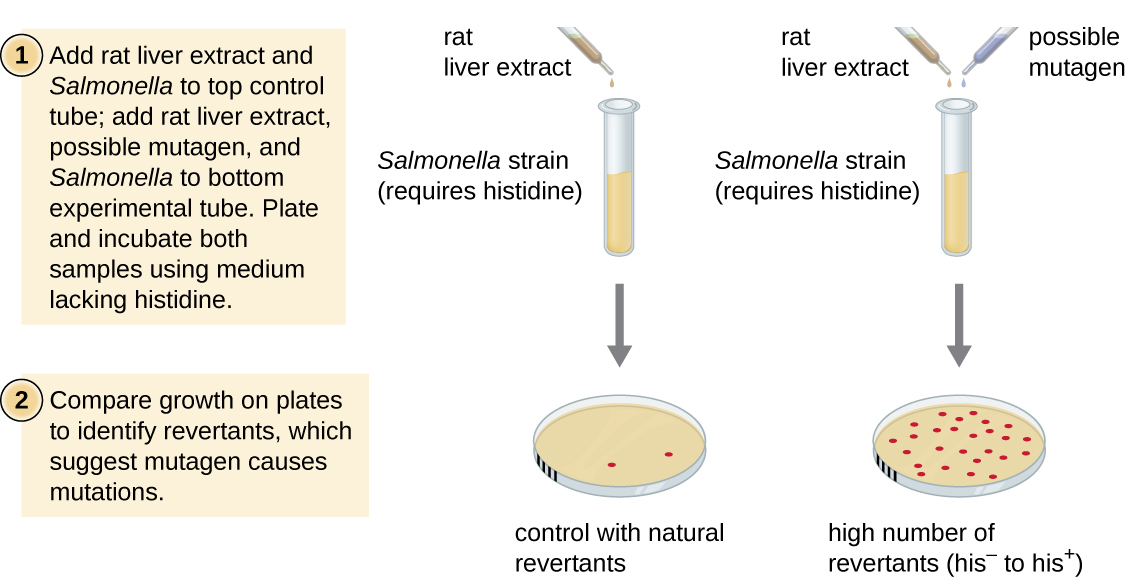
艾姆斯测试由布鲁斯·艾姆斯(Bruce Ames)(1928年—)在20世纪70年代开发,是一种利用细菌快速、廉价地筛选新化合物的致癌潜力的方法。 该测试测量了与接触该化合物相关的突变率,如果突变率升高,则可能表明接触该化合物会增加癌症风险。 艾姆斯测试使用一种鼠伤寒沙门氏菌菌株作为测试生物体,它是一种组氨酸 auxotrop h,由于合成所需的必需基因发生了突变,因此无法合成自己的组氨酸。 暴露于潜在诱变剂后,这些细菌会被培养到缺乏组氨酸的培养基上,记录恢复合成组氨酸能力的突变体数量,并与在没有潜在诱变剂的情况下产生的此类突变体的数量进行比较(图\(\PageIndex{8}\))。 在艾姆斯测试中,更具诱变性的化学物质将带来更多的突变体,从而恢复组氨酸合成。 由于许多化学物质不具有直接诱变作用,而是通过肝酶代谢成诱变形式,因此通常在本实验开始时使用大鼠肝提取物来模仿肝脏的新陈代谢。 在进行艾姆斯测试后,通过使用其他模型,包括小鼠和大鼠等动物模型,进一步测试被确定为致突变的化合物的潜在致癌特性。
练习\(\PageIndex{6}\)
- 在艾姆斯测试中,哪种突变被用作突变率的指标?
- 为什么艾姆斯测试可以作为致癌性的测试?
关键概念和摘要
- 突变是 DNA 中可遗传的变化。 突变可能导致蛋白质的氨基酸序列发生变化,从而可能影响其功能。
- 点数突变会影响单个碱基对。 如果mRNA密码子编码相同的氨基酸,则点突变可能导致无声突变;如果mRNA密码子编码不同的氨基酸,则可能导致错义突变;如果mRNA密码子变成终止密码子,则可能导致无意义突变。
- Missense 突变可能会保留功能,这取决于新氨基酸的化学成分及其在蛋白质中的位置。 胡说八道的突变会产生截断的、经常是无功能的蛋白质。
- frameshift 突变是由于插入或缺失了许多不是三的倍数的核苷酸造成的。 读取框架的变化会改变突变点之后的每种氨基酸,从而产生非功能性蛋白质。
- 自发突变是通过 DNA 复制错误发生的,而诱发的突变是通过暴露于诱变剂发生的。
- 诱变剂通常具有致癌性,但并非总是如此。 但是,几乎所有致癌物质都具有诱变性。
- 化学诱变剂包括碱基类似物和改变现有碱的化学物质。 在这两种情况下,突变都是在经过几轮DNA复制后引入的。
- 电离辐射,例如X射线和γ射线,会导致DNA的磷酸二酯骨干破裂,还可以化学修改碱基以改变其碱基配对规则。
- 像紫外线这样的@@ 非电离辐射可能会引入嘧啶(胸腺嘧啶)二聚体,这在DNA复制和转录过程中可能会引入帧移或点突变。
- 细胞具有修复自然发生的突变的机制。 DNA 聚合酶具有校对活性。 失配修复是在 DNA 复制完成后修复错误掺入的碱基的过程。
- 嘧啶二聚体也可以修复。 在核苷酸切除修复(暗色修复)中,酶识别嘧啶二聚体引入的变形,并使用未受损的DNA链作为模板,用正确的碱基替换受损链。 细菌和其他生物也可以使用直接修复,即光解酶在可见光下分解嘧啶。
- 通过比较整板上的生长和缺乏特定营养素的培养基上生长不足,可以识别出称为 auxotroph s的特定功能丧失突变体。
- 艾姆斯测试是一种廉价的方法,它使用营养不良细菌来测量化合物的诱变性。 致突变性是致癌潜力的指标。
脚注
- 1 世界卫生组织。“全球卫生观测站(GHO)数据,艾滋病毒/艾滋病。” http://www.who.int/gho/hiv/en/。 已于 2016 年 8 月 5 日访问。
- 2 世界卫生组织,“全球卫生观测站(GHO)数据,艾滋病毒/艾滋病。” http://www.who.int/gho/hiv/en/。 已于 2016 年 8 月 5 日访问。
- 3 K.R. Tindall 等人 “Lambda Phage 和 Prophage 的伽玛射线诱变引起的 DNA 碱基序列的变化。” 遗传学 118 第 4 期 (1988): 551—560。


