8.3: Kupumua kwa seli
- Page ID
- 174808
Malengo ya kujifunza
- Linganisha na kulinganisha mfumo wa usafiri wa elektroni, eneo na kazi katika kiini cha prokaryotic na kiini cha eukaryotic.
- Linganisha na kulinganisha tofauti kati ya kiwango cha substrate na phosphorylation ya oxidative
- Eleza uhusiano kati ya chemiosmosis na nguvu ya proton
- Eleza kazi na eneo la synthase ya ATP katika kiini cha prokaryotic dhidi ya eukaryotic
- Kulinganisha na kulinganisha kupumua aerobic na anaerobic
Sisi tu kujadiliwa njia mbili katika glucose catabolism-glycolysis na Krebs mzunguko-kwamba kuzalisha ATP na substrate ngazi phosphorylation. ATP nyingi, hata hivyo, huzalishwa wakati wa mchakato tofauti unaoitwa phosphorylation ya oxidative, ambayo hutokea wakati wa kupumua kwa seli. Kupumua kwa seli huanza wakati elektroni zinahamishwa kutoka NADH na FADH 2 -kufanywa katika glycolysis, mmenyuko wa mpito, na mzunguko wa Kreb-kupitia mfululizo wa athari za kemikali kwa kukubali elektroni isokaboni ya mwisho (ama oksijeni katika kupumua aerobic au molekuli zisizo oksijeni isokaboni katika anaerobic kupumua). Uhamisho huu wa elektroni unafanyika kwenye sehemu ya ndani ya utando wa seli za seli za prokaryotiki au katika complexes maalumu za protini katika utando wa ndani wa mitochondria ya seli za eukaryotiki. Nishati ya elektroni huvunwa ili kuzalisha gradient ya electrochemical kwenye membrane, ambayo hutumiwa kufanya ATP kwa phosphorylation oxidative.
Mfumo wa Usafiri wa Electron
Mfumo wa usafiri wa elektroni (ETS) ni sehemu ya mwisho inayohusika katika mchakato wa kupumua kwa seli; inajumuisha mfululizo wa complexes za protini zinazohusiana na membrane na flygbolag zinazohusiana na vifaa vya elektroni vya mkononi. Usafiri wa elektroni ni mfululizo wa athari za kemikali unaofanana na kikosi cha ndoo kwa kuwa elektroni kutoka NADH na FADH 2 hupitishwa haraka kutoka kwa mtoa elektroni mmoja wa ETS hadi mwingine. Wafanyabiashara hawa wanaweza kupitisha elektroni pamoja katika ETS kwa sababu ya uwezo wao wa redox. Kwa protini au kemikali kukubali elektroni, ni lazima iwe na uwezo wa redox chanya zaidi kuliko wafadhili wa elektroni. Kwa hiyo, elektroni huhamia kutoka kwa flygbolag za elektroni na uwezo zaidi wa redox hasi kwa wale walio na uwezo zaidi wa redox. Madarasa makubwa manne ya flygbolag za elektroni zinazohusika katika mifumo ya usafiri wa elektroni ya eukaryotic na prokaryotic ni cytochromes, flavoproteins, protini za chuma-sulfuri, na quinones.
Wakati aerobic kupumua mwisho elektroni kukubali (yaani, moja kuwa chanya zaidi redoksi uwezo) katika mwisho wa ETS - oksijeni molekuli (O 2), ambayo inakuwa kupunguzwa kwa maji (H 2 O) mwisho ETS carrier. Hii carrier elektroni, saitokromu oxidase, inatofautiana kati ya aina ya bakteria na inaweza kutumika kutofautisha bakteria karibu kuhusiana kwa ajili ya uchunguzi. Kwa mfano, mpinzani wa gramu-hasi Pseudomonas aeruginosa na kusababisha kipindupindu cha Gram-hasi Vibrio hutumia saitokromu c oxidase, ambayo inaweza kugunduliwa na mtihani wa oksidesi, wakati mwingine Enterobacteriaceae ya gramu-hasi, kama E. coli, ni hasi kwa hili mtihani kwa sababu kuzalisha aina tofauti saitokromu oxidase.
Kuna hali nyingi ambazo kupumua kwa aerobic haiwezekani, ikiwa ni pamoja na moja au zaidi ya yafuatayo:
- Kiini kinakosa jeni encoding saitokromu oksidesi inayofaa kwa kuhamisha elektroni kwa oksijeni mwishoni mwa mfumo wa usafiri wa elektroni.
- Kiini kinakosa jeni encoding enzymes ili kupunguza madhara makubwa ya radicals hatari oksijeni zinazozalishwa wakati wa kupumua aerobic, kama vile peroksidi hidrojeni (H 2 O 2) au superoxide\((\ce{O2-})\).
- Kiini hakina kiasi cha kutosha cha oksijeni ili kufanya kupumua kwa aerobic.
Njia moja inayowezekana kwa kupumua kwa aerobic ni kupumua kwa anaerobic, kwa kutumia molekuli isiyo ya kawaida isipokuwa oksijeni kama mpokeaji wa mwisho wa elektroni. Kuna aina nyingi za kupumua anaerobic zinazopatikana katika bakteria na archaea. Denitrifiers ni bakteria muhimu ya udongo ambayo hutumia nitrati\((\ce{NO3-})\) na nitriti\((\ce{NO2-})\) kama vibali vya mwisho vya elektroni, vinazalisha gesi ya nitrojeni (N 2). Bakteria nyingi za aerobically respiring, ikiwa ni pamoja na E. coli, kubadili kutumia nitrati kama mwokozi wa mwisho wa elektroni na kuzalisha nitriti wakati viwango vya oksijeni vimeharibika.
Viumbe vidogo vinavyotumia kupumua anaerobic huwa na mzunguko wa Krebs intact, hivyo viumbe hawa wanaweza kupata nishati ya molekuli ya NADH na FADH 2 iliyoundwa. Hata hivyo, respirers anaerobic kutumia kubadilishwa ETS flygbolag encoded na genomes yao, ikiwa ni pamoja na complexes tofauti kwa ajili ya uhamisho elektroni kwa receptors yao Gradients ndogo za electrochemical zinazalishwa kutoka kwa mifumo hii ya uhamisho wa elektroni, hivyo ATP chini hutengenezwa kupitia kupumua kwa anaerobic.
Zoezi\(\PageIndex{1}\)
Je, kupumua kwa aerobic na kupumua anaerobic hutumia mnyororo wa usafiri wa elektroni?
Chemiosmosis, Proton Motive Nguvu, na oxidative phosphorylation
Katika kila uhamisho wa elektroni kupitia ETS, elektroni inapoteza nishati, lakini kwa uhamisho fulani, nishati huhifadhiwa kama nishati inayoweza kuitumia kusukwa ioni za hidrojeni (H +) kwenye utando. Katika seli za prokaryotic, H + hupigwa kwa nje ya membrane ya cytoplasmic (inayoitwa nafasi ya periplasmic katika bakteria ya gram-hasi na gram-chanya), na katika seli za eukaryotic, hupigwa kutoka tumbo la mitochondrial kwenye utando wa ndani wa mitochondrial ndani ya nafasi ya intermembrane. Kuna usambazaji usio sawa wa H + kwenye utando unaoanzisha gradient ya electrochemical kwa sababu H + ions ni chaji chanya (umeme) na kuna mkusanyiko mkubwa (kemikali) upande mmoja wa utando. Gradient hii ya electrochemical inayotengenezwa na mkusanyiko wa H + (pia inajulikana kama protoni) upande mmoja wa utando ikilinganishwa na nyingine inajulikana kama nguvu ya motisha ya protoni (PMF). Kwa sababu ions zinazohusika ni H +, gradient ya pH pia imara, na upande wa membrane una mkusanyiko mkubwa wa H + kuwa tindikali zaidi. Zaidi ya matumizi ya PMF kufanya ATP, kama ilivyojadiliwa katika sura hii, PMF pia inaweza kutumika kuendesha michakato mingine yenye nguvu mbaya, ikiwa ni pamoja na usafiri wa virutubisho na mzunguko wa flagella kwa motility.
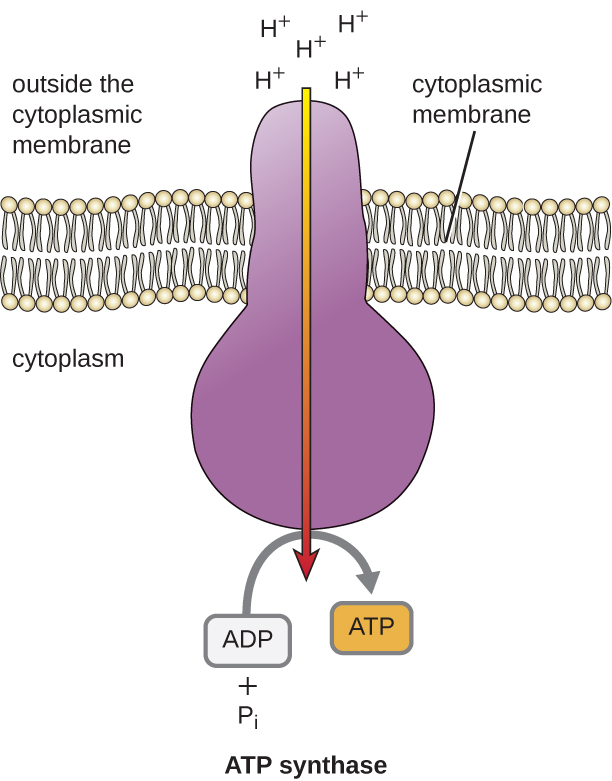
Nishati ya uwezo wa gradient hii ya electrochemical yanayotokana na ETS husababisha H + kuenea kwenye utando (utando wa plasma katika seli za prokaryotic na utando wa ndani katika mitochondria katika seli za eukaryotic). Mtiririko huu wa ioni za hidrojeni kwenye utando, unaoitwa chemiosmosis, lazima kutokea kwa njia ya kituo katika utando kupitia tata ya enzyme iliyofungwa kwa membrane inayoitwa ATP synthase (Kielelezo\(\PageIndex{1}\)). Tabia ya kusonga kwa njia hii ni kama maji yaliyokusanywa upande mmoja wa bwawa, kusonga kupitia bwawa wakati wa kufunguliwa. ATP synthase (kama mchanganyiko wa ulaji na jenereta ya bwawa la umeme) ni protini tata ambayo hufanya kazi kama jenereta ndogo, kugeuka kwa nguvu ya H + diffusing kupitia enzyme, chini electrochemical gradient yao kutoka ambapo kuna wengi pande repelling H + kwa ambapo kuna wachache H +. Katika seli za prokaryotic, H + inapita kutoka nje ya membrane ya cytoplasmic ndani ya cytoplasm, ambapo katika mitochondria ya eukaryotic, H + inapita kutoka nafasi ya intermembrane hadi tumbo la mitochondrial. Kugeuka kwa sehemu za mashine hii ya Masi hurejesha ATP kutoka ADP na phosphate isokaboni (P i) na phosphorylation oxidative, utaratibu wa pili wa kufanya ATP ambayo huvuna nishati uwezo kuhifadhiwa ndani ya gradient electrochemical.
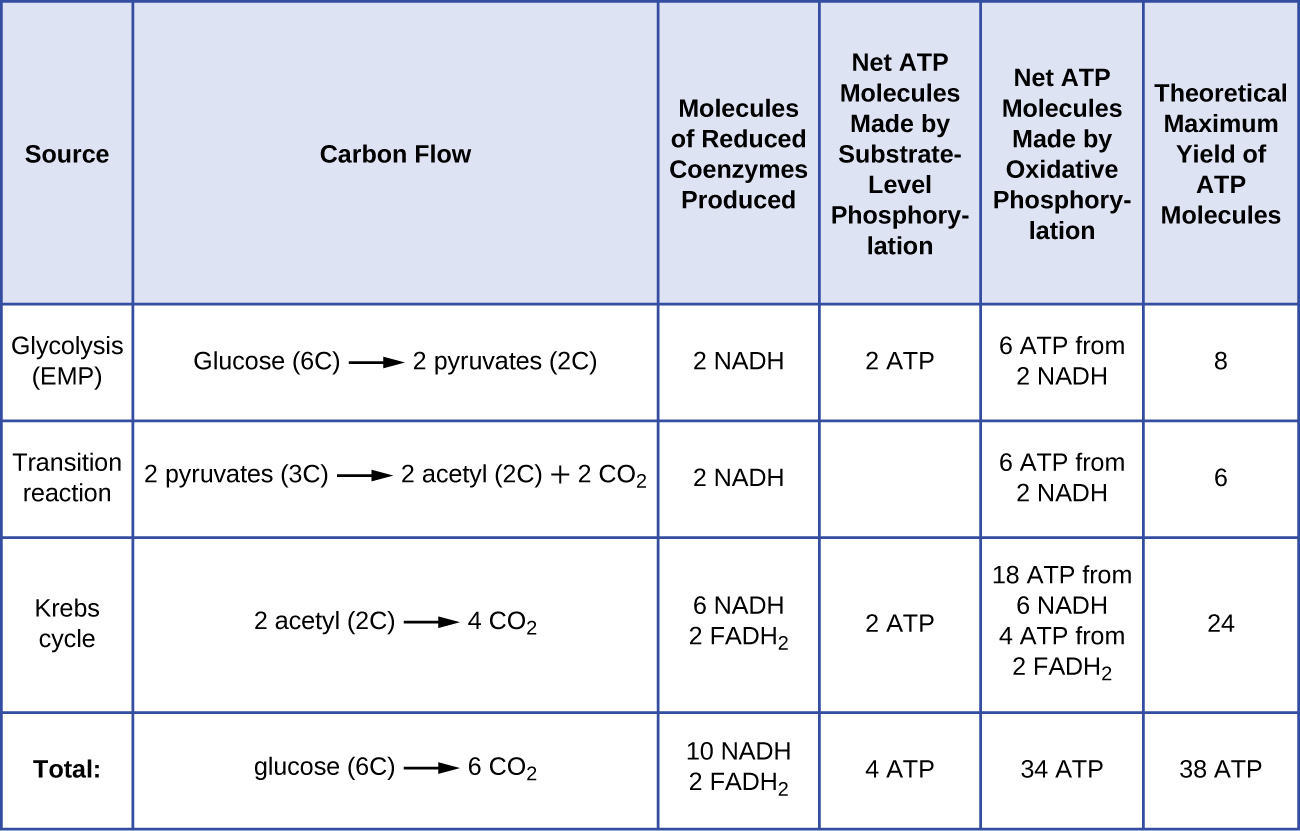
Idadi ya molekuli za ATP zinazozalishwa kutoka kwa catabolism ya glucose inatofautiana. Kwa mfano, idadi ya ioni za hidrojeni ambazo complexes za mfumo wa usafiri wa elektroni zinaweza kusukwa kupitia utando hutofautiana kati ya spishi mbalimbali za viumbe. Katika kupumua aerobic katika mitochondria, kifungu cha elektroni kutoka molekuli moja ya NADH inazalisha nguvu ya kutosha ya protoni nia ya kufanya molekuli tatu za ATP kwa phosphorylation oxidative, ambapo kifungu cha elektroni kutoka molekuli moja ya FADH 2 inazalisha nguvu za kutosha za protoni kufanya mbili tu ATP molekuli. Hivyo, molekuli 10 za NADH zilizofanywa kwa glucose wakati wa glycolysis, mmenyuko wa mpito, na mzunguko wa Krebs hubeba nishati ya kutosha kufanya molekuli 30 za ATP, wakati molekuli mbili za FADH 2 zilizofanywa kwa glucose wakati wa michakato hii hutoa nishati ya kutosha kufanya molekuli nne za ATP. Kwa ujumla, nadharia ya kiwango cha juu mavuno ATP alifanya wakati kamili aerobic kupumua ya glucose ni 38 molekuli, na nne kufanywa na substrate ngazi phosphorylation na 34 kufanywa na fosforasi oxidative (Kielelezo\(\PageIndex{2}\)). Kwa kweli, jumla ya mavuno ATP ni kawaida chini, kuanzia molekuli moja hadi 34 ATP, kulingana na kama seli ni kutumia kupumua aerobic au anaerobic kupumua; katika seli eukaryotic, nishati fulani hutumiwa kusafirisha intermediates kutoka cytoplasm ndani ya mitochondria, na kuathiri mavuno ATP.
Kielelezo\(\PageIndex{2}\) kinafupisha mavuno ya juu ya kinadharia ya ATP kutoka michakato mbalimbali wakati wa kupumua kamili ya aerobic ya molekuli moja ya glucose.
Zoezi\(\PageIndex{1}\)
Je! Ni kazi gani za nguvu ya nia ya proton?
Muhtasari
- Wengi ATP yanayotokana wakati wa kupumua kwa seli ya glucose hufanywa na phosphorylation ya oxidative.
- Mfumo wa usafiri wa elektroni (ETS) unajumuisha mfululizo wa complexes za protini zinazohusiana na membrane na flygbolag za elektroni zinazohusiana na ETS imeingizwa kwenye membrane ya cytoplasmic ya prokaryotes na membrane ya ndani ya mitochondrial ya eukaryotes.
- Kila tata ETS ina tofauti redox uwezo, na elektroni hoja kutoka flygbolag elektroni na zaidi hasi redox uwezo kwa wale walio na chanya zaidi redox uwezo.
- Ili kutekeleza kupumua kwa aerobic, kiini inahitaji oksijeni kama mpokeaji wa mwisho wa elektroni. Kiini pia inahitaji mzunguko kamili wa Krebs, saitokromu oxidase inayofaa, na enzymes ya detoxification ya oksijeni ili kuzuia madhara ya radicals ya oksijeni zinazozalishwa wakati wa kupumua aerobic.
- Viumbe kufanya anaerobic kupumua kutumia mbadala elektroni mfumo wa usafiri flygbolag kwa ajili ya uhamisho mwisho wa elektroni kwa mwisho yasiyo ya oksijeni elektroni acceptors.
- Microbes zinaonyesha tofauti kubwa katika muundo wa mifumo yao ya usafiri wa elektroni, ambayo inaweza kutumika kwa madhumuni ya uchunguzi ili kusaidia kutambua vimelea fulani.
- Kama elektroni zinapitishwa kutoka NADH na FADH 2 kupitia ETS, elektroni inapoteza nishati. Nishati hii imehifadhiwa kwa njia ya kusukumia H + kwenye membrane, na kuzalisha nguvu ya proton.
- Nishati ya nguvu hii ya motisha ya protoni inaweza kuunganishwa kwa kuruhusu ioni za hidrojeni kueneza nyuma kupitia utando kwa chemiosmosis kwa kutumia ATP synthase. Kama ioni za hidrojeni zinaenea kupitia chini ya gradient yao ya electrochemical, vipengele vya ATP synthase spin, na kufanya ATP kutoka ADP na P i kwa phosphorylation oxidative.
- Aerobic kupumua aina zaidi ATP (kiwango cha juu cha molekuli 34 ATP) wakati wa fosforasi oxidative kuliko anaerobic kupumua (kati ya molekuli moja na 32 ATP).


