7.4: Phosphorylation ya oxidative
- Page ID
- 175698
Ujuzi wa Kuendeleza
- Eleza jinsi elektroni hoja kupitia mlolongo wa usafiri wa elektroni na nini kinatokea kwa viwango vyao vya nishati
- Eleza jinsi gradient ya proton (H +) inavyoanzishwa na kudumishwa na mnyororo wa usafiri wa elektroni
Una tu kusoma kuhusu njia mbili katika glucose catabolism-glycolysis na citric acid mzunguko-kwamba kuzalisha ATP. Wengi wa ATP yanayotokana wakati wa catabolism ya aerobic ya glucose, hata hivyo, haijazalishwa moja kwa moja kutoka kwa njia hizi. Badala yake, inatokana na mchakato unaoanza na kusonga elektroni kupitia mfululizo wa wasafirishaji wa elektroni ambao hupitia athari za redox. Hii inasababisha ions hidrojeni kujilimbikiza ndani ya nafasi ya tumbo. Kwa hiyo, aina ya gradient ya mkusanyiko ambayo ioni za hidrojeni huenea nje ya nafasi ya tumbo kwa kupitia ATP synthase. Ya sasa ya ions hidrojeni inaimarisha hatua ya kichocheo cha ATP synthase, ambayo hufosforasi ADP, huzalisha ATP.
Electron usafiri mnyororo
Mlolongo wa usafiri wa elektroni (Kielelezo\(\PageIndex{1}\)) ni sehemu ya mwisho ya kupumua kwa aerobic na ni sehemu pekee ya kimetaboliki ya glucose ambayo hutumia oksijeni ya anga. Oksijeni huendelea kuenea ndani ya mimea; katika wanyama, huingia mwili kupitia mfumo wa kupumua. Usafiri wa elektroni ni mfululizo wa athari za redoksi zinazofanana na mbio ya relay au kikosi cha ndoo kwa kuwa elektroni hupitishwa haraka kutoka sehemu moja hadi nyingine, hadi mwisho wa mlolongo ambapo elektroni hupunguza oksijeni ya molekuli, kuzalisha maji. Kuna complexes nne linajumuisha protini, kinachoitwa I kupitia IV katika Kielelezo\(\PageIndex{1}\), na mkusanyiko wa complexes hizi nne, pamoja na simu zinazohusiana, vifaa vya elektroni flygbolag, inaitwa mnyororo wa usafiri wa elektroni. Mlolongo wa usafiri wa elektroni upo katika nakala nyingi katika utando wa ndani wa mitochondrial wa eukaryotes na utando wa plasma wa prokaryotes.
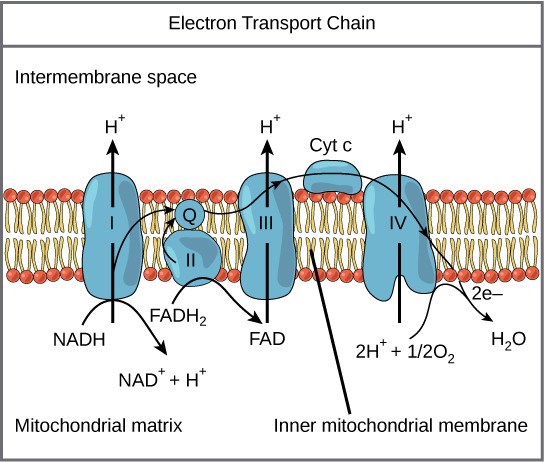
Complex mimi
Kuanza, elektroni mbili zinachukuliwa kwenye tata ya kwanza ndani ya NADH. Ugumu huu, ulioitwa I, linajumuisha mononucleotide ya flavin (FMN) na sulfuri ya chuma (Fe-S) yenye protini. FMN, inayotokana na vitamini B 2, pia huitwa riboflavin, ni moja ya makundi kadhaa ya prosthetic au mambo ya ushirikiano katika mlolongo wa usafiri wa elektroni. Kikundi cha prosthetic ni molekuli isiyo ya protini inayohitajika kwa shughuli za protini. Vikundi vya prosthetic ni kikaboni au isokaboni, molekuli zisizo za peptidi zinazofungwa na protini zinazowezesha kazi yake; vikundi vya prosthetic ni pamoja na enzymes za ushirikiano, ambazo ni makundi Enzyme katika ngumu I ni NADH dehydrogenase na ni protini kubwa sana, iliyo na minyororo 45 ya amino asidi. Complex naweza kusukwa ions nne hidrojeni katika utando kutoka tumbo katika nafasi ya intermembrane, na ni kwa njia hii ambayo hidrojeni ion gradient imara na kudumishwa kati ya compartments mbili kutengwa na ndani ya mitochondrial membrane.
Q na Complex II
Complex II moja kwa moja inapata FADH 2, ambayo haina kupita katika tata I. kiwanja kuunganisha complexes kwanza na ya pili kwa tatu ni ubiquinone (Q). Molekuli ya Q ni lipid mumunyifu na huenda kwa uhuru kupitia msingi wa hydrophobic wa membrane. Mara baada ya kupunguzwa, (QH 2), ubiquinone hutoa elektroni zake kwa tata inayofuata katika mlolongo wa usafiri wa elektroni. Q inapata elektroni inayotokana na NADH kutoka tata I na elektroni inayotokana na FADH 2 kutoka tata II, ikiwa ni pamoja na sucinate dehydrogenase. Enzyme hii na FADH 2 huunda tata ndogo ambayo hutoa elektroni moja kwa moja kwenye mnyororo wa usafiri wa elektroni, kwa kupitisha tata ya kwanza. Kwa kuwa elektroni hizi hupitia na hivyo hazizidi nguvu ya pampu ya protoni katika tata ya kwanza, molekuli chache za ATP zinafanywa kutoka kwa elektroni za FADH 2. Idadi ya molekuli za ATP hatimaye zilizopatikana ni sawia moja kwa moja na idadi ya protoni zilizopigwa kwenye utando wa ndani wa mitochondrial.
Complex III
Tata ya tatu inajumuisha saitokromu b, protini nyingine ya Fe-S, kituo cha Rieske (kituo cha 2Fe-2S), na protini za saitokromu c; tata hii pia inaitwa saitokromu oxidoreductase. Protini za cytochrome zina kikundi cha maambukizi ya heme. Molekuli ya heme ni sawa na heme katika hemoglobin, lakini hubeba elektroni, si oksijeni. Matokeo yake, ioni ya chuma katika msingi wake imepunguzwa na imeoksidishwa kama inapita elektroni, ikishuka kati ya majimbo tofauti ya oxidation: Fe ++ (kupunguzwa) na Fe +++ (iliyooksidishwa). Molekuli za heme katika cytochromes zina sifa tofauti kidogo kutokana na athari za protini tofauti zinazofunga, na kutoa sifa tofauti kidogo kwa kila tata. Complex III hupiga pampu protoni kupitia utando na hupita elektroni zake kwa saitokromu c kwa usafiri hadi tata ya nne ya protini na vimeng'enya (saitokromu c ni mpokeaji wa elektroni kutoka Q; hata hivyo, ilhali Q hubeba jozi za elektroni, saitokromu c inaweza kukubali moja tu kwa wakati).
Complex IV
Ngumu ya nne inajumuisha protini za cytochrome c, a, na a 3. Tata hii ina makundi mawili ya heme (moja katika kila moja ya cytochromes mbili, a, na a 3) na ions tatu za shaba (jozi ya Cu A na moja Cu B katika saitokromu a 3). Cytochromes hushikilia molekuli ya oksijeni imara sana kati ya ioni za chuma na shaba mpaka oksijeni imepunguzwa kabisa. Oksijeni iliyopunguzwa kisha huchukua ioni mbili za hidrojeni kutoka katikati ya jirani ili kutengeneza maji (H 2 O). Kuondolewa kwa ioni za hidrojeni kutoka kwenye mfumo huchangia kwenye gradient ya ion iliyotumiwa katika mchakato wa chemiosmosis.
Chemiosmosis
Katika chemiosmosis, nishati ya bure kutoka kwa mfululizo wa athari za redox zilizoelezwa tu hutumiwa kupiga ions hidrojeni (protoni) kwenye membrane. Usambazaji wa kutofautiana wa ioni za H + kwenye utando huanzisha mkusanyiko na gradients za umeme (kwa hiyo, gradient ya electrochemical), kutokana na malipo mazuri ya ioni ya hidrojeni na uggregation yao upande mmoja wa utando.
Kama utando walikuwa wazi kwa utbredningen na ions hidrojeni, ions ingekuwa huwa na kueneza nyuma katika tumbo, inaendeshwa na gradient yao electrochemical. Kumbuka kwamba ioni nyingi haziwezi kueneza kupitia mikoa isiyo ya polar ya membrane ya phospholipid bila msaada wa njia za ion. Vilevile, ioni za hidrojeni katika nafasi ya tumbo zinaweza tu kupita kwenye utando wa ndani wa mitochondrial kupitia protini muhimu ya utando inayoitwa ATP synthase (Kielelezo\(\PageIndex{2}\)). Protini hii ngumu hufanya kama jenereta ndogo, ikageuka na nguvu ya ions za hidrojeni zinazoenea kwa njia hiyo, chini ya gradient yao ya electrochemical. Kugeuka kwa sehemu za mashine hii ya Masi huwezesha kuongeza phosphate kwa ADP, kutengeneza ATP, kwa kutumia nishati ya uwezo wa gradient ya hidrojeni ion.
Sanaa Connection
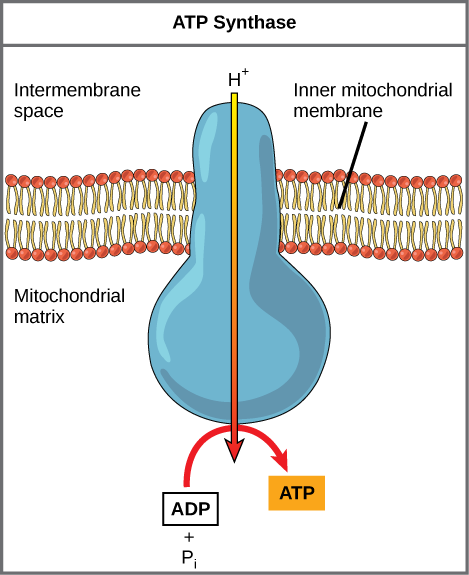
Dinitrophenol (DNP) ni uncoupler ambayo inafanya utando wa ndani wa mitochondrial uvujaji kwa protoni. Ilitumiwa hadi 1938 kama dawa ya kupoteza uzito. Ni athari gani unatarajia kuwa na DNP juu ya mabadiliko katika pH katika utando wa ndani wa mitochondrial? Kwa nini unafikiri hii inaweza kuwa dawa ya kupoteza uzito?
Chemiosmosis (Kielelezo\(\PageIndex{3}\)) hutumiwa kuzalisha asilimia 90 ya ATP iliyotengenezwa wakati wa catabolism ya aerobic ya glucose; pia ni njia inayotumiwa katika athari za mwanga wa photosynthesis ili kuunganisha nishati ya jua katika mchakato wa photophosphorylation. Kumbuka kwamba uzalishaji wa ATP kwa kutumia mchakato wa chemiosmosis katika mitochondria inaitwa phosphorylation oxidative. Matokeo ya jumla ya athari hizi ni uzalishaji wa ATP kutoka nishati ya elektroni zilizoondolewa kwenye atomi za hidrojeni. Atomi hizi awali zilikuwa sehemu ya molekuli ya glucose. Mwishoni mwa njia, elektroni hutumiwa kupunguza molekuli ya oksijeni kwa ions za oksijeni. Electroni za ziada kwenye oksijeni huvutia ions hidrojeni (protons) kutoka katikati ya jirani, na maji hutengenezwa.
Sanaa Connection
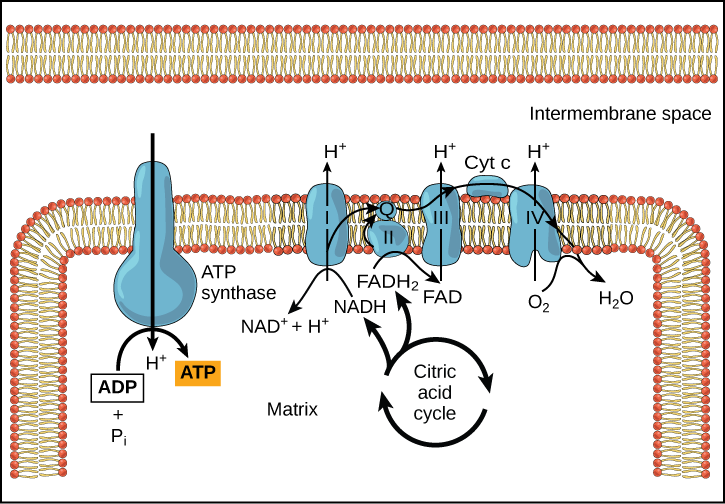
Cyanide inhibitisha cytochrome c oxidase, sehemu ya mnyororo wa usafiri wa elektroni. Ikiwa sumu ya cyanide hutokea, ungependa kutarajia pH ya nafasi ya intermembrane kuongezeka au kupungua? Nini athari ingekuwa cyanide juu ya ATP awali?
ATP mavuno
Idadi ya molekuli za ATP zinazozalishwa kutoka kwa catabolism ya glucose inatofautiana. Kwa mfano, idadi ya ioni za hidrojeni ambazo tata za mnyororo wa usafiri wa elektroni zinaweza kusukwa kupitia utando hutofautiana kati ya spishi. Chanzo kingine cha ugomvi kinatokana na kuhamishwa kwa elektroni kwenye utando wa mitochondria. (NADH yanayotokana na glycolysis haiwezi kuingia kwa urahisi mitochondria.) Hivyo, elektroni huchukuliwa ndani ya mitochondria na ama NAD + au FAD +. Kama umejifunza mapema, hizi molekuli za FAD + zinaweza kusafirisha ions chache; kwa hiyo, molekuli chache za ATP zinazalishwa wakati FAD + hufanya kama carrier. NAD + hutumika kama transporter elektroni katika ini na FAD + vitendo katika ubongo.
Sababu nyingine inayoathiri mavuno ya molekuli za ATP zinazozalishwa kutoka glucose ni ukweli kwamba misombo ya kati katika njia hizi hutumiwa kwa madhumuni mengine. Ukataji wa glucose unajumuisha na njia zinazojenga au kuvunja misombo mengine yote ya biochemical katika seli, na matokeo yake ni kiasi fulani zaidi kuliko hali bora zilizoelezwa hadi sasa. Kwa mfano, sukari isipokuwa glucose hutumiwa kwenye njia ya glycolytic ya uchimbaji wa nishati. Aidha, sukari tano za kaboni ambazo huunda asidi za nucleic zinafanywa kutoka kwa intermediates katika glycolysis. Baadhi ya asidi amino zisizo muhimu zinaweza kufanywa kutoka kwa kati ya glycolysis zote mbili na mzunguko wa asidi ya citric. Lipids, kama vile cholesterol na triglycerides, pia hufanywa kutoka kwa waamuzi katika njia hizi, na amino asidi na triglycerides huvunjika kwa nishati kupitia njia hizi. Kwa ujumla, katika mifumo ya maisha, hizi pathways ya glucose catabolism dondoo kuhusu asilimia 34 ya nishati zilizomo katika glucose.
Muhtasari
Mlolongo wa usafiri wa elektroni ni sehemu ya kupumua kwa aerobic inayotumia oksijeni ya bure kama mpokeaji wa elektroni wa mwisho wa elektroni iliyoondolewa kwenye misombo ya kati katika catabolism ya glucose. Mlolongo wa usafiri wa elektroni unajumuisha complexes nne kubwa, multiprotein zilizoingia ndani ya utando wa mitochondrial na flygbolag mbili ndogo za elektroni zinazotenganishwa kati yao. Electroni hupitia mfululizo wa athari za redox, huku kiasi kidogo cha nishati ya bure inayotumiwa kwa pointi tatu kusafirisha ioni za hidrojeni kwenye membrane. Utaratibu huu unachangia kwenye gradient kutumika katika chemiosmosis. Elektroni zinazopita katika mnyororo wa usafiri wa elektroni hatua kwa hatua hupoteza nishati, elektroni za nishati za juu zinazotolewa kwa mnyororo kwa ama NADH au FADH 2 zinakamilisha mlolongo, kwani elektroni za nishati za chini hupunguza molekuli za oksijeni na Kiwango cha nishati ya bure ya elektroni hupungua kutoka takriban 60 kcal/mol katika NADH au 45 kcal/mol katika FADH 2 hadi takriban 0 kcal/mol katika maji. Bidhaa za mwisho za mnyororo wa usafiri wa elektroni ni maji na ATP. Idadi ya misombo ya kati ya mzunguko wa asidi ya citric inaweza kuwa waliamua katika anabolism ya molekuli nyingine biochemical, kama vile nonessential amino asidi, sukari, na lipids. Molekuli hizi zinaweza kutumika kama vyanzo vya nishati kwa njia za glucose.
Sanaa Connections
Kielelezo\(\PageIndex{2}\): Dinitrophenol (DNP) ni uncoupler ambayo inafanya utando wa ndani wa mitochondrial uvujaji kwa protoni. Ilitumiwa hadi 1938 kama dawa ya kupoteza uzito. Ni athari gani unatarajia kuwa na DNP juu ya mabadiliko katika pH katika utando wa ndani wa mitochondrial? Kwa nini unafikiri hii inaweza kuwa dawa ya kupoteza uzito?
- Jibu
-
Baada ya sumu ya DNP, mnyororo wa usafiri wa elektroni hauwezi tena kuunda gradient ya proton, na synthase ya ATP haiwezi tena kufanya ATP. DNP ni dawa bora ya chakula kwa sababu haifai awali ya ATP; kwa maneno mengine, baada ya kuichukua, mtu hupata nishati kidogo nje ya chakula anachokula. Kushangaza, moja ya madhara mabaya zaidi ya dawa hii ni hyperthermia, au overheating ya mwili. Kwa kuwa ATP haiwezi kuundwa, nishati kutoka usafiri wa elektroni inapotea kama joto.
Kielelezo\(\PageIndex{3}\): Cyanide inhibitisha cytochrome c oxidase, sehemu ya mnyororo wa usafiri wa elektroni. Ikiwa sumu ya cyanide hutokea, ungependa kutarajia pH ya nafasi ya intermembrane kuongezeka au kupungua? Nini athari ingekuwa cyanide juu ya ATP awali?
- Jibu
-
Baada ya sumu ya cyanide, mnyororo wa usafiri wa elektroni hauwezi tena kupiga elektroni kwenye nafasi ya intermembrane. PH ya nafasi ya intermembrane itaongezeka, gradient ya pH ingepungua, na awali ya ATP ingeacha.
faharasa
- ATP synthase
- (pia, F1F0 ATP synthase) utando iliyoingia protini tata ambayo inaongeza phosphate kwa ADP na nishati kutoka protoni diffusing kwa njia hiyo
- kikundi cha prosthetic
- (pia, cofactor prosthetic) molekuli amefungwa kwa protini ambayo inawezesha kazi ya protini
- ubiquinone
- mumunyifu elektroni transporter katika mnyororo elektroni usafiri kwamba unajumuisha tata kwanza au ya pili ya tatu


