17.2: Viini vya Galvanic
- Page ID
- 176088
- Tumia notation ya seli kuelezea seli za galvanic
- Eleza vipengele vya msingi vya seli za galvanic
Seli za Galvanic, pia hujulikana kama seli za voltaic, ni seli za electrochemical ambazo athari za kupunguza oksidi za kutosha huzalisha nishati ya umeme. Kwa kuandika equations, mara nyingi ni rahisi kutenganisha athari za kupunguza oxidation katika athari za nusu ili kuwezesha kusawazisha usawa wa jumla na kusisitiza mabadiliko halisi ya kemikali.
Fikiria kinachotokea wakati kipande safi cha chuma cha shaba kinawekwa katika suluhisho la nitrati ya fedha (Kielelezo\(\PageIndex{1}\)). Mara baada ya chuma cha shaba kinaongezwa, chuma cha fedha huanza kuunda na ions za shaba hupita katika suluhisho. Rangi ya bluu ya suluhisho upande wa kulia inaonyesha uwepo wa ions za shaba. Majibu yanaweza kugawanywa katika athari zake mbili za nusu. Nusu-athari hutenganisha oxidation kutoka kupunguza, hivyo kila mmoja anaweza kuchukuliwa mmoja mmoja.
\ [kuanza {align}
&\ textrm {oxidation:}\ ce {Cu} (s)\ ce {Cu ^ 2+} (aq) +\ ce {2e-}\\
&\ kusisitiza {\ maandishi {kupunguza:} 2x (\ ce {Ag+} (aq) +\ ce {e-}\ ce {Ag} (s)\ {s} (s)\ hspace {40px}\ ce {au}\ nafasi {40px}\ ce {2Ag +} (aq) +\ ce {2e-}\ ce {2Ag} (s)}\\
&\ textrm {jumla:}\ ce {2Ag +} (aq) +\ ce {Cu} (s)\ ce {2Ag} (s) +\ ce {Cu ^ 2+} (aq)
\ mwisho {align}\ namba\]
Ulinganisho kwa nusu-mmenyuko wa kupunguza ulipaswa kuwa mara mbili hivyo elektroni za namba “zilizopatikana” katika kupunguza nusu-mmenyuko ililingana na idadi ya elektroni “zilizopotea” katika nusu-mmenyuko wa oksidi.

Seli za Galvanic au voltaic zinahusisha athari za electrochemical za hiari ambazo athari za nusu zinajitenga (Kielelezo\(\PageIndex{2}\)) ili sasa inaweza kuzunguka kupitia waya wa nje. Beaker upande wa kushoto wa takwimu inaitwa nusu-kiini, na ina 1 M ufumbuzi wa shaba (II) nitrate [Cu (NO 3) 2] na kipande cha chuma cha shaba sehemu iliyoingia katika suluhisho. Chuma cha shaba ni electrode. Shaba inafanyika oxidation; kwa hiyo, electrode ya shaba ni anode. Anode imeunganishwa na voltmeter na waya na terminal nyingine ya voltmeter imeshikamana na electrode ya fedha na waya. Fedha inapungua; kwa hiyo, electrode ya fedha ni cathode. Kiini cha nusu upande wa kulia wa takwimu kina electrode ya fedha katika suluhisho la 1 M la nitrati ya fedha (AgNo 3). Katika hatua hii, hakuna mtiririko wa sasa—yaani, hakuna mwendo mkubwa wa elektroni kupitia waya hutokea kwa sababu mzunguko umefunguliwa. Mzunguko umefungwa kwa kutumia daraja la chumvi, ambalo hupeleka sasa na ions zinazohamia. Daraja la chumvi lina ufumbuzi wa kujilimbikizia, usio na ufanisi, wa electrolyte kama vile ufumbuzi wa nitrati ya sodiamu (nano 3) iliyotumiwa katika mfano huu. Kama elektroni inapita kutoka kushoto kwenda kulia kwa njia ya electrode na waya, ions nitrate (anions) hupita kupitia kuziba porous upande wa kushoto ndani ya suluhisho la shaba (II) nitrate. Hii inaweka beaker upande wa kushoto umeme neutral kwa neutralizing malipo juu ya ions shaba (II) zinazozalishwa katika suluhisho kama chuma shaba ni oxidized. Wakati huo huo, ioni za nitrati zinahamia upande wa kushoto, ions za sodiamu (cations) zinahamia kulia, kwa njia ya kuziba porous, na kwenye ufumbuzi wa nitrati ya fedha upande wa kulia. Hizi cations aliongeza “kuchukua nafasi” ions fedha ambayo ni kuondolewa kutoka ufumbuzi kama wao walikuwa kupunguzwa kwa chuma fedha, kuweka beaker juu ya haki ya umeme neutral. Bila daraja la chumvi, vyumba havikubaki umeme neutral na hakuna sasa muhimu ingekuwa kati yake. Hata hivyo, ikiwa vyumba viwili vinawasiliana moja kwa moja, daraja la chumvi sio lazima. Papo hapo mzunguko umekamilika, voltmeter inasoma +0.46 V, hii inaitwa uwezo wa seli. Uwezo wa seli huundwa wakati metali mbili tofauti zinaunganishwa, na ni kipimo cha nishati kwa malipo ya kitengo kinachopatikana kutokana na mmenyuko wa kupunguza oksidi. Volt ni kitengo cha SI kilichotokana na uwezo wa umeme
\[\mathrm{volt=\mathit{V}=\dfrac{J}{C}} \nonumber \]
Katika equation hii, A ni ya sasa katika amperes na C malipo katika coulombs. Kumbuka kwamba volts lazima iongezwe na malipo katika coulombs (C) ili kupata nishati katika joules (J).
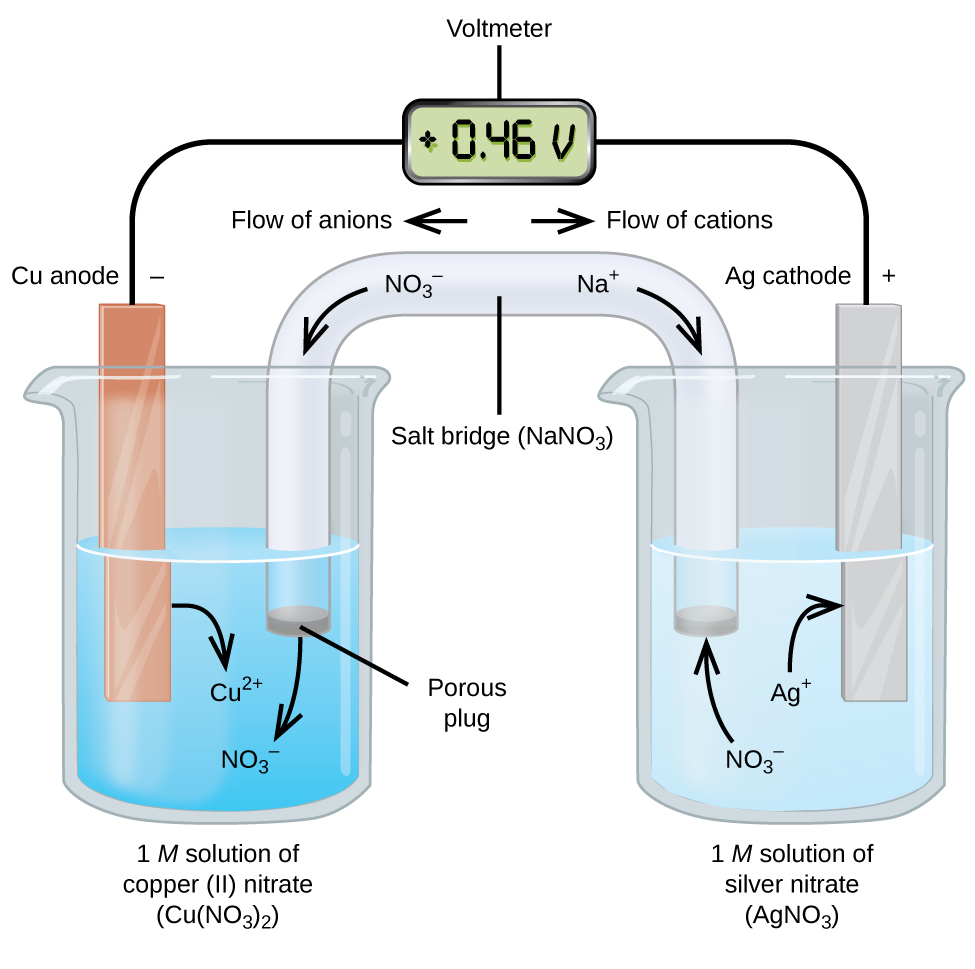
Wakati kiini cha electrochemical kinajengwa kwa mtindo huu, uwezo wa kiini chanya unaonyesha mmenyuko wa pekee na kwamba elektroni zinatoka upande wa kushoto kwenda kulia. Kuna mengi kinachoendelea katika Kielelezo\(\PageIndex{2}\), hivyo ni muhimu kwa muhtasari mambo kwa ajili ya mfumo huu:
- Electroni hutoka kutoka kwa anode hadi cathode: kushoto kwenda kulia katika kiini cha kawaida cha galvanic katika takwimu.
- Electrode katika nusu ya kiini cha kushoto ni anode kwa sababu oxidation hutokea hapa. Jina linamaanisha mtiririko wa anioni katika daraja la chumvi kuelekea humo.
- Electrode katika nusu ya kiini sahihi ni cathode kwa sababu kupunguza hutokea hapa. Jina linamaanisha mtiririko wa cations katika daraja la chumvi kuelekea hilo.
- Oxidation hutokea kwenye anode (kiini cha nusu ya kushoto katika takwimu).
- Kupunguza hutokea kwenye cathode (kiini cha nusu sahihi katika takwimu).
- Uwezo wa seli, +0.46 V, katika kesi hii, unatokana na tofauti za asili katika asili ya vifaa vinavyotumiwa kufanya seli mbili za nusu.
- Daraja la chumvi lazima liwepo karibu (kukamilisha) mzunguko na wote oxidation na kupunguza lazima kutokea kwa sasa inapita.
Kuna seli nyingi za galvanic zinazowezekana, hivyo notation ya shorthand hutumiwa kuwaelezea. Nukuu ya seli (wakati mwingine huitwa mchoro wa seli) hutoa taarifa kuhusu spishi mbalimbali zinazohusika katika mmenyuko. Uthibitisho huu pia unafanya kazi kwa aina nyingine za seli. Mstari wa wima, │, unaashiria mipaka ya awamu na mstari wa mara mbili,, daraja la chumvi. Taarifa kuhusu anode imeandikwa upande wa kushoto, ikifuatiwa na suluhisho la anode, kisha daraja la chumvi (wakati wa sasa), kisha suluhisho la cathode, na hatimaye, habari kuhusu cathode kwa haki. notation kiini kwa kiini galvanic katika Kielelezo\(\PageIndex{2}\) ni basi
\[\ce{Cu}(s)│\ce{Cu^2+}(aq,\: 1\:M)║\ce{Ag+}(aq,\: 1\:M)│\ce{Ag}(s) \nonumber \]
Kumbuka kuwa ions za mtazamaji hazijumuishwa na kwamba fomu rahisi ya kila majibu ya nusu ilitumiwa. Inapojulikana, viwango vya awali vya ions mbalimbali hujumuishwa.
Moja ya seli rahisi ni kiini cha Daniell. Inawezekana kujenga betri hii kwa kuweka electrode ya shaba chini ya jar na kufunika chuma na suluhisho la sulfate ya shaba. Suluhisho la sulfate ya zinki linazunguka juu ya suluhisho la sulfate ya shaba; kisha electrode ya zinki imewekwa katika suluhisho la sulfate ya zinki. Kuunganisha electrode ya shaba kwenye electrode ya zinki inaruhusu sasa umeme uingie. Huu ni mfano wa kiini bila daraja la chumvi, na ions zinaweza kuingilia kati ya interface kati ya ufumbuzi wawili.
Baadhi ya athari za kupunguza oksidi huhusisha aina ambazo ni makondakta maskini wa umeme, na hivyo electrode hutumiwa ambayo haina kushiriki katika athari. Mara kwa mara, electrode ni platinamu, dhahabu, au grafiti, ambayo yote ni inert kwa athari nyingi za kemikali. Mfumo mmoja huo umeonyeshwa kwenye Kielelezo\(\PageIndex{3}\). Magnesiamu inakabiliwa na oxidation katika anode upande wa kushoto katika takwimu na ions hidrojeni hupungua kwa cathode upande wa kulia. Majibu yanaweza kufupishwa kama
\ [kuanza {align}
&\ textrm {oxidation:}\ ce {Mg} (s)\ ce {Mg ^ 2+} (q) +\ ce {2e-}\\
&\ maandishi {kupunguza:}\ ce {2H +} (q) +\ ce {2e-}\ ce {H2} (g)\\
& overline {\ maandishi {{jumla:}\ ce {Mg} (s) +\ ce {2H +} (aq)\ ce {Mg ^ 2+} (aq) +\ ce {H2} (g)}
\ mwisho {align}\ nonumber\]
Kiini kilitumia waya ya platinum ya inert kwa cathode, hivyo notation ya seli ni
\[\ce{Mg}(s)│\ce{Mg^2+}(aq)║\ce{H+}(aq)│\ce{H2}(g)│\ce{Pt}(s) \nonumber \]
Electrode ya magnesiamu ni electrode ya kazi kwa sababu inashiriki katika mmenyuko wa kupunguza oxidation. Electrodes ya inert, kama electrode ya platinum katika Kielelezo\(\PageIndex{3}\), usishiriki katika mmenyuko wa kupunguza oxidation na upo ili sasa sasa inaweza kuzunguka kupitia seli. Platinamu au dhahabu kwa ujumla hufanya electrodes nzuri ya inert kwa sababu hazina kemikali.

Fikiria kiini cha galvanic kilicho na
\[\ce{2Cr}(s)+\ce{3Cu^2+}(aq)⟶\ce{2Cr^3+}(aq)+\ce{3Cu}(s) \nonumber \]
Andika oxidation na kupunguza athari za nusu na uandike majibu kwa kutumia notation ya seli. Ambayo mmenyuko hutokea kwenye anode? Cathode?
Suluhisho
Kwa ukaguzi, Cr inaoksidishwa wakati elektroni tatu zinapotea kuunda Cr 3 +, na Cu 2 + hupunguzwa kwani inapata elektroni mbili kuunda Cu. Kusawazisha malipo inatoa
\ [kuanza {align}
&\ textrm {oxidation:}\ ce {2Cr} (s)\ ce {2Cr ^ 3+} (aq) +\ ce {6e-}\\
&\ textrm {kupunguza:}\ ce {3Cu ^ 2+} (q) +\ ce {6e-}\ ce {3Cu} (s)\\
&\ overline {\ textrm {jumla:}\ ce {2Cr} (s) +\ ce {3Cu ^ 2+} (aq)\ ce {2Cr ^ 3+} (aq) +\ ce {3Cu} (s)}
\ mwisho {align}\ hakuna idadi\]
Uthibitishaji wa kiini hutumia fomu rahisi ya kila equations, na huanza na majibu kwenye anode. Hakuna viwango vilivyotajwa hivyo:
\[\ce{Cr}(s)│\ce{Cr^3+}(aq)║\ce{Cu^2+}(aq)│\ce{Cu}(s). \nonumber \]
Oxidation hutokea kwenye anode na kupunguza kwenye cathode.
Fikiria kiini cha galvanic kilicho na
\[\ce{5Fe^2+}(aq)+\ce{MnO4-}(aq)+\ce{8H+}(aq)⟶\ce{5Fe^3+}(aq)+\ce{Mn^2+}(aq)+\ce{4H2O}(l) \nonumber \]
Andika oxidation na kupunguza athari za nusu na uandike majibu kwa kutumia notation ya seli. Ambayo mmenyuko hutokea kwenye anode? Cathode?
Suluhisho
Kwa ukaguzi, Fe 2 + inakabiliwa na oxidation wakati elektroni moja inapotea kuunda Fe 3 +, na MNo 4 - imepunguzwa kama inapata elektroni tano kuunda Mn 2 +. Kusawazisha malipo inatoa
\ [kuanza {align}
&\ textrm {oxidation:} 5 (\ ce {Fe ^ 2+} (aq)\ ce {Fe ^ 3+} (aq) +\ ce {e-})\\
&\ kusisitiza {\ maandishi {kupunguza:}\ ce {mNO4-} (aq) +\ ce {5e-}\ ce {Mn ^ 2+} (aq) +\ ce {4H2O} (l)}\\
&\ maandishi {jumla:}\ ce {5Fe ^ 2+} (aq) +\ ce {mNO4-} (aq) +\ ce {8H +} (aq)\ ce {5Fe ^ 3+} (aq ) +\ ce {Mn ^ 2+} (aq) +\ ce {4H2O} (l)
\ mwisho {align}\ nonumber\]
Uthibitishaji wa kiini hutumia fomu rahisi ya kila equations, na huanza na majibu kwenye anode. Ni muhimu kutumia electrode ya inert, kama vile platinum, kwa sababu hakuna chuma sasa kufanya elektroni kutoka anode hadi cathode. Hakuna viwango vilivyotajwa hivyo:
\[\ce{Pt}(s)│\ce{Fe^2+}(aq),\: \ce{Fe^3+}(aq)║\ce{MnO4-}(aq),\: \ce{H+}(aq),\: \ce{Mn^2+}(aq)│\ce{Pt}(s). \nonumber \]
Oxidation hutokea kwenye anode na kupunguza kwenye cathode.
Tumia nukuu za seli kuelezea kiini cha galvaniki ambako ioni za shaba (II) zinapunguzwa kuwa chuma cha shaba na chuma cha zinki kinaoksidishwa kwa ioni za zinki.
- Jibu
-
Kutoka kwa habari iliyotolewa katika tatizo:
\ [kuanza {align}
&\ textrm {anode (oxidation):}\ ce {Zn} (s)\ ce {Zn ^ 2+} (aq) +\ ce {2e-}\\
&\ textrm {cathode (kupunguza):}\ ce {Cu}\\\ overline {\
textrm {jumla:}\ ce {Zn} (s) +\ ce {Cu ^ 2+} (aq)\ ce {Zn ^ 2+} (aq) +\ ce {Cu} (s)}
\ mwisho {align}\ nonumber\]Kutumia notation ya seli:
\[\ce{Zn}(s)│\ce{Zn^2+}(aq)║\ce{Cu^2+}(aq)│\ce{Cu}(s) \nonumber. \nonumber \]
Muhtasari
Seli za electrochemical kawaida zinajumuisha seli mbili za nusu. Seli za nusu hutenganisha majibu ya nusu ya oxidation kutoka kwa nusu ya mmenyuko wa kupunguza na kufanya iwezekanavyo kwa sasa kupitia waya wa nje. Kiini kimoja cha nusu, kwa kawaida kinachoonyeshwa upande wa kushoto katika takwimu, kina anode. Oxidation hutokea kwenye anode. Anode imeshikamana na cathode katika nusu nyingine ya kiini, mara nyingi huonyeshwa upande wa kulia katika takwimu. Kupunguza hutokea kwenye cathode. Kuongeza daraja la chumvi hukamilisha mzunguko kuruhusu sasa kuingia. Anions katika daraja la chumvi hutembea kuelekea anode na cations katika mtiririko wa daraja la chumvi kuelekea cathode. Mwendo wa ions hizi hukamilisha mzunguko na huweka kila nusu-kiini electrically neutral. Seli za electrochemical zinaweza kuelezewa kwa kutumia notation ya seli. Katika maelezo haya, habari kuhusu mmenyuko kwenye anode inaonekana upande wa kushoto na habari kuhusu mmenyuko kwenye cathode upande wa kulia. Daraja la chumvi linawakilishwa na mstari wa mara mbili, 合. Awamu imara, kioevu, au maji ya ndani ya nusu ya kiini hutenganishwa na mstari mmoja, │. Awamu na ukolezi wa aina mbalimbali hujumuishwa baada ya jina la spishi. Electrodes zinazoshiriki katika mmenyuko wa kupunguza oxidation huitwa electrodes hai. Electrodes ambazo hazishiriki katika mmenyuko wa kupunguza oxidation lakini kuna kuruhusu sasa kuzunguka ni electrodes ya inert. Electrodes ya inert mara nyingi hufanywa kutoka platinamu au dhahabu, ambayo haibadilishwa na athari nyingi za kemikali.
faharasa
- electrode hai
- electrode ambayo inashiriki katika mmenyuko wa kupunguza oxidation ya kiini cha electrochemical; wingi wa mabadiliko ya electrode ya kazi wakati wa mmenyuko wa kupunguza oxidation
- anodi
- electrode katika kiini electrochemical ambayo oxidation hutokea; habari kuhusu anode imeandikwa upande wa kushoto wa daraja la chumvi katika notation ya seli
- kathodi
- electrode katika kiini electrochemical ambayo kupunguza hutokea; habari kuhusu cathode imeandikwa upande wa kulia wa daraja la chumvi katika notation ya seli
- kiini nukuu
- shorthand njia ya kuwakilisha athari katika kiini electrochemical
- uwezo wa seli
- tofauti katika uwezo wa umeme unaojitokeza wakati metali tofauti zinaunganishwa; nguvu ya kuendesha gari kwa mtiririko wa malipo (sasa) katika athari za kupunguza oxidation
- kiini cha galvanic
- kiini cha electrochemical kinachohusisha mmenyuko wa kupunguza oxidation; seli za electrochemical zilizo na uwezo wa seli nzuri; pia huitwa kiini cha voltaic
- electrode ya ajizi
- electrode ambayo inaruhusu sasa inapita, lakini hiyo haina kushiriki katika mmenyuko wa kupunguza oxidation katika kiini electrochemical; wingi wa electrode ya inert haubadilika wakati wa mmenyuko wa kupunguza oxidation; electrodes ya inert mara nyingi hutengenezwa kwa platinamu au dhahabu kwa sababu metali hizi ni kemikali unreactive.
- kiini cha voltaic
- jina jingine kwa kiini cha galvanic


