14.2: pH na PoH
- Page ID
- 176954
- Eleza Tabia ya ufumbuzi wa maji kama tindikali, msingi, au neutral
- Express viwango vya hidroniamu na hidroksidi ioni kwenye mizani ya pH na poH
- Fanya mahesabu yanayohusiana na pH na PoH
Kama ilivyojadiliwa hapo awali, ioni za hidroniamu na hidroksidi zipo katika maji safi na katika ufumbuzi wote wa maji, na viwango vyao ni inversely sawia kama ilivyoelezwa na bidhaa ion ya maji (\(K_w\)). Viwango vya ioni hizi katika suluhisho mara nyingi ni vitambulisho muhimu vya mali ya suluhisho na tabia za kemikali za solutes zake nyingine, na msamiati maalum umeandaliwa kuelezea viwango hivi kwa maneno ya jamaa. Suluhisho ni neutral ikiwa ina viwango sawa vya ioni za hidroniamu na hidroksidi; tindikali ikiwa ina mkusanyiko mkubwa wa ioni za hidroniamu kuliko ioni za hidroksidi; na msingi ikiwa ina mkusanyiko mdogo wa ioni za hidroniamu kuliko ioni za hidroksidi.
Njia ya kawaida ya kuelezea kiasi, maadili ambayo yanaweza kuagiza amri nyingi za ukubwa, ni kutumia kiwango cha logarithmic. Kiwango kimoja ambacho kinajulikana sana kwa viwango vya kemikali na vipindi vya usawa hutegemea p-kazi, hufafanuliwa kama inavyoonyeshwa ambapo “X” ni wingi wa riba na “logi” ni logarithm ya msingi ya 10:
\[\mathrm{pX=−\log X} \label{1} \]
Kwa hiyo pH ya suluhisho hufafanuliwa kama inavyoonekana hapa, ambapo [H 3 O +] ni mkusanyiko wa molar wa ioni ya hidroniamu katika suluhisho:
\[\mathrm{pH=-\log[H_3O^+]}\label{\(\PageIndex{2}\)} \]
Kurekebisha equation hii ili kutenganisha molarity ya hydronium ion huzaa kujieleza sawa:
\[\mathrm{[H_3O^+]=10^{−pH}}\label{\(\PageIndex{3}\)} \]
Vivyo hivyo, molarity ya ioni ya hidroksidi inaweza kuelezwa kama p-kazi, au oH:
\[\mathrm{pOH=-\log [OH^−]}\label{\(\PageIndex{4}\)} \]
au
\[\mathrm{[OH^-]=10^{−pOH}} \label{\(\PageIndex{5}\)} \]
Hatimaye, uhusiano kati ya hizi mbili ion mkusanyiko walionyesha kama p-kazi ni rahisi inayotokana na\(K_w\) kujieleza:
\[K_\ce{w}=\ce{[H_3O^+][OH^- ]} \label{\(\PageIndex{6}\)} \]
\[-\log K_\ce{w}=\mathrm{-\log([H_3O^+][OH^−])=-\log[H_3O^+] + -\log[OH^-]}\label{\(\PageIndex{7}\)} \]
\[\mathrm{p\mathit{K}_w=pH + pOH} \label{\(\PageIndex{8}\)} \]
Katika 25 °C, thamani ya\(K_w\) ni\(1.0 \times 10^{−14}\), na hivyo:
\[\mathrm{14.00=pH + pOH} \label{\(\PageIndex{9}\)} \]
Molarity ioni ya hidroniamu katika maji safi (au suluhisho lolote la neutral) ni\( 1.0 \times 10^{-7}\; M\) saa 25 °C. pH na poH ya suluhisho la neutral katika joto hili ni kwa hiyo:
\[\mathrm{pH=-\log[H_3O^+]=-\log(1.0\times 10^{−7}) = 7.00} \label{10} \]
\[\mathrm{pOH=-\log[OH^−]=-\log(1.0\times 10^{−7}) = 7.00} \label{11} \]
Na hivyo, katika joto hili, ufumbuzi tindikali ni wale walio na hidronium ion molarities kubwa kuliko\( 1.0 \times 10^{-7}\; M\) na hidroksidi ion molarities chini ya\( 1.0 \times 10^{-7}\; M\) (sambamba na maadili ya pH chini ya 7.00 na maadili PoH zaidi ya 7.00). Ufumbuzi wa msingi ni wale walio na molarities ya ioni ya hidroniamu chini ya\( 1.0 \times 10^{-7}\; M\) na molarities ya ioni ya hidroksidi zaidi kuliko\( 1.0 \times 10^{-7}\; M\) (sambamba na maadili ya pH zaidi ya 7.00 na maadili ya pH chini ya 7.00).
Kwa kuwa mara kwa mara ya autoionization\(K_w\) ni tegemezi ya joto, uhusiano huu kati ya maadili ya pH na vivumishi vya asidi/neutral/msingi zitakuwa tofauti katika joto lingine zaidi ya 25 °C Kwa mfano, molarity ya hidroniamu ya maji safi kwenye 80 °C ni 4.9 × 10 -7 M, ambayo inalingana na maadili ya pH na PoH ya:
\[\begin{align*} pH &=-\log[\ce{H_3O^+}] \\[4pt] &= -\log(4.9\times 10^{−7}) \\[4pt] &=6.31 \label{12} \end{align*} \]
\[\begin{align*} pOH &=-\log[\ce{OH^-}]\\[4pt] & =-\log(4.9\times 10^{−7}) \\[4pt] &=6.31 \label{13}\end{align*} \]
Kwa joto hili, basi, ufumbuzi wa neutral unaonyesha pH = PoH = 6.31, ufumbuzi wa tindikali huonyesha pH chini ya 6.31 na poH kubwa kuliko 6.31, wakati ufumbuzi wa msingi unaonyesha pH kubwa kuliko 6.31 na PoH chini ya 6.31. Tofauti hii inaweza kuwa muhimu wakati wa kusoma michakato fulani ambayo hutokea kwa joto lisilo na kiwango, kama vile athari za enzyme katika viumbe vyenye joto. Isipokuwa isipotajwa vinginevyo, marejeo ya maadili ya pH yanadhaniwa kuwa yale yaliyo kwenye joto la kawaida (25 °C) (Jedwali\(\PageIndex{1}\)).
| Uainishaji | Jamaa Ion Viwango | pH saa 25 °C |
|---|---|---|
| tindikali | [H 3 O +] > [OH -] | pH <7 |
| upande wowote | [H 3 O +] = [OH ∙] | pH = 7 |
| msingi | [H 3 O +] <[ OH ∙] | pH > 7 |
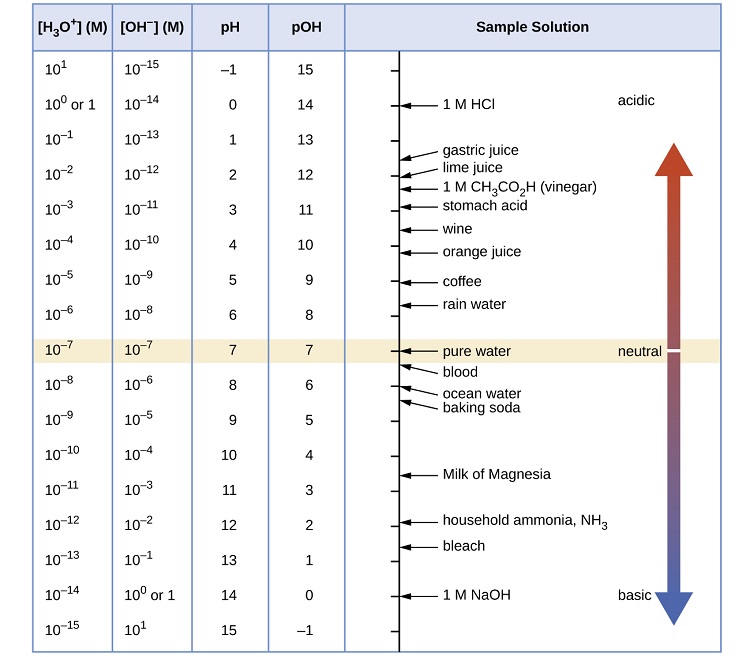
Kielelezo\(\PageIndex{1}\) kinaonyesha uhusiano kati ya [H 3 O +], [OH-], pH, na PoH, na hutoa maadili kwa mali hizi kwa joto la kawaida kwa vitu vingine vya kawaida.
Je, ni pH ya asidi ya tumbo, suluhisho la HCl na mkusanyiko wa ioni ya hydronium\(1.2 \times 10^{−3}\; M\)?
Suluhisho
\[\begin{align*} pH &=-\log [H_3O^+] \\[4pt] &= -\log(1.2 \times 10^{−3}) \\[4pt] &=−(−2.92) \\[4pt]&=2.92 \end{align*} \nonumber \]
Maji yaliyo wazi kwa hewa yana asidi ya kaboni, H 2 CO 3, kutokana na mmenyuko kati ya dioksidi kaboni na maji:
\[\ce{CO2(aq) + H2O (l) \rightleftharpoons H2CO3(aq)} \nonumber \]
Hewa ulijaa maji ina hydronium ion mkusanyiko unasababishwa na\(\ce{CO_2}\) kufutwa ya\(2.0 \times 10^{−6}\; M\), kuhusu 20 mara kubwa kuliko ile ya maji safi. Tumia pH ya suluhisho saa 25 °C.
- Jibu
-
5.70
Tumia mkusanyiko wa ioni ya hydronium ya damu, pH ambayo ni 7.3 (kidogo ya alkali).
Suluhisho
\[\mathrm{pH=-\log[H_3O^+]=7.3} \nonumber \]
\[\mathrm{\log[H_3O^+]=−7.3} \nonumber \]
\[\mathrm{[H_3O^+]=10^{−7.3}} \nonumber \]
au
\[[\ce{H_3O^+}]=\textrm{antilog of} −7.3 \nonumber \]
\[[\ce{H_3O^+}]=5\times 10^{−8}\;M \nonumber \]
(Katika calculator chukua antilog, au logi “inverse”, ya -7.3, au uhesabu 10 -7.3.)
Tumia mkusanyiko wa ioni ya hydronium ya suluhisho na pH ya -1.07.
- Jibu
-
12 M
Sayansi ya Mazingira
Maji ya mvua ya kawaida yana pH kati ya 5 na 6 kutokana na kuwepo kwa CO 2 iliyovunjwa ambayo huunda asidi kaboniki:
\[\ce{H2O (l) + CO2(g) ⟶ H2CO3(aq)} \label{14} \]
\[\ce{H2CO3(aq) \rightleftharpoons H^+(aq) + HCO3^- (aq)} \label{15} \]
Mvua ya asidi ni maji ya mvua ambayo ina pH ya chini ya 5, kutokana na aina mbalimbali za oksidi zisizo za metali, ikiwa ni pamoja na CO 2, SO 2, SO 3, NO, na NO 2 zinazopasuka ndani ya maji na kuitikia nayo ili kuunda si tu asidi kaboni, bali asidi sulfuriki na asidi nitriki. Uundaji na ionization inayofuata ya asidi sulfuriki huonyeshwa hapa:
\[\ce{H2O (l) + SO3(g) ⟶ H2SO4(aq)} \label{16} \]
\[\ce{H2SO4(aq) ⟶ H^+(aq) + HSO4^- (aq)} \label{17} \]
Dioksidi kaboni ni kawaida sasa katika anga kwa sababu sisi na viumbe wengine wengi kuzalisha kama bidhaa taka ya kimetaboliki. Dioksidi kaboni hutengenezwa pia wakati moto unapotoa kaboni iliyohifadhiwa katika uoto au tunapochoma kuni au mafuta ya kisukuku. Trioxide ya sulfuri katika anga ni kawaida zinazozalishwa na shughuli za volkeno, lakini pia inatokana na kuchoma mafuta ya mafuta, ambayo yana athari za sulfuri, na kutokana na mchakato wa “kuchoma” ores ya sulfidi za chuma katika mchakato wa kusafisha chuma. Oksidi za nitrojeni hutengenezwa katika inji za mwako ndani ambapo joto la juu hufanya iwezekanavyo kwa nitrojeni na oksijeni katika hewa ili kuchanganya kemikali.
Mvua ya asidi ni tatizo hasa katika maeneo ya viwanda ambako bidhaa za mwako na smelting hutolewa hewani bila kuvuliwa kwa oksidi za sulfuri na nitrojeni. Katika Amerika ya Kaskazini na Ulaya hadi miaka ya 1980, ilikuwa na jukumu la uharibifu wa misitu na maziwa ya maji safi, wakati asidi ya mvua kweli iliua miti, udongo ulioharibiwa, na kufanya maziwa yasiyoweza kuishi kwa wote lakini aina nyingi zinazovumilia asidi. Mvua ya asidi pia hupunguza maonyesho ya statuary na kujenga ambayo yanafanywa kwa marumaru na chokaa (Kielelezo\(\PageIndex{2}\)). Kanuni zinazopunguza kiasi cha oksidi za sulfuri na nitrojeni ambazo zinaweza kutolewa katika anga na sekta na magari zimepunguza ukali wa uharibifu wa asidi kwa mazingira ya asili na ya kibinadamu katika Amerika ya Kaskazini na Ulaya. Kwa sasa ni tatizo kubwa katika maeneo ya viwanda ya China na India.

PoH na pH ya ufumbuzi wa 0.0125-M ya hidroksidi ya potasiamu, KOH?
Suluhisho
Hidroksidi ya potasiamu ni kiwanja cha ioniki yenye mumunyifu na hutenganisha kabisa wakati wa kufutwa katika suluhisho la kuondokana, hutoa [OH -] = 0.0125 M:
\[\mathrm{pOH=-\log[OH^− ]=-\log 0.0125} \nonumber \]
\[=−(−1.903)=1.903 \nonumber \]
PH inaweza kupatikana kutoka kwa\(\ce{pOH}\):
\[\mathrm{pH+pOH=14.00} \nonumber \]
\[\mathrm{pH=14.00−pOH=14.00−1.903=12.10} \nonumber \]
Mkusanyiko wa ioni ya hidronium ya siki ni takriban\(4 \times 10^{−3}\; M\). Je! Ni maadili gani yanayofanana ya PoH na pH?
- Jibu
-
PoH = 11.6,
pH = 14.00 - poH = 2.4
Asidi ya suluhisho ni kawaida tathmini experimentally kwa kipimo cha pH yake. PoH ya suluhisho haipatikani kwa kawaida, kwa kuwa inahesabiwa kwa urahisi kutoka kwa thamani ya pH ya majaribio. PH ya suluhisho inaweza kupimwa moja kwa moja kwa kutumia mita ya pH (Kielelezo\(\PageIndex{3}\)).

PH ya suluhisho inaweza pia kuibua inakadiriwa kutumia viashiria vya rangi (Kielelezo\(\PageIndex{3}\)).

Muhtasari
Mkusanyiko wa ioni ya hidroniamu katika suluhisho la asidi ndani ya maji ni kubwa kuliko\( 1.0 \times 10^{-7}\; M\) saa 25 °C. mkusanyiko wa ioni hidroksidi katika suluhisho la msingi katika maji ni kubwa kuliko\( 1.0 \times 10^{-7}\; M\) saa 25 °C Mkusanyiko wa H 3 O + katika suluhisho unaweza kuelezwa kama pH ya suluhisho;\(\ce{pH} = -\log \ce{H3O+}\). Mkusanyiko wa OH - unaweza kuelezwa kama PoH ya suluhisho:\(\ce{pOH} = -\log[\ce{OH-}]\). Katika maji safi, pH = 7.00 na PoH = 7.00
Mlinganyo muhimu
- \(\ce{pH}=-\log[\ce{H3O+}]\)
- \(\ce{pOH} = -\log[\ce{OH-}]\)
- [H 3 O +] = 10 -pH
- [OH -] = 10 —poh
- pH + poH = p K w = 14.00 saa 25 °C
faharasa
- tindikali
- inaelezea suluhisho ambalo [H 3 O +] > [OH -]
- msingi
- inaelezea suluhisho ambalo [H 3 O +] <[ OH ∙]
- upande wowote
- inaelezea suluhisho ambalo [H 3 O +] = [OH -]
- pH
- kipimo cha logarithmic ya mkusanyiko wa ions hydronium katika suluhisho
- oH
- kipimo cha logarithmic ya mkusanyiko wa ions hidroksidi katika suluhisho


