4.3: Stoichiometry ya mmenyuko
- Page ID
- 176921
- Eleza dhana ya stoichiometry kama inavyohusiana na athari za kemikali
- Tumia usawa wa kemikali ulinganifu ili kupata mambo ya stoichiometric yanayohusiana na kiasi cha reactants na bidhaa
- Kufanya mahesabu stoichiometric kuwashirikisha molekuli, moles, na molarity ufumbuzi
usawa kemikali equation hutoa mpango mkubwa wa habari katika format succinct sana. Fomu za kemikali hutoa utambulisho wa reactants na bidhaa zinazohusika katika mabadiliko ya kemikali, kuruhusu uainishaji wa mmenyuko. Coefficients hutoa idadi ya jamaa ya aina hizi za kemikali, kuruhusu tathmini ya kiasi cha mahusiano kati ya kiasi cha vitu vinavyotumiwa na zinazozalishwa na majibu. Mahusiano haya ya upimaji yanajulikana kama stoichiometri ya mmenyuko, neno linalotokana na maneno ya Kigiriki stoicheion (maana yake “elementi”) na metroni (maana yake “kipimo”). Katika moduli hii, matumizi ya usawa wa kemikali ya usawa kwa maombi mbalimbali ya stoichiometric inachunguzwa.
Njia ya jumla ya kutumia mahusiano ya stoichiometric ni sawa na dhana kwa jinsi watu wanavyoenda kuhusu shughuli nyingi za kawaida. Kupika, kwa mfano, hutoa kulinganisha sahihi. Tuseme kichocheo cha kufanya pancakes nane huita mchanganyiko wa kikombe 1 cha pancake, maziwa ya\(\dfrac{3}{4}\) kikombe, na yai moja. “Equation” inayowakilisha maandalizi ya pancakes kwa mapishi hii ni
\[\mathrm{1\:cup\: mix+\dfrac{3}{4}\:cup\: milk+1\: egg \rightarrow 8\: pancakes} \label{4.4.1} \]
Ikiwa pancakes mbili mbili zinahitajika kwa kifungua kinywa cha familia kubwa, kiasi cha viungo lazima kiongezwe kwa kiasi kikubwa kulingana na kiasi kilichotolewa katika mapishi. Kwa mfano, idadi ya mayai inahitajika kufanya pancakes 24 ni
\[\mathrm{24\: \cancel{pancakes} \times \dfrac{1\: egg}{8\: \cancel{pancakes}}=3\: eggs} \label{4.4.2} \]
Ulinganifu wa kemikali wenye usawa hutumiwa kwa kiasi sawa ili kuamua kiasi cha reactant moja inayotakiwa kuguswa na kiasi fulani cha reactant nyingine, au kutoa kiasi fulani cha bidhaa, na kadhalika. Coefficients katika equation uwiano hutumiwa kupata mambo stoichiometric ambayo inaruhusu hesabu ya kiasi taka. Ili kuonyesha wazo hili, fikiria uzalishaji wa amonia kwa mmenyuko wa hidrojeni na nitrojeni:
\[\ce{N2}(g)+\ce{3H2}(g)\rightarrow \ce{2NH3}(g) \label{4.4.3} \]
Ulinganisho huu unaonyesha kwamba molekuli za amonia huzalishwa kutoka kwa molekuli za hidrojeni katika uwiano wa 2:3, na mambo ya stoichiometri yanaweza kutolewa kwa kutumia kitengo chochote cha kiasi (namba):
\[\ce{\dfrac{2NH3 \: molecules}{3H2 \: molecules}\: or \: \dfrac{2 \: doz \: NH3\: molecules}{3\: doz\:H2 \:molecules} \: or \: \dfrac{2\: mol\: NH3\: molecules}{3\: mol\: H2\: molecules}} \label{4.4.4} \]
Sababu hizi za stoichiometri zinaweza kutumika kukokotoa idadi ya molekuli za amonia zinazozalishwa kutokana na idadi fulani ya molekuli za hidrojeni, au idadi ya molekuli za hidrojeni zinazohitajika kuzalisha idadi fulani ya molekuli za amonia. Sababu zinazofanana zinaweza kupatikana kwa jozi yoyote ya vitu katika equation yoyote ya kemikali.
Ni moles ngapi ya I 2 inahitajika kuguswa na 0.429 mol ya Al kulingana na equation ifuatayo (angalia Kielelezo\(\PageIndex{2}\))?
\[\ce{2Al + 3I2 \rightarrow 2AlI3} \label{4.4.5} \]

Suluhisho
Akizungumzia usawa wa kemikali, sababu ya stoichiometric inayohusiana na vitu viwili vya riba ni\(\ce{\dfrac{3\: mol\: I2}{2\: mol\: Al}}\). Kiasi cha molar cha iodini kinatokana na kuzidisha kiasi cha molar kilichotolewa cha alumini kwa sababu hii:

\[\begin{align*} \mathrm{mol\: I_2} &=\mathrm{0.429\: \cancel{mol\: Al}\times \dfrac{3\: mol\: I_2}{2\:\cancel{mol\: Al}}} \\[4pt] &=\mathrm{0.644\: mol\: I_2} \end{align*} \nonumber \]
Ni moles ngapi za Ca (OH) 2 zinahitajika kuguswa na 1.36 mol ya H 3 PO 4 ili kuzalisha Ca 3 (PO 4) 2 kulingana na equation\(\ce{3Ca(OH)2 + 2H3PO4 \rightarrow Ca3(PO4)2 + 6H2O}\)?
- Jibu
-
2.04 mol
Ni molekuli ngapi za dioksidi kaboni zinazalishwa wakati 0.75 mol ya propane inawaka kulingana na equation hii?
\[\ce{C3H8 + 5O2 \rightarrow 3CO2 + 4H2O} \label{4.4.6} \]
Suluhisho la Marekani
Mbinu hapa ni sawa na kwa Mfano\(\PageIndex{1}\), ingawa idadi kamili ya molekuli ni ombi, si idadi ya moles ya molekuli. Hii itahitaji tu matumizi ya sababu ya uongofu wa moles-kwa-nambari, nambari ya Avogadro.
Ulinganisho wa usawa unaonyesha kwamba dioksidi kaboni huzalishwa kutoka propane katika uwiano wa 3:1:
\[\ce{\dfrac{3\: mol\: CO2}{1\: mol\: C3H8}} \label{4.4.7} \]
Kutumia sababu hii ya stoichiometric, kiasi cha molar kilichotolewa cha propane, na idadi ya Avogadro,

\[\mathrm{0.75\: \cancel{mol\: C_3H_8}\times \dfrac{3\: \cancel{mol\: CO_2}}{1\:\cancel{mol\:C_3H_8}}\times \dfrac{6.022\times 10^{23}\:CO_2\:molecules}{\cancel{mol\:CO_2}}=1.4\times 10^{24}\:CO_2\:molecules} \label{4.4.8} \]
Ni molekuli ngapi za NH 3 zinazozalishwa na mmenyuko wa 4.0 mol ya Ca (OH) 2 kulingana na equation ifuatayo:
\[\ce{(NH4)2SO4 + Ca(OH)2 \rightarrow 2NH3 + CaSO4 + 2H2O} \label{4.4.9} \]
- Jibu
-
4.8 × 10 24 NH 3 molekuli
Mifano hizi zinaonyesha urahisi ambao kiasi cha vitu vinavyohusika katika mmenyuko wa kemikali wa stoichiometry inayojulikana inaweza kuwa na uhusiano. Moja kwa moja kupima idadi ya atomi na molekuli ni, hata hivyo, si kazi rahisi, na matumizi ya vitendo ya stoichiometry inahitaji kwamba sisi kutumia kwa urahisi zaidi kipimo mali ya molekuli.
Ni umati gani wa hidroksidi ya sodiamu, NaOH, itahitajika kuzalisha 16 g ya maziwa ya antacid ya magnesia [hidroksidi magnesiamu, Mg (OH) 2] kwa majibu yafuatayo?
Suluhisho la Marekani
Mbinu kutumika hapo awali katika Mifano\(\PageIndex{1}\) na\(\PageIndex{2}\) ni vivyo hivyo kutumika hapa; yaani, ni lazima hupata sahihi stoichiometric sababu kutoka usawa kemikali equation na matumizi yake kuhusiana kiasi cha dutu mbili ya riba. Katika kesi hii, hata hivyo, raia (si kiasi cha molar) hutolewa na kuombwa, hivyo hatua za ziada za aina zilizojifunza katika sura ya awali zinahitajika. Mahesabu yanayotakiwa yanatajwa katika chati hii:
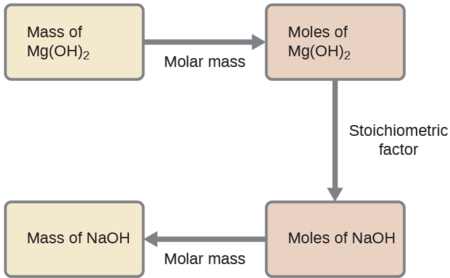
\[\mathrm{16\:\cancel{g\: Mg(OH)_2} \times \dfrac{1\:\cancel{mol\: Mg(OH)_2}}{58.3\:\cancel{g\: Mg(OH)_2}}\times \dfrac{2\:\cancel{mol\: NaOH}}{1\:\cancel{mol\: Mg(OH)_2}}\times \dfrac{40.0\: g\: NaOH}{\cancel{mol\: NaOH}}=22\: g\: NaOH} \nonumber \]
Ni kiasi gani cha oksidi ya galliamu, Ga 2 O 3, inaweza kuandaliwa kutoka 29.0 g ya chuma cha gallium? Equation kwa mmenyuko ni\(\ce{4Ga + 3O2 \rightarrow 2Ga2O3}\).
- Jibu
-
39.0 g
Ni kiasi gani cha gesi ya oksijeni, O 2, kutoka hewa hutumiwa katika mwako wa 702 g ya octane, C 8 H 18, moja ya vipengele vikuu vya petroli?
\[\ce{2C8H18 + 25O2 \rightarrow 16CO2 + 18H2O} \nonumber \]
Suluhisho la Marekani
Mbinu inahitajika hapa ni sawa na kwa Mfano\(\PageIndex{3}\), tofauti tu kwa kuwa raia zinazotolewa na ombi ni wote kwa ajili ya aina reactant.
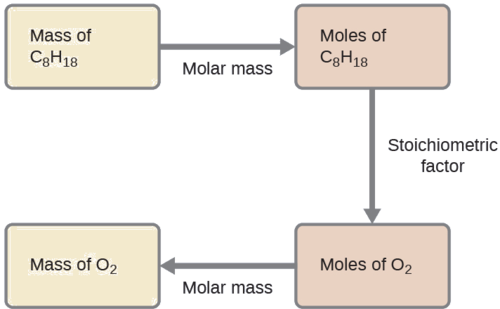
\(\mathrm{702\:\cancel{g\:\ce{C8H18}}\times \dfrac{1\:\cancel{mol\:\ce{C8H18}}}{114.23\:\cancel{g\:\ce{C8H18}}}\times \dfrac{25\:\cancel{mol\:\ce{O2}}}{2\:\cancel{mol\:\ce{C8H18}}}\times \dfrac{32.00\: g\:\ce{O2}}{\cancel{mol\:\ce{O2}}}=2.46\times 10^3\:g\:\ce{O2}}\)
Ni molekuli gani ya CO inahitajika kuitikia na 25.13 g ya Fe 2 O 3 kulingana na equation\(\ce{Fe2O3 + 3CO \rightarrow 2Fe + 3CO2}\)?
- Jibu
-
13.22 g
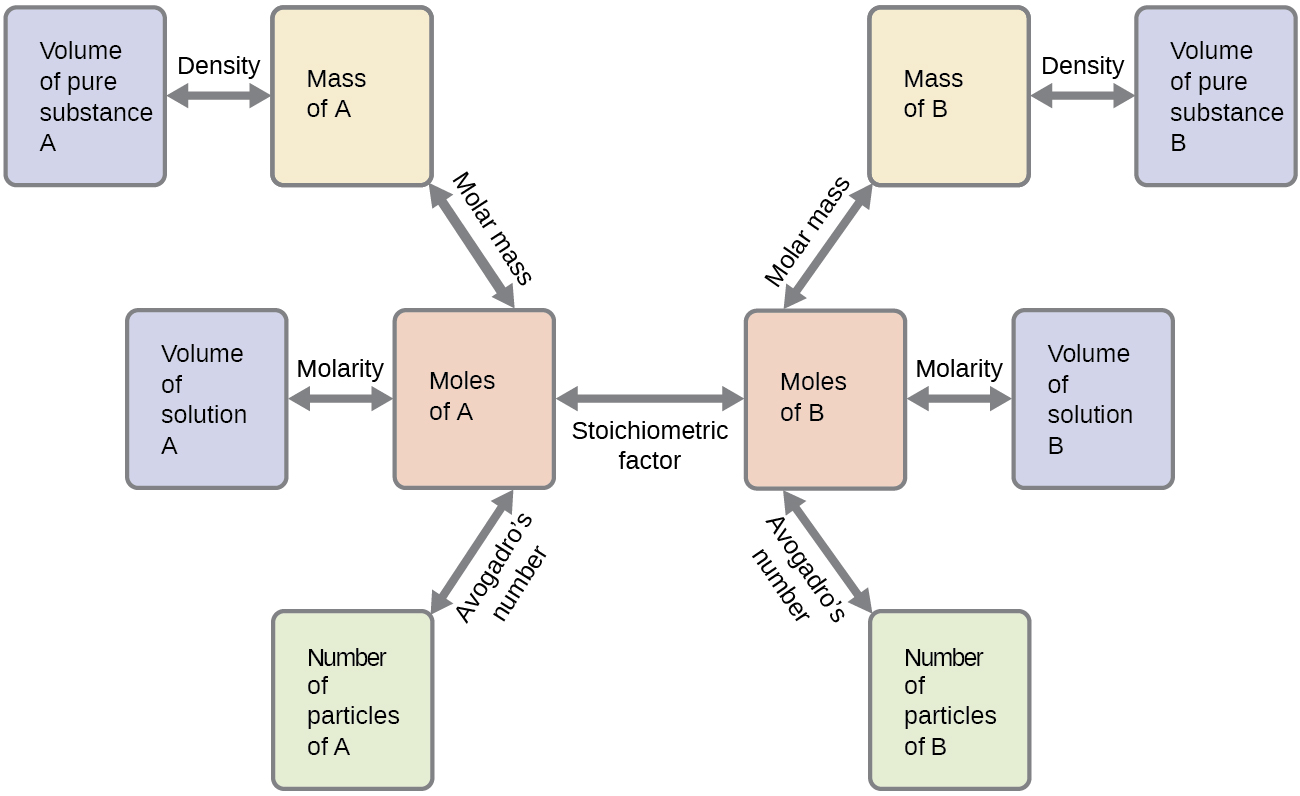
Mifano hii kuonyesha matukio machache tu ya hesabu mmenyuko stoichiometry. Tofauti nyingi juu ya mwanzo na mwisho hatua za kuhesabu zinawezekana kulingana na kiasi gani fulani kinachotolewa na kutafutwa (kiasi, viwango vya ufumbuzi, na kadhalika). Bila kujali maelezo, mahesabu haya yote hushiriki sehemu muhimu ya kawaida: matumizi ya mambo ya stoichiometric inayotokana na usawa wa kemikali. Kielelezo\(\PageIndex{2}\) hutoa muhtasari wa jumla wa hatua mbalimbali computational kuhusishwa na wengi majibu mahesabu stoichiometry.
Airbags (Kielelezo\(\PageIndex{3}\)) ni kipengele cha usalama kilichotolewa katika magari mengi tangu miaka ya 1990. Uendeshaji bora wa airbag inahitaji kuwa umechangiwa haraka na kiasi sahihi (kiasi) cha gesi wakati gari linahusika katika mgongano. Mahitaji haya yanatidhika katika mifumo mingi ya airbag ya magari kupitia matumizi ya athari za kemikali za kulipuka, uchaguzi mmoja wa kawaida kuwa utengano wa azide ya sodiamu, NaN 3. Wakati sensorer katika gari kuchunguza mgongano, sasa umeme hupitishwa kwa kiasi kikubwa kipimo cha NaN 3 ili kuanzisha utengano wake:
\[\ce{2NaN3}(s)\rightarrow \ce{3N2}(g)+\ce{2Na}(s) \nonumber \]
Tabia hii ni ya haraka sana, inayozalisha nitrojeni ya gesi ambayo inaweza kupeleka na kuingiza kikamilifu airbag ya kawaida katika sehemu ya pili (~0.03—0.1 s). Miongoni mwa masuala mengi ya uhandisi, kiasi cha azidi ya sodiamu inayotumiwa lazima iwe sahihi kwa kuzalisha gesi ya nitrojeni ya kutosha ili kuingiza kikamilifu mfuko wa hewa na kuhakikisha kazi yake sahihi. Kwa mfano, molekuli ndogo (~100 g) ya NaN 3 itazalisha takriban 50 L ya N 2.

Muhtasari
uwiano kemikali equation inaweza kutumika kuelezea stoichiometry mmenyuko (uhusiano kati ya kiasi cha reactants na bidhaa). Coefficients kutoka equation hutumiwa hupata mambo stoichiometric ambayo hatimaye inaweza kutumika kwa ajili ya hesabu zinazohusiana raia reactant na bidhaa, kiasi molar, na mali nyingine upimaji.
faharasa
- sababu ya stoichiometric
- uwiano wa coefficients katika usawa wa kemikali, kutumika katika hesabu zinazohusiana na kiasi cha reactants na bidhaa
- stoichiometry
- uhusiano kati ya kiasi cha reactants na bidhaa za mmenyuko wa kemikali


