3.4: Vitengo vingine vya viwango vya ufumbuzi
- Page ID
- 175778
- Eleza vitengo vya ukolezi wa asilimia ya molekuli, asilimia ya kiasi, asilimia ya wingi, sehemu-kwa-milioni (ppm), na sehemu kwa kila bilioni (ppb)
- Fanya hesabu zinazohusiana na mkusanyiko wa suluhisho na kiasi cha vipengele vyake na/au raia kwa kutumia vitengo hivi
Katika sehemu iliyopita, tulianzisha molarity, kitengo muhimu sana cha kupima kwa kutathmini ufumbuzi wa ufumbuzi. Hata hivyo, molarity ni kipimo kimoja tu cha ukolezi. Katika sehemu hii, sisi kuanzisha baadhi ya vitengo vingine ya ukolezi kwamba ni kawaida kutumika katika maombi mbalimbali, ama kwa urahisi au kwa mkataba.
Asilimia ya Misa
Mapema katika sura hii, tulianzisha muundo wa asilimia kama kipimo cha kiasi cha jamaa cha kipengele kilichopewa katika kiwanja. Asilimia pia hutumiwa kuelezea muundo wa mchanganyiko, ikiwa ni pamoja na ufumbuzi. Asilimia kubwa ya sehemu ya suluhisho hufafanuliwa kama uwiano wa wingi wa sehemu kwa wingi wa suluhisho, umeelezwa kama asilimia:
\[ \text{mass percentage} = \dfrac{\text{mass of component}}{\text{mass of solution}} \times100\% \label{3.5.1} \]
Kwa ujumla tunavutiwa na asilimia kubwa ya solutes, lakini pia inawezekana kukokotoa asilimia kubwa ya kutengenezea.
Asilimia Misa pia inajulikana kwa majina sawa kama vile asilimia molekuli, asilimia uzito, uzito/uzito asilimia, na tofauti nyingine juu ya mada hii. Ishara ya kawaida kwa asilimia kubwa ni ishara ya asilimia tu,%, ingawa alama za kina zaidi hutumiwa mara nyingi ikiwa ni pamoja na %umati, %uzito, na (w/w)%. Matumizi ya alama hizi za kina zaidi zinaweza kuzuia machafuko ya asilimia ya wingi na aina nyingine za asilimia, kama vile asilimia kiasi (kujadiliwa baadaye katika sehemu hii).
Asilimia ya misa ni vitengo vya ukolezi maarufu kwa bidhaa za walaji. Lebo ya chupa ya kawaida ya kioevu ya bleach (Kielelezo\(\PageIndex{1}\)) inataja mkusanyiko wa viungo vyake vya kazi, hypochlorite ya sodiamu (\(\ce{NaOCl}\)), kama 7.4%. Sampuli ya 100.0-g ya bleach ingekuwa na 7.4 g ya\(\ce{NaOCl}\).

Sampuli ya 5.0-g ya maji ya mgongo ina 3.75 mg (0.00375 g) ya glucose. Ni asilimia gani kwa wingi wa glucose katika maji ya mgongo?
Suluhisho
Sampuli ya maji ya mgongo ina takribani 4 mg ya glucose katika 5000 mg ya maji, hivyo sehemu kubwa ya glucose inapaswa kuwa kidogo chini ya sehemu moja katika 1000, au kuhusu 0.1%. Kubadilisha raia waliopewa katika equation kufafanua mavuno ya asilimia molekuli:
\[\mathrm{\%\,glucose=\dfrac{3.75\;mg \;glucose \times \frac{1\;g}{1000\; mg}}{5.0\;g \;spinal\; fluid}=0.075\%} \nonumber \]
Asilimia ya molekuli iliyohesabiwa inakubaliana na makadirio yetu mabaya (ni kidogo chini ya 0.1%).
Kumbuka kuwa wakati kitengo chochote cha molekuli kinaweza kutumika kukokotoa asilimia ya wingi (mg, g, kg, oz, na kadhalika), kitengo hicho kinatakiwa kutumika kwa solute na suluhisho ili vitengo vya wingi kufuta, kutoa uwiano usio na kipimo. Katika kesi hii, tulibadilisha vitengo vya solute katika nambari kutoka mg hadi g ili kufanana na vitengo katika denominator. Tunaweza tu kwa urahisi kuwa waongofu denominator kutoka g kwa mg badala. Kwa muda mrefu kama vitengo vya molekuli vinavyofanana vinatumiwa kwa solute na suluhisho, asilimia ya molekuli ya computed itakuwa sahihi.
Chupa ya utakaso wa tile ina 135 g ya\(\ce{HCl}\) na 775 g ya maji. Ni nini asilimia kwa wingi wa\(\ce{HCl}\) katika cleanser hii?
- Jibu
-
14.8%
“Kujilimbikizia” asidi hidrokloriki ni suluhisho la maji la 37.2%\(\ce{HCl}\) ambalo hutumiwa kama reagent ya maabara. Uzito wa suluhisho hili ni 1.19 g/ml. Ni wingi gani\(\ce{HCl}\) unao katika 0.500 L ya suluhisho hili?
Suluhisho
Mkusanyiko wa HCl ni karibu 40%, hivyo sehemu ya 100-g ya suluhisho hili ingekuwa na 40 g ya HCl. Kwa kuwa wiani wa suluhisho sio tofauti sana na ule wa maji (1 g/ml), makadirio ya busara ya wingi wa HCl katika 500 g (0.5 L) ya suluhisho ni karibu mara tano zaidi kuliko ile katika sehemu 100 g, au\(\mathrm{5 \times 40 = 200\: g}\). Ili kupata wingi wa solute katika suluhisho kutoka asilimia yake ya wingi, tunahitaji kujua molekuli sambamba ya suluhisho. Kutumia wiani wa ufumbuzi uliotolewa, tunaweza kubadilisha kiasi cha suluhisho kwa wingi, na kisha tumia asilimia ya molekuli iliyotolewa ili kuhesabu molekuli ya solute. Mbinu hii ya hisabati imeainishwa katika chati hii:
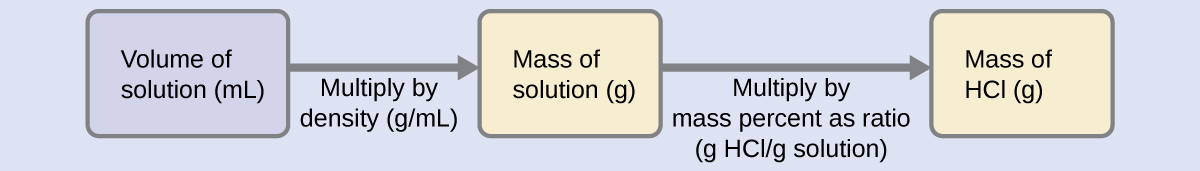
Kwa kufuta kitengo sahihi, kiasi cha 0.500-L kinabadilishwa kuwa 500 ml, na asilimia ya wingi huelezwa kama uwiano, 37.2 g Hcl/g ufumbuzi:
\[ \mathrm{500\; mL\; solution \left(\dfrac{1.19\;g \;solution}{mL \;solution}\right) \left(\dfrac{37.2\;g\; HCl}{100\;g \;solution}\right)=221\;g\; HCl} \nonumber \]
Masi hii ya HCl ni sawa na makadirio yetu mabaya ya takriban 200 g.
Ni kiasi gani cha ufumbuzi wa HCl iliyojilimbikizia ina 125 g ya HCl?
- Jibu
-
282 ml
Kiasi Asilimia
Kiasi cha maji ya juu ya ukubwa mbalimbali hupimwa kwa urahisi kwa kutumia vifaa vya kawaida na vya gharama nafuu vya maabara. Mkusanyiko wa suluhisho linaloundwa na kufuta solute ya kioevu katika kutengenezea kioevu mara nyingi huonyeshwa kama asilimia ya kiasi, %vol au (v/v)%:
\[ \text{volume percentage} = \dfrac{\text{volume solute}}{\text{volume solution}} \times100\% \label{3.5.2} \]
Kunywa pombe (isopropanol) mara nyingi huuzwa kama suluhisho la maji ya vol 70%. Ikiwa wiani wa pombe ya isopropyl ni 0.785 g/ml, ni gramu ngapi za pombe ya isopropyl zilizopo kwenye chupa ya 355 ml ya kunywa pombe?
Suluhisho
Kwa ufafanuzi wa asilimia ya kiasi, kiasi cha isopropanol ni 70% ya jumla ya kiasi cha suluhisho. Kuzidisha kiasi cha isopropanol kwa wiani wake huzalisha wingi ulioombwa:
\[ \text {355 mL solution}(\frac{\text{70 mL isopropyl alcohol}}{\text{100 mL solution}})(\frac{\text{0.785 g isopropyl alcohol}}{\text{1 mL isopropyl alcohol}})=\text{195 g isopropyl alcohol} \nonumber \]
Mvinyo ni takriban 12% ethanol (\(\ce{CH_3CH_2OH}\)) kwa kiasi. Ethanol ina molekuli ya molar ya 46.06 g/mol na wiani 0.789 g/ml. Ni moles ngapi za ethanol zilizopo katika chupa ya divai ya 750-ml?
- Jibu
-
1.5 mol ethanol
Asilimia ya Misa ya Kiasi
“Mchanganyiko” vitengo vya asilimia, vinavyotokana na wingi wa solute na kiasi cha suluhisho, vinajulikana kwa matumizi fulani ya biochemical na matibabu. Asilimia ya kiasi kikubwa ni uwiano wa molekuli ya solute kwa kiasi cha suluhisho kilichoonyeshwa kama asilimia. Vitengo maalum vinavyotumiwa kwa wingi wa solute na kiasi cha suluhisho vinaweza kutofautiana, kulingana na suluhisho. Kwa mfano, ufumbuzi wa chumvi ya kisaikolojia, uliotumiwa kuandaa maji ya ndani, una mkusanyiko wa 0.9% ya molekuli/kiasi (m/v), kuonyesha kuwa muundo ni 0.9 g ya solute kwa 100 ml ya suluhisho. Mkusanyiko wa glucose katika damu (kawaida inajulikana kama “sukari ya damu”) pia huelezwa kwa suala la uwiano wa wingi. Ingawa si walionyesha wazi kama asilimia, mkusanyiko wake ni kawaida kutolewa katika miligramu ya glucose kwa deciliter (100 ml) ya damu (Kielelezo\(\PageIndex{2}\)).

Sehemu kwa Milioni na Sehemu kwa Bilioni
Viwango vya chini sana vya solute huonyeshwa mara nyingi kwa kutumia vitengo vidogo vilivyofaa kama sehemu kwa milioni (ppm) au sehemu kwa bilioni (ppb). Kama asilimia (“sehemu kwa mia”) vitengo, ppm na ppb inaweza kuelezwa katika suala la raia, kiasi, au mchanganyiko wingi kiasi vitengo. Kuna pia vitengo vya ppm na ppb vinavyofafanuliwa kuhusiana na idadi ya atomi na molekuli.
Ufafanuzi wa wingi wa ppm na ppb hutolewa hapa:
\[\text{ppm}=\dfrac{\text{mass solute}}{\text{mass solution}} \times 10^6\; \text{ppm} \label{3.5.3A} \]
\[\text{ppb}=\dfrac{\text{mass solute}}{\text{mass solution}} \times 10^9\; \text{ppb} \label{3.5.3B} \]
Wote ppm na ppb ni vitengo rahisi kwa kuripoti viwango vya uchafuzi na uchafu mwingine wa kufuatilia katika maji. Viwango vya uchafuzi huu ni kawaida chini sana katika maji ya kutibiwa na asili, na viwango vyao haviwezi kuzidi vizingiti vya ukolezi mdogo bila kusababisha athari mbaya kwa afya na wanyamapori. Kwa mfano, EPA imetambua kiwango cha juu cha salama cha ion ya fluoride katika maji ya bomba kuwa 4 ppm. Filters za maji ya ndani zimeundwa ili kupunguza mkusanyiko wa fluoride na uchafuzi mwingine wa kiwango cha kufuatilia katika maji ya bomba (Kielelezo\(\PageIndex{3}\)).

Kwa mujibu wa EPA, wakati mkusanyiko wa risasi katika maji ya bomba unafikia 15 ppb, hatua fulani za kurekebisha lazima zichukuliwe. Je! Hii ni mkusanyiko gani katika ppm? Katika mkusanyiko huu, ni wingi gani wa risasi (μg) ungekuwa katika glasi ya kawaida ya maji (300 ml)?
Suluhisho
Ufafanuzi wa vitengo vya ppm na ppb inaweza kutumika kubadili mkusanyiko uliotolewa kutoka ppb hadi ppm. Kulinganisha ufafanuzi huu wa kitengo mbili unaonyesha kwamba ppm ni mara 1000 zaidi kuliko ppb (1 ppm = 10 3 ppb). Hivyo:
\[ \mathrm{15\; \cancel{ppb} \times \dfrac{1\; ppm}{10^3\;\cancel{ppb}} =0.015\; ppm} \nonumber \]
Ufafanuzi wa kitengo cha ppb inaweza kutumika kuhesabu molekuli iliyoombwa ikiwa wingi wa suluhisho hutolewa. Hata hivyo, tu kiasi cha suluhisho (300 mL) kinatolewa, kwa hiyo tunapaswa kutumia wiani ili kupata molekuli inayofanana. Tunaweza kudhani wiani wa maji ya bomba kuwa sawa na ile ya maji safi (~1.00 g/ml), kwani viwango vya vitu vyenye kufutwa haipaswi kuwa kubwa sana. Kupanga upya equation kufafanua kitengo cha ppb na kubadilisha kiasi kilichopewa mavuno:
\[\text{ppb}=\dfrac{\text{mass solute}}{\text{mass solution}} ×10^9\; \text{ppb} \nonumber \]
\[\text{mass solute} = \dfrac{\text{ppb} \times \text{mass solution}}{10^9\;\text{ppb}} \nonumber \]
\[\text{mass solute}=\mathrm{\dfrac{15\:ppb×300\:mL×\dfrac{1.00\:g}{mL}}{10^9\:ppb}=4.5 \times 10^{-6}\;g} \nonumber \]
Hatimaye, kubadilisha molekuli hii kwa kitengo kilichoombwa cha micrograms:
\[\mathrm{4.5 \times 10^{−6}\;g \times \dfrac{1\; \mu g}{10^{−6}\;g} =4.5\; \mu g} \nonumber \]
Sampuli ya 50.0-g ya maji machafu ya viwanda iliamua kuwa na 0.48 mg ya zebaki. Eleza mkusanyiko wa zebaki wa maji machafu katika vitengo vya ppm na ppb.
- Jibu
-
9.6 ppm, 9600 ppb
Muhtasari
Mbali na molarity, vitengo vingine vya ukolezi wa ufumbuzi hutumiwa katika matumizi mbalimbali. Viwango vya asilimia kulingana na raia wa vipengele vya ufumbuzi, kiasi, au vyote viwili ni muhimu kwa kuonyesha viwango vya juu, wakati viwango vya chini vinaelezwa kwa urahisi kwa kutumia vitengo vya ppm au ppb. Vitengo hivi ni maarufu katika mazingira, matibabu, na maeneo mengine ambapo vitengo vya mole-msingi kama vile molarity si kama kawaida kutumika.
faharasa
- asilimia ya molekuli
- uwiano wa molekuli solute-kwa-ufumbuzi walionyesha kama asilimia
- asilimia ya molekuli
- uwiano wa molekuli solute kwa kiasi ufumbuzi, walionyesha kama asilimia
- sehemu kwa bilioni (ppb)
- uwiano wa molekuli ya solute-kwa-suluhisho imeongezeka kwa 10 9
- sehemu kwa milioni (ppm)
- uwiano wa molekuli ya solute-kwa-suluhisho imeongezeka kwa 10 6
- asilimia ya kiasi
- uwiano wa kiasi solute-kwa-ufumbuzi walionyesha kama asilimia


