8.2: Orbitais atômicos híbridos
- Page ID
- 184686
- Explicar o conceito de hibridização orbital atômica
- Determine os orbitais híbridos associados a várias geometrias moleculares
Pensar em termos de sobreposição de orbitais atômicos é uma forma de explicarmos como as ligações químicas se formam nas moléculas diatômicas. No entanto, para entender como moléculas com mais de dois átomos formam ligações estáveis, precisamos de um modelo mais detalhado. Como exemplo, vamos considerar a molécula de água, na qual temos um átomo de oxigênio ligado a dois átomos de hidrogênio. O oxigênio tem a configuração eletrônica 1 s 2 2 2 p 4, com dois elétrons desemparelhados (um em cada um dos dois orbitais 2 p). A teoria da ligação de valência prediria que as duas ligações O-H se formam a partir da sobreposição desses dois orbitais de 2 p com os orbitais de 1 s dos átomos de hidrogênio. Se fosse esse o caso, o ângulo de ligação seria de 90°, conforme mostrado na Figura\(\PageIndex{1}\), porque os orbitais p são perpendiculares entre si. Evidências experimentais mostram que o ângulo de ligação é 104,5°, não 90°. A previsão do modelo da teoria da ligação de valência não corresponde às observações do mundo real de uma molécula de água; um modelo diferente é necessário.
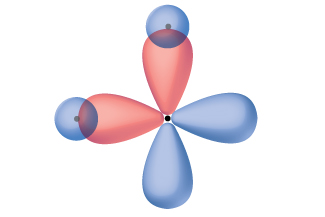
Cálculos de mecânica quântica sugerem por que os ângulos de ligação observados em H 2 O diferem daqueles previstos pela sobreposição do orbital 1 s dos átomos de hidrogênio com os orbitais 2 p do átomo de oxigênio. A expressão matemática conhecida como função de onda,, contém informações sobre cada orbital e as propriedades ondulatórias dos elétrons em um átomo isolado. Quando os átomos são unidos em uma molécula, as funções de onda se combinam para produzir novas descrições matemáticas com formas diferentes. Esse processo de combinação das funções de onda para orbitais atômicos é chamado de hibridização e é matematicamente realizado pela combinação linear de orbitais atômicos, LCAO, (uma técnica que encontraremos novamente mais tarde). Os novos orbitais resultantes são chamados de orbitais híbridos. Os orbitais de valência em um átomo de oxigênio isolado são um orbital de 2 s e três orbitais de 2 p. Os orbitais de valência em um átomo de oxigênio em uma molécula de água são diferentes; eles consistem em quatro orbitais híbridos equivalentes que apontam aproximadamente para os cantos de um tetraedro (Figura\(\PageIndex{2}\)). Consequentemente, a sobreposição dos orbitais O e H deve resultar em um ângulo de ligação tetraédrico (109,5°). O ângulo observado de 104,5° é uma evidência experimental da qual os cálculos de mecânica quântica fornecem uma explicação útil: a teoria da ligação de valência deve incluir um componente de hibridização para fornecer previsões precisas.
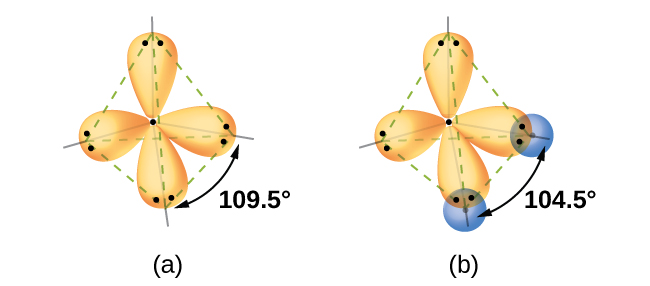
As ideias a seguir são importantes para entender a hibridização:
- Os orbitais híbridos não existem em átomos isolados. Eles são formados apenas em átomos ligados covalentemente.
- Os orbitais híbridos têm formas e orientações muito diferentes das dos orbitais atômicos em átomos isolados.
- Um conjunto de orbitais híbridos é gerado pela combinação de orbitais atômicos. O número de orbitais híbridos em um conjunto é igual ao número de orbitais atômicos que foram combinados para produzir o conjunto.
- Todos os orbitais em um conjunto de orbitais híbridos são equivalentes em forma e energia.
- O tipo de orbitais híbridos formados em um átomo ligado depende de sua geometria de par de elétrons, conforme previsto pela teoria VSEPR.
- Os orbitais híbridos se sobrepõem para formar ligações σ. Orbitais não hibridizados se sobrepõem para formar ligações π.
Nas seções a seguir, discutiremos os tipos comuns de orbitais híbridos.
hibridização sp
O átomo de berílio em uma molécula gasosa de BeCl 2 é um exemplo de átomo central sem pares solitários de elétrons em um arranjo linear de três átomos. Existem duas regiões de densidade eletrônica de valência na molécula BeCl 2 que correspondem às duas ligações Be-Cl covalentes. Para acomodar esses dois domínios de elétrons, dois dos quatro orbitais de valência do átomo de Be se misturarão para produzir dois orbitais híbridos. Esse processo de hibridização envolve a mistura do orbital de valência s com um dos orbitais de valência p para produzir dois orbitais híbridos sp equivalentes que são orientados em uma geometria linear (Figura\(\PageIndex{3}\)). Nesta figura, o conjunto de orbitais sp parece semelhante em forma ao orbital p original, mas há uma diferença importante. O número de orbitais atômicos combinados sempre é igual ao número de orbitais híbridos formados. O orbital p é um orbital que pode conter até dois elétrons. O conjunto sp é composto por dois orbitais equivalentes que apontam 180° um do outro. Os dois elétrons que estavam originalmente no orbital s agora estão distribuídos para os dois orbitais sp, que estão meio cheios. No BeCl 2 gasoso, esses orbitais híbridos meio preenchidos se sobreporão aos orbitais dos átomos de cloro para formar duas ligações σ idênticas.
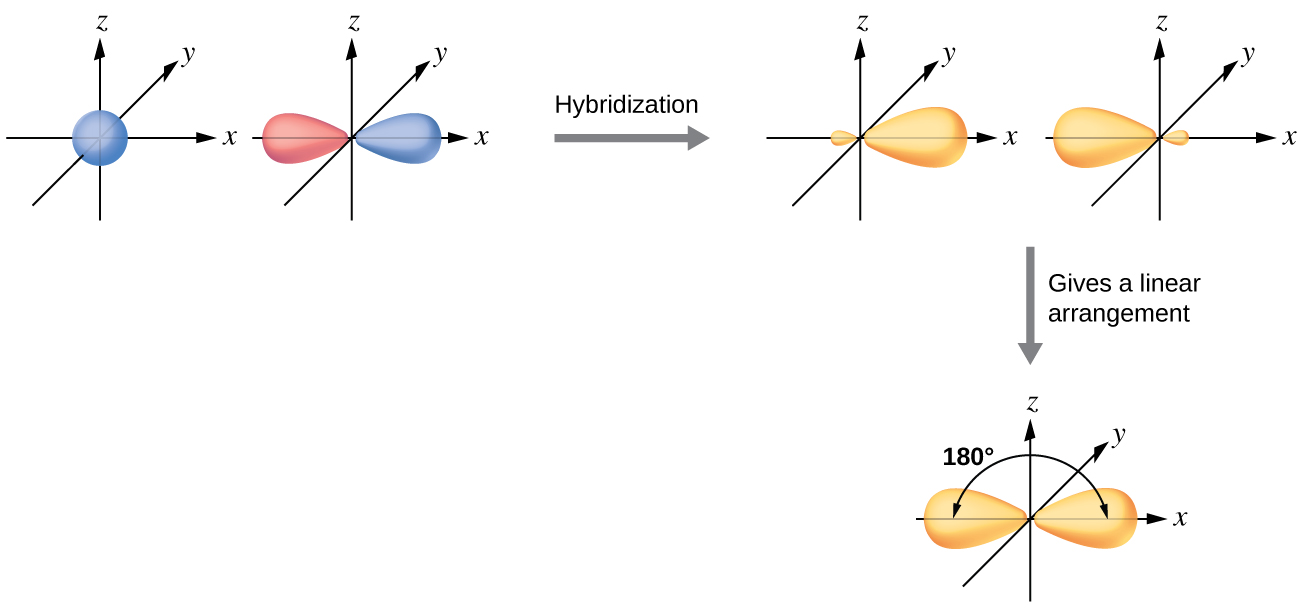
Ilustramos as diferenças eletrônicas em um átomo de Be isolado e no átomo de Be ligado no diagrama de nível de energia orbital na Figura\(\PageIndex{4}\). Esses diagramas representam cada orbital por uma linha horizontal (indicando sua energia) e cada elétron por uma seta. A energia aumenta na parte superior do diagrama. Usamos uma seta para cima para indicar um elétron em um orbital e duas setas (para cima e para baixo) para indicar dois elétrons de rotação oposta.
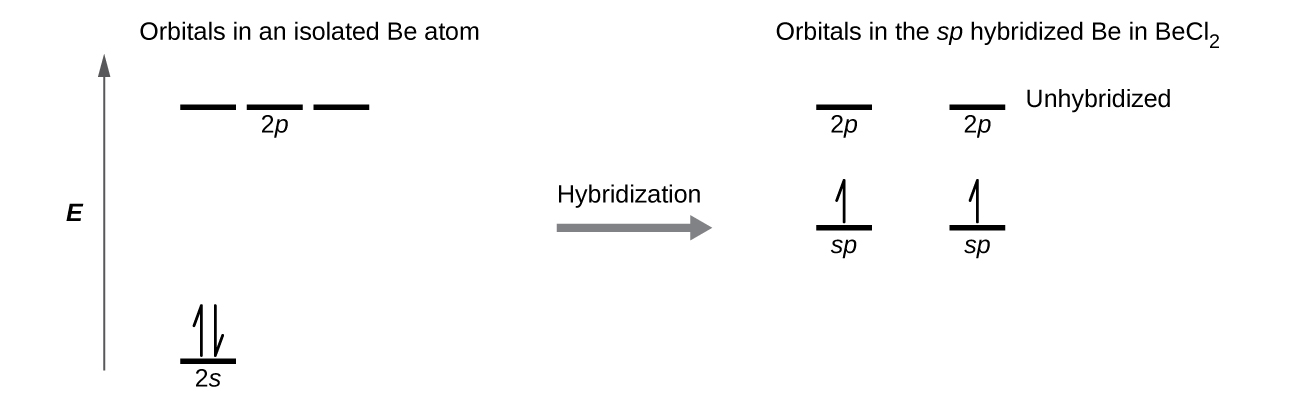
Quando os orbitais atômicos hibridizam, os elétrons de valência ocupam os orbitais recém-criados. O átomo de Be tinha dois elétrons de valência, então cada um dos orbitais sp recebe um desses elétrons. Cada um desses elétrons se emparelha com o elétron não pareado em um átomo de cloro quando um orbital híbrido e um orbital de cloro se sobrepõem durante a formação das ligações Be-Cl. Qualquer átomo central cercado por apenas duas regiões de densidade eletrônica de valência em uma molécula exibirá hibridização sp. Outros exemplos incluem o átomo de mercúrio na molécula linear de HgCl 2, o átomo de zinco em Zn (CH 3) 2, que contém um arranjo linear C—Zn-C, e os átomos de carbono em HCCH e CO 2.
sp 2 Hibridização
Os orbitais de valência de um átomo central cercado por três regiões de densidade eletrônica consistem em um conjunto de três orbitais híbridos sp 2 e um orbital p não hibridizado. Esse arranjo resulta da hibridização sp 2, da mistura de um orbital s e dois orbitais p para produzir três orbitais híbridos idênticos orientados em uma geometria plana trigonal (Figura\(\PageIndex{5}\)).
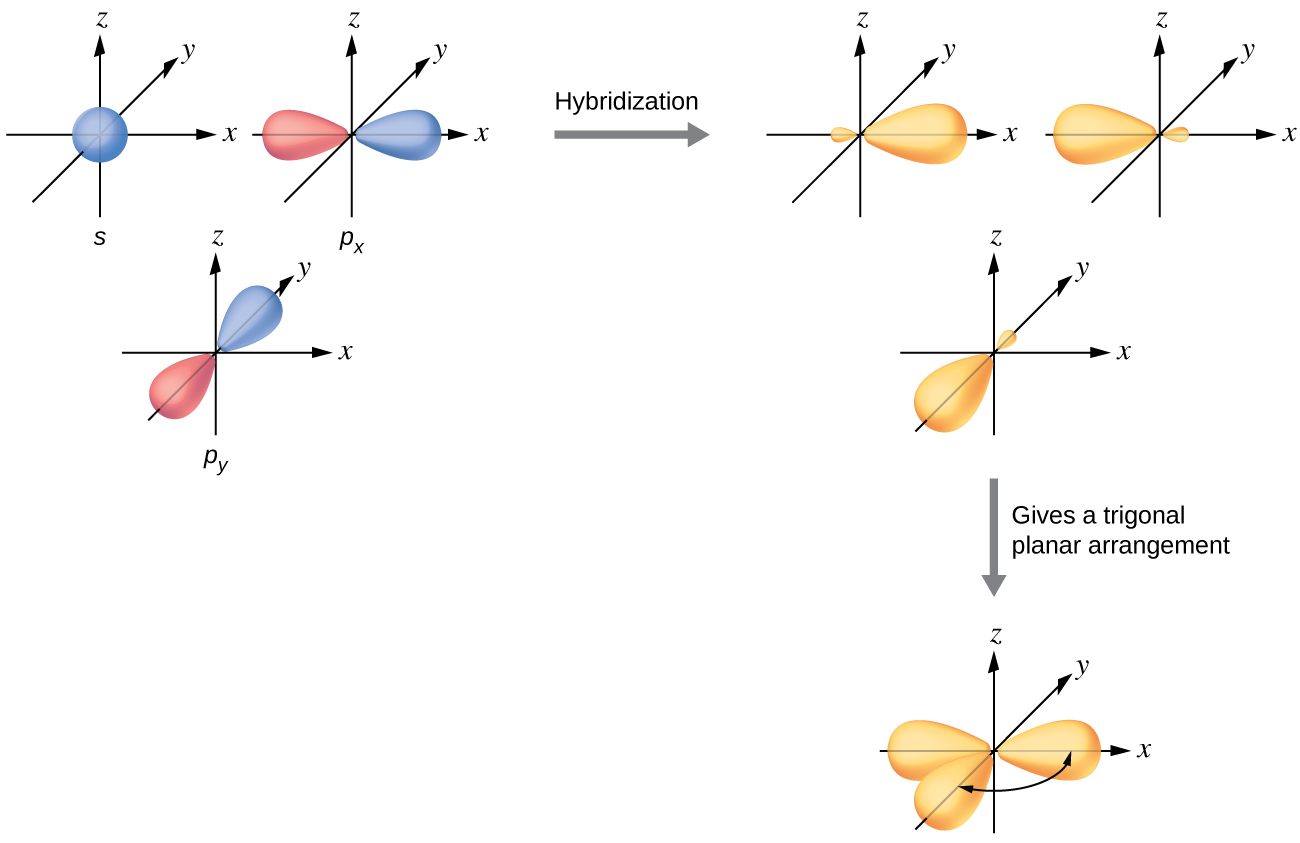
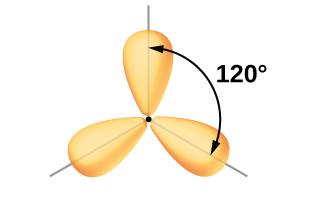
Embora a mecânica quântica produza os lóbulos orbitais “rechonchudos”, conforme descrito na Figura\(\PageIndex{5}\), às vezes, para maior clareza, esses orbitais são desenhados mais finos e sem os lóbulos menores, como na Figura\(\PageIndex{6}\), para evitar obscurecer outras características de uma determinada ilustração. Usaremos essas representações “mais finas” sempre que a visão real estiver muito cheia para ser facilmente visualizada.
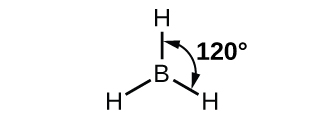
A estrutura observada da molécula de borano, BH 3, sugere hibridização sp 2 para boro neste composto. A molécula é trigonal plana e o átomo de boro está envolvido em três ligações aos átomos de hidrogênio (Figura\(\PageIndex{7}\)).
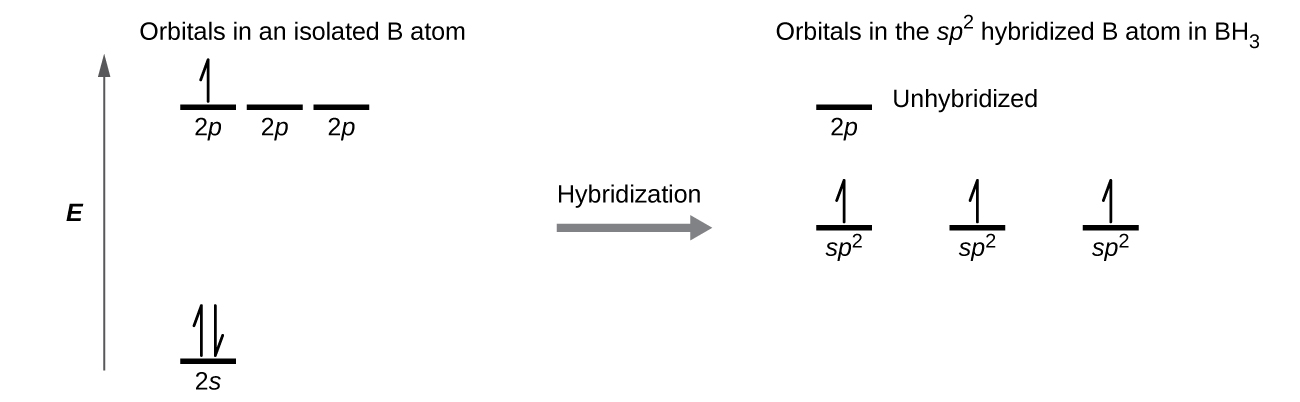
Podemos ilustrar a comparação dos orbitais e da distribuição de elétrons em um átomo de boro isolado e no átomo ligado em BH 3, conforme mostrado no diagrama do nível de energia orbital na Figura\(\PageIndex{8}\). Nós redistribuímos os três elétrons de valência do átomo de boro nos três orbitais híbridos sp 2, e cada elétron de boro emparelha com um elétron de hidrogênio quando as ligações B-H se formam.
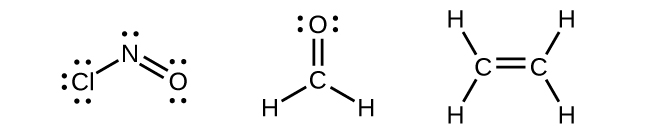
Qualquer átomo central cercado por três regiões de densidade eletrônica exibirá hibridização sp 2. Isso inclui moléculas com um par solitário no átomo central, como ClNO (Figura\(\PageIndex{9}\)), ou moléculas com duas ligações simples e uma ligação dupla conectada ao átomo central, como no formaldeído, CH 2 O e eteno, H 2 CCH 2.
sp 3 Hibridização
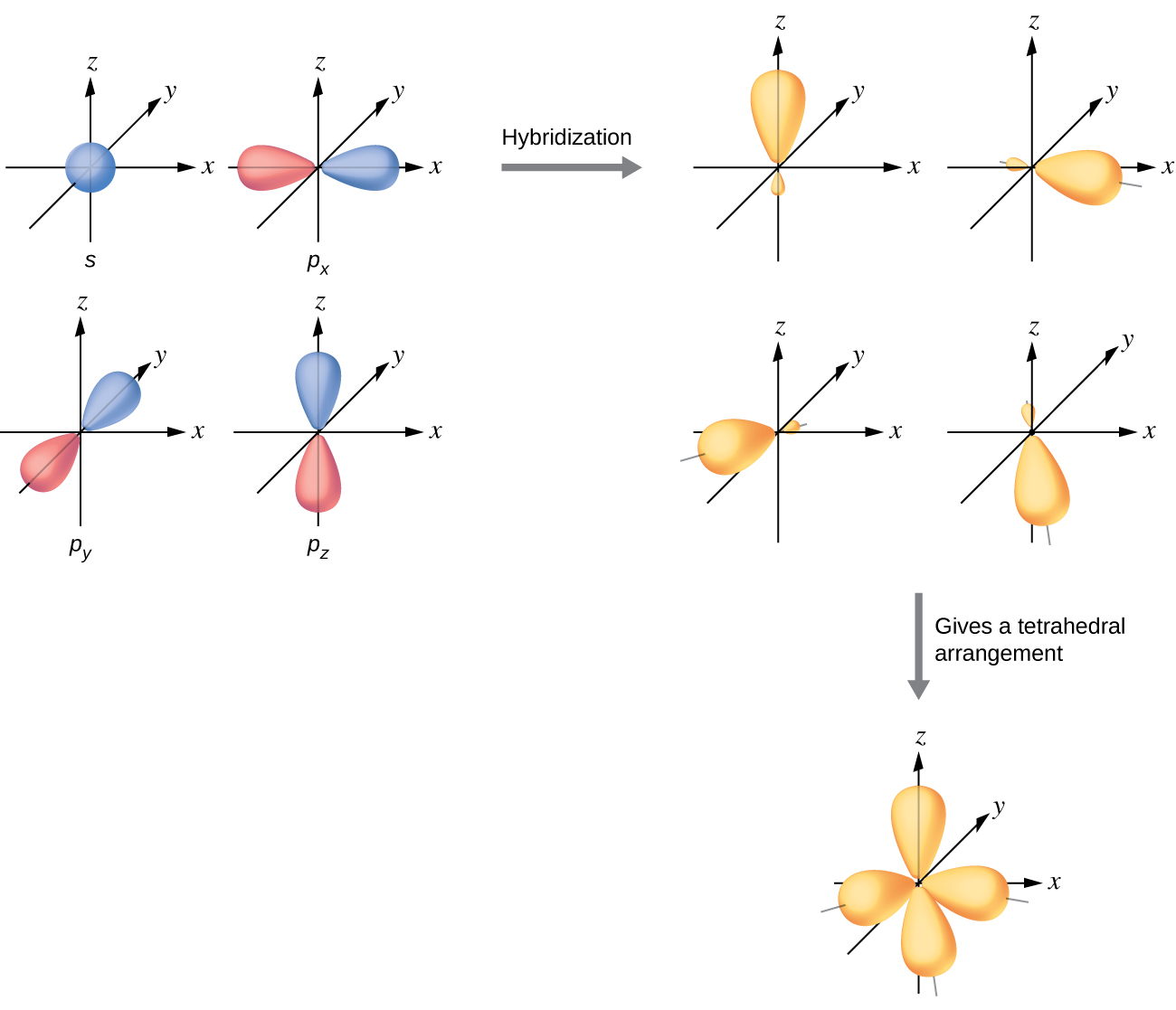
Os orbitais de valência de um átomo cercado por um arranjo tetraédrico de pares de ligação e pares solitários consistem em um conjunto de quatro orbitais híbridos sp 3. Os híbridos resultam da mistura de um orbital s e todos os três orbitais p que produzem quatro orbitais híbridos sp 3 idênticos (Figura\(\PageIndex{10}\)). Cada um desses orbitais híbridos aponta para um canto diferente de um tetraedro.
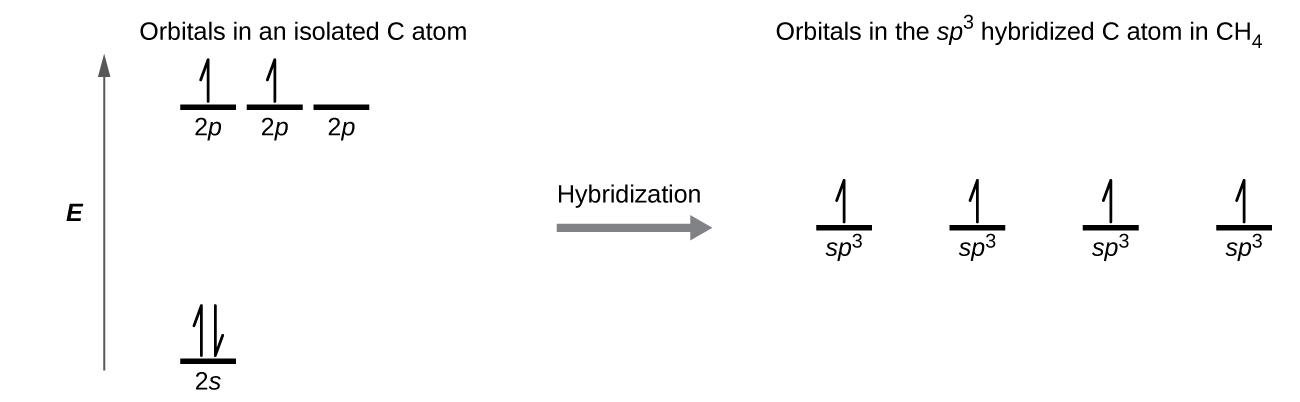
Uma molécula de metano, CH 4, consiste em um átomo de carbono cercado por quatro átomos de hidrogênio nos cantos de um tetraedro. O átomo de carbono no metano exibe hibridização sp 3. Ilustramos os orbitais e a distribuição de elétrons em um átomo de carbono isolado e no átomo ligado em CH 4 na Figura\(\PageIndex{11}\). Os quatro elétrons de valência do átomo de carbono são distribuídos igualmente nos orbitais híbridos, e cada elétron de carbono é emparelhado com um elétron de hidrogênio quando as ligações C-H se formam.
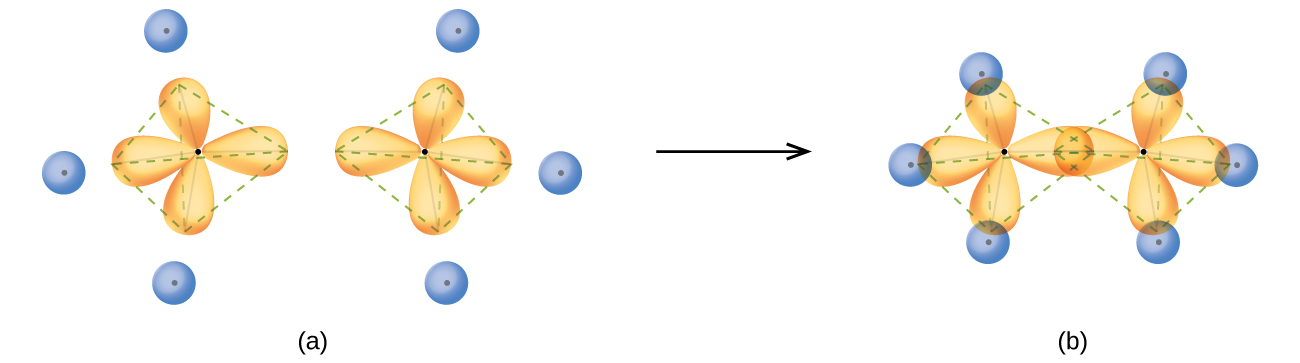
Em uma molécula de metano, o orbital 1 s de cada um dos quatro átomos de hidrogênio se sobrepõe a um dos quatro orbitais sp 3 do átomo de carbono para formar uma ligação sigma (σ). Isso resulta na formação de quatro ligações covalentes fortes e equivalentes entre o átomo de carbono e cada um dos átomos de hidrogênio para produzir a molécula de metano, CH 4.
A estrutura do etano, C 2 H 6, é semelhante à do metano, pois cada carbono no etano tem quatro átomos vizinhos dispostos nos cantos de um tetraedro - três átomos de hidrogênio e um átomo de carbono (Figura\(\PageIndex{10}\)). No entanto, no etano, um orbital sp 3 de um átomo de carbono se sobrepõe de ponta a ponta com um orbital sp 3 de um segundo átomo de carbono para formar uma ligação σ entre os dois átomos de carbono. Cada um dos orbitais híbridos sp 3 restantes se sobrepõe a um orbital s de um átomo de hidrogênio para formar ligações carbono-hidrogênio σ. A estrutura e o contorno geral dos orbitais de ligação do etano são mostrados na Figura\(\PageIndex{12}\). A orientação dos dois grupos CH 3 não é fixa em relação um ao outro. Evidências experimentais mostram que a rotação em torno das ligações σ ocorre facilmente.
Um orbital híbrido sp 3 também pode conter um único par de elétrons. Por exemplo, o átomo de nitrogênio na amônia é cercado por três pares de ligações e um único par de elétrons direcionado para os quatro cantos de um tetraedro. O átomo de nitrogênio é sp 3 hibridizado com um orbital híbrido ocupado pelo par solitário.
A estrutura molecular da água é consistente com um arranjo tetraédrico de dois pares solitários e dois pares de elétrons de ligação. Assim, dizemos que o átomo de oxigênio é hibridizado sp 3, com dois dos orbitais híbridos ocupados por pares solitários e dois por pares de ligação. Como pares solitários ocupam mais espaço do que pares de união, estruturas que contêm pares solitários têm ângulos de união ligeiramente distorcidos em relação ao ideal. Os tetraedros perfeitos têm ângulos de 109,5°, mas os ângulos observados em amônia (107,3°) e água (104,5°) são um pouco menores. Outros exemplos de hibridização sp 3 incluem cCl 4, pCl 3 e NCl 3.
hibridização sp 3 d e sp 3 d 2
Para descrever os cinco orbitais de ligação em um arranjo bipiramidal trigonal, devemos usar cinco dos orbitais atômicos da camada de valência (o orbital s, os três orbitais p e um dos orbitais d), o que dá cinco sp 3 d orbitais híbridos. Com um arranjo octaédrico de seis orbitais híbridos, devemos usar seis orbitais atômicos da camada de valência (o orbital s, os três orbitais p e dois dos orbitais d em sua camada de valência), o que dá seis sp 3 d 2 orbitais híbridos. Essas hibridizações só são possíveis para átomos que têm orbitais d em suas subcamadas de valência (ou seja, não aqueles no primeiro ou segundo período).

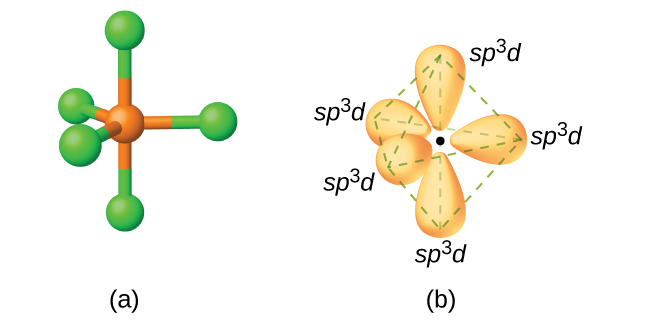
Em uma molécula de pentacloreto de fósforo, PCl 5, existem cinco ligações P-Cl (portanto, cinco pares de elétrons de valência ao redor do átomo de fósforo) direcionadas para os cantos de uma bipirâmide trigonal. Usamos o orbital 3 s, os três orbitais de 3 p e um dos orbitais 3 d para formar o conjunto de cinco orbitais híbridos sp 3 d (Figura\(\PageIndex{13}\)) que estão envolvidos nas ligações P-Cl. Outros átomos que exibem hibridização sp 3 d incluem o átomo de enxofre em SF 4 e os átomos de cloro em ClF 3 e in\(\ce{ClF4+}\). (Os elétrons nos átomos de flúor são omitidos para maior clareza.)
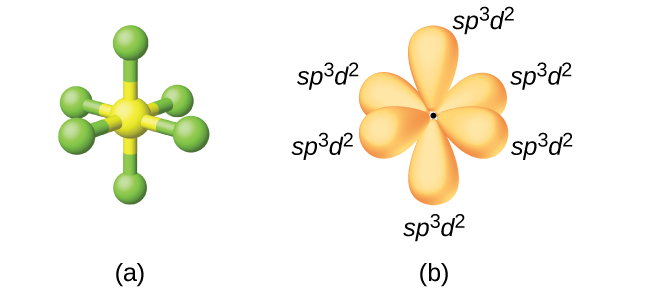
O átomo de enxofre no hexafluoreto de enxofre, SF 6, exibe hibridização sp 3 d 2. Uma molécula de hexafluoreto de enxofre tem seis pares de elétrons que conectam seis átomos de flúor a um único átomo de enxofre. Não há pares solitários de elétrons no átomo central. Para unir seis átomos de flúor, o orbital 3 s, os três orbitais 3 p e dois dos orbitais 3 d formam seis orbitais híbridos sp 3 d 2 equivalentes, cada um direcionado para um canto diferente de um octaedro. Outros átomos que exibem hibridização sp 3 d 2 incluem o átomo de fósforo em\(\ce{PCl6-}\), o átomo de iodo nos interhalogênios\(\ce{IF6+}\), IF 5\(\ce{IF4-}\) e o átomo de xenônio em XeF 4.\(\ce{ICl4-}\)
Atribuição de orbitais híbridos a átomos centrais
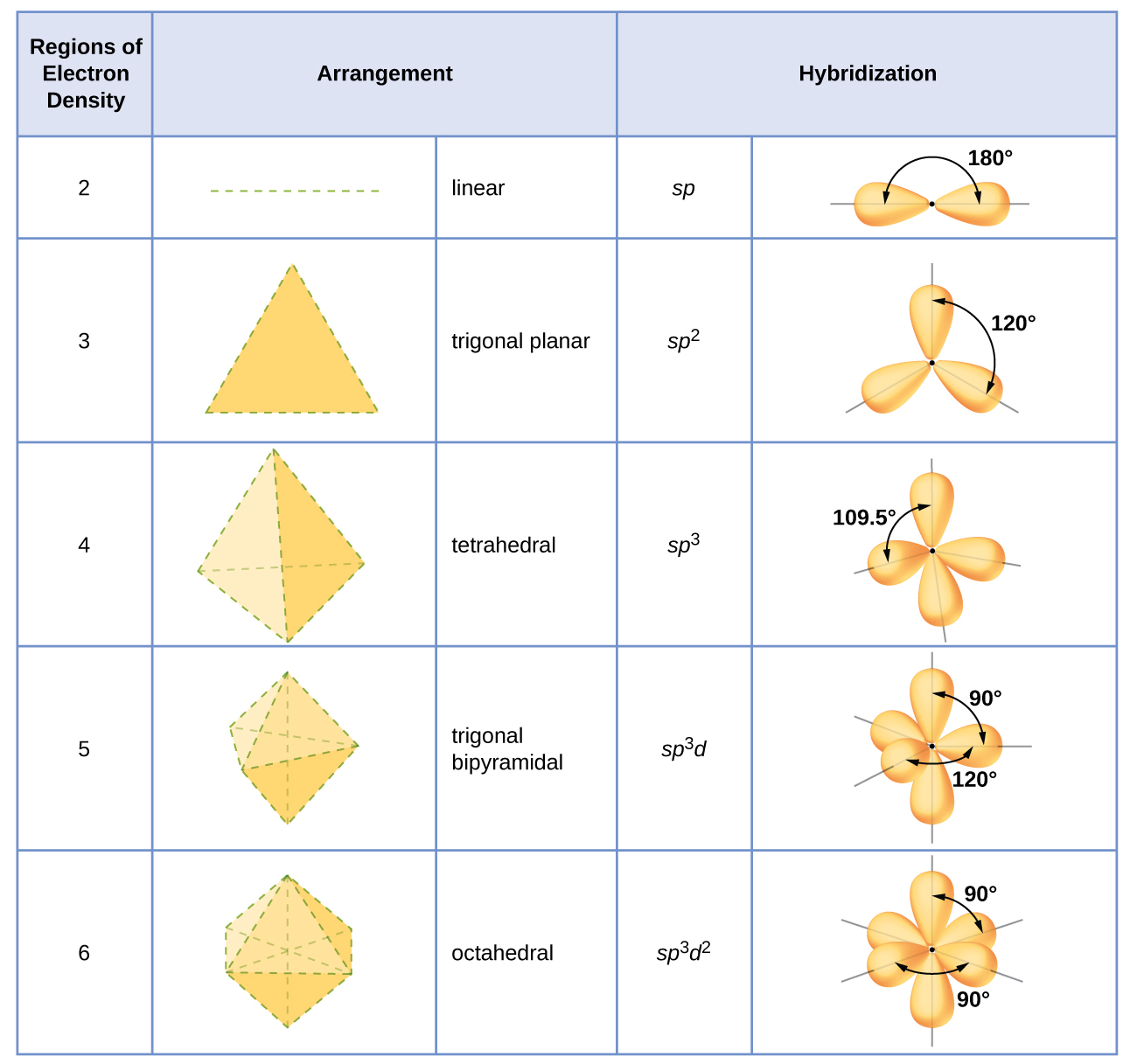
A hibridização de um átomo é determinada com base no número de regiões de densidade eletrônica que o cercam. Os arranjos geométricos característicos dos vários conjuntos de orbitais híbridos são mostrados na Figura\(\PageIndex{16}\). Esses arranjos são idênticos aos das geometrias de pares de elétrons previstas pela teoria VSEPR. A teoria VSEPR prevê as formas das moléculas, e a teoria orbital híbrida fornece uma explicação de como essas formas são formadas. Para encontrar a hibridização de um átomo central, podemos usar as seguintes diretrizes:
- Determine a estrutura de Lewis da molécula.
- Determine o número de regiões de densidade de elétrons ao redor de um átomo usando a teoria VSEPR, na qual ligações simples, ligações múltiplas, radicais e pares solitários contam como uma região.
- Atribua o conjunto de orbitais hibridizados da Figura\(\PageIndex{16}\) que corresponde a essa geometria.
É importante lembrar que a hibridização foi concebida para racionalizar geometrias moleculares observadas experimentalmente, e não o contrário.
O modelo funciona bem para moléculas contendo pequenos átomos centrais, nos quais os pares de elétrons de valência estão próximos no espaço. No entanto, para átomos centrais maiores, os pares de elétrons da camada de valência estão mais distantes do núcleo e há menos repulsões. Seus compostos exibem estruturas que muitas vezes não são consistentes com a teoria VSEPR, e orbitais hibridizados não são necessários para explicar os dados observados.
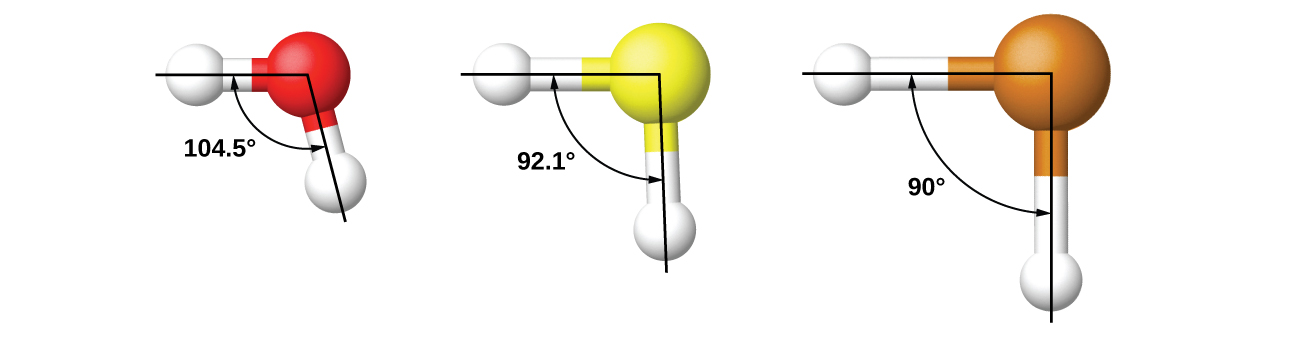
Por exemplo, discutimos o ângulo de ligação H—O—H em H 2 O, 104,5°, que é mais consistente com orbitais híbridos sp 3 (109,5°) no átomo central do que com orbitais 2 p (90°). O enxofre está no mesmo grupo do oxigênio e o H 2 S tem uma estrutura de Lewis semelhante. No entanto, ele tem um ângulo de ligação muito menor (92,1°), o que indica muito menos hibridização no enxofre do que no oxigênio. Continuando no grupo, o telúrio é ainda maior que o enxofre e, para H 2 Te, o ângulo de ligação observado (90°) é consistente com a sobreposição dos orbitais de 5 p, sem invocar hibridização. Invocamos a hibridização onde é necessário explicar as estruturas observadas.
Ammonium sulfate is important as a fertilizer. What is the hybridization of the sulfur atom in the sulfate ion, \(\ce{SO4^2-}\)?
Solution
The Lewis structure of sulfate shows there are four regions of electron density.
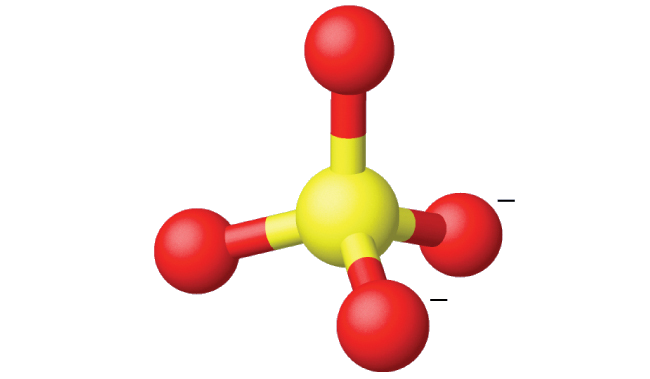
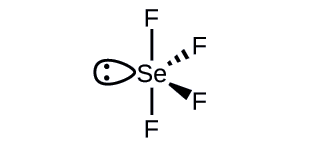
What is the hybridization of the selenium atom in SeF4?
- Answer
-
The selenium atom is sp3d hybridized.
Urea, NH2C(O)NH2, is sometimes used as a source of nitrogen in fertilizers. What is the hybridization of each nitrogen and carbon atom in urea?
Solution
The Lewis structure of urea is
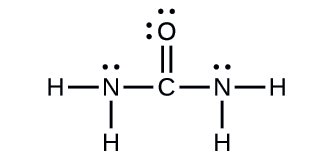
The carbon atom is surrounded by three regions of electron density, positioned in a trigonal planar arrangement. The hybridization in a trigonal planar electron pair geometry is sp2 (Figure \(\PageIndex{16}\)), which is the hybridization of the carbon atom in urea.
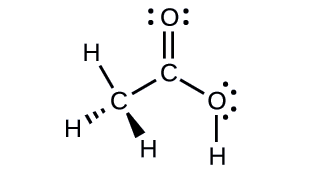
Acetic acid, H3CC(O)OH, is the molecule that gives vinegar its odor and sour taste. What is the hybridization of the two carbon atoms in acetic acid?
- Answer
-
H3C, sp3; C(O)OH, sp2
Summary
We can use hybrid orbitals, which are mathematical combinations of some or all of the valence atomic orbitals, to describe the electron density around covalently bonded atoms. These hybrid orbitals either form sigma (σ) bonds directed toward other atoms of the molecule or contain lone pairs of electrons. We can determine the type of hybridization around a central atom from the geometry of the regions of electron density about it. Two such regions imply sp hybridization; three, sp2 hybridization; four, sp3 hybridization; five, sp3d hybridization; and six, sp3d2 hybridization. Pi (π) bonds are formed from unhybridized atomic orbitals (p or d orbitals).
Footnotes
- Note that orbitals may sometimes be drawn in an elongated “balloon” shape rather than in a more realistic “plump” shape in order to make the geometry easier to visualize.
Glossary
- hybrid orbital
- orbital created by combining atomic orbitals on a central atom
- hybridization
- model that describes the changes in the atomic orbitals of an atom when it forms a covalent compound
- sp hybrid orbital
- one of a set of two orbitals with a linear arrangement that results from combining one s and one p orbital
- sp2 hybrid orbital
- one of a set of three orbitals with a trigonal planar arrangement that results from combining one s and two p orbitals
- sp3 hybrid orbital
- one of a set of four orbitals with a tetrahedral arrangement that results from combining one s and three p orbitals
- sp3d hybrid orbital
- one of a set of five orbitals with a trigonal bipyramidal arrangement that results from combining one s, three p, and one d orbital
- sp3d2 hybrid orbital
- one of a set of six orbitals with an octahedral arrangement that results from combining one s, three p, and two d orbitals


