1.3: Propriedades físicas e químicas
- Page ID
- 185212
- Descreva a diferença entre propriedades físicas e químicas ou alteradas.
- Identifique uma propriedade ou transformação como física ou química usando representações simbólicas, particuladas ou macroscópicas.
- Identifique as propriedades da matéria como extensas ou intensivas.
- Reconheça e descreva as partes do diamante perigoso NFPA.
As características que nos permitem distinguir uma substância de outra são chamadas de propriedades. Uma propriedade física é uma característica da matéria que não está associada a uma mudança em sua composição química. Exemplos familiares de propriedades físicas incluem densidade, cor, dureza, pontos de fusão e ebulição e condutividade elétrica. Podemos observar algumas propriedades físicas, como densidade e cor, sem alterar o estado físico da matéria observada. Outras propriedades físicas, como a temperatura de fusão do ferro ou a temperatura de congelamento da água, só podem ser observadas quando a matéria sofre uma mudança física. Uma mudança física é uma mudança no estado ou nas propriedades da matéria sem qualquer alteração associada em sua composição química (as identidades das substâncias contidas na matéria). Observamos uma mudança física quando a cera derrete, quando o açúcar se dissolve no café e quando o vapor se condensa em água líquida (Figura\(\PageIndex{1}\)). Outros exemplos de mudanças físicas incluem magnetização e desmagnetização de metais (como é feito com etiquetas de segurança antifurto comuns) e trituração de sólidos em pó (o que às vezes pode produzir mudanças visíveis na cor). Em cada um desses exemplos, há uma mudança no estado físico, na forma ou nas propriedades da substância, mas nenhuma mudança em sua composição química.

A mudança de um tipo de matéria para outro tipo (ou a incapacidade de mudar) é uma propriedade química. Exemplos de propriedades químicas incluem inflamabilidade, toxicidade, acidez, reatividade (muitos tipos) e calor de combustão. O ferro, por exemplo, se combina com o oxigênio na presença de água para formar ferrugem; o cromo não oxida (Figura\(\PageIndex{2}\)). A nitroglicerina é muito perigosa porque explode facilmente; o néon quase não representa nenhum risco porque não é muito reativo.

Para identificar uma propriedade química, procuramos uma mudança química. Uma mudança química sempre produz um ou mais tipos de matéria que diferem da matéria presente antes da mudança. A formação de ferrugem é uma mudança química porque a ferrugem é um tipo de matéria diferente do ferro, oxigênio e água presentes antes da formação da ferrugem. A explosão da nitroglicerina é uma mudança química porque os gases produzidos são tipos de matéria muito diferentes da substância original. Outros exemplos de mudanças químicas incluem reações que são realizadas em laboratório (como cobre reagindo com ácido nítrico), todas as formas de combustão (queima) e alimentos sendo cozidos, digeridos ou apodrecendo (Figura\(\PageIndex{3}\)).

As propriedades da matéria se enquadram em uma das duas categorias. Se a propriedade depende da quantidade de matéria presente, é uma propriedade extensa. A massa e o volume de uma substância são exemplos de propriedades extensas; por exemplo, um galão de leite tem uma massa e um volume maiores do que uma xícara de leite. O valor de uma propriedade extensa é diretamente proporcional à quantidade de matéria em questão. Se a propriedade de uma amostra de matéria não depende da quantidade de matéria presente, é uma propriedade intensiva. A temperatura é um exemplo de propriedade intensiva. Se o galão e a xícara de leite estiverem a 20 °C (temperatura ambiente), quando combinados, a temperatura permanece em 20 °C. Como outro exemplo, considere as propriedades distintas, mas relacionadas, do calor e da temperatura. Uma gota de óleo de cozinha quente salpicada em seu braço causa um pequeno e breve desconforto, enquanto uma panela com óleo quente produz queimaduras graves. Tanto a gota quanto a panela de óleo estão na mesma temperatura (uma propriedade intensiva), mas a panela claramente contém muito mais calor (propriedade extensa).
Diamante Hazard
Você pode ter visto o símbolo mostrado na Figura\(\PageIndex{4}\) em recipientes de produtos químicos em um laboratório ou local de trabalho. Às vezes chamado de “diamante de fogo” ou “diamante perigoso”, esse diamante de risco químico fornece informações valiosas que resumem brevemente os vários perigos dos quais você deve estar ciente ao trabalhar com uma substância específica.
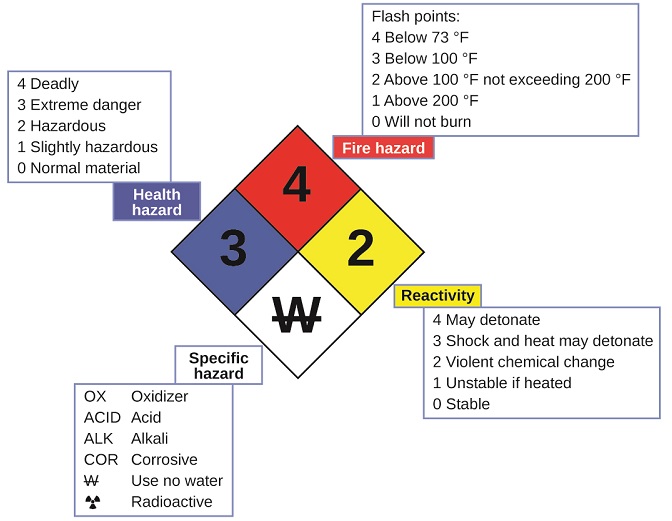
O Sistema de Identificação de Perigos 704 da Agência Nacional de Proteção contra Incêndios (NFPA) foi desenvolvido pela NFPA para fornecer informações de segurança sobre determinadas substâncias. O sistema detalha inflamabilidade, reatividade, saúde e outros riscos. Dentro do símbolo geral do diamante, o diamante superior (vermelho) especifica o nível de risco de incêndio (faixa de temperatura para o ponto de inflamação). O diamante azul (esquerdo) indica o nível de risco à saúde. O diamante amarelo (direito) descreve riscos de reatividade, como a rapidez com que a substância sofrerá detonação ou uma mudança química violenta. O diamante branco (inferior) aponta riscos especiais, como se fosse um oxidante (que permite que a substância queime na ausência de ar/oxigênio), sofrer uma reação incomum ou perigosa com a água, ser corrosivo, ácido, alcalino, um risco biológico, radioativo e assim por diante. Cada perigo é classificado em uma escala de 0 a 4, com 0 sendo nenhum perigo e 4 sendo extremamente perigoso.
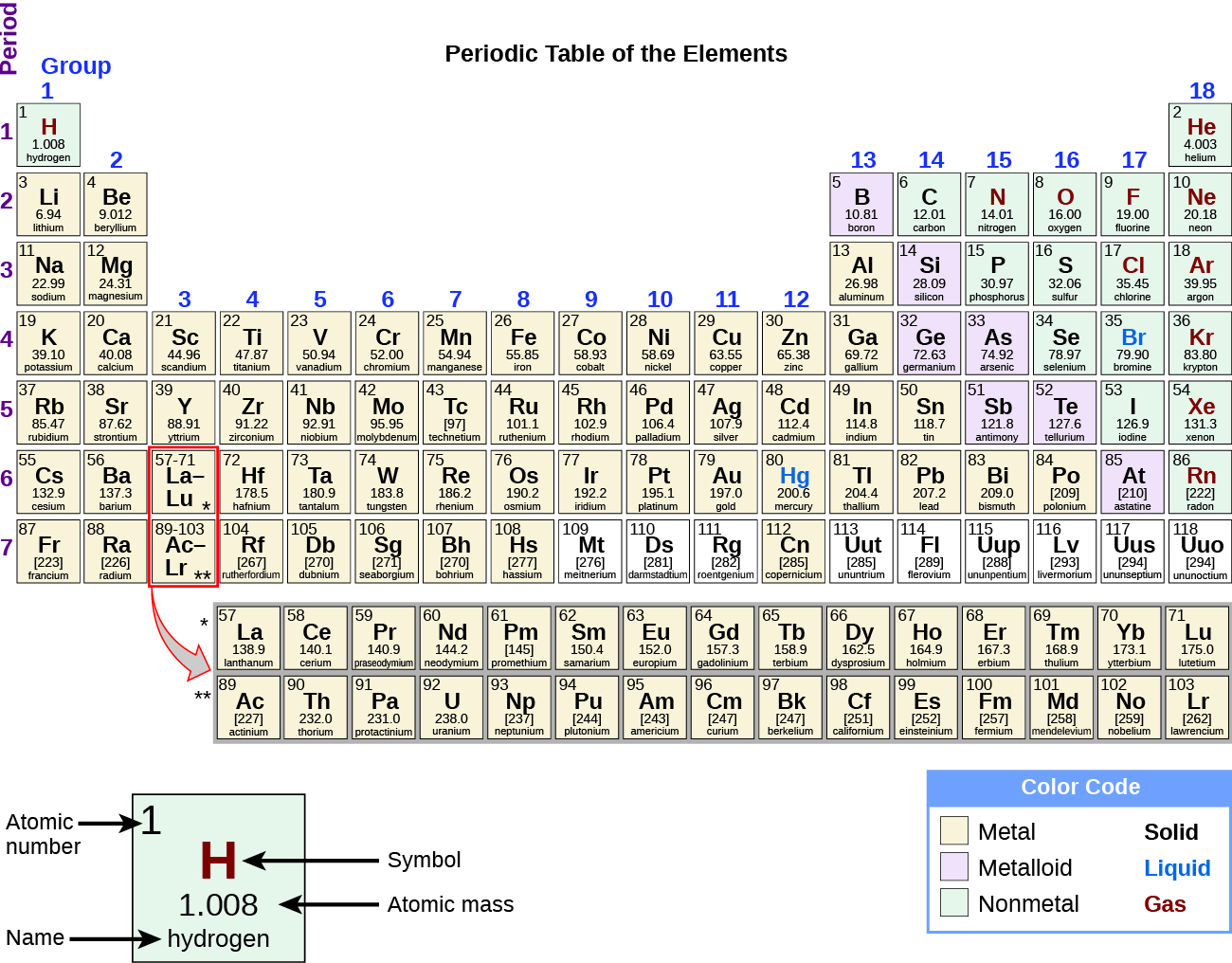
Embora muitos elementos difiram dramaticamente em suas propriedades químicas e físicas, alguns elementos têm propriedades semelhantes. Podemos identificar conjuntos de elementos que exibem comportamentos comuns. Por exemplo, muitos elementos conduzem bem o calor e a eletricidade, enquanto outros são maus condutores. Essas propriedades podem ser usadas para classificar os elementos em três classes: metais (elementos que conduzem bem), não metais (elementos que conduzem mal) e metalóides (elementos que têm propriedades tanto de metais quanto de não metais).
A tabela periódica é uma tabela de elementos que coloca os elementos com propriedades semelhantes próximos (Figura\(\PageIndex{5}\)). Você aprenderá mais sobre a tabela periódica ao continuar seus estudos de química.
Resumo
Todas as substâncias têm propriedades físicas e químicas distintas e podem sofrer alterações físicas ou químicas. Propriedades físicas, como dureza e ponto de ebulição, e mudanças físicas, como fusão ou congelamento, não envolvem uma mudança na composição da matéria. Propriedades químicas, como inflamabilidade e acidez, e mudanças químicas, como ferrugem, envolvem a produção de matéria que difere daquela presente anteriormente.
As propriedades mensuráveis se enquadram em uma das duas categorias. As propriedades extensas dependem da quantidade de matéria presente, por exemplo, da massa de ouro. As propriedades intensivas não dependem da quantidade de matéria presente, por exemplo, da densidade do ouro. O calor é um exemplo de uma propriedade extensa, e a temperatura é um exemplo de propriedade intensiva.
Glossário
- mudança química
- mudança produzindo um tipo diferente de matéria do tipo original de matéria
- propriedade química
- comportamento relacionado à mudança de um tipo de matéria em outro tipo de matéria
- propriedade extensa
- propriedade de uma substância que depende da quantidade da substância
- propriedade intensiva
- propriedade de uma substância que é independente da quantidade da substância
- mudança física
- mudança no estado ou nas propriedades da matéria que não envolva uma mudança em sua composição química
- propriedade física
- característica da matéria que não está associada a nenhuma alteração em sua composição química


