26.3: Doenças Acelulares Patogênicas do Sistema Nervoso
- Page ID
- 181681
Objetivos de
- Identifique os patógenos acelulares mais comuns que podem causar infecções do sistema nervoso
- Compare as principais características de doenças virais específicas que afetam o sistema nervoso
Vários vírus e partículas subvirais diferentes podem causar doenças que afetam o sistema nervoso. As doenças virais tendem a ser mais comuns do que as infecções bacterianas do sistema nervoso atualmente. Felizmente, as infecções virais geralmente são mais leves do que as bactérias e geralmente se resolvem espontaneamente. Alguns dos patógenos acelulares mais importantes do sistema nervoso são descritos nesta seção.
Meningite viral
Embora seja muito mais comum do que a meningite bacteriana, a meningite viral geralmente é menos grave. Muitos vírus diferentes podem levar à meningite como sequela da infecção primária, incluindo aqueles que causam herpes, gripe, sarampo e caxumba. A maioria dos casos de meningite viral se resolve espontaneamente, mas casos graves ocorrem.
Encefalite arboviral
Vários tipos de vírus transmitidos por insetos podem causar encefalite. Coletivamente, esses vírus são chamados de arbovírus (porque são tropodérmicos) e as doenças que causam são descritas como encefalite arboviral. A maioria dos arbovírus é endêmica em regiões geográficas específicas. As doenças da encefalite arborviral encontradas nos Estados Unidos incluem encefalite equina oriental (EEE), encefalite equina ocidental (WEE), encefalite de St. Louis e encefalite do Nilo Ocidental (WNE). A expansão dos arbovírus para além de suas regiões endêmicas às vezes ocorre, geralmente como resultado de mudanças ambientais favoráveis ao vírus ou ao seu vetor. O aumento das viagens de humanos, animais ou vetores infectados também permitiu que os arbovírus se espalhassem para novas regiões.
Na maioria dos casos, as infecções arbovirais são assintomáticas ou levam a uma doença leve. No entanto, quando os sintomas ocorrem, eles incluem febre alta, calafrios, dores de cabeça, vômitos, diarréia e agitação. Em pacientes idosos, a encefalite arboviral grave pode levar rapidamente a convulsões, coma e morte.
Os mosquitos são os vetores biológicos mais comuns dos arbovírus, que tendem a ser vírus ssRNA envoltos. Assim, a prevenção de infecções arbovirais é melhor evitando mosquitos — usando repelente de insetos, usando calças e mangas compridas, dormindo em quartos bem protegidos, usando mosquiteiros, etc.
O diagnóstico de encefalite arboviral é baseado em sintomas clínicos e testes sorológicos de soro ou LCR. Não existem medicamentos antivirais para tratar nenhuma dessas doenças arbovirais, portanto, o tratamento consiste em cuidados de suporte e tratamento dos sintomas.
A encefalite equina oriental (EEE) é causada pelo vírus da encefalite equina oriental (EEEV), que pode causar doenças graves em cavalos e humanos. As aves são reservatórios para EEEV com transmissão acidental para cavalos e humanos pelas espécies de mosquitos Aedes, Coquillettidia e Culex. Nem cavalos nem humanos servem como reservatórios. O EEE é mais comum na Costa do Golfo dos EUA e nos estados do Atlântico. O EEE é uma das doenças transmitidas por mosquitos mais graves nos Estados Unidos, mas, felizmente, é uma doença muito rara nos Estados Unidos (Figura\(\PageIndex{1}\)). 1 2
A encefalite equina ocidental (WEE) é causada pelo vírus da encefalite equina ocidental (WEEV). O WEEV geralmente é transmitido a cavalos e humanos pelos mosquitos Culex tarsalis e, na última década, causou pouquíssimos casos de encefalite em humanos nos Estados Unidos. Em humanos, os sintomas do WEE são menos graves do que o EEE e incluem febre, calafrios e vômitos, com uma taxa de mortalidade de 3 a 4%. Como o EEEV, os pássaros são o reservatório natural do WEEV. Periodicamente, por motivos indeterminados, epidemias em casos humanos ocorreram na América do Norte no passado. O maior já registrado foi em 1941, com mais de 3400 casos. 3
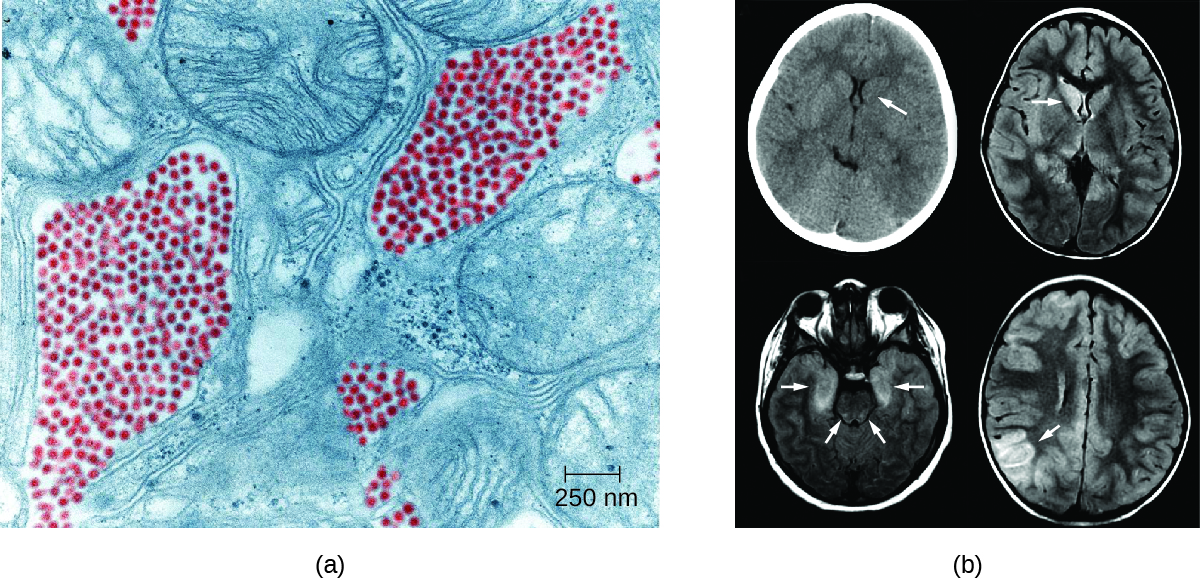
A encefalite de St. Louis (LES), causada pelo vírus da encefalite de St. Louis (SLEV), é uma forma rara de encefalite com sintomas que ocorrem em menos de 1% dos pacientes infectados. Os reservatórios naturais do SLEV são pássaros. O SLEV é mais frequentemente encontrado na bacia do rio Ohio-Mississippi, no centro dos Estados Unidos, e recebeu o nome de um surto grave no Missouri em 1934. O pior surto de encefalite de St. Louis ocorreu em 1975, com mais de 2000 casos relatados. 4 Os humanos são infectados quando picados por mosquitos C. tarsalis, C. quinquefasciatus ou C. pipiens portadores de SLEV. A maioria dos pacientes é assintomática, mas em um pequeno número de indivíduos, os sintomas variam de síndromes leves semelhantes à gripe a encefalite fatal. A taxa de mortalidade geral para pacientes sintomáticos é de 5 a 15%. 5
A encefalite japonesa, causada pelo vírus da encefalite japonesa (JEV), é a principal causa de encefalite evitável por vacina em humanos e é endêmica em alguns dos países mais populosos do mundo, incluindo China, Índia, Japão e todo o Sudeste Asiático. O JEV é transmitido aos humanos pelos mosquitos Culex, geralmente da espécie C. tritaeniorhynchus. Os reservatórios biológicos do JEV incluem porcos e aves pernaltas. A maioria dos pacientes com infecções por JEV é assintomática, com sintomas ocorrendo em menos de 1% dos indivíduos infectados. No entanto, cerca de 25% das pessoas que desenvolvem encefalite morrem e, entre aquelas que se recuperam, 30 a 50% têm comprometimento psiquiátrico, neurológico ou cognitivo. 6 Felizmente, existe uma vacina eficaz que pode prevenir a infecção pelo JEV. O CDC recomenda essa vacina para viajantes que esperam passar mais de um mês em áreas endêmicas.
Como o nome sugere, o vírus do Nilo Ocidental (WNV) e sua doença associada, a encefalite do Nilo Ocidental (WNE), não se originaram na América do Norte. Até 1999, era endêmico no Oriente Médio, África e Ásia; no entanto, os primeiros casos nos EUA foram identificados em Nova York em 1999 e, em 2004, o vírus havia se espalhado por todo o continente dos Estados Unidos. Mais de 35.000 casos, incluindo 1400 mortes, foram confirmados no período de cinco anos entre 1999 e 2004. A infecção por WNV permanece relatável ao CDC.
O WNV é transmitido aos humanos pelos mosquitos Culex a partir de seu reservatório natural, aves infectadas, com 70 a 80% dos pacientes infectados sem sintomas. A maioria dos casos sintomáticos envolve apenas sintomas leves, semelhantes aos da gripe, mas menos de 1% das pessoas infectadas desenvolvem encefalite ou meningite grave e às vezes fatal. A taxa de mortalidade em pacientes com WNV que desenvolvem doenças neurológicas é de cerca de 10%. Mais informações sobre o vírus do Nilo Ocidental podem ser encontradas em Modos de transmissão de doenças.
Este mapa interativo identifica casos de várias doenças arbovirais em humanos e espécies de reservatórios por estado e ano para os Estados Unidos.
Exercício\(\PageIndex{1}\)
- Por que é improvável que os vírus da encefalite arboviral sejam erradicados no futuro?
- Qual é a forma mais comum de encefalite viral nos Estados Unidos?
Foco clínico: Parte 2
A levofloxacina é um antibiótico de quinolona frequentemente prescrito para tratar infecções bacterianas do trato respiratório, incluindo pneumonia e bronquite. Mas depois de tomar o medicamento por uma semana, David voltou ao médico mais doente do que antes. Ele alegou que o antibiótico não teve efeito sobre seus sintomas anteriores. Além disso, ele agora estava com dores de cabeça, rigidez no pescoço e dificuldade de se concentrar no trabalho. Ele também mostrou ao médico uma erupção cutânea que se desenvolveu em seus braços na semana passada. Seu médico, mais preocupado agora, começou a perguntar sobre as atividades de David nas últimas duas semanas.
David explicou que estava trabalhando recentemente em um projeto para desmontar um antigo celeiro. Seu médico coletou amostras de escarro e raspagens da erupção cutânea de David para culturas. Uma punção lombar também foi realizada para examinar o LCR de David. O exame microscópico de seu LCR revelou células de levedura encapsuladas. Com base nesse resultado, o médico prescreveu uma nova terapia antimicrobiana com anfotericina B e flucitosina.
Exercício\(\PageIndex{2}\)
- Por que o tratamento original foi ineficaz?
- Por que a presença de uma cápsula é clinicamente importante?
Infecção pelo zika vírus
A infecção pelo vírus Zika é uma doença arboviral emergente associada a doenças humanas na África, Sudeste Asiático e América do Sul e Central; no entanto, seu alcance está se expandindo como resultado da ampla variedade de seu mosquito vetor. Os primeiros casos originários dos Estados Unidos foram relatados em 2016. O vírus Zika foi inicialmente descrito em 1947 em macacos na Floresta Zika de Uganda por meio de uma rede que monitorava a febre amarela. Não era considerado um patógeno humano grave até que os primeiros surtos em grande escala ocorreram na Micronésia em 2007; 7 no entanto, o vírus ganhou notoriedade na última década, pois surgiu como causa de sintomas semelhantes a outras infecções arbovirais que incluem febre, erupções cutâneas, conjuntivite, dores musculares e articulares, mal-estar e dor de cabeça. Os mosquitos do gênero Aedes são os principais vetores, embora o vírus também possa ser transmitido sexualmente, da mãe para o bebê durante a gravidez ou por meio de uma transfusão de sangue.
A maioria das infecções pelo vírus Zika resulta em sintomas leves, como febre, erupção cutânea leve ou conjuntivite. No entanto, infecções em mulheres grávidas podem afetar adversamente o desenvolvimento do feto. Relatórios de 2015 indicam que infecções fetais podem resultar em danos cerebrais, incluindo um grave defeito congênito chamado microcefalia, no qual o bebê nasce com uma cabeça anormalmente pequena (Figura\(\PageIndex{2}\)). 8
O diagnóstico de Zika é baseado principalmente nos sintomas clínicos. No entanto, o FDA autorizou recentemente o uso de um ensaio de RNA do vírus Zika, Trioplex RT-PCR e Zika MAC-ELISA para testar o sangue e a urina do paciente para confirmar a doença pelo vírus Zika. Atualmente, não há tratamentos antivirais ou vacinas para o vírus Zika, e o tratamento é limitado aos cuidados de suporte.
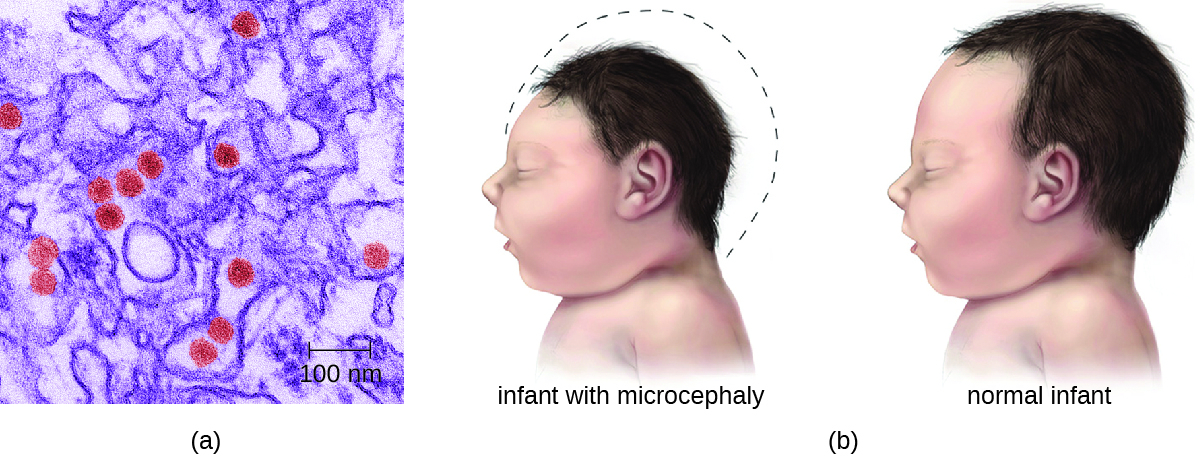
Exercício\(\PageIndex{3}\)
- Quais são os sinais e sintomas da infecção pelo vírus Zika em adultos?
- Por que a infecção pelo vírus Zika é considerada uma séria ameaça à saúde pública?
Raiva
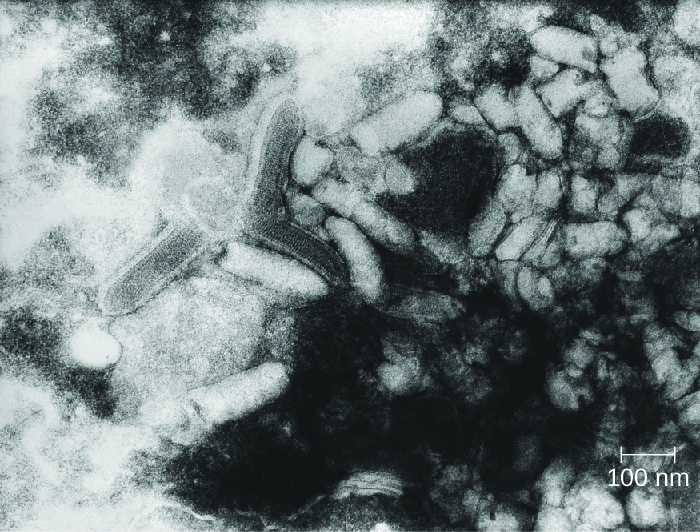
A raiva é uma doença zoonótica mortal conhecida desde a antiguidade. A doença é causada pelo vírus da raiva (RV), membro da família Rhabdoviridae, e é transmitida principalmente pela picada de um mamífero infectado. Rhabdoviridae são vírus de RNA envelopados que têm uma forma de bala distinta (Figura\(\PageIndex{3}\)); eles foram estudados pela primeira vez por Louis Pasteur, que obteve o vírus da raiva de cães raivosos e cultivou o vírus em coelhos. Ele preparou com sucesso uma vacina contra a raiva usando tecidos nervosos secos de animais infectados. Esta vacina foi usada pela primeira vez para tratar um ser humano infectado em 1885.
Os reservatórios mais comuns nos Estados Unidos são animais selvagens, como guaxinins (30,2% de todos os casos de animais em 2014), morcegos (29,1%), gambás (26,3%) e raposas (4,1%); coletivamente, esses animais foram responsáveis por um total de 92,6% dos casos de raiva animal nos Estados Unidos em 2014. Os 7,4% restantes dos casos daquele ano foram em animais domesticados, como cães, gatos, cavalos, mulas, ovelhas, cabras e lhamas. 9 Embora normalmente ocorram apenas um ou dois casos humanos por ano nos Estados Unidos, a raiva ainda causa dezenas de milhares de mortes humanas por ano em todo o mundo, principalmente na Ásia e na África.
A baixa incidência de raiva nos Estados Unidos é principalmente resultado da ampla vacinação de cães e gatos. Uma vacina oral também é usada para proteger animais selvagens, como guaxinins e raposas, contra infecções. Os programas de vacinas orais tendem a se concentrar em áreas geográficas onde a raiva é endêmica. 10 A vacina oral geralmente é entregue em um pacote de isca que é jogado de avião, embora a isca em áreas urbanas seja feita manualmente para maximizar a segurança. 11 Muitos países exigem uma quarentena ou prova de vacinação anti-rábica para animais domésticos trazidos para o país. Esses procedimentos são especialmente rigorosos em nações insulares onde a raiva ainda não está presente, como a Austrália.
O período de incubação da raiva pode ser longo, variando de várias semanas ou meses a mais de um ano. À medida que o vírus se replica, ele se move do local da picada para os axônios motores e sensoriais dos nervos periféricos e se espalha de nervo em nervo usando um processo chamado transporte retrógrado, chegando ao SNC através dos gânglios espinhais. Quando o vírus da raiva chega ao cérebro, a infecção leva à encefalite causada pela interrupção da função normal dos neurotransmissores, resultando nos sintomas associados à raiva. Os viriões atuam nos espaços sinápticos como concorrentes de uma variedade de neurotransmissores para receptores de acetilcolina, GABA e glicina. Assim, a ação do vírus da raiva é neurotóxica e não citotóxica. Depois que o vírus da raiva infecta o cérebro, ele pode continuar a se espalhar por outras vias neuronais, saindo do SNC para tecidos como as glândulas salivares, onde o vírus pode ser liberado. Como resultado, à medida que a doença progride, o vírus pode ser encontrado em muitos outros tecidos, incluindo glândulas salivares, papilas gustativas, cavidade nasal e lágrimas.
Os primeiros sintomas da raiva incluem desconforto no local da picada, febre e dor de cabeça. Quando o vírus chega ao cérebro e, posteriormente, os sintomas aparecem, a doença é sempre fatal. Os casos terminais de raiva podem terminar de duas maneiras: raiva furiosa ou paralítica. Indivíduos com raiva furiosa ficam muito agitados e hiperativos. A hidrofobia (medo da água) é comum em pacientes com raiva furiosa, causada por espasmos musculares na garganta ao engolir ou pensar em água. O excesso de salivação e o desejo de morder podem causar espuma na boca. Esses comportamentos servem para aumentar a probabilidade de transmissão viral, embora o contato com secreções infectadas, como saliva ou lágrimas, por si só, seja suficiente para a infecção. A doença culmina após apenas alguns dias com terror e confusão, seguidos de parada cardiovascular e respiratória. Em contraste, indivíduos com raiva paralítica geralmente seguem um curso mais longo da doença. Os músculos no local da infecção ficam paralisados. Durante um período de tempo, a paralisia se espalha lentamente por todo o corpo. Essa forma paralítica de doença culmina em coma e morte.
Antes que os métodos diagnósticos atuais estivessem disponíveis, o diagnóstico da raiva era feito por meio da história clínica do caso e do exame histopatológico dos tecidos de biópsia ou autópsia, procurando a presença de corpos de Negri. Agora sabemos que essas alterações histológicas não podem ser usadas para confirmar o diagnóstico de raiva. Não há testes que possam detectar o vírus da raiva em humanos no momento da picada ou logo depois. Depois que o vírus começa a se replicar (mas antes que os sintomas clínicos ocorram), o vírus pode ser detectado por meio de um teste de imunofluorescência nos nervos cutâneos encontrados na base dos folículos pilosos. A saliva também pode ser testada para material genético viral por transcrição reversa seguida pela reação em cadeia da polimerase (RT-PCR). Mesmo quando esses testes são realizados, a maioria das infecções suspeitas é tratada como positiva na ausência de evidências contrárias. É melhor que os pacientes façam terapia desnecessária por causa de um resultado falso positivo, em vez de morrer como resultado de um resultado falso-negativo.
As infecções humanas por raiva são tratadas pela imunização com várias doses de uma vacina atenuada para desenvolver imunidade ativa no paciente (consulte o recurso Clinical Focus no capítulo sobre patógenos acelulares). A vacinação de um indivíduo já infectado tem o potencial de funcionar devido ao lento progresso da doença, o que dá tempo para o sistema imunológico do paciente desenvolver anticorpos contra o vírus. Os pacientes também podem ser tratados com imunoglobulina humana contra a raiva (anticorpos contra o vírus da raiva) para estimular a imunidade passiva. Esses anticorpos neutralizarão quaisquer partículas virais livres. Embora a infecção por raiva progrida lentamente nos tecidos periféricos, os pacientes normalmente não conseguem montar uma resposta imune protetora sozinhos.
Exercício\(\PageIndex{4}\)
- Como a picada de um animal infectado transmite a raiva?
- Qual é o objetivo dos programas de vacinação contra a raiva contra a vida selvagem?
- Como a raiva é tratada em humanos?
Poliomielite
A poliomielite (poliomielite), causada pelo poliovírus, é uma doença principalmente intestinal que, em uma pequena porcentagem dos casos, segue para o sistema nervoso, causando paralisia e, potencialmente, morte. O poliovírus é altamente contagioso, com transmissão ocorrendo pela via fecal-oral ou por transmissão por aerossol ou gotículas. Aproximadamente 72% de todas as infecções por poliovírus são assintomáticas; outros 25% resultam apenas em doenças intestinais leves, produzindo náuseas, febre e cefaleia. 12 No entanto, mesmo na ausência de sintomas, os pacientes infectados com o vírus podem eliminá-lo nas fezes e secreções orais, potencialmente transmitindo o vírus a outras pessoas. Em cerca de um caso em cada 200, o poliovírus afeta as células do SNC. 13
Depois de entrar pela boca, a replicação inicial do poliovírus ocorre no local da implantação na faringe e no trato gastrointestinal. Conforme a infecção progride, o poliovírus geralmente está presente na garganta e nas fezes antes do início dos sintomas. Uma semana após o início dos sintomas, há menos poliovírus na garganta, mas por várias semanas o poliovírus continua sendo excretado nas fezes. O poliovírus invade o tecido linfóide local, entra na corrente sanguínea e, em seguida, pode infectar as células do SNC. A replicação do poliovírus nos neurônios motores das células do corno anterior na medula espinhal, tronco cerebral ou córtex motor resulta na destruição celular e leva à paralisia flácida. Em casos graves, isso pode envolver o sistema respiratório, levando à morte. Pacientes com comprometimento da função respiratória são tratados com sistemas de ventilação com pressão positiva. No passado, os pacientes às vezes ficavam confinados aos respiradores Emerson, também conhecidos como pulmões de ferro (Figura\(\PageIndex{4}\)).
A detecção direta do poliovírus na garganta ou nas fezes pode ser obtida por meio de PCR de transcriptase reversa (RT-PCR) ou sequenciamento genômico para identificar o genótipo do poliovírus que infecta o paciente. Os testes sorológicos podem ser usados para determinar se o paciente foi previamente vacinado. Não há medidas terapêuticas para a poliomielite; o tratamento é limitado a várias medidas de suporte. Isso inclui analgésicos, repouso, terapia térmica para aliviar espasmos musculares, fisioterapia e aparelhos corretivos, se necessário, para ajudar na caminhada, e ventilação mecânica para auxiliar na respiração, se necessário.

Duas vacinas diferentes foram introduzidas na década de 1950 que levaram à diminuição dramática da poliomielite em todo o mundo (Figura\(\PageIndex{5}\)). A vacina Salk é um vírus inativado da poliomielite que foi introduzido pela primeira vez em 1955. Esta vacina é administrada por injeção intramuscular. A vacina Sabin é uma vacina oral contra a poliomielite que contém um vírus atenuado; foi licenciada para uso em 1962. Existem três sorotipos de poliovírus que causam doenças em humanos; as vacinas Salk e Sabin são eficazes contra as três.
Os vírus atenuados da vacina Sabin são eliminados nas fezes de indivíduos imunizados e, portanto, têm o potencial de infectar indivíduos não imunizados. No final da década de 1990, os poucos casos de pólio originados nos Estados Unidos poderiam ser atribuídos à vacina Sabin. Nesses casos, mutações do vírus atenuado após a vacinação provavelmente permitiram que o micróbio voltasse à forma virulenta. Por esse motivo, os Estados Unidos mudaram exclusivamente para a vacina Salk em 2000. Como a vacina Salk contém um vírus inativado, não há risco de transmissão para outras pessoas (consulte Vacinas). Atualmente, quatro doses da vacina são recomendadas para crianças: com 2, 4 e 6 a 18 meses de idade e 4 a 6 anos de idade.
Em 1988, a OMS lançou a Iniciativa Global de Erradicação da Pólio com o objetivo de erradicar a pólio em todo o mundo por meio da imunização. Esse objetivo agora está perto de ser realizado. Atualmente, a pólio é endêmica em apenas alguns países, incluindo Afeganistão, Paquistão e Nigéria, onde os esforços de vacinação foram interrompidos por conflitos militares ou instabilidade política.

O terror da poliomielite
Nos anos após a Segunda Guerra Mundial, os Estados Unidos e a União Soviética entraram em um período conhecido como Guerra Fria. Embora não tenha havido conflito armado, as duas superpotências estavam diplomática e economicamente isoladas uma da outra, representadas pela chamada Cortina de Ferro entre a União Soviética e o resto do mundo. Depois de 1950, migrar ou viajar para fora da União Soviética foi extremamente difícil e foi igualmente difícil para estrangeiros entrarem na União Soviética. Os Estados Unidos também impuseram limites estritos à entrada de soviéticos no país. Durante o governo Eisenhower, apenas 20 estudantes de pós-graduação da União Soviética podiam estudar nos Estados Unidos por ano.
No entanto, até mesmo a Cortina de Ferro não era páreo para a pólio. A vacina Salk tornou-se amplamente disponível no Ocidente em 1955 e, quando a vacina Sabin estava pronta para testes clínicos, a maioria da população suscetível nos Estados Unidos e no Canadá já havia sido vacinada contra a poliomielite. Sabin precisava procurar outros participantes do estudo. No auge da Guerra Fria, Mikhail Chumakov foi autorizado a vir aos Estados Unidos para estudar o trabalho de Sabin. Da mesma forma, Sabin, um microbiologista americano, foi autorizado a viajar para a União Soviética para iniciar os testes clínicos. Chumakov organizou a produção soviética e gerenciou os testes experimentais para testar a nova vacina na União Soviética. Em 1959, mais de dez milhões de crianças soviéticas haviam sido tratadas com segurança com a vacina de Sabin.
Como resultado de uma campanha global de vacinação com a vacina Sabin, a incidência geral da poliomielite caiu drasticamente. Hoje, a pólio quase foi eliminada em todo o mundo e raramente é vista nos Estados Unidos. Talvez um dia em breve, a pólio se torne a terceira doença microbiana a ser erradicada da população em geral [a varíola e a peste bovina (a causa da peste bovina) são as duas primeiras].
Exercício\(\PageIndex{5}\)
- Como o poliovírus é transmitido?
- Compare os prós e os contras de cada uma das duas vacinas contra a poliomielite.
Encefalopatias espongiformes transmissíveis
Agentes infecciosos acelulares chamados príons são responsáveis por um grupo de doenças relacionadas conhecidas como encefalopatias espongiformes transmissíveis (TSEs) que ocorrem em humanos e outros animais (veja Viróides, Virusóides e Príons). Todas as TSEs são doenças neurológicas degenerativas e fatais que ocorrem quando o tecido cerebral é infectado por príons. Essas doenças têm um início lento; os sintomas podem não se tornar aparentes até depois de um período de incubação de anos e talvez décadas, mas a morte geralmente ocorre dentro de meses a alguns anos após o aparecimento dos primeiros sintomas.
As EET em animais incluem o tremor epizoótico, uma doença em ovinos que é conhecida desde 1700, e a doença debilitante crônica, uma doença de veados e alces nos Estados Unidos e Canadá. A doença da vaca louca é observada em bovinos e pode ser transmitida aos humanos por meio do consumo de tecidos nervosos infectados. As doenças priônicas humanas incluem a doença de Creutzfeldt-Jakob e o kuru, uma doença rara endêmica da Papua Nova Guiné.
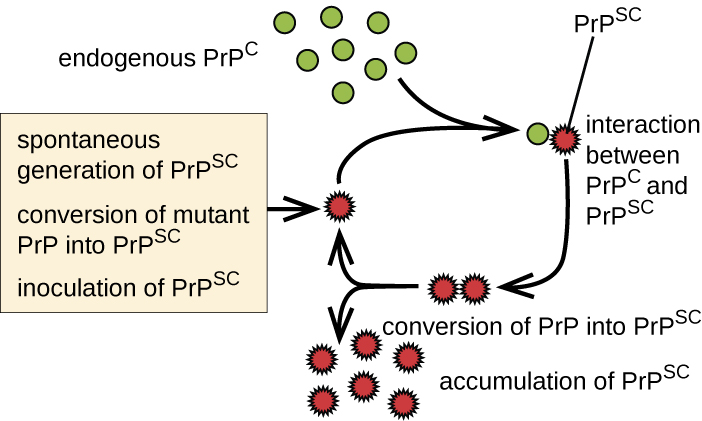
Os príons são partículas proteináceas infecciosas que não são vírus e não contêm ácido nucléico. Eles geralmente são transmitidos pela exposição e ingestão de tecidos infectados do sistema nervoso, transplantes de tecidos, transfusões de sangue ou fômites contaminados. As proteínas priônicas são normalmente encontradas em um tecido cerebral saudável em uma forma chamada PrP C. No entanto, se essa proteína for mal dobrada em uma forma desnaturada (PrP Sc), ela pode causar doenças. Embora a função exata do PrP C não seja compreendida atualmente, a proteína se dobra principalmente em hélices alfa e se liga ao cobre. A proteína nociva, por outro lado, se dobra predominantemente em folhas beta-plissadas e é resistente à proteólise. Além disso, o PrP Sc pode induzir o PrP C a ficar mal dobrado e produzir mais proteína nociva (Figura\(\PageIndex{6}\)).
À medida que o PrP Sc se acumula, ele se agrega e forma fibrilas dentro das células nervosas. Esses complexos proteicos acabam fazendo com que as células morram. Como consequência, os tecidos cerebrais de indivíduos infectados formam massas de emaranhados neurofibrilares e placas amiloides que dão ao cérebro uma aparência esponjosa, razão pela qual essas doenças são chamadas de encefalopatia espongiforme (Figura 6.4.3). Danos no tecido cerebral resultam em uma variedade de sintomas neurológicos. Mais comumente, os indivíduos afetados sofrem de perda de memória, alterações de personalidade, visão turva, movimentos descoordenados e insônia. Esses sintomas pioram gradualmente com o tempo e culminam em coma e morte.
O padrão-ouro para o diagnóstico de TSE é o exame histológico de biópsias cerebrais para detectar a presença de placas amiloides características, vacúolos e proteínas priônicas. Muito cuidado deve ser tomado pelos médicos ao manusear materiais suspeitos de infecção por priões para evitar que eles mesmos sejam infectados. Outros ensaios teciduais buscam a presença da proteína 14-3-3, um marcador para doenças do príon, como a doença de Creutzfeldt-Jakob. Novos ensaios, como o RT-Quic (conversão induzida por tremores em tempo real), oferecem uma nova esperança de detectar com eficácia as proteínas priônicas anormais nos tecidos mais cedo no curso da infecção. As doenças priônicas não podem ser curadas. No entanto, alguns medicamentos podem ajudar a retardar seu progresso. O suporte médico é focado em manter os pacientes o mais confortáveis possível, apesar dos sintomas progressivos e debilitantes.
Como os materiais contaminados com príons são fontes potenciais de infecção para médicos e cientistas clínicos, tanto a Organização Mundial da Saúde quanto o CDC fornecem informações para informar, educar e minimizar o risco de infecções causadas por príons.
Exercício\(\PageIndex{6}\)
- Os príons se reproduzem no sentido convencional?
- Qual é a conexão entre príons e a remoção de subprodutos animais da alimentação de animais de fazenda?
Infecções acelulares do sistema nervoso
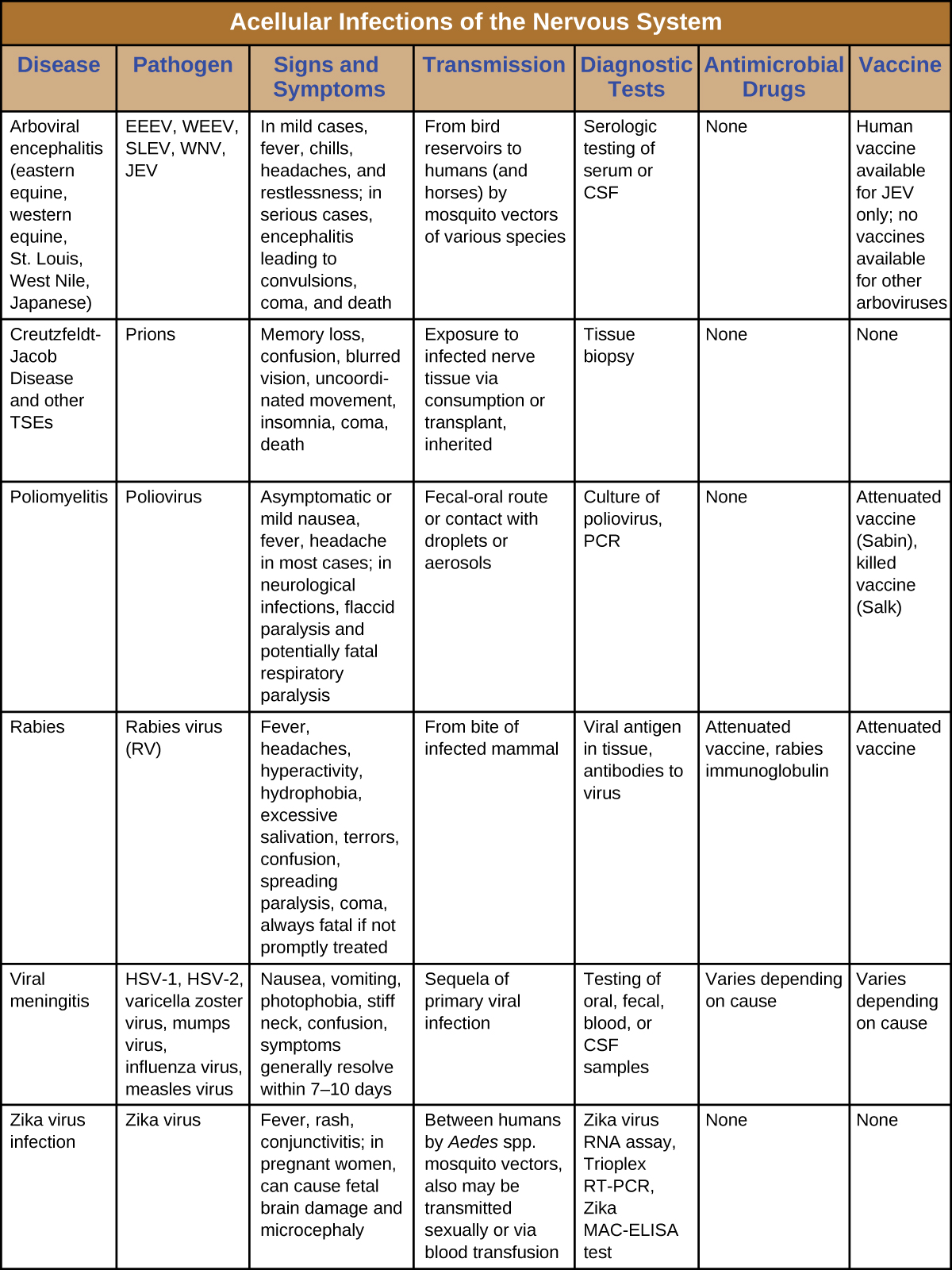
Consequências graves são o fio condutor comum entre essas doenças neurológicas. Vários causam paralisia debilitante, e alguns, como a doença de Creutzfeldt-Jakob e a raiva, são sempre ou quase sempre fatais. Como poucos medicamentos estão disponíveis para combater essas infecções, o controle vetorial e a vacinação são fundamentais para a prevenção e contenção. A figura\(\PageIndex{7}\) resume algumas infecções virais e priônicas importantes do sistema nervoso.
Conceitos principais e resumo
- A meningite viral é mais comum e geralmente menos grave do que a meningite bacteriana. Pode resultar de sequelas secundárias de muitos vírus ou ser causada por infecções de arbovírus.
- Vários tipos de encefalite arboviral estão concentrados em localizações geográficas específicas em todo o mundo. Essas infecções virais do sistema nervoso transmitidas por mosquitos geralmente são leves, mas podem ser fatais em alguns casos.
- O vírus Zika é uma infecção arboviral emergente com sintomas geralmente leves na maioria dos indivíduos, mas infecções de mulheres grávidas podem causar a microcefalia do defeito congênito.
- A poliomielite geralmente é uma infecção intestinal leve, mas pode ser prejudicial ou fatal se evoluir para uma doença neurológica.
- A raiva quase sempre é fatal quando não tratada e continua sendo um problema significativo em todo o mundo.
- As encefalopatias espongiformes transmissíveis, como a doença de Creutzfeldt-Jakob e o kuru, são causadas por príons. Essas doenças são intratáveis e, em última análise, fatais. Doenças priônicas similares são encontradas em animais.
Notas de pé
- 1 Centros dos EUA para Controle e Prevenção de Doenças, “Casos e mortes do vírus da encefalite equina oriental relatados ao CDC por ano e apresentação clínica, 2004—2013”, 2014. www.CDC.gov/Easternequineence... _2004-2013.pdf.
- 2 Centros de Controle e Prevenção de Doenças dos EUA, “Eastern Equine Encephalitis, Symptoms & Treatment, 2016”, acessado em 29 de junho de 2016. https://www.cdc.gov/easternequineenc... /symptoms.html.
- 3 Centros dos EUA para Controle e Prevenção de Doenças, “Western Equine Encephalitis—United States and Canada, 1987”, Morbidity and Mortality Weekly Report 36, nº 39 (1987): 655.
- 4 Centros de Controle e Prevenção de Doenças dos EUA, “Saint Louis encephalitis, Epidemiology & Geographic Distribution”, acessado em 30 de junho de 2016. http://www.cdc.gov/sle/technical/epi.html.
- 5 Centros de Controle e Prevenção de Doenças dos EUA, “Encefalite, Sintomas e Tratamento de Saint Louis”, acessado em 30 de junho de 2016. http://www.cdc.gov/sle/technical/symptoms.html.
- 6 Centros de Controle e Prevenção de Doenças dos EUA, “Encefalite Japonesa, Sintomas e Tratamento”, acessado em 30 de junho de 2016. www.cdc.gov/japaneseencephali... oms/index.html.
- 7 Sikka, Veronica, Vijay Kumar Chattu, Raaj K. Popli, Sagar C. Galwankar, Dhanashree Kelkar, Stanley G. Sawicki, Stanislaw P. Stawicki e Thomas J. Papadimos, “O surgimento do vírus Zika como uma ameaça à segurança sanitária global: uma revisão e uma declaração de consenso do Grupo de Trabalho Conjunto INDUSEM (JWG),” Jornal de Doenças Infecciosas Globais 8, nº 1 (2016): 3.
- 8 Mlakar, Jernej, Misa Korva, Nataša Tul, Mara Popović, Mateja Poljšak-Prijatelj, Jerica Mraz, Marko Kolenc et al., “Vírus Zika associado à microcefalia”, New England Journal of Medicine 374, nº 10 (2016): 951-8.
- 9 Centros dos EUA para Controle e Prevenção de Doenças, “Raiva, Animais Selvagens”, 2016. Acessado em 13 de setembro de 2016. www.cdc.gov/rabies/location/u... d_animals.html.
- 10 Slate, Dennis, Charles E. Rupprecht, Jane A. Rooney, Dennis Donovan, Donald H. Lein e Richard B. Chipman, “Status da vacinação oral contra a raiva em carnívoros selvagens nos Estados Unidos”, Virus Research 111, nº 1 (2005): 68-76.
- 11 Finnegan, Christopher J., Sharon M. Brookes, Nicholas Johnson, Jemma Smith, Karen L. Mansfield, Victoria L. Keene, Lorraine M. McElhinney e Anthony R. Fooks, “Raiva na América do Norte e na Europa”, Journal of the Royal Society of Medicine 95, nº 1 (2002): 9-13. www.ncbi.nlm.nih.gov/pmc/articles/PMC1279140/.
- 12 Centros de Controle e Prevenção de Doenças dos EUA, “Saúde Global — Polio”, 2014. Acessado em 30 de junho de 2016. http://www.cdc.gov/polio/about/index.htm.
- 13 Centros de Controle e Prevenção de Doenças dos EUA, “Saúde Global — Polio”, 2014. Acessado em 30 de junho de 2016. http://www.cdc.gov/polio/about/index.htm.


