8.3: Respiração celular
- Page ID
- 181442
Objetivos de
- Compare e contraste a localização e a função do sistema de transporte de elétrons em uma célula procariótica e uma célula eucariótica
- Compare e contraste as diferenças entre o nível do substrato e a fosforilação oxidativa
- Explicar a relação entre quimiosmose e força motriz de prótons
- Descreva a função e a localização da ATP sintase em uma célula procariótica versus eucariótica
- Compare e contraste a respiração aeróbica e anaeróbica
Acabamos de discutir duas vias no catabolismo da glicose - a glicólise e o ciclo de Krebs - que geram ATP por fosforilação em nível de substrato. A maior parte do ATP, no entanto, é gerada durante um processo separado chamado fosforilação oxidativa, que ocorre durante a respiração celular. A respiração celular começa quando os elétrons são transferidos do NADH e do FADH 2 - feitos na glicólise, na reação de transição e no ciclo de Krebs - por meio de uma série de reações químicas para um aceitador de elétrons inorgânicos final (oxigênio na respiração aeróbica ou moléculas inorgânicas não oxigênio em respiração anaeróbica). Essas transferências de elétrons ocorrem na parte interna da membrana celular das células procarióticas ou em complexos proteicos especializados na membrana interna das mitocôndrias das células eucarióticas. A energia dos elétrons é coletada para gerar um gradiente eletroquímico através da membrana, que é usado para produzir ATP por fosforilação oxidativa.
Sistema de transporte de elétrons
O sistema de transporte de elétrons (ETS) é o último componente envolvido no processo de respiração celular; compreende uma série de complexos proteicos associados à membrana e portadores de elétrons acessórios móveis associados. O transporte de elétrons é uma série de reações químicas que se assemelha a uma brigada de caçamba, pois os elétrons do NADH e do FADH 2 são passados rapidamente de um transportador de elétrons ETS para o próximo. Esses portadores podem transmitir elétrons no ETS por causa de seu potencial redox. Para que uma proteína ou substância química aceite elétrons, ela deve ter um potencial redox mais positivo do que o doador de elétrons. Portanto, os elétrons se movem de portadores de elétrons com mais potencial redox negativo para aqueles com mais potencial redox positivo. As quatro principais classes de transportadores de elétrons envolvidos nos sistemas de transporte de elétrons eucarióticos e procarióticos são os citocromos, as flavoproteínas, as proteínas ferro-enxofre e as quinonas.
Na respiração aeróbica, o aceitador final de elétrons (ou seja, aquele com o potencial redox mais positivo) no final do ETS é uma molécula de oxigênio (O 2) que é reduzida a água (H 2 O) pelo transportador final de ETS. Esse transportador de elétrons, a citocromo oxidase, difere entre os tipos bacterianos e pode ser usado para diferenciar bactérias estreitamente relacionadas para diagnósticos. Por exemplo, o oportunista gram-negativo Pseudomonas aeruginosa e o Vibrio cholerae, causador de cólera gram-negativa, usam a citocromo c oxidase, que pode ser detectada pelo teste da oxidase, enquanto outras Enterobacteriaceae gram-negativas, como E. coli, são negativas para isso teste porque eles produzem diferentes tipos de citocromo oxidase.
Há muitas circunstâncias em que a respiração aeróbica não é possível, incluindo qualquer uma ou mais das seguintes:
- A célula carece de genes que codificam uma citocromo oxidase apropriada para transferir elétrons para o oxigênio no final do sistema de transporte de elétrons.
- A célula não possui genes que codificam enzimas para minimizar os efeitos severamente prejudiciais dos perigosos radicais de oxigênio produzidos durante a respiração aeróbica, como peróxido de hidrogênio (H 2 O 2) ou superóxido\((\ce{O2-})\).
- A célula não tem uma quantidade suficiente de oxigênio para realizar a respiração aeróbica.
Uma alternativa possível à respiração aeróbica é a respiração anaeróbica, usando uma molécula inorgânica diferente do oxigênio como aceitador final de elétrons. Existem muitos tipos de respiração anaeróbica encontrados em bactérias e arquéias. Os desnitrificadores são importantes bactérias do solo que usam nitrato\((\ce{NO3-})\) e nitrito\((\ce{NO2-})\) como aceitadores finais de elétrons, produzindo gás nitrogênio (N 2). Muitas bactérias que respiram aerobicamente, incluindo E. coli, passam a usar nitrato como aceitador final de elétrons e a produzir nitrito quando os níveis de oxigênio estão esgotados.
Os micróbios que usam respiração anaeróbica geralmente têm um ciclo de Krebs intacto, então esses organismos podem acessar a energia das moléculas de NADH e FADH 2 formadas. No entanto, os respiradores anaeróbicos usam portadores de ETS alterados codificados por seus genomas, incluindo complexos distintos para transferência de elétrons para seus aceitadores de elétrons finais. Gradientes eletroquímicos menores são gerados a partir desses sistemas de transferência de elétrons, portanto, menos ATP é formado por meio da respiração anaeróbica.
Exercício\(\PageIndex{1}\)
Tanto a respiração aeróbica quanto a respiração anaeróbica usam uma cadeia de transporte de elétrons?
Quimiosmose, força motriz de prótons e fosforilação oxidativa
Em cada transferência de um elétron através do ETS, o elétron perde energia, mas com algumas transferências, a energia é armazenada como energia potencial usando-a para bombear íons de hidrogênio (H +) através de uma membrana. Nas células procarióticas, o H+ é bombeado para o exterior da membrana citoplasmática (chamado espaço periplasmático em bactérias gram-negativas e gram-positivas) e, nas células eucarióticas, elas são bombeadas da matriz mitocondrial através da membrana mitocondrial interna para o espaço intermembranar. Há uma distribuição desigual de H + através da membrana que estabelece um gradiente eletroquímico porque os íons H + são carregados positivamente (elétricos) e há uma maior concentração (química) em um lado da membrana. Esse gradiente eletroquímico formado pelo acúmulo de H + (também conhecido como próton) em um lado da membrana em comparação com o outro é chamado de força motriz do próton (PMF). Como os íons envolvidos são H +, um gradiente de pH também é estabelecido, com o lado da membrana com a maior concentração de H + sendo mais ácido. Além do uso do PMF para produzir ATP, conforme discutido neste capítulo, o PMF também pode ser usado para conduzir outros processos energeticamente desfavoráveis, incluindo transporte de nutrientes e rotação de flagelos para motilidade.
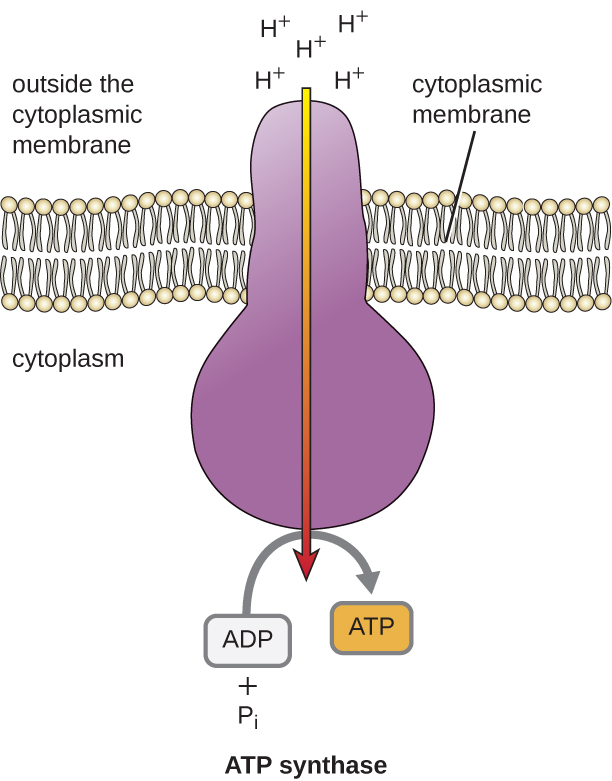
A energia potencial desse gradiente eletroquímico gerado pelo ETS faz com que o H+ se difunda por uma membrana (a membrana plasmática nas células procarióticas e a membrana interna nas mitocôndrias nas células eucarióticas). Esse fluxo de íons de hidrogênio através da membrana, chamado quimiosmose, deve ocorrer por meio de um canal na membrana por meio de um complexo enzimático ligado à membrana chamado ATP sintase (Figura\(\PageIndex{1}\)). A tendência de movimento dessa maneira é muito parecida com a água acumulada em um lado de uma barragem, movendo-se pela barragem quando aberta. A ATP sintase (como uma combinação da ingestão e do gerador de uma barragem hidrelétrica) é uma proteína complexa que atua como um pequeno gerador, girando pela força do H + que se difunde através da enzima, descendo seu gradiente eletroquímico de onde existem muitos H + que se repelem mutuamente para onde há menos H +. Nas células procarióticas, o H+ flui do exterior da membrana citoplasmática para o citoplasma, enquanto nas mitocôndrias eucarióticas, o H+ flui do espaço intermembranar para a matriz mitocondrial. O torneamento das partes dessa máquina molecular regenera o ATP do ADP e do fosfato inorgânico (P i) por fosforilação oxidativa, um segundo mecanismo para produzir ATP que coleta a energia potencial armazenada em um gradiente eletroquímico.
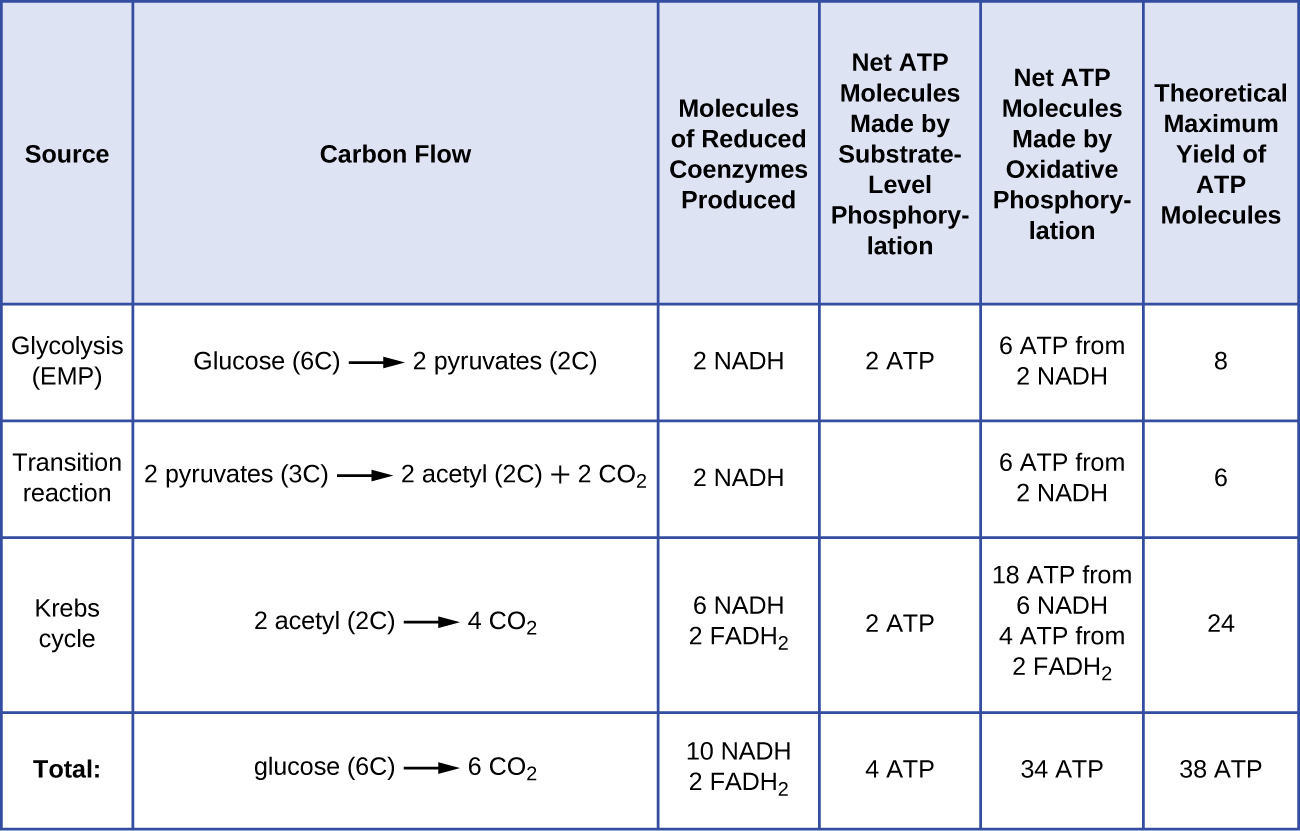
O número de moléculas de ATP geradas pelo catabolismo da glicose varia. Por exemplo, o número de íons de hidrogênio que os complexos do sistema de transporte de elétrons podem bombear através da membrana varia entre diferentes espécies de organismos. Na respiração aeróbica nas mitocôndrias, a passagem de elétrons de uma molécula de NADH gera força motriz de prótons suficiente para produzir três moléculas de ATP por fosforilação oxidativa, enquanto a passagem de elétrons de uma molécula de FADH 2 gera força motriz de prótons suficiente para fazer apenas duas Moléculas de ATP. Assim, as 10 moléculas de NADH produzidas por glicose durante a glicólise, a reação de transição e o ciclo de Krebs carregam energia suficiente para produzir 30 moléculas de ATP, enquanto as duas moléculas de FADH 2 produzidas por glicose durante esses processos fornecem energia suficiente para produzir quatro moléculas de ATP. No geral, o rendimento máximo teórico de ATP obtido durante a respiração aeróbica completa da glicose é de 38 moléculas, com quatro sendo produzidas por fosforilação em nível de substrato e 34 sendo produzidas por fosforilação oxidativa (Figura\(\PageIndex{2}\)). Na realidade, o rendimento total de ATP geralmente é menor, variando de uma a 34 moléculas de ATP, dependendo se a célula está usando respiração aeróbica ou respiração anaeróbica; nas células eucarióticas, alguma energia é gasta para transportar intermediários do citoplasma para as mitocôndrias, afetando a produção de ATP.
A figura\(\PageIndex{2}\) resume os rendimentos máximos teóricos de ATP de vários processos durante a respiração aeróbica completa de uma molécula de glicose.
Exercício\(\PageIndex{1}\)
Quais são as funções da força motriz do próton?
Resumo
- A maior parte do ATP gerado durante a respiração celular da glicose é produzida por fosforilação oxidativa.
- Um sistema de transporte de elétrons (ETS) é composto por uma série de complexos proteicos associados à membrana e portadores de elétrons acessórios móveis associados. O ETS está incorporado na membrana citoplasmática dos procariontes e na membrana mitocondrial interna dos eucariotos.
- Cada complexo ETS tem um potencial redox diferente, e os elétrons se movem de portadores de elétrons com mais potencial redox negativo para aqueles com potencial redox mais positivo.
- Para realizar a respiração aeróbica, uma célula precisa de oxigênio como aceitador final de elétrons. Uma célula também precisa de um ciclo completo de Krebs, uma citocromo oxidase apropriada e enzimas de desintoxicação de oxigênio para evitar os efeitos nocivos dos radicais de oxigênio produzidos durante a respiração aeróbica.
- Organismos que realizam respiração anaeróbica usam transportadores alternativos do sistema de transporte de elétrons para a transferência final de elétrons para os aceitadores finais de elétrons não oxigênio.
- Os micróbios apresentam uma grande variação na composição de seus sistemas de transporte de elétrons, que podem ser usados para fins de diagnóstico para ajudar a identificar certos patógenos.
- À medida que os elétrons passam do NADH e do FADH 2 por um ETS, o elétron perde energia. Essa energia é armazenada por meio do bombeamento de H + através da membrana, gerando uma força motriz de prótons.
- A energia dessa força motriz do próton pode ser aproveitada permitindo que os íons de hidrogênio se difundam de volta pela membrana por quimiosmose usando a ATP sintase. À medida que os íons de hidrogênio se difundem através de seu gradiente eletroquímico, os componentes da ATP sintase giram, produzindo ATP do ADP e P i por fosforilação oxidativa.
- A respiração aeróbica forma mais ATP (um máximo de 34 moléculas de ATP) durante a fosforilação oxidativa do que a respiração anaeróbica (entre uma e 32 moléculas de ATP).


