28.2 : Développement embryonnaire
- Page ID
- 194936
Objectifs d'apprentissage
- Distinguer les étapes du développement embryonnaire qui se produisent avant l'implantation
- Décrire le processus d'implantation
- Énumérer et décrire quatre membranes embryonnaires
- Expliquer la gastrulation
- Décrire comment se forme le placenta et identifier ses fonctions
- Expliquer comment un embryon passe d'un disque de cellules plat à une forme tridimensionnelle ressemblant à celle d'un être humain
- Résumez le processus d'organogenèse
Tout au long de ce chapitre, nous exprimerons l'âge embryonnaire et foetal en termes de semaines à compter de la fécondation, communément appelée conception. La période requise pour le développement complet du fœtus in utero est appelée gestation (gestare = « porter » ou « porter »). Elle peut être subdivisée en périodes gestationnelles distinctes. Les deux premières semaines du développement prénatal sont appelées stade préembryonnaire. Un être humain en développement est considéré comme un embryon pendant les semaines 3 à 8, et un fœtus de la neuvième semaine de gestation jusqu'à la naissance. Dans cette section, nous aborderons les stades de développement préembryonnaire et embryonnaire, caractérisés par la division cellulaire, la migration et la différenciation. À la fin de la période embryonnaire, tous les systèmes organiques sont structurés sous une forme rudimentaire, bien que les organes eux-mêmes soient soit non fonctionnels, soit seulement semi-fonctionnels.
Développement embryonnaire préimplantatoire
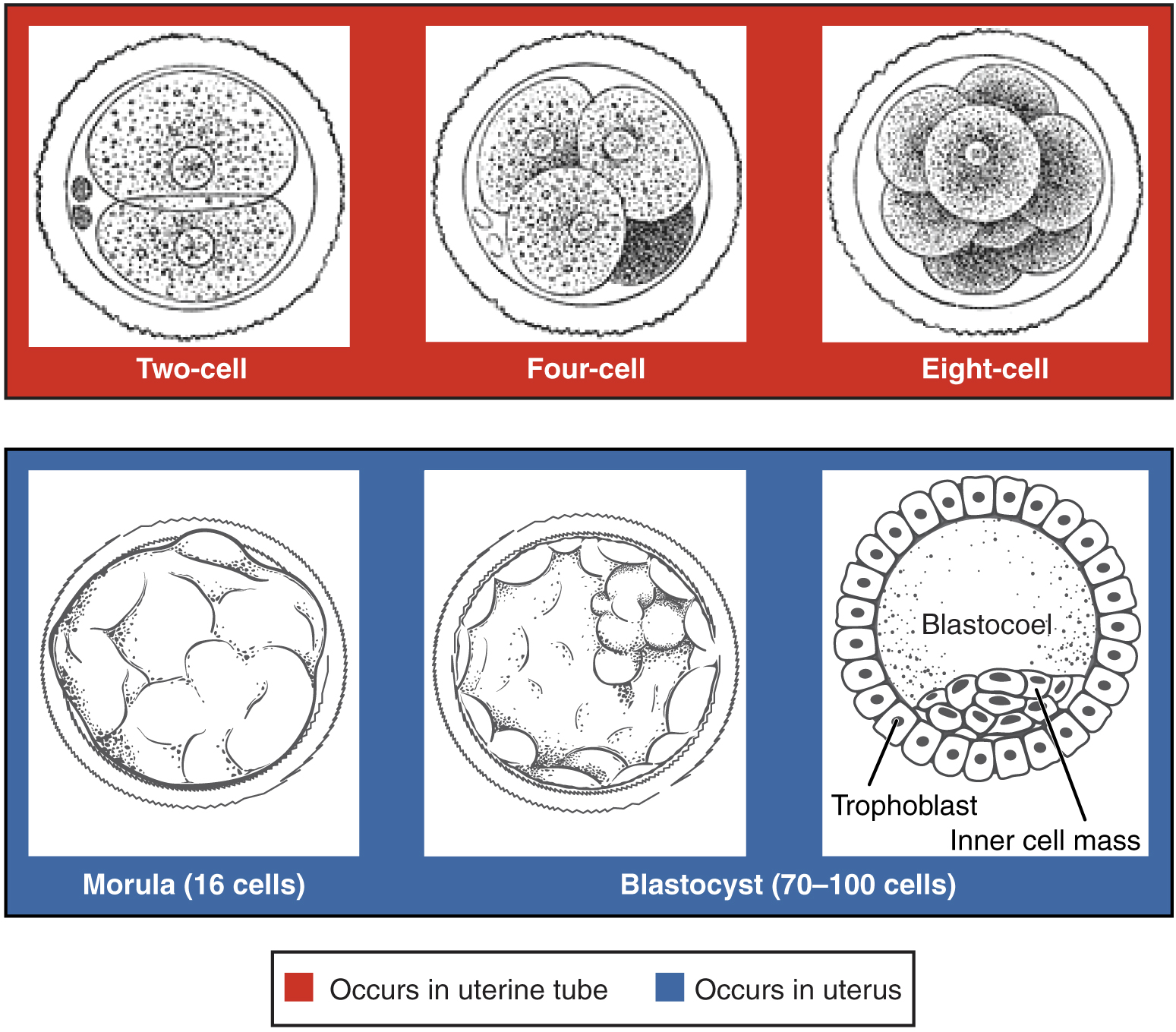
Après la fécondation, le zygote et ses membranes associées, appelées ensemble conceptus, continuent d'être projetés vers l'utérus par le péristaltisme et les battements des cils. Au cours de son trajet vers l'utérus, le zygote subit cinq ou six divisions cellulaires mitotiques rapides. Bien que chaque clivage entraîne la formation d'un plus grand nombre de cellules, il n'augmente pas le volume total du conceptus (Figure\(\PageIndex{1}\)). Chaque cellule fille produite par le clivage est appelée blastomère (blastos = « germe », au sens d'une graine ou d'une pousse).
Environ 3 jours après la fécondation, un conceptus à 16 cellules atteint l'utérus. Les cellules qui avaient été regroupées de manière lâche sont maintenant compactées et ressemblent davantage à une masse solide. Le nom donné à cette structure est la morula (morula = « petit mûrier »). Une fois à l'intérieur de l'utérus, le conceptus flotte librement pendant plusieurs jours. Il continue de se diviser, créant une boule d'environ 100 cellules et consommant des sécrétions endométriales nutritives appelées lait utérin pendant que la muqueuse utérine s'épaissit. La boule de cellules désormais étroitement liées commence à sécréter du liquide et à s'organiser autour d'une cavité remplie de liquide, le blastocoel. À ce stade de développement, le conceptus est appelé blastocyste. Au sein de cette structure, un groupe de cellules forme une masse cellulaire interne qui est destinée à devenir l'embryon. Les cellules qui forment l'enveloppe externe sont appelées trophoblastes (trophe = « nourrir » ou « nourrir »). Ces cellules se développeront dans le sac chorionique et dans la partie fœtale du placenta (organe d'échange de nutriments, de déchets et de gaz entre la mère et la progéniture en développement).
La masse interne des cellules embryonnaires est totipotente à ce stade, ce qui signifie que chaque cellule a le potentiel de se différencier en n'importe quel type de cellule du corps humain. La totipotence ne dure que quelques jours avant que le destin des cellules ne soit défini comme étant les précurseurs d'une lignée cellulaire spécifique.
Regardez ce film en accéléré d'un conceptus dès le troisième jour. Quelle est la première structure que vous voyez ? À quel moment du film le blastocoel apparaît-il pour la première fois ? Quel événement se produit à la fin du film ?
Implantation
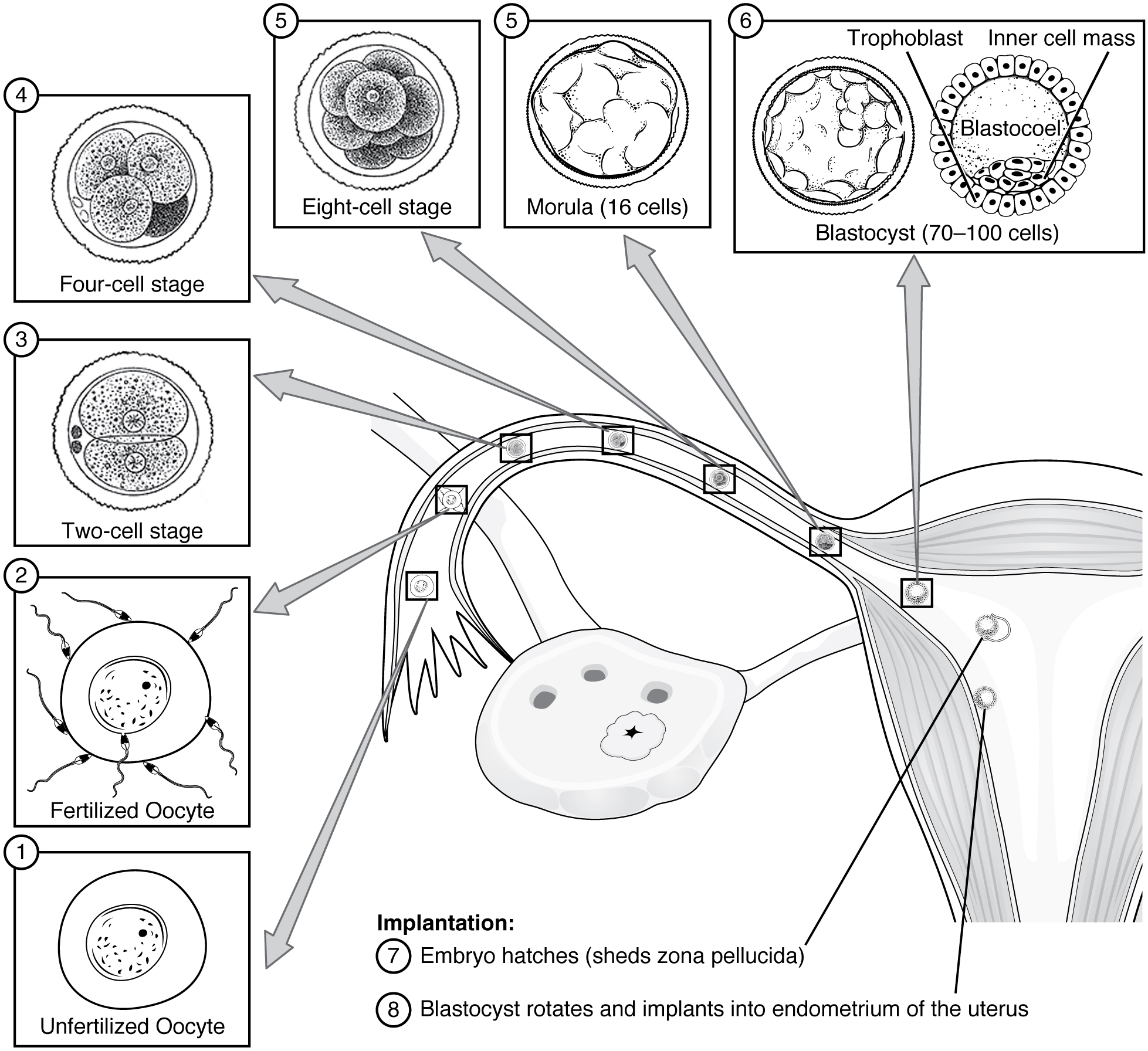
À la fin de la première semaine, le blastocyste entre en contact avec la paroi utérine et y adhère en s'intégrant dans la paroi utérine via les cellules trophoblastiques. Ainsi commence le processus d'implantation, qui marque la fin du stade de développement préembryonnaire (Figure\(\PageIndex{2}\)). L'implantation peut s'accompagner de saignements mineurs. Le blastocyste s'implante généralement dans le fond de l'utérus ou sur la paroi postérieure. Toutefois, si l'endomètre n'est pas complètement développé et prêt à recevoir le blastocyste, celui-ci se détachera et trouvera un meilleur endroit. Un pourcentage important (50 à 75 %) de blastocystes ne parviennent pas à s'implanter ; lorsque cela se produit, le blastocyste est éliminé avec l'endomètre pendant les règles. Le taux élevé d'échec de l'implantation est l'une des raisons pour lesquelles la grossesse nécessite généralement plusieurs cycles d'ovulation pour être réalisée.
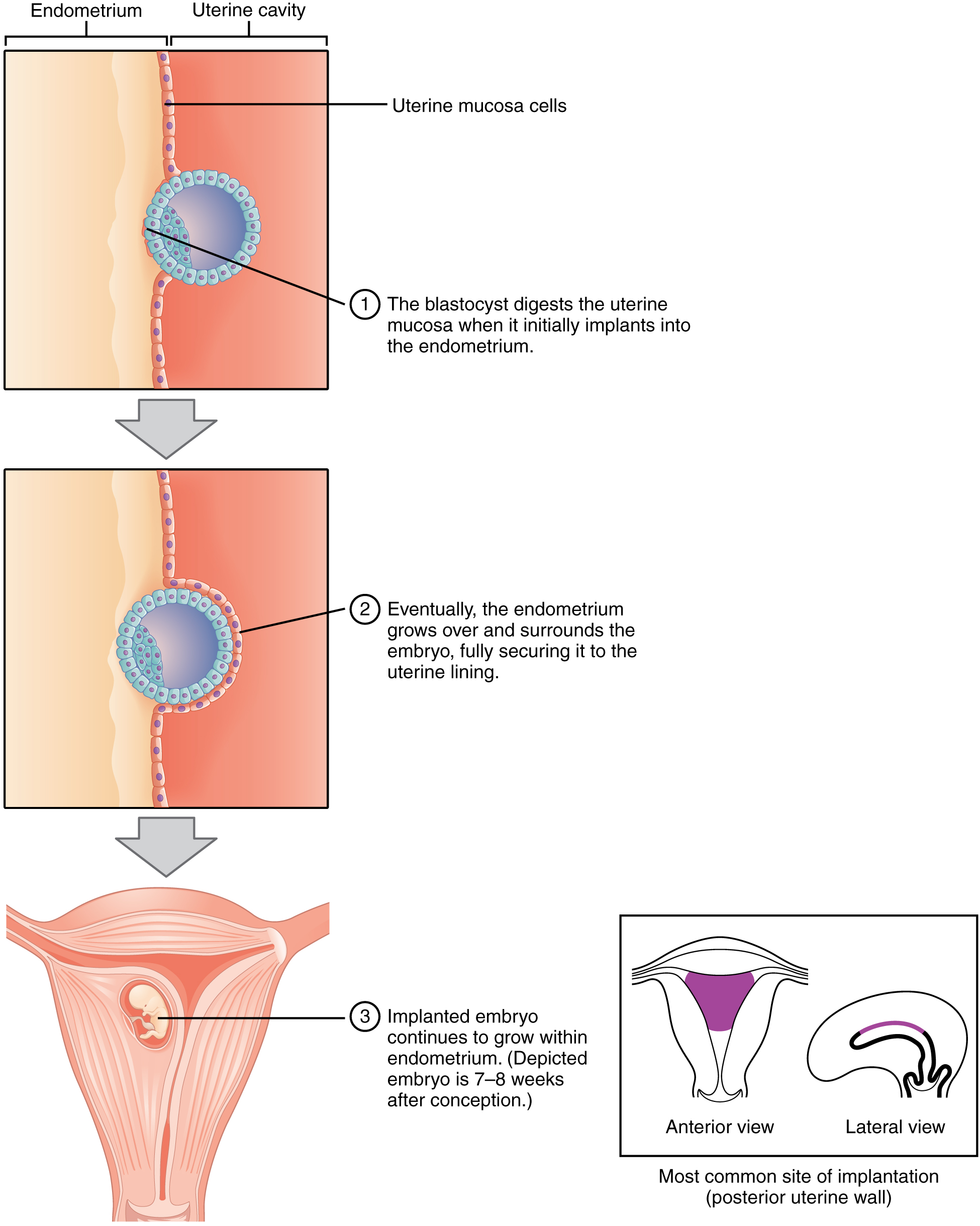
Lorsque l'implantation réussit et que le blastocyste adhère à l'endomètre, les cellules superficielles du trophoblaste fusionnent entre elles pour former le syncytiotrophoblaste, un corps multinucléé qui digère les cellules endométriales pour fixer fermement le blastocyste à la paroi utérine. En réponse, la muqueuse utérine se reconstruit et enveloppe le blastocyste (Figure\(\PageIndex{3}\)). Le trophoblaste sécrète de la gonadotrophine chorionique humaine (hCG), une hormone qui permet au corps jaune de survivre, de grossir et de continuer à produire de la progestérone et des œstrogènes pour supprimer les règles. Ces fonctions de l'hCG sont nécessaires pour créer un environnement adapté à l'embryon en développement. En raison de cette production accrue, l'hCG s'accumule dans le sang maternel et est excrétée dans les urines. L'implantation est terminée au milieu de la deuxième semaine. Quelques jours seulement après l'implantation, le trophoblaste a sécrété suffisamment d'hCG pour qu'un test de grossesse urinaire à domicile donne un résultat positif.
La plupart du temps, un embryon s'implante dans le corps de l'utérus à un endroit qui peut favoriser la croissance et le développement. Cependant, dans un à deux pour cent des cas, l'embryon s'implante soit à l'extérieur de l'utérus (grossesse extra-utérine), soit dans une région de l'utérus qui peut entraîner des complications pendant la grossesse. Si l'embryon s'implante dans la partie inférieure de l'utérus, le placenta peut potentiellement se développer au-dessus de l'ouverture du col de l'utérus, une affection appelée placenta praevia.
TROUBLES DE LA... Développement de l'embryon
Dans la grande majorité des grossesses extra-utérines, l'embryon ne termine pas son trajet jusqu'à l'utérus et s'implante dans le tube utérin, ce que l'on appelle une grossesse tubaire. Cependant, il existe également des grossesses extra-utérines ovariennes (dans lesquelles l'ovule n'a jamais quitté l'ovaire) et des grossesses extra-utérines abdominales (au cours desquelles un ovule a été « perdu » dans la cavité abdominale lors du transfert de l'ovaire au tube utérin, ou au cours desquelles un embryon issu d'une grossesse tubaire a été réimplanté dans l'abdomen). Une fois dans la cavité abdominale, un embryon peut s'implanter dans n'importe quelle structure bien vascularisée : la cavité recto-utérine (poche de Douglas), le mésentère des intestins et le grand épiploon sont des sites courants.
Les grossesses tubaires peuvent être causées par le tissu cicatriciel contenu dans le tube à la suite d'une infection bactérienne sexuellement transmissible. Le tissu cicatriciel empêche l'embryon de pénétrer dans l'utérus ; dans certains cas, il « accroche » l'embryon et, dans d'autres cas, bloque complètement le tube. Environ la moitié des grossesses tubaires disparaissent spontanément. L'implantation dans un tube utérin provoque des saignements qui semblent stimuler les contractions des muscles lisses et l'expulsion de l'embryon. Dans les autres cas, une intervention médicale ou chirurgicale est nécessaire. Si une grossesse extra-utérine est détectée tôt, le développement de l'embryon peut être arrêté par l'administration du méthotrexate, un médicament cytotoxique, qui inhibe le métabolisme de l'acide folique. Si le diagnostic est tardif et que le tube utérin est déjà rompu, une réparation chirurgicale est essentielle.
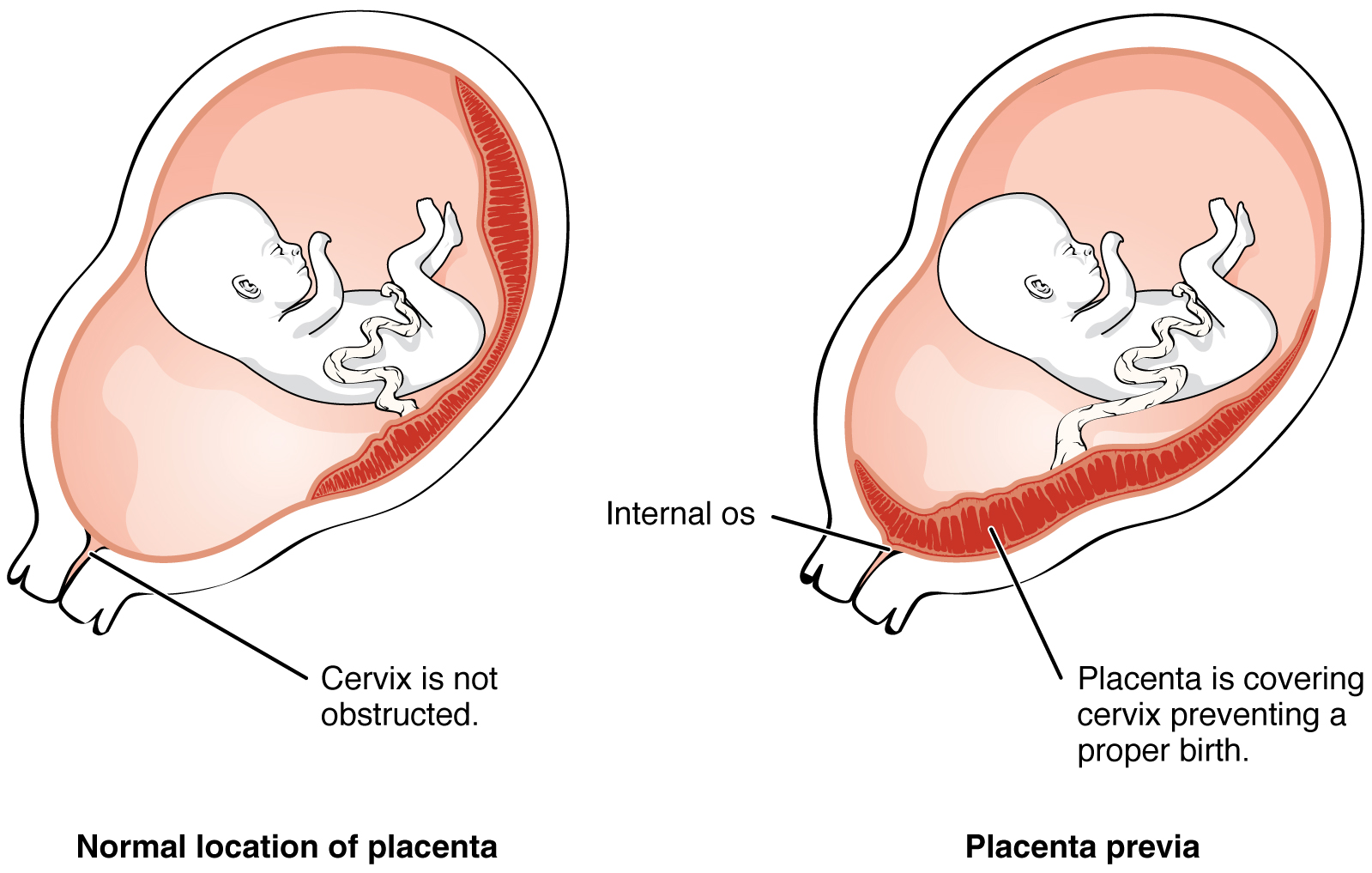
Figure\(\PageIndex{4}\) : Placenta Previa. Un embryon qui s'implante trop près de l'ouverture du col de l'utérus peut entraîner la formation du placenta praevia, une affection caractérisée par le fait que le placenta recouvre partiellement ou complètement le col de l'utérus.
Même si l'embryon parvient à se frayer un chemin jusqu'à l'utérus, il ne s'implante pas toujours à un endroit optimal (le fond d'œil ou la paroi postérieure de l'utérus). Le placenta praevia peut résulter de l'implantation d'un embryon à proximité de l'orifice interne de l'utérus (ouverture interne du col de l'utérus). À mesure que le fœtus grandit, le placenta peut recouvrir partiellement ou complètement l'ouverture du col de l'utérus (Figure\(\PageIndex{4}\)). Bien qu'il ne survienne que dans 0,5 % des grossesses, le placenta praevia est la principale cause d'hémorragie prénatale (saignements vaginaux abondants après la 24e semaine de grossesse mais avant l'accouchement).
Membranes embryonnaires
Au cours de la deuxième semaine de développement, lorsque l'embryon est implanté dans l'utérus, les cellules du blastocyste commencent à s'organiser en couches. Certaines se développent pour former les membranes extra-embryonnaires nécessaires au maintien et à la protection de l'embryon en croissance : l'amnios, le sac vitellin, l'allantois et le chorion.
Au début de la deuxième semaine, les cellules de la masse cellulaire interne forment un disque à deux couches de cellules embryonnaires, et un espace, la cavité amniotique, s'ouvre entre celui-ci et le trophoblaste (Figure\(\PageIndex{5}\)). Les cellules de la couche supérieure du disque (épiblaste) s'étendent autour de la cavité amniotique, créant un sac membraneux qui se transforme en amnios à la fin de la deuxième semaine. L'amnios se remplit de liquide amniotique et finit par se développer pour entourer l'embryon. Au début du développement, le liquide amniotique est presque entièrement constitué d'un filtrat de plasma maternel, mais lorsque les reins du fœtus commencent à fonctionner vers la huitième semaine, ils ajoutent de l'urine au volume de liquide amniotique. Flottant dans le liquide amniotique, l'embryon, et plus tard, le fœtus, est protégé contre les traumatismes et les changements rapides de température. Il peut se déplacer librement dans le liquide et se préparer à avaler et à respirer par l'utérus.
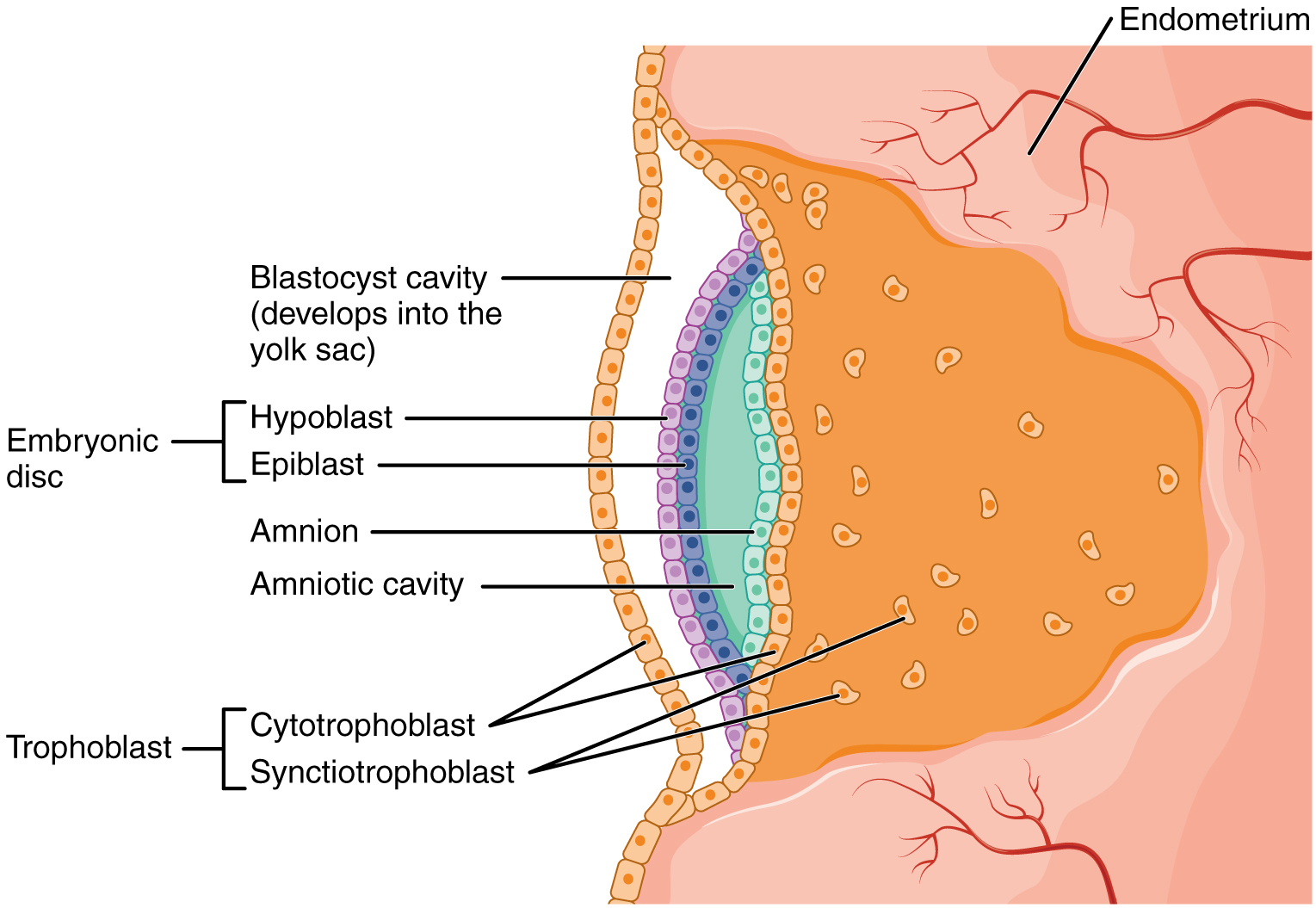
Sur la face ventrale du disque embryonnaire, opposée à l'amnios, les cellules de la couche inférieure du disque embryonnaire (l'hypoblaste) pénètrent dans la cavité du blastocyste et forment un sac vitellin. Le sac vitellin fournit certains nutriments absorbés par le trophoblaste et assure également la circulation sanguine primitive vers l'embryon en développement pendant la deuxième et la troisième semaine de développement. Lorsque le placenta prend le relais pour nourrir l'embryon vers la semaine 4, la taille du sac vitellin a été considérablement réduite et sa fonction principale est de servir de source de cellules sanguines et de cellules germinales (cellules qui donneront naissance aux gamètes). Au cours de la troisième semaine, le sac vitellin se forme en forme de doigt et se transforme en allantois, un canal excréteur primitif de l'embryon qui fera partie de la vessie. Ensemble, les tiges du sac vitellin et de l'allantois établissent la structure externe du cordon ombilical.
La dernière membrane extra-embryonnaire est le chorion, qui est la seule membrane qui entoure toutes les autres. Le développement du chorion sera discuté plus en détail sous peu, en ce qui concerne la croissance et le développement du placenta.
Embryogenèse
Au début de la troisième semaine de développement, le disque cellulaire à deux couches devient un disque à trois couches grâce au processus de gastrulation, au cours duquel les cellules passent de la totipotence à la multipotence. L'embryon, qui prend la forme d'un disque ovale, forme une indentation appelée strie primitive le long de la surface dorsale de l'épiblaste. Un nœud situé à l'extrémité caudale ou « queue » de la strie primitive émet des facteurs de croissance qui incitent les cellules à se multiplier et à migrer. Les cellules migrent vers et à travers la bande primitive, puis se déplacent latéralement pour créer deux nouvelles couches de cellules. La première couche est l'endoderme, une feuille de cellules qui déplace l'hypoblaste et se trouve à proximité du sac vitellin. La deuxième couche de cellules se remplit en tant que couche intermédiaire, ou mésoderme. Les cellules de l'épiblaste qui restent (n'ayant pas migré à travers la strie primitive) deviennent l'ectoderme (Figure\(\PageIndex{6}\)).
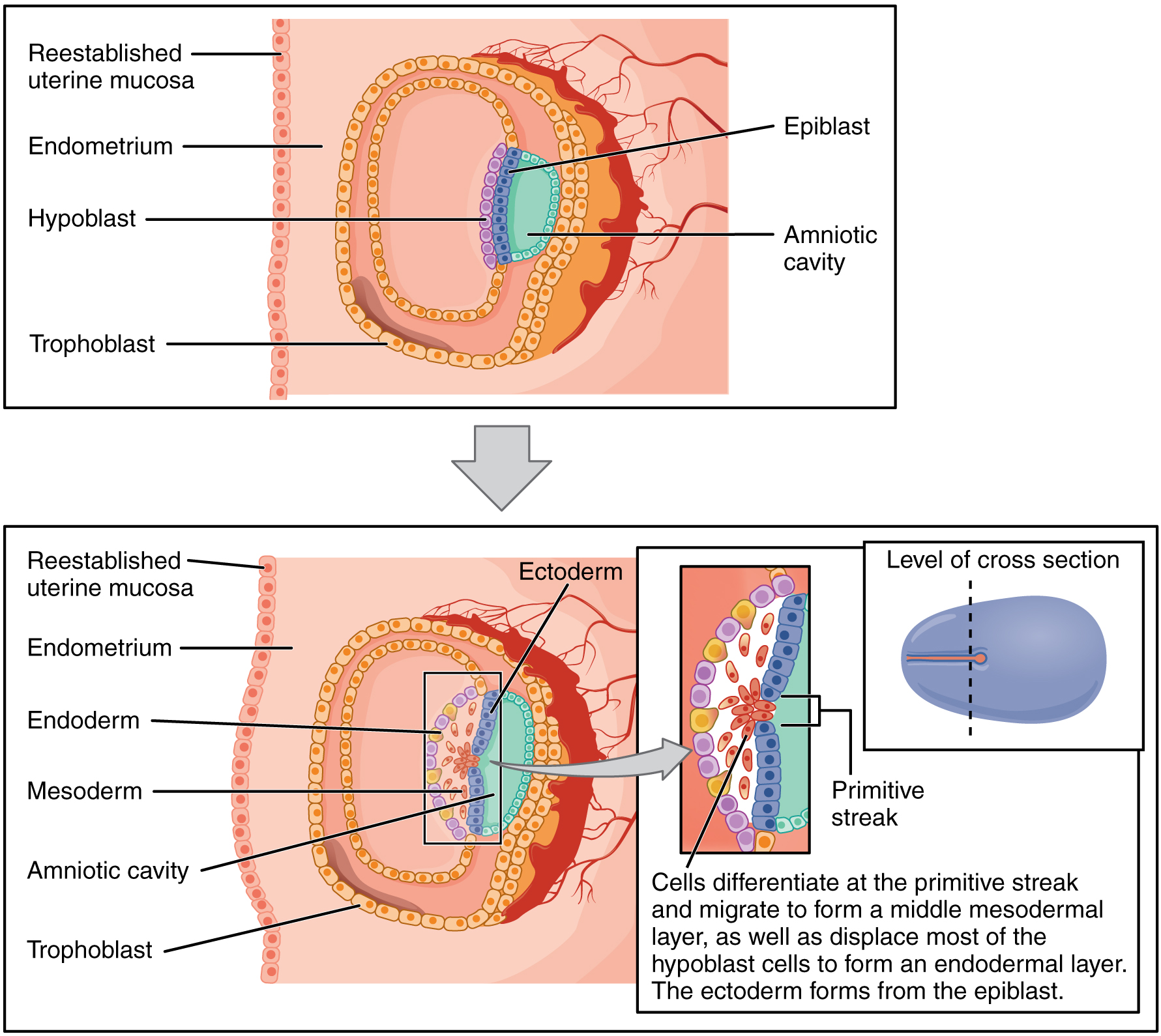
Chacune de ces couches germinales se transformera en structures spécifiques dans l'embryon. Alors que l'ectoderme et l'endoderme forment des couches épithéliales étroitement liées, les cellules mésodermiques sont moins organisées et existent sous la forme d'une communauté cellulaire faiblement connectée. L'ectoderme donne naissance à des lignées cellulaires qui se différencient pour former les systèmes nerveux central et périphérique, les organes sensoriels, l'épiderme, les cheveux et les ongles. Les cellules mésodermiques finissent par devenir le squelette, les muscles, le tissu conjonctif, le cœur, les vaisseaux sanguins et les reins. L'endoderme forme ensuite la paroi épithéliale du tractus gastro-intestinal, du foie et du pancréas, ainsi que des poumons (Figure\(\PageIndex{7}\)).
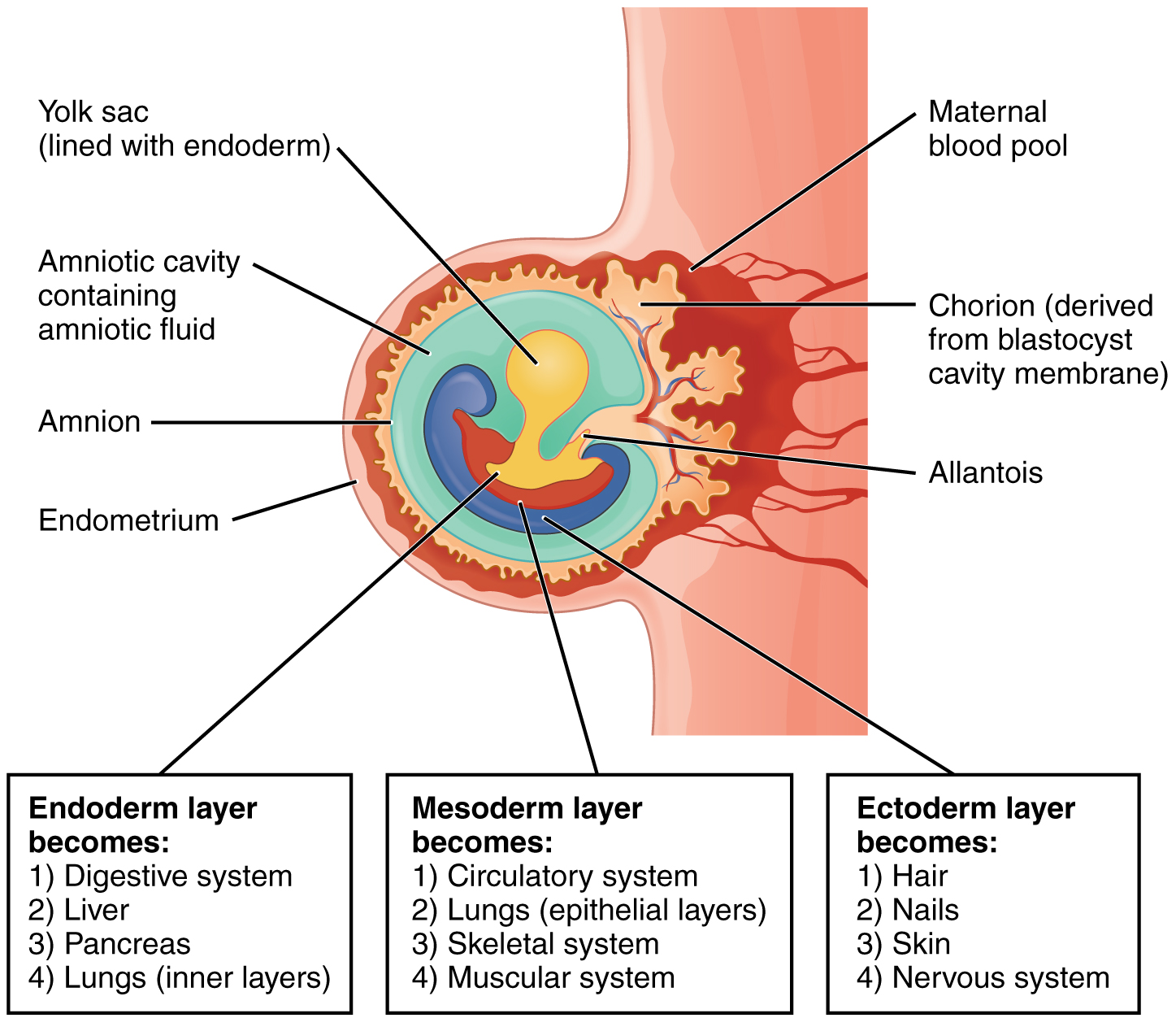
Développement du placenta
Au cours des premières semaines de développement, les cellules de l'endomètre, appelées cellules déciduales, nourrissent l'embryon naissant. Au cours des semaines prénatales 4 à 12, le placenta en développement assume progressivement le rôle d'alimentation de l'embryon, et les cellules déciduales ne sont plus nécessaires. Le placenta mature est composé de tissus dérivés de l'embryon, ainsi que de tissus maternels de l'endomètre. Le placenta est relié au conceptus par le cordon ombilical, qui transporte le sang désoxygéné et les déchets du fœtus par deux artères ombilicales ; les nutriments et l'oxygène sont transportés de la mère au fœtus par l'intermédiaire d'une seule veine ombilicale. Le cordon ombilical est entouré par l'amnios, et les espaces du cordon entourant les vaisseaux sanguins sont remplis de gelée de Wharton, un tissu conjonctif muqueux.
La partie maternelle du placenta se développe à partir de la couche la plus profonde de l'endomètre, le decidua basalis. Pour former la partie embryonnaire du placenta, le syncytiotrophoblaste et les cellules sous-jacentes du trophoblaste (cellules cytotrophoblastiques) commencent à proliférer en même temps qu'une couche de cellules mésodermiques extraembryonnaires. Ils forment la membrane chorionique, qui enveloppe l'ensemble du conceptus sous forme de chorion. La membrane chorionique forme des structures semblables à des doigts appelées villosités choriales qui s'enfouissent dans l'endomètre comme des racines d'arbres et constituent la partie fœtale du placenta. Les cellules du cytotrophoblaste perforent les villosités choriales, s'enfouissent plus profondément dans l'endomètre et remodèlent les vaisseaux sanguins maternels pour augmenter le flux sanguin maternel autour des villosités. Pendant ce temps, les cellules mésenchymateuses foetales dérivées du mésoderme remplissent les villosités et se différencient en vaisseaux sanguins, y compris les trois vaisseaux sanguins ombilicaux qui relient l'embryon au placenta en développement (Figure\(\PageIndex{8}\)).
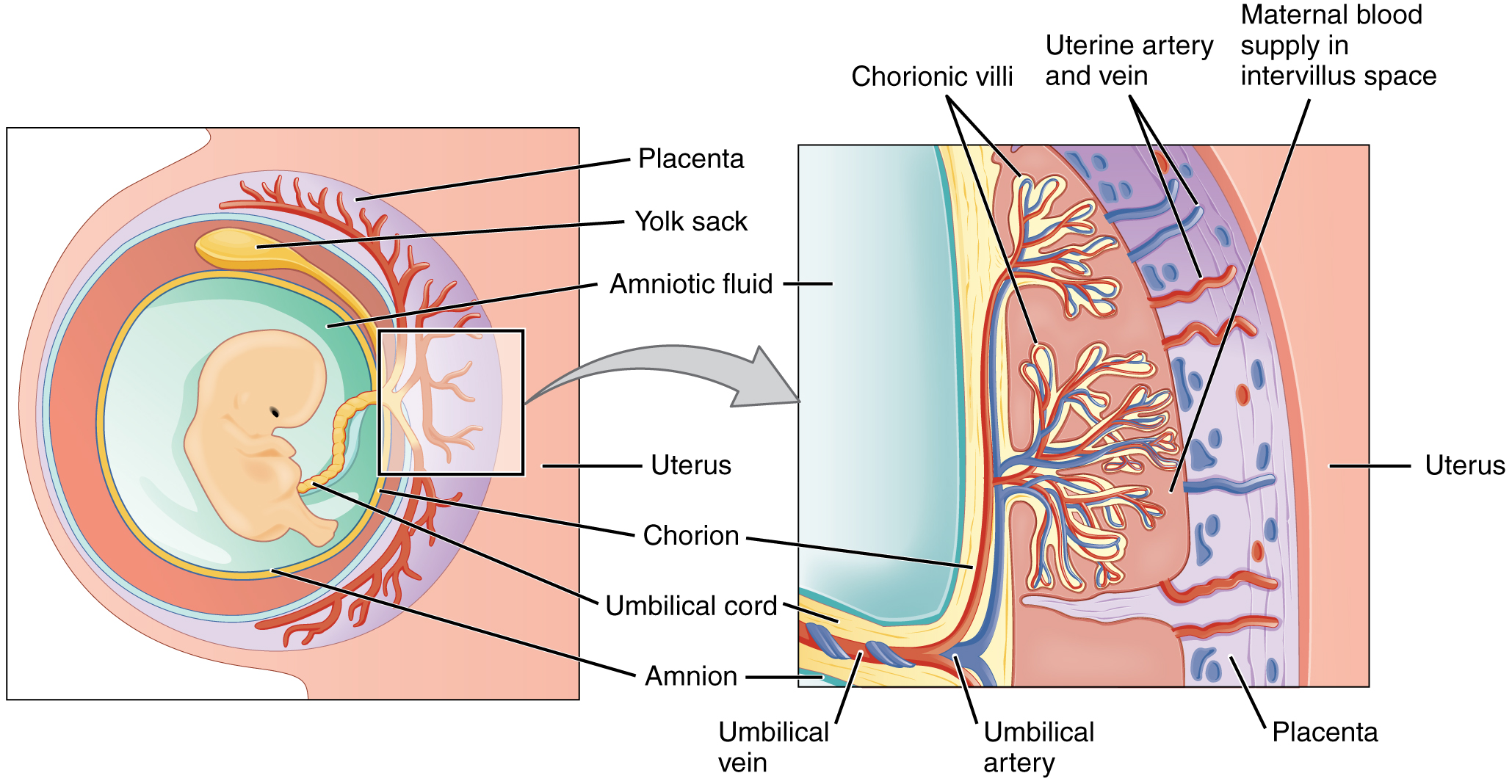
Le placenta se développe tout au long de la période embryonnaire et pendant les premières semaines de la période foetale ; la placentation est terminée aux semaines 14 à 16. En tant qu'organe pleinement développé, le placenta assure la nutrition et l'excrétion, la respiration et la fonction endocrinienne (Tableau\(\PageIndex{1}\) et Figure\(\PageIndex{9}\)). Il reçoit le sang du fœtus par les artères ombilicales. Les capillaires situés dans les villosités choriales filtrent les déchets foetaux du sang et renvoient le sang propre et oxygéné au fœtus par la veine ombilicale. Les nutriments et l'oxygène sont transférés du sang maternel entourant les villosités à travers les capillaires et dans la circulation sanguine foetale. Certaines substances traversent le placenta par simple diffusion. L'oxygène, le dioxyde de carbone et toute autre substance liposoluble empruntent cette voie. D'autres substances se déplacent par diffusion facilitée. Cela inclut le glucose hydrosoluble. Le fœtus a une forte demande en acides aminés et en fer, et ces substances sont transportées à travers le placenta par transport actif.
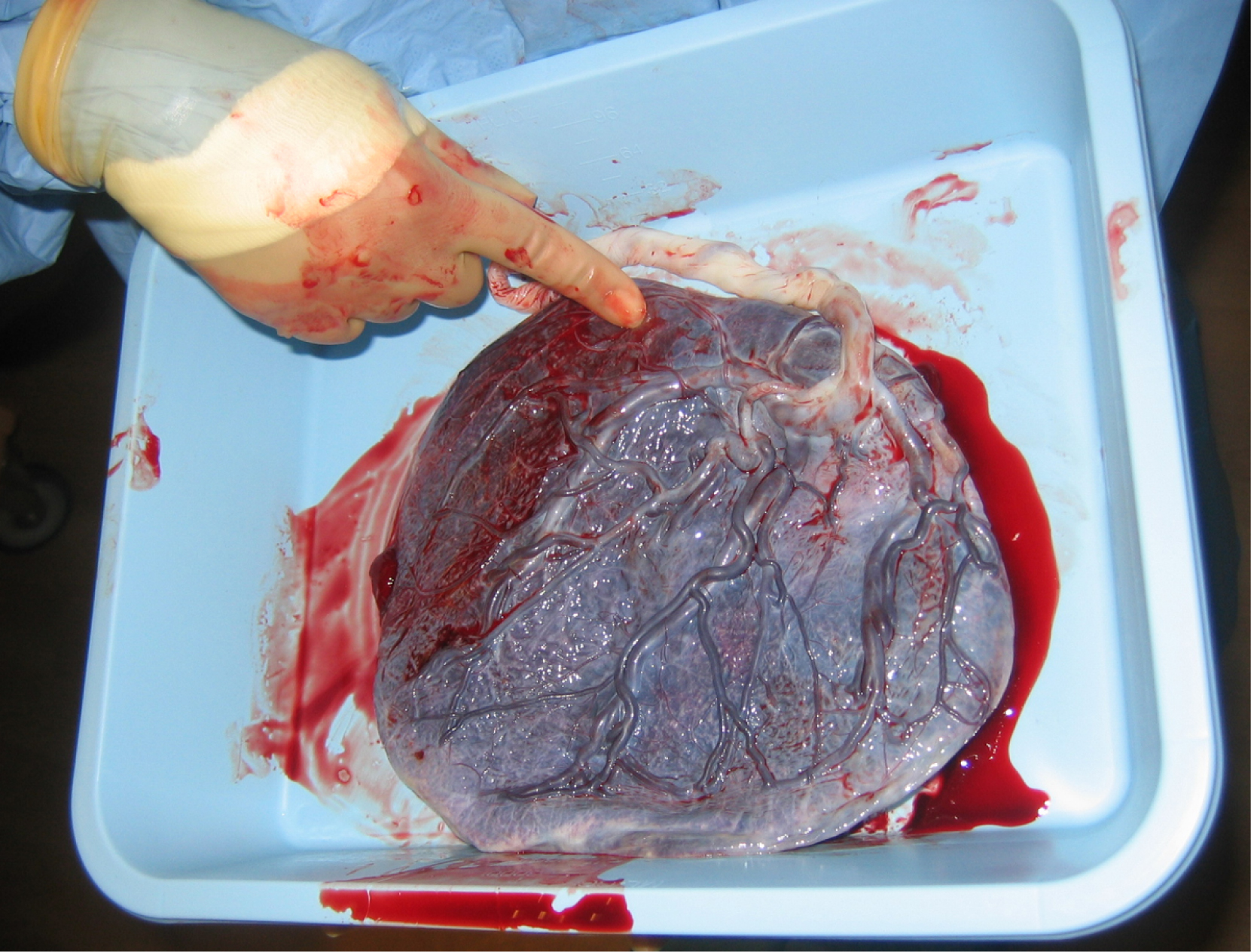
Figure\(\PageIndex{9}\) : Placenta. Ce placenta et ce cordon ombilical (blanc) après l'expulsion sont vus du côté foetal.
Le sang maternel et foetal ne se mélange pas parce que les cellules sanguines ne peuvent pas traverser le placenta. Cette séparation empêche les lymphocytes T cytotoxiques de la mère d'atteindre puis de détruire le fœtus, qui est porteur d'antigènes « non personnels ». De plus, il garantit que les globules rouges du fœtus ne pénètrent pas dans la circulation de la mère et déclenchent le développement d'anticorps (s'ils sont porteurs d'antigènes « non personnels »), au moins jusqu'aux derniers stades de la grossesse ou de l'accouchement. C'est la raison pour laquelle, même en l'absence de traitement préventif, une mère Rh − ne développe pas d'anticorps susceptibles de provoquer une maladie hémolytique chez son premier fœtus Rh +.
Bien que les cellules sanguines ne soient pas échangées, les villosités choriales offrent une surface suffisante pour l'échange bidirectionnel de substances entre le sang maternel et le sang foetal. Le taux d'échange augmente tout au long de la gestation à mesure que les villosités s'amincissent et se ramifient. Le placenta est perméable aux substances foetotoxiques liposolubles : alcool, nicotine, barbituriques, antibiotiques, certains agents pathogènes et de nombreuses autres substances qui peuvent être dangereuses ou mortelles pour l'embryon ou le fœtus en développement. Pour ces raisons, les femmes enceintes doivent éviter les substances foetotoxiques. La consommation d'alcool par les femmes enceintes, par exemple, peut entraîner toute une série d'anomalies appelées troubles du spectre de l'alcoolisation foetale (TSAF). Il s'agit notamment des malformations des organes et du visage, ainsi que des troubles cognitifs et comportementaux.
| Nutrition et digestion | Respiration | Fonction endocrinienne |
|---|---|---|
|
|
|
Organogenèse
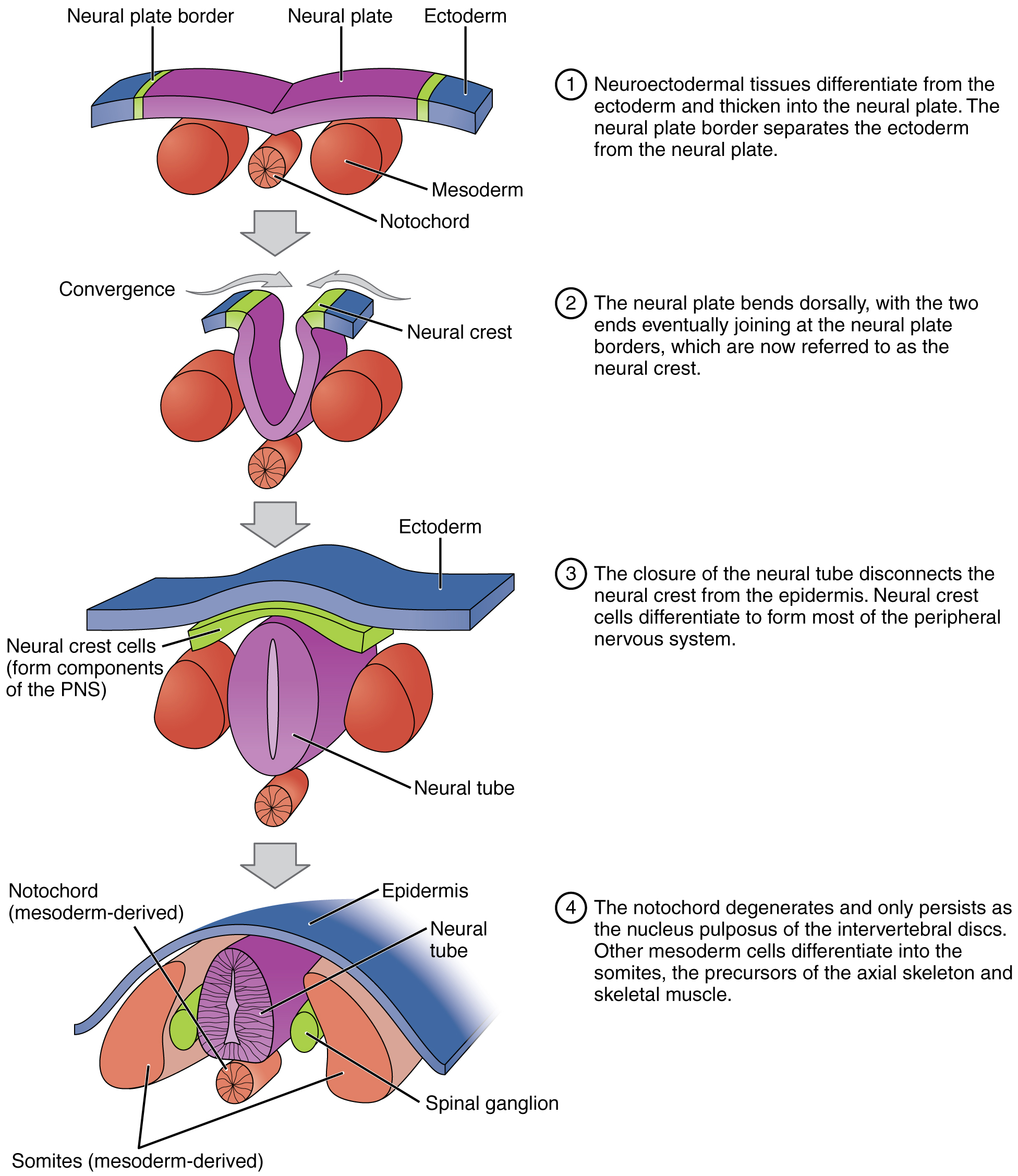
Après la gastrulation, des rudiments du système nerveux central se développent à partir de l'ectoderme au cours du processus de neurulation (Figure\(\PageIndex{10}\)). Les tissus neuroectodermiques spécialisés le long de l'embryon s'épaississent dans la plaque neurale. Au cours de la quatrième semaine, les tissus de chaque côté de la plaque se replient vers le haut pour former un pli neural. Les deux plis convergent pour former le tube neural. Le tube repose sur un notochord en forme de bâtonnet dérivé du mésoderme, qui finit par devenir le noyau pulpeux des disques intervertébraux. Des structures en forme de blocs appelées somites se forment de chaque côté du tube et finissent par se différencier en squelette axial, en muscle squelettique et en derme. Au cours des quatrième et cinquième semaines, le tube neural antérieur se dilate et se subdivise pour former des vésicules qui deviendront les structures cérébrales.
Le folate, l'une des vitamines B, est important pour le développement sain du tube neural. Une carence en acide folique maternelle au cours des premières semaines de grossesse peut entraîner des anomalies du tube neural, y compris le spina bifida, une anomalie congénitale caractérisée par le fait que le tissu rachidien fait saillie à travers la colonne vertébrale du nouveau-né, qui n'a pas réussi à se refermer complètement. Une anomalie plus grave du tube neural est l'anencéphalie, c'est-à-dire l'absence partielle ou totale de tissu cérébral.
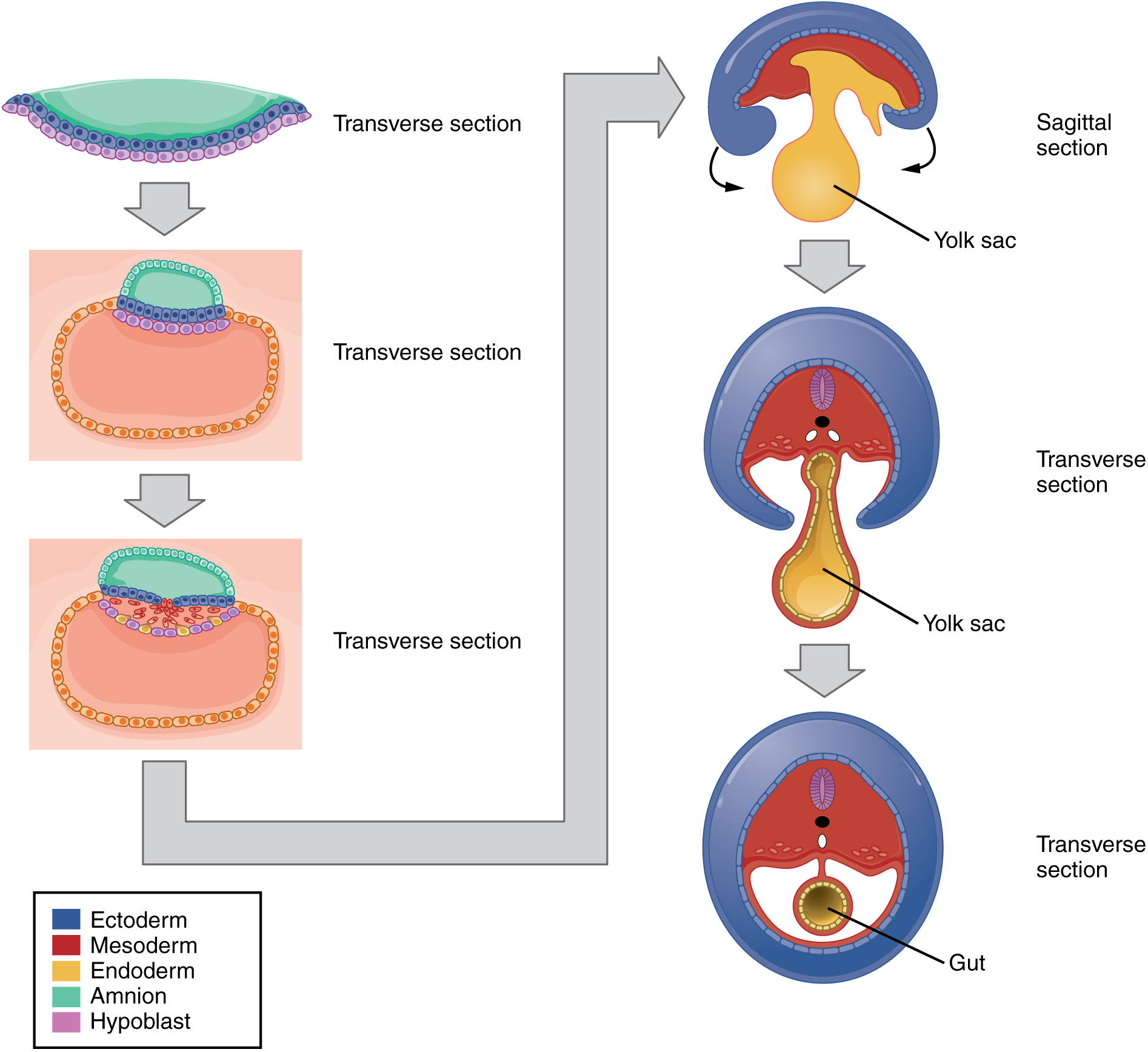
L'embryon, qui commence par une feuille plate de cellules, commence à acquérir une forme cylindrique par le biais du processus de pliage embryonnaire (Figure\(\PageIndex{11}\)). L'embryon se replie latéralement et de nouveau à chaque extrémité, formant un C avec des extrémités distinctes de la tête et de la queue. L'embryon enveloppe une partie du sac vitellin, qui dépasse avec le cordon ombilical de ce qui deviendra l'abdomen. Le pliage crée essentiellement un tube, appelé intestin primitif, qui est tapissé par l'endoderme. Le sac amniotique, qui se trouvait au-dessus de l'embryon plat, enveloppe l'embryon lorsqu'il se plie.
Au cours des 8 premières semaines de gestation, un embryon en développement établit les structures rudimentaires de tous ses organes et tissus à partir de l'ectoderme, du mésoderme et de l'endoderme. Ce processus s'appelle l'organogenèse.
Comme le système nerveux central, le cœur commence également son développement dans l'embryon sous la forme d'une structure tubulaire, reliée par des capillaires aux villosités choriales. Les cellules du cœur primitif en forme de tube sont capables de conduction et de contraction électriques. Le cœur commence à battre au début de la quatrième semaine, mais il ne pompe le sang embryonnaire qu'une semaine plus tard, lorsque le foie surdimensionné a commencé à produire des globules rouges. (Il s'agit d'une responsabilité temporaire du foie embryonnaire que la moelle osseuse assumera au cours du développement du fœtus.) Au cours des semaines 4 à 5, les fosses oculaires se forment, les bourgeons des membres apparaissent et les rudiments du système pulmonaire se forment.
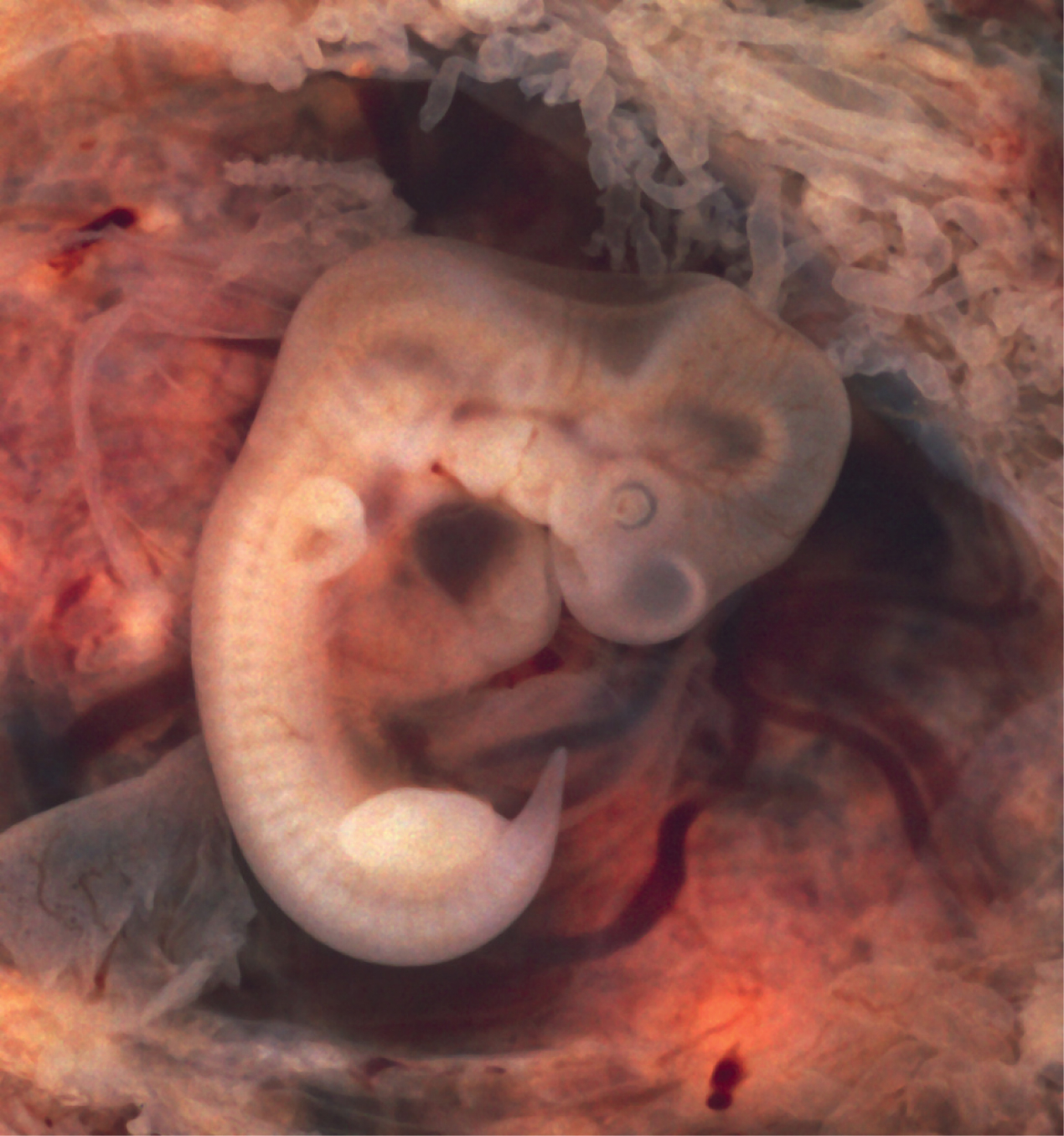
Au cours de la sixième semaine, des mouvements incontrôlés des membres du fœtus commencent à se produire. Le système gastro-intestinal se développe trop rapidement pour que l'abdomen embryonnaire puisse s'y adapter, et les intestins s'enroulent temporairement dans le cordon ombilical. Les mains et les pieds en forme de pagaie développent les doigts et les orteils par le processus d'apoptose (mort cellulaire programmée), qui provoque la désintégration des tissus situés entre les doigts. À la semaine 7, la structure du visage devient plus complexe et comprend les narines, les oreilles externes et les lentilles (Figure\(\PageIndex{12}\)). À la huitième semaine, la tête est presque aussi grande que le reste du corps de l'embryon et toutes les principales structures cérébrales sont en place. Les organes génitaux externes sont apparents, mais à ce stade, il est impossible de distinguer les embryons mâles et femelles. L'os commence à remplacer le cartilage du squelette embryonnaire par le biais du processus d'ossification. À la fin de la période embryonnaire, l'embryon se trouve à environ 3 cm (1,2 po) de la couronne à la croupe et pèse environ 8 g (0,25 oz).

Révision du chapitre
Lorsque le zygote se déplace vers l'utérus, il subit de nombreux clivages au cours desquels le nombre de cellules double (blastomères). Lorsqu'il atteint l'utérus, le conceptus est devenu une sphère de cellules serrées appelée morula, qui se forme ensuite en un blastocyste constitué d'une masse cellulaire interne à l'intérieur d'une cavité remplie de liquide entourée de trophoblastes. Le blastocyste s'implante dans la paroi utérine, les trophoblastes fusionnent pour former un syncytiotrophoblaste et le conceptus est enveloppé par l'endomètre. Quatre membranes embryonnaires se forment pour soutenir l'embryon en croissance : l'amnios, le sac vitellin, l'allantois et le chorion. Les villosités choriales du chorion s'étendent jusqu'à l'endomètre pour former la partie fœtale du placenta. Le placenta fournit de l'oxygène et des nutriments à l'embryon en croissance ; il élimine également le dioxyde de carbone et d'autres déchets métaboliques.
Après l'implantation, les cellules embryonnaires subissent une gastrulation, au cours de laquelle elles se différencient et se séparent en un disque embryonnaire et forment trois couches germinales primaires (l'endoderme, le mésoderme et l'ectoderme). Grâce au processus de repliement embryonnaire, le fœtus commence à prendre forme. La neurulation déclenche le processus de développement des structures du système nerveux central et l'organogenèse établit le plan de base pour tous les systèmes organiques.
Questions sur les liens interactifs
Regardez ce film en accéléré d'un conceptus dès le troisième jour. Quelle est la première structure que vous voyez ? À quel moment du film le blastocoel apparaît-il pour la première fois ? Quel événement se produit à la fin du film ?
Réponse : La première structure illustrée est la morula. Le blastocoel apparaît au bout de 20 secondes environ. Le film se termine par l'éclosion du conceptus.
Utilisez cet outil interactif pour visualiser le processus d'embryogenèse du point de vue du conceptus (panneau de gauche), ainsi que le développement du fœtus vu d'une coupe transversale maternelle (panneau de droite). Pouvez-vous identifier le moment où la neurulation se produit dans l'embryon ?
Réponse : La neurulation commence à la semaine 4.
Questions de révision
Q. Le clivage produit des cellules filles appelées ________.
A. trophoblastes
B. blastocystes
C. morulae
D. blastomères
Réponse : D
Q. Le conceptus, lorsqu'il atteint l'utérus, commence par ________.
A. implants
B. divise
C. se désintègre
D. écoutilles
Réponse : B
Q. La masse cellulaire interne du blastocyste est destinée à devenir le ________.
A. embryon
B. trophoblaste
C. villosités choriales
D. placenta
Réponse : A
Q. Quelle couche germinale primaire a donné naissance aux cellules qui sont finalement devenues le système nerveux central ?
A. endoderme
B. ectoderme
C. acrosome
D. mésoderme
Réponse : B
Q. Que se passerait-il si le trophoblaste ne sécrétait pas d'hCG lors de l'implantation du blastocyste ?
R. Les cellules ne continueraient pas à se diviser.
B. Le corps jaune continuerait à produire de la progestérone et des œstrogènes.
C. Les règles élimineraient le blastocyste de l'utérus.
D. La muqueuse utérine n'envelopperait pas le blastocyste.
Réponse : C
Q. Au cours de quel processus l'amnios enveloppe-t-il l'embryon ?
A. repliement embryonnaire
B. gastrulation
C. implantation
D. organogenèse
Réponse : A
Q. Le placenta est formé à partir de ________.
A. les cellules mésenchymateuses de l'embryon
B. l'endomètre de la mère uniquement
C. l'endomètre de la mère et la membrane chorionique de l'embryon
D. l'endomètre de la mère et le cordon ombilical de l'embryon
Réponse : C
Questions sur la pensée critique
Q. Environ 3 semaines après ses dernières règles, une femme sexuellement active éprouve un bref épisode de crampes abdomino-pelviennes et de saignements mineurs. Quelle pourrait en être l'explication ?
Réponse : Le moment de l'apparition de cette gêne et de ce saignement suggère qu'ils sont probablement causés par l'implantation du blastocyste dans la paroi utérine.
Q. Le Food and Nutrition Board de l'Institute of Medicine recommande à toutes les femmes susceptibles de devenir enceintes de consommer au moins 400 µg/jour d'acide folique provenant de suppléments ou d'aliments enrichis. Pourquoi ?
Réponse : Le folate, l'une des vitamines B, est important pour la formation saine du tube neural embryonnaire, qui se produit dans les premières semaines suivant la conception, souvent avant même que la femme ne réalise qu'elle est enceinte. Un environnement déficient en acide folique augmente le risque d'une anomalie du tube neural, telle que le spina bidifa, chez le nouveau-né.
Lexique
- allantois
- l'empochement du sac vitellin en forme de doigt forme le canal excréteur primitif de l'embryon, précurseur de la vessie
- amnios
- sac membraneux transparent qui entoure le fœtus en développement et se remplit de liquide amniotique
- cavité amniotique
- cavité qui s'ouvre entre la masse cellulaire interne et le trophoblaste ; se transforme en amnios
- blastocoel
- cavité remplie de liquide du blastocyste
- blastocyste
- terme désignant le conceptus au stade du développement, composé d'environ 100 cellules façonnées en une masse cellulaire interne destinée à devenir l'embryon et en un trophoblaste externe destiné à devenir les membranes fœtales et le placenta associés
- blastomère
- cellule fille d'un clivage
- chœur
- membrane qui se développe à partir du syncytiotrophoblaste, du cytotrophoblaste et du mésoderme ; entoure l'embryon et forme la partie fœtale du placenta à travers les villosités choriales
- membrane chorionique
- précurseur du chorion ; formes issues de cellules mésodermiques extra-embryonnaires
- villosités choriales
- des projections de la membrane chorionique qui s'enfouissent dans l'endomètre et se développent dans le placenta
- décolleté
- forme de division cellulaire mitotique dans laquelle la cellule se divise mais le volume total reste inchangé ; ce processus permet de produire des cellules de plus en plus petites
- conceptus
- stade préimplantatoire d'un ovule fécondé et de ses membranes associées
- ectoderme
- couche germinale primaire qui se développe dans les systèmes nerveux central et périphérique, les organes sensoriels, l'épiderme, les cheveux et les ongles
- grossesse extra-utérine
- implantation d'un embryon à l'extérieur de l'utérus
- embryon
- humain en développement au cours des semaines 3 à 8
- pliage embryonnaire
- processus par lequel un embryon passe d'un disque plat de cellules à une forme tridimensionnelle ressemblant à un cylindre
- endoderme
- couche germinale primaire qui forme ensuite le tractus gastro-intestinal, le foie, le pancréas et les poumons
- épiblaste
- couche supérieure de cellules du disque embryonnaire qui se forme à partir de la masse cellulaire interne ; donne naissance aux trois couches germinales
- fœtus
- être humain en développement pendant la période comprise entre la fin de la période embryonnaire (semaine 9) et la naissance
- gastrulation
- processus de migration et de différenciation cellulaires en trois couches germinales primaires après clivage et implantation
- gestation
- dans le développement humain, la période requise pour le développement embryonnaire et foetal in utero ; grossesse
- gonadotrophine chorionique humaine (hCG)
- hormone qui permet au corps jaune de survivre, de grossir et de continuer à produire de la progestérone et des œstrogènes afin de supprimer les règles et de créer un environnement propice au développement de l'embryon
- hypoblaste
- couche inférieure de cellules du disque embryonnaire qui s'étend dans le blastocoel pour former le sac vitellin
- implantation
- processus par lequel un blastocyste s'incruste dans l'endomètre utérin
- masse cellulaire interne
- groupe de cellules à l'intérieur du blastocyste qui est destiné à devenir l'embryon
- mésoderme
- couche germinale primaire qui devient le squelette, les muscles, le tissu conjonctif, le cœur, les vaisseaux sanguins et les reins
- morula
- sphère serrée de blastomères qui a atteint l'utérus mais qui ne s'est pas encore implantée
- plaque neurale
- couche épaisse de neuroépithélium qui s'étend longitudinalement le long de la surface dorsale de l'embryon et donne naissance au tissu du système nerveux
- pli neural
- bord surélevé du sillon neural
- tube neural
- précurseur des structures du système nerveux central, formé par l'invagination et la séparation du neuroépithélium
- neurulation
- processus embryonnaire qui établit le système nerveux central
- pas d'accord
- structure en forme de bâtonnet dérivée du mésoderme qui soutient la croissance du fœtus
- organogenèse
- développement des structures rudimentaires de tous les organes de l'embryon à partir des couches germinales
- placenta
- organe qui se forme pendant la grossesse pour nourrir le fœtus en développement ; régule également les déchets et les échanges de gaz entre la mère et le fœtus
- placenta praevia
- un faible placement du fœtus dans l'utérus fait que le placenta recouvre partiellement ou complètement l'ouverture du col de l'utérus au fur et à mesure de sa croissance
- placentation
- formation du placenta ; complète aux semaines 14 à 16 de la grossesse
- traînée primitive
- indentation le long de la surface dorsale de l'épiblaste à travers laquelle les cellules migrent pour former l'endoderme et le mésoderme lors de la gastrulation
- somite
- l'un des blocs de tissu appariés et répétés situés de chaque côté de la notocorde chez l'embryon précoce
- syncytiotrophoblaste
- cellules superficielles du trophoblaste qui fusionnent pour former un corps multinucléé qui digère les cellules endométriales pour fixer fermement le blastocyste à la paroi utérine
- trophoblaste
- enveloppe de cellules squameuses remplie de liquide destinée à devenir les villosités choriales, le placenta et les membranes foetales associées
- cordon ombilical
- lien entre le conceptus en développement et le placenta ; transporte le sang désoxygéné et les déchets du fœtus et renvoie les nutriments et l'oxygène de la mère
Contributeurs et attributions
- yolk sac
- membrane associated with primitive circulation to the developing embryo; source of the first blood cells and germ cells and contributes to the umbilical cord structure
- Template:ContribOpenStaxAP


