26.2: 神经系统的细菌性疾病
- Page ID
- 200410
学习目标
- 识别可能导致神经系统感染的最常见细菌
- 比较影响神经系统的特定细菌疾病的主要特征
影响神经系统的细菌感染很严重,可能危及生命。 幸运的是,只有少数几种细菌通常与神经系统感染有关。
细菌性脑膜炎
细菌性脑膜炎是最严重的脑膜炎形式之一。 引起脑膜炎的细菌通常在创伤后或由于细菌毒素的作用而通过血液进入中枢神经系统。 细菌也可能从上呼吸道的结构中传播,例如口咽、鼻咽、鼻窦和中耳。 头部受伤或植入人工耳蜗(置于内耳的电子设备)的患者也有患脑膜炎的风险。
许多可能引起脑膜炎的细菌通常存在于健康人群中。 非新生儿细菌性脑膜炎的最常见原因是脑膜炎奈瑟菌、肺炎链球菌和流感嗜血杆菌。 所有这三种细菌病原体都通过呼吸道分泌物在人与人之间传播。 每个人都能定植并穿过口咽和鼻咽的粘膜,然后进入血液。 一旦进入血液,这些病原体就可以在全身传播,并且能够在包括脑膜在内的任何身体部位产生感染和引发炎症(图\(\PageIndex{1}\))。 如果没有适当的全身抗菌治疗,病死率可能高达70%,其中20%的幸存者可能遭受不可逆转的神经损伤或组织破坏,从而导致听力损失、神经系统障碍或肢体丧失。 在有适当的治疗药物和预防性疫苗的人群中,死亡率要低得多(低至15%)。 1
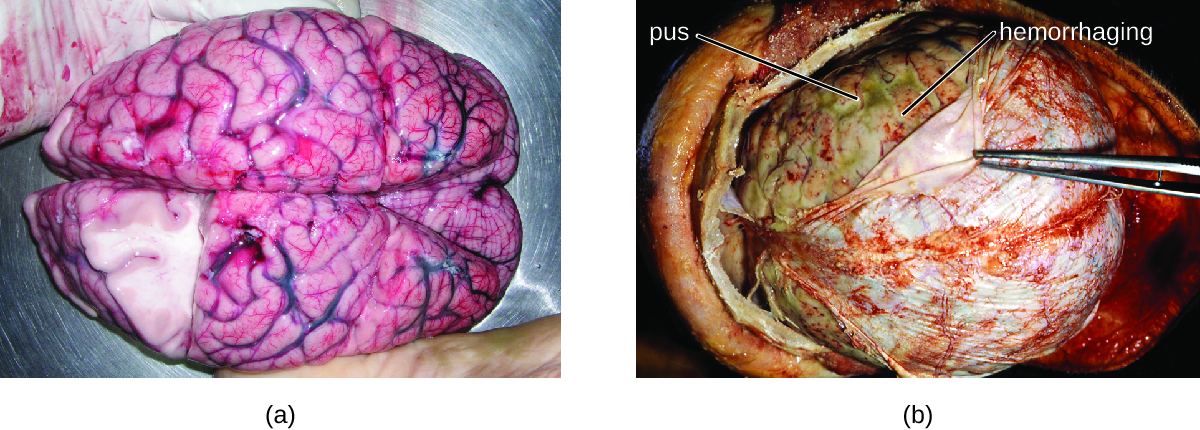
其他各种细菌,包括单核细胞增生李斯特菌和大肠杆菌,也能够引起脑膜炎。 这些细菌通过血液循环传播或通过鼻窦或鼻咽感染传播后,会引起蛛网膜和脑脊液的感染。 无@@ 乳链球菌常见于阴道和胃肠道的微生物群中,也可能在出生前或出生期间从母亲传播后在新生儿中引起细菌性脑膜炎。
这些微生物引起的严重炎症可能导致早期症状,包括剧烈头痛、发烧、精神错乱、恶心、呕吐、畏光和脖子僵硬。 与某些类型的细菌性脑膜炎相关的全身性炎症反应可能导致皮肤出血和紫癜性病变,然后是更严重的疾病,包括休克、抽搐、昏迷和死亡,在某些情况下,在短短几个小时内。
对腰椎穿刺获得的脑脊液进行分析最能证实细菌性脑膜炎的诊断。 脑< 45 mg/dL), and protein (> 脊液中多形核中性粒细胞(pmNs)(> 10 pmnS/mm 3)和葡萄糖(45 mg/dL)水平异常提示细菌性脑膜炎。 2 特定形式的细菌性脑膜炎的特征将在以下小节中详细介绍。
脑膜炎球菌脑膜炎
脑膜炎球菌脑膜炎是由革兰氏阴性球菌 N. 脑膜炎引起的严重感染。 在某些情况下,死亡可能在症状出现后的几个小时内发生。 非致命病例可能导致不可逆转的神经损伤,导致听力损失和脑损伤,或因组织坏死而截肢。
脑膜炎球菌脑膜炎可以感染任何年龄的人,但在婴儿、青少年和年轻人中,其患病率最高。 3 脑膜炎球菌脑膜炎曾经是人类脑膜炎流行的最常见原因。 在被称为脑膜炎地带的撒哈拉以南非洲的大片地区,情况仍然如此,但由于脑膜炎球菌疫苗的使用,脑膜炎球菌脑膜炎的流行在大多数其他地区已变得罕见。 但是,疫情仍可能发生在人们有密切直接接触的社区、学校、学院、监狱和其他人群中。
脑膜炎杆菌对口咽和鼻咽的粘膜具有很高的亲和力。 接触含有脑膜炎球菌的呼吸道分泌物是一种有效的传播方式。 导致脑膜炎快速发展的毒力因子增强了脑膜炎球菌的致病性。 其中包括低聚脂糖(LOS)内毒素、用于附着在宿主组织上的IV型pili以及帮助细胞避免吞噬作用和补体介导杀伤的多糖胶囊。 其他毒力因子包括 IgA 蛋白酶(可分解 IgA 抗体)、侵袭因子 Opa、Opc 和 porin(促进经细胞通过血脑屏障进入)、铁摄取因子(从宿主细胞中去除血红蛋白中的血红素单位并将其用于生长)和压力保护细菌免受活性氧分子侵害的蛋白质。
脑膜炎球菌脑膜炎的一个独特征兆是在皮肤或粘膜上形成点状皮疹,其特征是微小、红色、扁平的出血性病变。 这种皮疹在疾病发作后不久出现,是对 LOS 内毒素和粘附性毒力因子的反应,这些因子会破坏皮肤毛细血管和小静脉的内皮细胞。 血管中断会触发微小血块的形成,导致血液泄漏到周围组织中。 随着感染的进展,毒力因子水平增加,随着血液继续泄漏到组织中,出血性病变的大小可能会增加。 大于 1.0 cm 的病变通常发生在出现休克的患者身上,因为毒力因素会导致出血增多和血块形成。 由脑膜炎球菌毒力因子引起的全身性损伤导致的败血症可导致快速多器官衰竭、休克、弥散性血管内凝血和死亡。
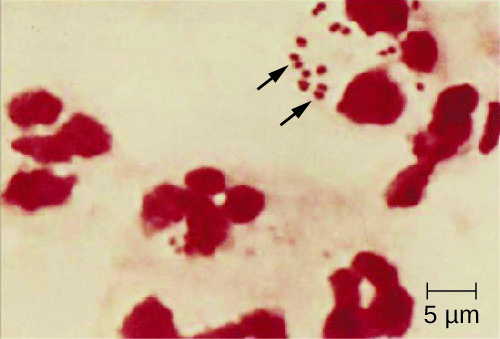
由于脑膜炎球菌脑膜炎进展如此之快,需要更多种类的临床样本才能及时发现脑膜炎球菌。 所需标本可能包括血液、脑脊液、鼻咽和口咽拭子、尿道和宫颈内拭子、瘀点吸气和活检。 处理和运输疑似含有脑膜炎杆菌的标本时应始终遵守安全规程,因为暴露于患者标本中的飞沫或气溶胶的医护人员会出现致命的脑膜炎球菌病例。 通过革兰染色直接评估脑脊液,发现细胞外和细胞内革兰氏阴性双球菌具有与PMN相关的独特咖啡豆微观形态时,可以迅速推定诊断脑膜炎球菌脑膜炎(图\(\PageIndex{2}\))。 也可以使用针对脑膜炎杆菌的乳胶凝集和免疫层析快速诊断检测,直接从脑脊液中进行鉴定。 也可以使用基于DNA序列的分型方案对脑膜炎球菌的超可变外膜蛋白进行物种鉴定,这种分型已经取代了血清(亚型)分型。
脑膜炎球菌感染可以通过抗生素疗法治疗,最常使用第三代头孢菌素。 但是,由于即使经过治疗,结果也可能为阴性,因此预防性疫苗接种是最好的治疗形式。 2010 年,非洲脑膜炎地带的国家开始使用一种新的血清型 A 型脑膜炎球菌偶联疫苗。 该计划通过赋予个体和群体免疫力,极大地减少了脑膜炎球菌脑膜炎的病例数量。
已知存在十二种不同的脑膜炎球菌囊血清型。 血清型 A、B、C、W、X 和 Y 是全球最普遍的。 疾病预防控制中心建议11-12岁的儿童接种单剂四价疫苗,该疫苗可预防血清型A、C、W和Y,并在16岁时加强疫苗。 4 在高风险环境中(例如大学校园爆发疫情)的个人,可以额外接种或注射血清型乙型脑膜炎球菌疫苗。
校园脑膜炎
住在宿舍或公共住房中的大学生感染流行性脑膜炎的风险增加。 从2011年到2015年,美国大学校园中至少爆发了九起脑膜炎球菌疫情。 这些事件共涉及43名学生(其中四人死亡)。 5 尽管进行了快速诊断和积极的抗微生物药物治疗,但仍有几名幸存者患有截肢或严重的神经系统问题。
疾病预防控制中心建议对住在宿舍的一年级大学生进行预防性疫苗接种,保险公司现在为大学宿舍的学生提供脑膜炎球菌疫苗接种。 一些大学要求某些进入大学的学生接种脑膜炎球菌偶联疫苗(图\(\PageIndex{3}\))。
肺炎球菌脑膜炎
肺炎球菌脑膜炎由封装的革兰阳性细菌 S. pneumoniae(肺炎球菌,也称为链球菌)引起。 根据采样方法,这种生物通常存在于30-70%的幼儿咽部微生物群中,而在不到5%的健康成年人中可以发现肺炎杆菌。 尽管这种微生物通常没有疾病症状,但它可以在易感人群中穿过血脑屏障。 在某些情况下,它还可能导致败血症。 自从引入乙型流感嗜血杆菌疫苗以来,肺炎杆菌已成为2个月至成年期人类脑膜炎的主要病因。
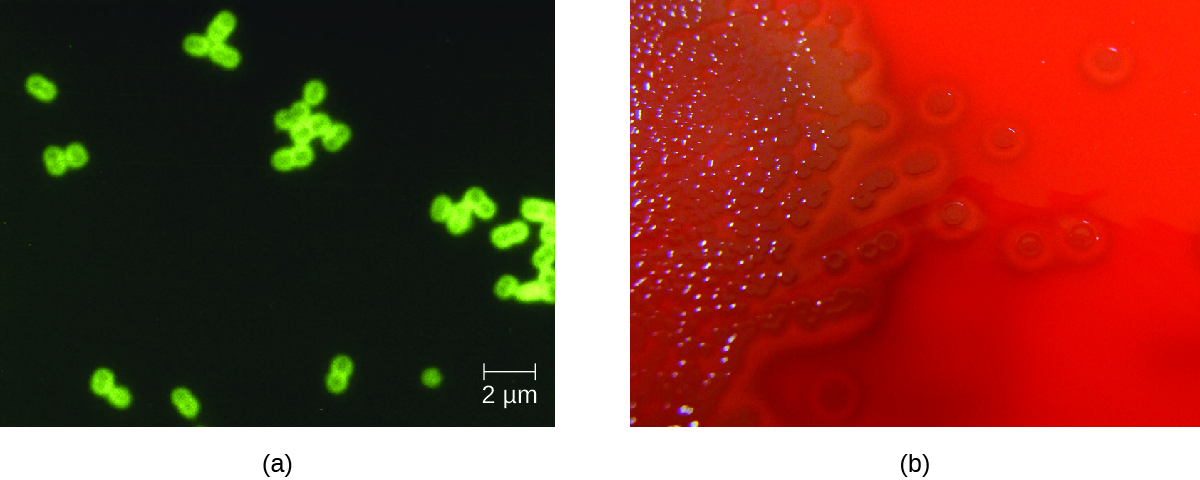
肺炎杆菌可以在脑脊液样本中使用革兰染色标本、乳胶凝集和特异性肺炎杆菌的免疫层析RDT进行鉴定。 在革兰氏染色样本中,肺炎球菌表现为革兰氏阳性、柳叶刀形双球菌(图\(\PageIndex{4}\))。 肺炎杆菌的鉴定也可以使用脑脊液和血液培养来实现,根据对独特囊多糖的quellung反应,至少可以鉴定出93种不同的血清型。 聚合酶链反应和逆转录聚合酶链反应检测也可用于确认鉴定。
肺炎杆菌产生的主要毒力因子包括用于粘附宿主细胞(肺炎球菌粘附性)的 PI-1 pilin 和用于附着在呼吸道细胞上的毒力因子 B(pa VB);与上皮细胞结合并干扰免疫因子 IgA 的胆碱结合蛋白(cbPA)和 C3;以及触发炎症反应的细胞质细菌毒素肺溶素。
随着肺炎杆菌耐药菌株的出现,肺炎球菌脑膜炎通常使用广谱抗生素治疗,例如左氧氟沙星、头孢噻辛、青霉素或其他β-内酰胺抗生素。 呼吸道细菌感染中描述了两种可用的肺炎球菌疫苗。
b 型流感嗜血杆菌
由于使用了有效的乙型流感杆菌疫苗,由乙型流感杆菌(Hib)(一种封装的多态革兰氏阴性球菌)引起的脑膜炎现在在大多数国家并不常见。 如果不使用乙型流感嗜血杆菌疫苗,流感杆菌可能是2个月至5岁儿童脑膜炎的主要原因。 流感杆菌可以在健康个体的喉咙中找到,包括婴儿和幼儿。 到五岁时,大多数孩子已经对这种微生物产生了免疫力。 但是,2个月以上的婴儿不会产生足够的保护性抗体反应,并且容易患上严重疾病。 这种感染引起的颅内压导致幸存者死亡率为5%,耳聋或脑损伤的发生率为20%。 6
流感杆菌产生至少16种不同的毒力因子,包括引发炎症的LOS和有助于附着和侵入呼吸道上皮细胞的嗜血杆菌粘附和渗透因子(Hap)。 该细菌还含有有助于避免吞噬作用的多糖胶囊,以及允许其逃避粘膜分泌的抗体的IgA1蛋白酶和P2蛋白等因子。 此外,血红蛋白结合蛋白(Hgp)和转铁蛋白结合蛋白(Tbp)等因子分别从血红蛋白和转铁蛋白中获取铁,用于细菌生长。
流感杆菌感染的初步诊断可以通过直接聚合酶链反应和脑脊液涂片作出。 染色涂片将发现细胞内和细胞外的 PMN 具有小型、多态性、革兰氏阴性的球杆菌或丝状形式,是流感杆菌的特征。 该属的初步确认可以基于它在巧克力琼脂上的挑剔生长。 对外源生化生长辅助因子NAD和血红素(由MALDI-TOF提供)、乳胶凝集和逆转录聚合酶链反应的要求证实了鉴定。
由流感杆菌引起的脑膜炎通常使用强力霉素、氟喹诺酮类、第二代和第三代头孢菌素以及碳青霉烯类药物治疗。 预防流感杆菌感染的最佳方法是使用乙型流感多糖偶联疫苗。 建议所有儿童在2、4和6个月大时接种这种疫苗,最后的加强剂量在12至15个月大时接种。 7
新生儿脑膜炎
S. agalactiae,B 组链球菌 (GBS),是一种封装的革兰氏阳性细菌,是新生儿脑膜炎的最常见病因,新生儿脑膜炎是指发生在 3 个月以下婴儿的脑膜炎。 8 S. agalactiae 还可以在所有年龄段的人群中引起脑膜炎,存在于大约 10-30% 的人的泌尿生殖系统和胃肠道微生物群中。
新生儿感染的发生要么是早发性疾病,要么是迟发性疾病。 早发性疾病定义为发生在 7 天以下的婴儿身上。 婴儿最初是在分娩时感染无乳酸杆菌,那时细菌可能会从母亲的阴道转移出来。 通过在分娩期间给母亲静脉注射抗生素,可以大大降低早发的新生儿脑膜炎的发病率。
迟发的新生儿脑膜炎发生在 1 周至 3 个月大的婴儿身上。 在泌尿生殖道中患有无乳糖杆菌的母亲所生的婴儿患迟发脑膜炎的风险更高,但迟发的感染可以从母亲以外的来源传播;感染源通常不明。 过早出生的婴儿(在怀孕 37 周之前)或母亲发烧的婴儿感染迟发的新生儿脑膜炎的风险也更大。
早发性疾病的体征和症状包括体温不稳定、呼吸暂停(呼吸停止)、心动过缓(心率缓慢)、低血压、喂食困难、烦躁和软弱。 睡着时,宝宝可能很难醒来。 迟发性疾病的症状更可能包括癫痫发作、额叶凸起(情有独钟)、脖子僵硬、半瘫(身体一侧无力)和 opisthotonos(身体僵硬,背部拱起,头部向后倾斜)。
S. agalactiae 产生至少 12 种毒力因子,包括附着在宿主细胞表面蛋白上的 fbSA、促进人类内皮细胞入侵的 PI-1 pilithat、一种防止替代补体途径激活并抑制吞噬作用的多糖胶囊,以及毒素 CAMP 因子,它在宿主细胞膜中形成毛孔并与 IgG 和 IgM 抗体结合。
脑脊液或血液培养的阳性结果往往证实了新生儿脑膜炎的诊断,但并不统一。 测试包括常规培养、通过酶免疫分析进行抗原检测、不同胶囊类型的血清分型、聚合酶链反应和逆转录聚合酶链反应。 它通常使用β-内酰胺抗生素治疗,例如静脉注射青霉素或氨苄西林加庆大霉素。 即使经过治疗,受感染的新生儿死亡率仍约为10%。 9
练习\(\PageIndex{1}\)
- 哪些群体最容易感染每种细菌性脑膜炎疾病?
- 目前有针对哪些细菌性脑膜炎疾病的疫苗可用?
- 哪种生物会导致流行性脑膜炎?
梭状芽孢杆菌相关疾病
梭状芽孢杆菌属中的物种是革兰氏阳性、形成内孢子的棒,是专属厌氧菌。 梭菌属的内孢子在自然界中很普遍,常见于土壤、水、粪便、污水和海洋沉积物中。 梭菌属产生的蛋白质外毒素类型比任何其他细菌属都要多,包括两种具有蛋白酶活性的外毒素,它们是已知最有效的生物毒素:肉毒杆菌神经毒素(BonT)和破伤风神经毒素(TenT)。 这两种毒素的致死剂量为每千克体重0.2—10 ng。
BonT 可以由独特的丁酸梭菌和巴拉蒂梭菌菌株产生;但是,它主要与肉毒杆菌和肉毒中毒状况有关。 导致破伤风的 TenT 仅由破伤风杆菌产生。 这些强大的神经外毒素是这些病原体的主要毒力因子。 细菌和病毒病原体的毒力因子中描述了这些毒素的作用模式,如图 15.3.7 所示。
破伤风或肉毒中毒的诊断通常涉及生物测定,检测粪便标本、血液(血清)或可疑食物中是否存在 BonT 和 TenT。 此外,可以使用市售的厌氧菌培养基分离和培养肉毒杆菌和破伤风梭菌。 还提供酶联免疫吸附和逆转录聚合酶链反应检测。
破伤风
破伤风是一种非传染性疾病,其特征是由 TenT 的作用引起的无法控制的肌肉痉挛(收缩)。 它通常发生在破伤杆菌感染伤口并产生 tEn T 时,TenT 会迅速与神经组织结合,从而导致神经元中毒(中毒)。 根据感染部位和程度,破伤风病例可以描述为局部性、头部性或全身性。 发生在新生儿身上的全身性破伤风称为新生儿破伤风。
当 TenT 仅影响受伤部位附近的肌肉群时,就会发生局部破伤风。 没有中枢神经系统受累,症状通常较轻,局部肌肉痉挛是由周围神经元功能障碍引起的。 具有部分免疫力的人,尤其是以前接种过疫苗但没有接种推荐的强化疫苗的人,最有可能因破伤风杆菌感染穿刺伤口而出现局部破伤风。
头部破伤风是一种罕见的局部破伤风,通常与头部或面部伤口有关。 在极少数情况下,它发生在中耳炎(中耳感染)中。 头部破伤风通常会导致患者看到双重图像,因为痉挛会影响控制眼球运动的肌肉。
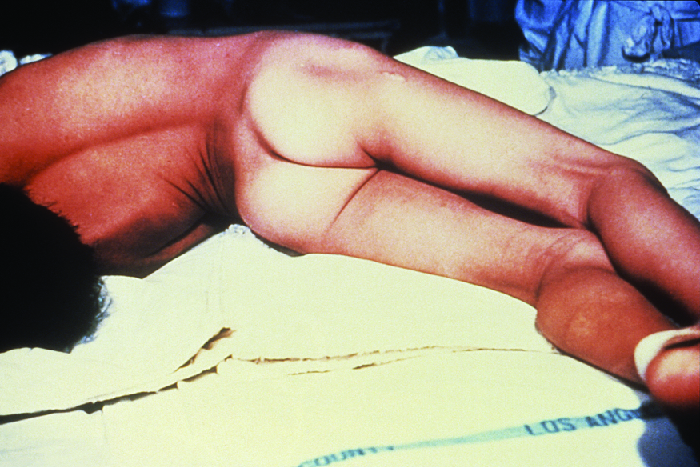
如果 tenT 能够进一步扩散到人体组织中,则局部破伤风和头部破伤风都可能发展为全身性破伤风,这是一种更为严重的疾病。 在全身性破伤风中,TenT 会进入 PNS 的神经元。 从那里开始,TenT 从伤口部位(通常位于身体四肢)向中枢神经系统中的抑制性神经元逆行(向后)传播。 在那里,它可以防止伽玛氨基丁酸(GABA)的释放,伽玛氨基丁酸(GABA)是负责肌肉松弛的神经递质。 由此产生的肌肉痉挛通常首先发生在下巴肌肉中,导致下巴闭锁的典型症状(无法张开嘴巴)。 随着毒素逐渐继续阻断神经递质的释放,其他肌肉也会受到影响,导致无法控制的突然肌肉痉挛,其强度足以导致肌腱断裂和骨折。 颈部、背部和腿部肌肉的痉挛可能导致身体形成僵硬、僵硬的足弓,这种姿势叫做 opisthotonos(图\(\PageIndex{5}\))。 喉部、隔膜和胸部肌肉的痉挛限制了患者的吞咽和呼吸能力,最终导致窒息(氧气供应不足)死亡。
新生儿破伤风通常发生在分娩后脐带的树桩被破伤风孢子污染时。 尽管这种情况在美国很少见,但新生儿破伤风是导致婴儿死亡的主要原因,这些国家的孕产妇没有接种破伤风疫苗,而且分娩通常在不卫生的条件下。 在出生的第一周结束时,受感染的婴儿会变得烦躁,进食不良,并因痉挛而变得僵硬。 新生儿破伤风的预后很差,死亡率为 70% — 100%。 10
破伤风患者的治疗包括使用呼吸机辅助呼吸、伤口清创、体液平衡以及使用甲硝唑或青霉素进行抗生素治疗以阻止破伤风梭菌的生长。 此外,患者接受TenT抗毒素治疗,优选以人免疫球蛋白的形式治疗以中和非固定毒素和苯二氮卓类药物以增强GABA对肌肉松弛和焦虑的作用。
破伤风类毒素(TT)疫苗可用于保护和预防破伤风。 它是 dTaP、Tdap 和 Td 等疫苗的 T 成分。 疾病预防控制中心建议儿童在 2、4、6 和 15-18 个月大时接种一剂 dTaP 疫苗,在 4-6 岁时再接种一剂 dTaP 疫苗。 建议青少年和成人每 10 年服用一剂 Td 作为 TT 增强剂。 11
肉毒中毒
肉毒中毒是一种罕见但经常致命的疾病,由 BonT 中毒引起。 它可能是由于肉毒杆菌感染而发生的,在这种情况下,细菌会在体内产生 BonT,也可以是直接将 BonT 引入组织中造成的。
体内感染和产生 BonT 可导致伤口肉毒中毒、婴儿肉毒中毒和成人肠道毒血症。 伤口肉毒中毒通常发生在创伤性损伤、深层穿刺伤口或注射部位后将肉毒杆菌直接引入伤口时。 婴儿肉毒中毒(发生在 1 岁以下的婴儿身上)和成人肠道毒血症(发生在免疫功能低下的成年人身上)是由摄入食物中的肉毒杆菌内孢子引起的。 内孢子在体内发芽,导致肠道中产生 BonT。
当 BonT 在体外产生,然后通过食物(食源性肉毒中毒)、空气(吸入肉毒中毒)或临床程序(医源性肉毒中毒)直接引入体内时,就会发生中毒。 食源性肉毒中毒是其中最常见的形式,发生在受污染的食物中产生 BonT,然后与食物一起摄入(回想一下案例:不良聚餐的连胜纪录)。 吸入性肉毒中毒很少见,因为 BonT 作为气溶胶不稳定,在自然界中不会发生;但是,它可以在实验室生产,并在 20 世纪 90 年代被日本的恐怖分子用作生物武器(未成功)。 还发生了几起意外吸入肉毒中毒的病例。 医源性肉毒中毒也很少见;它与注射用于美容目的的 BoNT 有关(参见 Micro Connections:肉毒杆菌毒素的药用用途)。
当 BonT 进入胃肠道、伤口或肺部的血液时,它会被转移到运动神经元的神经肌肉连接处,在那里它不可逆地与突触前膜结合,防止乙酰胆碱从运动神经元的突触前末端释放到神经肌肉交界处。 阻止乙酰胆碱释放的后果是肌肉活动丧失,导致肌肉松弛,最终导致瘫痪。
如果 BonT 通过胃肠道吸收,肉毒中毒的早期症状包括视力模糊、眼睑下垂、吞咽困难、腹部绞痛、恶心、呕吐、便秘或可能出现腹泻。 随之而来的是渐进性松弛麻痹,肌肉逐渐减弱和失去控制。 患者的经历可能特别可怕,因为听力保持正常,意识不会丧失,他或她完全意识到自己病情的进展。 在婴儿中,肉毒中毒的明显症状包括哭声弱、哺乳能力下降和张力减退(头部或身体软弱)。 最终,肉毒中毒以上呼吸道、隔膜和胸部肌肉进行性麻痹引起的呼吸衰竭死亡而告终。
肉毒中毒使用 BonT 特异性抗毒素治疗。 如果及时给药,抗毒素可以阻止麻痹的进展,但不能逆转麻痹的进展。 使用抗毒素后,患者将慢慢恢复神经功能,但这可能需要数周或数月的时间,具体取决于病例的严重程度。 在康复期间,患者通常必须住院并通过呼吸机接受呼吸帮助。
练习\(\PageIndex{2}\)
- 成人应多久更新一次破伤风疫苗?
- 肉毒中毒的最常见原因是什么?
- 为什么肉毒中毒不能用抗生素治疗?
李斯特菌病
单核细胞增生李斯特菌是一种非封装、非孢子化、革兰氏阳性的棒状物,也是一种导致李斯特菌病的食源性病原体。 高危人群包括孕妇、新生儿、老年人和免疫功能低下者(回想一下微生物生长和微生物致病机制中的临床焦点案例研究)。 在大约20%的病例中,李斯特菌病会导致脑膜炎,尤其是新生儿和60岁以上的患者。 疾病预防控制中心将李斯特菌病确定为食源性疾病导致的第三大死亡原因,总体死亡率达到16%。 12 在孕妇中,李斯特菌病也可能导致孕妇自然流产,因为病原体具有穿过胎盘的独特能力。
单核细胞增生杆菌通常是通过被用作肥料的土壤或动物粪便污染而引入食物中的。 通常与李斯特菌病相关的食物包括新鲜水果和蔬菜、冷冻蔬菜、加工肉类、软奶酪和生牛奶。 13 与大多数其他食源性病原体不同,李斯特菌能够在0°C至50°C的温度下生长,因此即使在冷藏食品中也可以继续生长。
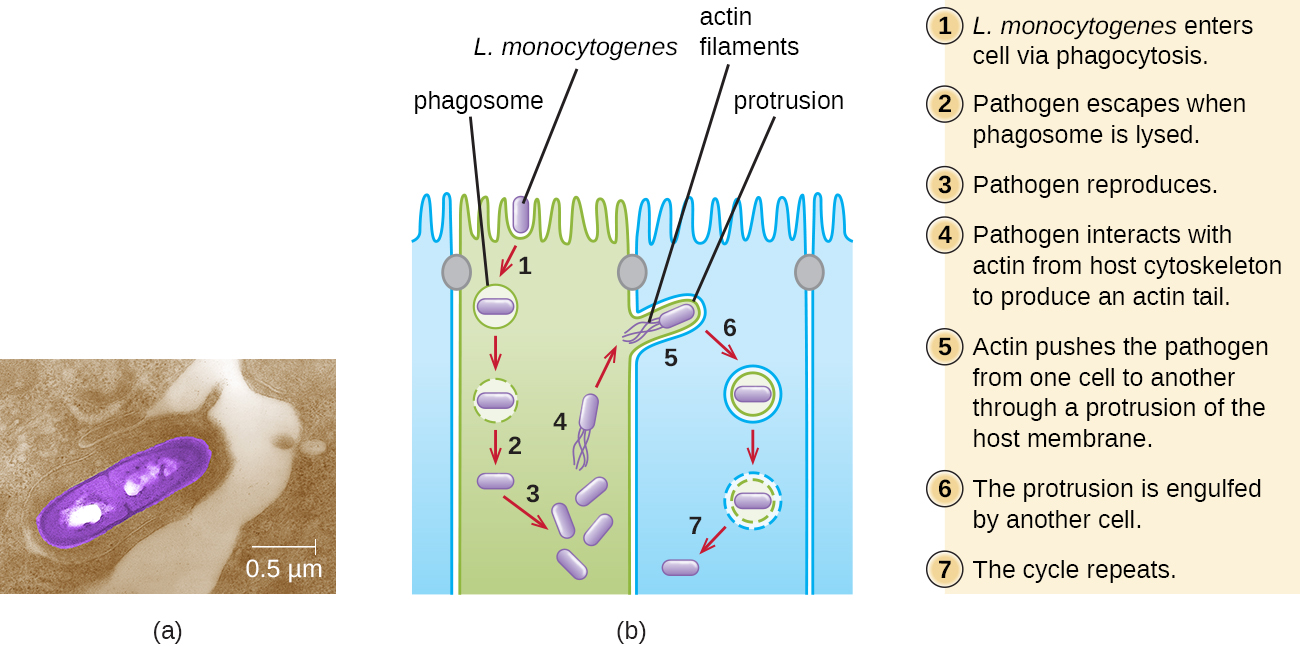
摄入受污染的食物最初会导致胃肠道感染。 但是,单核细胞增生杆菌会产生几种独特的毒力因子,使其能够穿过肠道屏障并扩散到其他身体系统。 被称为 internalins 的表面蛋白(inLA 和 inLB)帮助单核细胞增生杆菌侵入非吞噬细胞和组织,穿透肠壁并通过循环和淋巴系统传播。 Internalins 还使单核细胞增生杆菌能够突破其他重要屏障,包括血脑屏障和胎盘。 在组织内,单核细胞增生杆菌使用其他称为李斯特菌素O和ActA的蛋白质来促进细胞间运动,从而使感染在细胞之间传播(图\(\PageIndex{6}\))。
单核细胞增生杆菌通常通过培养来自正常无菌部位(例如血液或脑脊液)的样本来鉴定。 通过冷富集,将样品在 4 °C 的肉汤中孵育一周或更长时间,可以提高活生物的回收率。 区分单核细胞增生杆菌的类型和亚型——诊断和流行病学的重要步骤——通常使用脉冲场凝胶电泳来完成。 也可以使用化学发光 DNA 探针测定和 MALDI-TOF 进行鉴定。
李斯特菌病的治疗包括抗生素治疗,最常见的是氨苄青霉素和庆大霉素。 没有疫苗可用。
练习\(\PageIndex{3}\)
李斯特菌如何进入神经系统?
汉森氏病(麻风)
汉森氏病(也称为麻风病)是由一种长而细的丝状杆状细菌麻风分枝杆菌引起的,它是一种专用的细胞内病原体。 麻风杆菌被归类为革兰氏阳性细菌,但最好使用耐酸染色剂进行显微镜观察,通常被称为耐酸细菌。 汉森氏病会影响PNS,导致永久性损伤和附属物或其他身体部位的丢失。
汉森氏病具有传染性,但传染性不强;大约 95% 的人口不容易感染,因为他们对麻风杆菌具有天然免疫力。 人与人之间的传播是通过吸入鼻粘膜或长期反复接触受感染皮肤而发生的。 犰狳,仅有的五种易患汉森氏病的哺乳动物之一,也与某些病例的传播有关。 14
在人体内,麻风杆菌在鼻子、脚趾、手指和耳朵等外周组织中较低的温度下生长得最好。 一些导致麻风杆菌致病性的毒力因子位于细菌的胶囊和细胞壁上。 这些毒力因子使其能够与施旺细胞结合并入侵 Schwann 细胞,导致进行性脱髓鞘化,逐渐破坏 PNS 的神经元。 神经元功能丧失会导致受感染病变感觉减退(麻木)。 麻风杆菌很容易被巨噬细胞吞噬,但能够在巨噬细胞中存活,部分原因是中和吞噬体氧化爆发中产生的活性氧。 像单核细胞增生杆菌一样,麻风杆菌也可以直接在巨噬细胞之间移动,以避免被免疫因子清除。
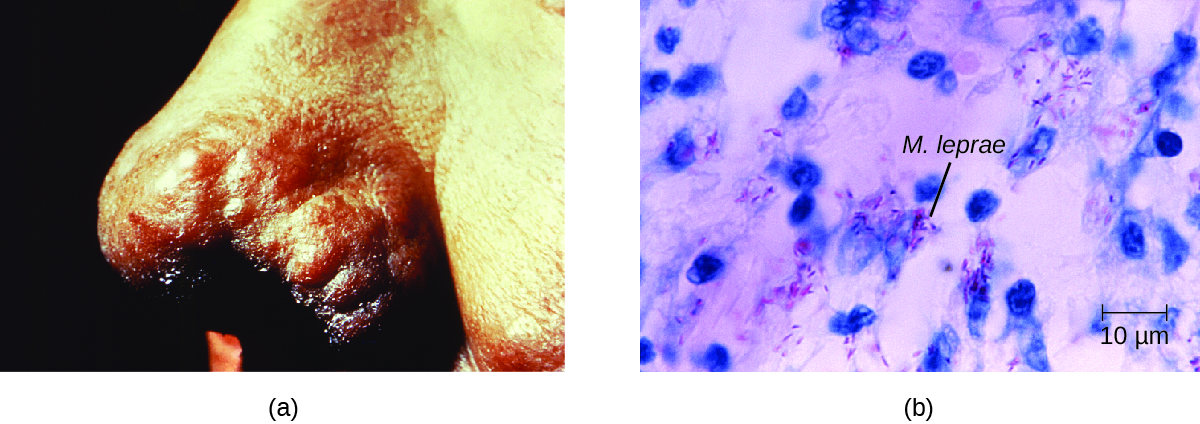
疾病的程度与患者的免疫反应有关。 最初的症状可能在感染后的 2 到 5 年内不会出现。 这些通常始于皮肤上较小、变白、麻木的区域。 在大多数人中,这些症状会自发消退,但有些病例可能会发展为更严重的疾病。 结核病(paucibacillary)汉森氏病的特点是存在相对较少(三个或更少)的扁平、漂白的皮肤病变,边缘有小结节,病变中存在细菌很少。 尽管这些病变可以持续数年或数十年,但包括细胞介导的细胞毒性在内的有效免疫反应会控制细菌。 无法控制感染的人以后可能会患上麻风病(多杆菌)汉森氏病。 这是一种进展性疾病,其特征是结节中充斥着耐酸杆菌和巨噬细胞。 受感染的 Schwann 细胞功能受损会导致周围神经损伤,从而导致感官丧失,从而导致溃疡、畸形和骨折。 麻风杆菌对尺神经(手腕内)的损伤是导致手部瘫痪的最常见原因之一。 在某些情况下,慢性组织损伤最终会导致手指或脚趾流失。 当还涉及粘膜组织时,也可能出现鼻部和面部的毁容性病变(图\(\PageIndex{7}\))。
汉森氏病是根据该病的临床体征和症状诊断的,皮肤涂片或皮肤活检标本中存在耐酸杆菌证实了这一点(图\(\PageIndex{7}\))。 麻风杆菌不会在任何已知的实验室培养基上体外生长,但可以通过在实验室小鼠或犰狳的脚垫中进行体内培养来识别。 必要时,可以对受感染的人体组织中的麻风杆菌 DNA 进行聚合酶链反应和基因分型,用于诊断和流行病学。
汉森氏病对治疗反应良好,如果及早诊断和治疗,不会导致残疾。 在美国,大多数汉森氏病患者在主要城市的门诊诊所接受国家汉森氏病计划的治疗,该计划是美国唯一专门治疗汉森氏病的机构。 自1995年以来,世卫组织向全世界所有患者免费提供汉森氏病的多药治疗。 结果,汉森氏病的全球发病率已从1985年的约520万例下降到2014年的约17.6万例。 15 多药疗法包括所有患者的氨苯磺和利福平,以及用于多杆菌病患者的第三种药物氯法齐明。
目前,尚无普遍接受的汉森氏病疫苗。 印度和巴西使用结核疫苗预防汉森氏病,因为这两种疾病都是由分枝杆菌引起的。 但是,这种方法的有效性值得怀疑,因为该疫苗似乎在某些人群中起作用,而在另一些人群中却不起作用。
练习\(\PageIndex{4}\)
- 什么能阻止结核病发展为麻风麻风?
- 为什么汉森氏病通常会影响四肢神经?
麻风病殖民地
历史上,麻风病等毁容性致命疾病在许多文化中一直受到污名化。 在人们理解麻风病之前,受害者经常被隔离在麻风病人聚居地,这种习俗在包括圣经在内的古代文献中经常被提及。 但是麻风病人殖民地不仅仅是古代世界的人工制品。 在夏威夷,十九世纪末建立的麻风病人殖民地一直持续到二十世纪中叶,其居民被迫生活在恶劣的条件下。 16 尽管麻风病是一种传染病,但它不被认为具有传染性(容易传染),而且它构成的威胁肯定不足以成为永久隔离其受害者的理由。 今天,我们将隔离和隔离的做法保留给患有更危险疾病的患者,例如埃博拉或结核分枝杆菌和金黄色葡萄球菌等耐多药细菌。 这种做法的伦理论据是,隔离感染的患者对于防止高度传染性疾病的传播和传播是必要的,即使这违背了患者的意愿。
当然,证明临时临床隔离的做法比像麻风病人聚居地那样的永久性社会隔离要容易得多。 1980年代,一些团体呼吁为艾滋病感染者建立营地。 尽管这个想法从未真正实现,但它引出了一个问题——我们在哪里划清界限? 永久隔离营或殖民地在医学或社会上是否合理? 假设爆发了一种无法治疗的致命传染性疾病。 对患有这种疾病的人实行社会隔离是否合理? 我们将如何平衡感染者的权利与他们对他人构成的风险? 社会应该在多大程度上期望个人为了人道地对待他人而将自己的健康置于危险之中?
神经系统的细菌感染
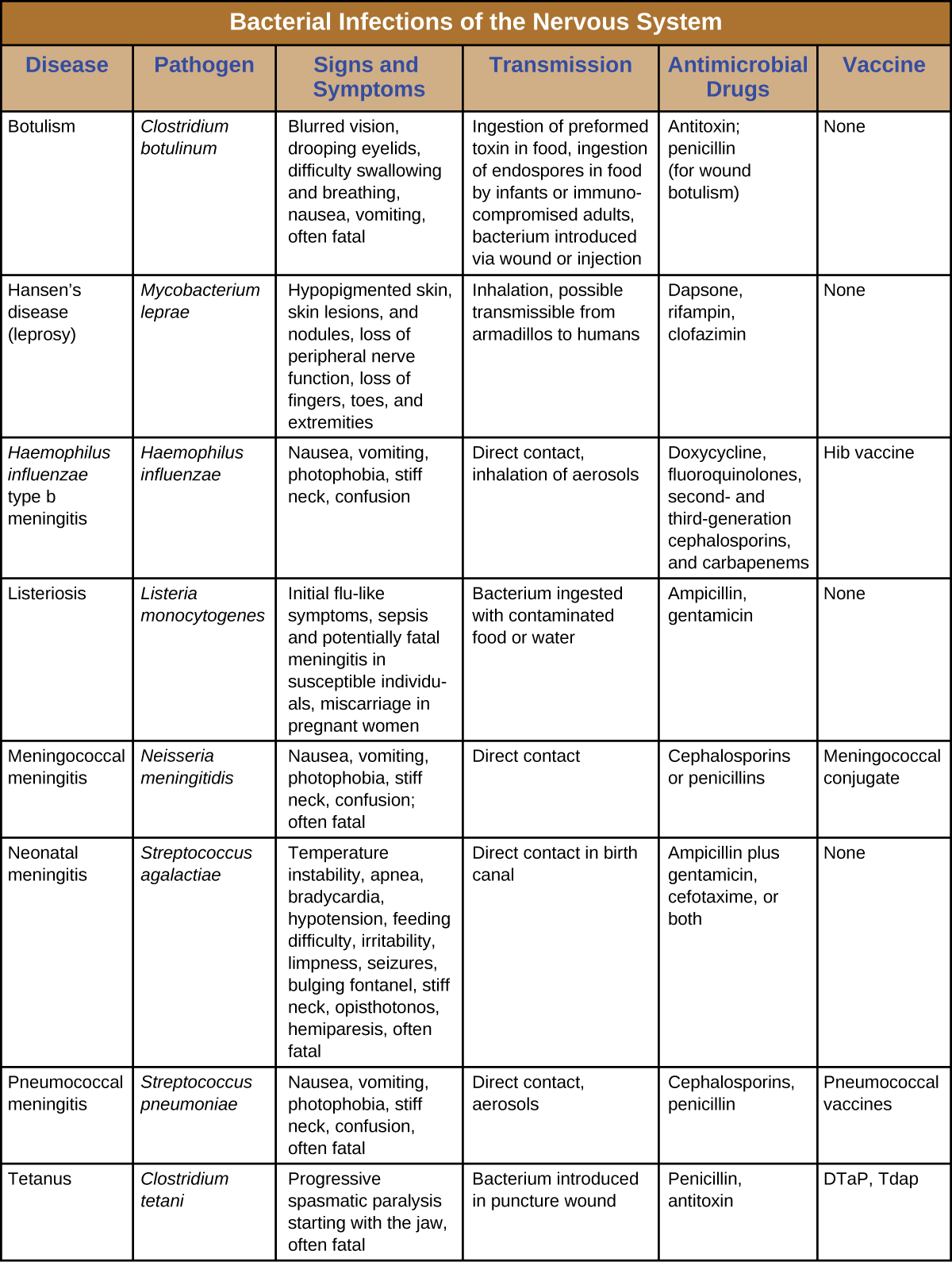
尽管有强大的防御能力保护神经系统,但已知有许多细菌病原体会导致中枢神经系统或肺动脉综合征的严重感染。 不幸的是,这些感染往往很严重,危及生命。 该图\(\PageIndex{8}\)总结了神经系统的一些重要感染。
关键概念和摘要
- 细菌性脑膜炎可由多种封装细菌引起,包括流感嗜血杆菌、脑膜炎奈瑟菌、肺炎链球菌和无乳链球菌(B 组链球菌)。 流感杆菌主要影响幼儿和新生儿,脑膜炎杆菌是唯一的传染性病原体,主要影响儿童和青少年,肺炎杆菌主要影响幼儿,而无乳酸杆菌影响新生儿期间或不久之后出生后。
- 细菌性脑膜炎的症状包括发热、颈部僵硬、头痛、精神错乱、抽搐、昏迷和死亡。
- 细菌性脑膜炎的诊断是通过观察和培养脑脊液中的生物来做出的。 细菌性脑膜炎用抗生素治疗。 流感杆菌和脑膜炎球菌有疫苗可用。
- 梭状芽孢杆菌会产生干扰神经递质释放的强效神经毒素,从而导致神经系统疾病,包括肉毒中毒和破伤风。 PNS 通常会受到影响。 只有通过早期诊断,使用抗生素控制感染,使用抗生素在内毒素进入细胞之前将其中和,才能有效治疗梭状芽孢杆菌感染。
- 单核细胞增生李斯特菌是一种食源性病原体,可以感染中枢神经系统,导致脑膜炎。 感染可以通过胎盘传播给胎儿。 通过血液或脑脊液培养进行诊断。 用抗生素治疗,没有疫苗。
- 汉森氏病(麻风病)是由细胞内寄生虫麻风分枝杆菌引起的。 感染会导致神经元脱落,导致外周附属物和身体部位的感觉降低。 治疗采用多药抗生素疗法,没有普遍认可的疫苗。
脚注
- 1 Thigpen、Michael C.、Cynthia G. Whitney、Nancy E. Messonnier、伊丽莎白 ·R· 泽尔、露丝·林菲尔德、詹姆斯·哈德勒、李·哈里森等,“1998-2007 年美国的细菌性脑膜炎”,《新英格兰医学杂志》第 364 期,第 21 期(2011):2016-25。
- 2 波波维奇、T. 等。 世界卫生组织,《诊断脑膜炎奈瑟菌、肺炎链球菌和流感嗜血杆菌引起的脑膜炎实验室手册》,1999年。
- 3 美国疾病控制与预防中心,《脑膜炎球菌病》,2015年8月5日。 已于 2015 年 6 月 28 日访问。www.cdc.gov/meningococcal/sur... nce/index.html。
- 4 美国疾病控制与预防中心,“2016 年美国 0 至 18 岁人群的推荐免疫接种时间表”,2016 年 2 月 1 日。 已于 2016 年 6 月 28 日访问。www.cdc.gov/vaccines/schedule... dolescent.html。
- 5 全国脑膜炎协会,“美国大学校园中的血清B型脑膜炎球菌病疫情”,2016年。 已于 2016 年 6 月 28 日访问。 http://www.nmaus.org/disease-prevent...ase/outbreaks/。
- 6 美国卫生与公共服务部,“Hib(乙型流感嗜血杆菌)”,已于2016年6月28日访问。 http://www.vaccines.gov/diseases/hib/ #。
- 7 美国疾病控制与预防中心,“脑膜炎球菌病,疾病趋势”,2015。 已于 2016 年 9 月 13 日访问。www.cdc.gov/meningococcal/sur... nce/index.html。
- 8 Thigpen、Michael C.、Cynthia G. Whitney、Nancy E. Messonnier、伊丽莎白 ·R· 泽尔、露丝·林菲尔德、詹姆斯·哈德勒、李·哈里森等,“1998-2007 年美国的细菌性脑膜炎”,《新英格兰医学杂志》第 364 期,第 21 期(2011):2016-25。
- 9 Thigpen、Michael C.、Cynthia G. Whitney、Nancy E. Messonnier、伊丽莎白 ·R· 泽尔、露丝·林菲尔德、詹姆斯·哈德勒、李 H. Harrison 等,“1998-2007 年美国的细菌性脑膜炎”,《新英格兰医学杂志》,第 21 期(2011):2016-25;Heath、Paul T.、Gail Balfour、Abbie M.Weisner、Androulla Efstratiou、Theresa L. Lamagni、Helen Tighe、Liam AF O'Connell 等,“英国的 B 组链球菌病和 90 天以下的爱尔兰婴儿”,《柳叶刀》363,第 9405 号(2004):292-4。
- 10 人口基金、联合国儿童基金会世卫组织,“到2005年消灭孕产妇和新生儿破伤风”,2000年。www.unicef.org/immunization/f... tegy_paper.pdf。
- 11 美国疾病控制与预防中心,《破伤风疫苗接种》,2013年。 已于 2016 年 6 月 29 日访问。 http://www.cdc.gov/tetanus/vaccination.html。
- 12 Scallan、Elaine、Robert M. Hoekstra、Frederick J. Angulo、Robert V. Tauxe、Marc-Alain Widdowson、Sharon L. Roy、Jeffery L. Jones 和 Patricia M. Griffin,“在美国获得的食源性疾病——主要病原体”,新兴传染病 17,第 1 期(2011):7-15。
- 13 美国疾病控制与预防中心,《李斯特菌疫情》,2016 年。 已于 2016 年 6 月 29 日访问。 https://www.cdc.gov/listeria/outbreaks/index.html。
- 14 夏尔马、拉胡尔、普什彭德拉·辛格、W. J. Loughry、J. Mitchell Lockhart、W. Barry Inman、Malcolm S. Duthie、Maria T. Pena 等,“美国东南部的人畜共患麻风病”,《新兴传染病 21》,第 12 期(2015):2127-34。
- 15 世界卫生组织,《麻风病情况说明书》,2016年。 已于 2016 年 9 月 13 日访问。 http://www.who.int/mediacentre/factsheets/fs101/en/。
- 16 国家公园管理局,《卡劳帕帕简史》,已于 2016 年 2 月 2 日访问。www.nps.gov/kala/learn/Histor... -kalaupapa.htm。


