15.3: 毒力因子
- Page ID
- 200156
学习目标
- 解释毒力因素如何导致传染病的体征和症状
- 区分内毒素和外毒素
- 描述和区分各种类型的外毒素
- 描述病毒用于粘附和抗原变异的机制
在上一节中,我们解释了某些病原体比其他病原体更具毒性。 这是由于单个病原体产生的独特毒力因子,这些因素决定了它们可能引起的疾病的程度和严重程度。 病原体的毒力因子由基因编码,这些基因可以使用分子科赫的假设进行识别。 当编码毒力因子的基因失活时,病原体中的毒力就会降低。 在本节中,我们将研究毒性因子的各种类型和具体示例,以及它们如何影响发病机制的每个步骤。
粘附的毒力因子
如上一节所述,发病机制的前两个步骤是暴露和粘附。 回想一下,粘附素是一种存在于病原体表面的蛋白质或糖蛋白,它附着在宿主细胞上的受体上。 粘附素存在于细菌、病毒、真菌和原生动物病原体上。 细菌粘附素的一个例子是 1 型纤维粘附素,这种分子存在于产生肠毒素的大肠杆菌(ETEC)的纤维尖端。 回想一下,纤维是细胞表面的毛状蛋白质刷毛。 1 型纤维粘附素允许 ETEC 细胞的纤维附着在肠道上皮细胞上表达的甘露糖聚糖上。 下表\(\PageIndex{1}\)列出了我们已讨论或将在本章后面看到的一些病原体中发现的常见粘附素。
| 病原体 | 疾病 | 粘附素 | 附件网站 | |
|---|---|---|---|---|
| 化脓性链球菌 | 喉炎链球菌 | 蛋白质 F | 呼吸道上皮细胞 | |
| 变异链球菌 | 龋齿 | 粘合剂 P1 | 牙齿 | |
| 淋病奈瑟菌 | 淋病 | IV 型 pili | 尿道上皮细胞 | |
| 产生肠毒素的大肠杆菌 (ETEC) | 旅行者腹泻 | 1 型纤维 | 肠道上皮细胞 | |
| 霍乱弧菌 | 霍乱 | N-甲基苯丙氨酸 pili | 肠道上皮细胞 |
临床重点:第 3 部分
迈克尔血液中存在细菌是感染的征兆,因为血液通常是无菌的。 没有迹象表明细菌是通过受伤进入血液的。 相反,看来入口是胃肠道的入口。 根据迈克尔的症状、血液检查结果以及迈克尔是家庭中唯一一个吃过热狗的人这一事实,医生怀疑迈克尔患有李斯特菌病病例。
单核细胞增生李斯特菌是导致李斯特菌病的兼性细胞内病原体,是午餐肉类和乳制品等即食食品中的常见污染物。 一旦摄入,这些细菌就会侵入肠道上皮细胞并转移到肝脏,然后在肝细胞内生长。 利斯特菌病在大约五分之一的正常健康人中是致命的,而已经存在减弱免疫反应的疾病的患者的死亡率略高。 在致病岛上编码的一组毒性基因是造成单核细胞增生杆菌致病性的原因。 这些基因受一种称为肽链释放因子 1 (prFA) 的转录因子的调节。 prFA 调节的基因之一是 hyl,它编码一种叫做 listeriolysin O(LLO)的毒素,它允许细菌在进入宿主细胞时逃脱液泡。 prfA调控的第二个基因是A ctA,它编码一种称为肌动蛋白组装诱导蛋白(ActA)的表面蛋白。 ActA 在李斯特菌表面表达,聚合宿主肌动蛋白。 这使细菌能够产生肌动蛋白尾巴,在细胞的细胞质中移动,并在细胞之间扩散,而无需进入细胞外隔室。
迈克尔的病情已经开始恶化了。 他现在正经历脖子僵硬和偏瘫(身体一侧无力)。 由于担心感染正在蔓延,医生决定进行额外的检查,以确定是什么原因导致了这些新症状。
练习\(\PageIndex{1}\)
- 什么样的病原体会导致李斯特菌病,哪些毒性因素会导致迈克尔正在经历的体征和症状?
- 感染有可能从迈克尔的血液中传播吗? 如果是这样,这又如何解释他的新症状?
细菌外酶和毒素作为毒力因子
在暴露和粘附之后,发病机制的下一步是入侵,这可能涉及酶和毒素。 许多病原体通过进入血液实现入侵,这是一种有效的传播手段,因为血管靠近体内的每个细胞。 这种传播机制的缺点是血液中还包含许多免疫系统的元素。 以—emia结尾的各种术语用于描述血液中是否存在病原体。 血液中细菌的存在称为菌血症。 涉及化脓原(脓液形成细菌)的菌血症称为贫血。 当血液中发现病毒时,它被称为病毒血症。 毒血症一词描述了血液中发现毒素时的状况。 如果血液中既存在细菌又繁殖,这种情况称为败血症。
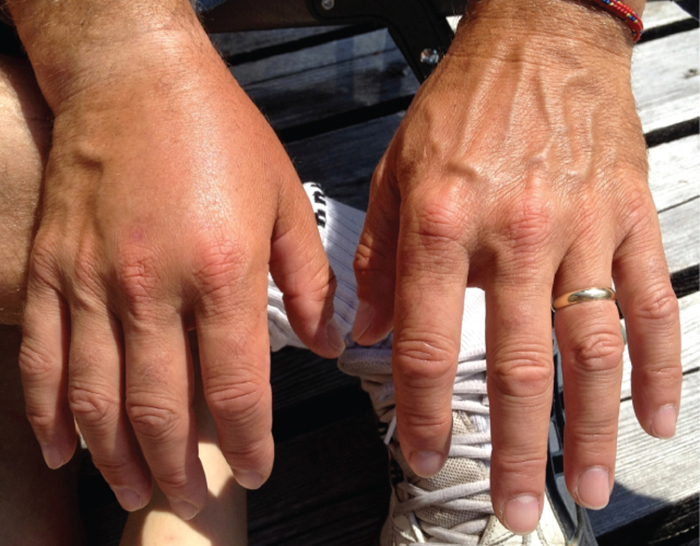
败血症患者被描述为败血症,可导致休克,这是一种危及生命的血压降低(收缩压<90 mm Hg),使细胞和器官无法获得足够的氧气和营养。 有些细菌可以通过释放毒素(可能导致组织损伤的毒性因子)引起休克,并导致低血压。 革兰氏阴性细菌被免疫系统吞噬,吞噬细胞然后释放肿瘤坏死因子,一种与炎症和发烧有关的分子。 肿瘤坏死因子与毛细血管结合以增加其渗透性,使液体从血管流入组织,从而导致肿胀或水肿(图\(\PageIndex{1}\))。 由于肿瘤坏死因子浓度高,炎症反应非常严重,循环系统流失了足够的液体,血压降至危险的低水平。 这可能会造成可怕的后果,因为心脏、肺部和肾脏依赖正常血压来维持正常的功能;因此,可能发生多器官衰竭、休克和死亡。
外酶
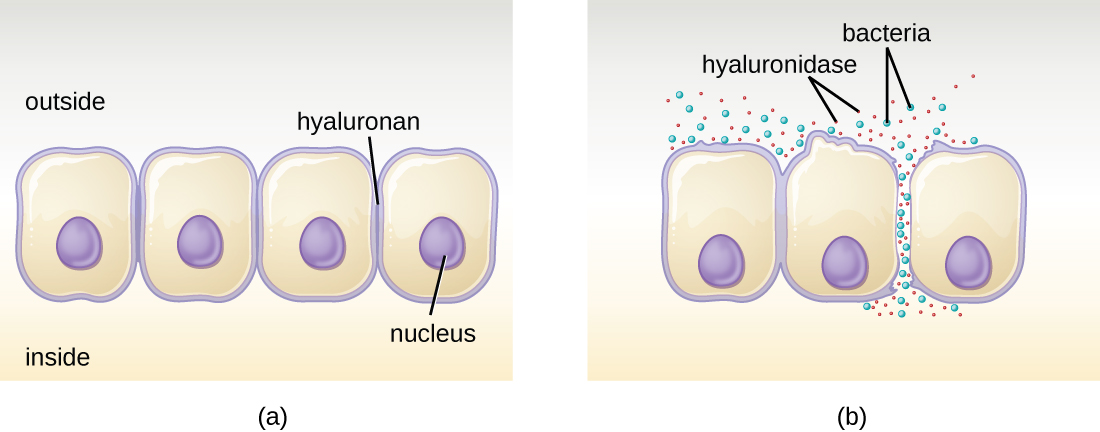
一些病原体会产生细胞外酶或外生酶,使它们能够侵入宿主细胞和更深层的组织。 外酶有各种各样的靶标。 表中列出了一些一般类别的外酶和相关病原体\(\PageIndex{2}\)。 这些外酶中的每一种都在特定的组织结构中起作用,以促进入侵或支持其自身的生长并抵御免疫系统。 例如,透明质酸酶 S 是一种由金黄色葡萄球菌、化脓性链球菌和产气荚膜梭状芽孢杆菌等病原体产生的酶,它会降解糖苷 hylauronan(透明质酸),后者充当结缔细胞中相邻细胞之间的细胞间粘合剂纸巾(图\(\PageIndex{2}\))。 这使病原体能够穿过入口处的组织层并在体内其他部位传播(图\(\PageIndex{2}\))。
| 班级 | 示例 | 函数 |
|---|---|---|
| 糖水解酶 | 金黄色葡萄球菌中的透明质酸酶 S | 降解透明质酸,透明质酸将细胞凝聚在一起,促进组织扩散 |
| 核酸酶 | 金黄色葡萄球菌产生的 DNase | 降解可捕获细菌的垂死细胞(细菌和宿主细胞)释放的 DNA,从而促进传播 |
| 磷脂酶 | 炭疽芽孢杆菌的磷脂酶 C | 降解宿主细胞的磷脂双层,导致细胞裂解,并降解吞噬体膜以使其能够逸出到细胞质中 |
| 蛋白酶 | 产气荚膜梭菌中的胶原酶 | 降解结缔组织中的胶原蛋白以促进传播 |
病原体产生的核酸酶,例如金黄色葡萄球菌产生的DNA酶,会降解细胞外DNA,以此作为逃逸和在组织中传播的一种手段。 当细菌和宿主细胞在感染部位死亡时,它们会裂解并释放细胞内内容物。 DNA染色体是细胞内最大的分子,大量的细胞外DNA可以捕获细菌并阻止其传播。 金黄@@ 色葡萄球菌会产生 DNase 来降解细胞外 DNA 的网格,因此它可以逃脱并扩散到邻近的组织。 金黄色葡萄球菌和其他病原体也使用这种策略来降解和逃离免疫系统吞噬细胞产生的细胞外DNA网,以捕获细菌。
降解细胞膜磷脂的酶称为磷脂酶。 它们的作用取决于它们作用的磷脂类型以及它们在何处酶解分子。 造成炭疽的病原体 B. anthracis 会产生磷脂酶 C。当炭疽杆菌被免疫系统的吞噬细胞摄入时,磷脂酶 C 在吞噬体与溶酶体融合之前会降解吞噬体的膜,从而使病原体逸出到细胞质和繁殖。 磷脂酶还可以靶向包围吞噬细胞内吞噬体的膜。 如本章前面所述,这是单核细胞增生杆菌和立克次体等细胞内病原体用来逃避吞噬体并在吞噬细胞的细胞质中繁殖的机制。 磷脂酶在细菌毒力中的作用不仅限于吞噬体逃逸。 许多病原体会产生磷脂酶,其作用是降解细胞膜并导致靶细胞裂解。 这些磷脂酶参与红细胞、白细胞和组织细胞的裂解。
细菌病原体还会产生各种蛋白质消化酶或蛋白酶。 蛋白酶可以根据其底物靶点进行分类(例如,丝氨酸蛋白酶靶向氨基酸丝氨酸的蛋白),或者它们的活性位点是否含有金属(例如,锌金属蛋白酶含有锌离子,这是酶活性所必需的)。
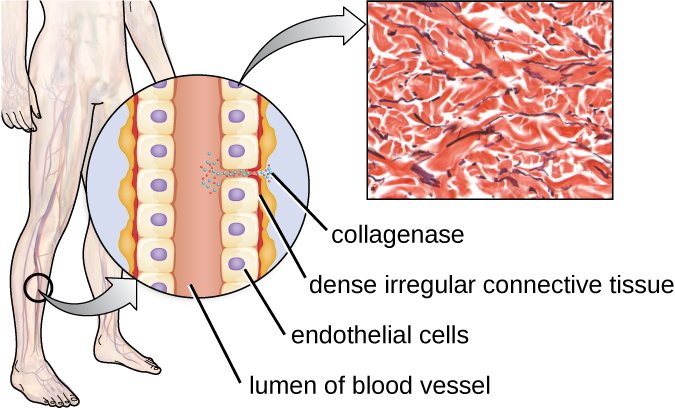
含有金属离子的蛋白酶的一个例子是外酶胶原酶。 胶原酶消化胶原蛋白,这是结缔组织中的显性蛋白。 胶原蛋白可以在细胞外基质中找到,尤其是在粘膜、血管、神经和皮肤层附近。 与透明质酸酶类似,胶原酶允许病原体通过消化这种结缔组织蛋白穿透宿主组织并扩散。 例如,革兰氏阳性细菌产气荚膜梭菌产生的胶原酶允许细菌穿过组织层,然后进入血液并在血液中繁殖(败血症)。 然后,产@@ 气荚膜梭菌使用毒素和磷脂酶引起细胞裂解和坏死。 一旦宿主细胞死亡,细菌就会通过发酵肌肉碳水化合物产生气体。 组织和伴随气体的广泛坏死是被称为气性坏疽的病症的特征(图\(\PageIndex{3}\))。
毒素
除外源酶外,某些病原体还能够产生毒素,即有助于其入侵和损害组织的生物毒药。 病原体产生毒素对宿主细胞造成损害的能力称为毒性。
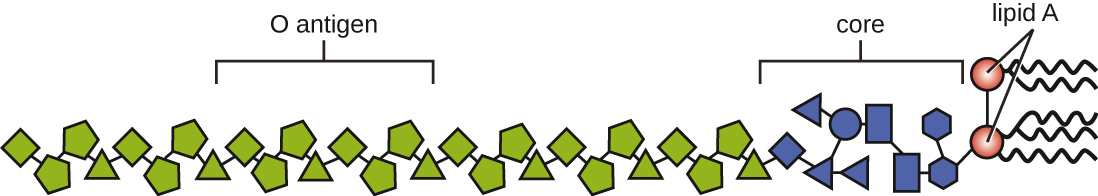
毒素可以分为内毒素或外毒素。 在革兰氏阴性细菌外膜上发现的脂多糖(LPS)称为内毒素(图\(\PageIndex{4}\))。 在感染和发病期间,革兰氏阴性细菌病原体会在细胞死亡导致膜分解或细菌经历二元裂变时释放内毒素。 内毒素的脂质成分脂质A是造成LPS分子毒性特性的原因。 不同属的革兰氏阴性细菌中的脂质A相对保守;因此,无论革兰氏阴性病原体如何,脂质A的毒性特性都是相似的。 脂质A以与肿瘤坏死因子相似的方式触发免疫系统的炎症反应(参见炎症和发热)。 如果体内毒素浓度低,炎症反应可以为宿主提供有效的感染防御;另一方面,血液中高浓度的内毒素会导致过度的炎症反应,导致血压严重下降,多器官失败和死亡。
检测内毒素的经典方法是使用 Limulus amebocyte 裂解物(LAL)测试。 在这个过程中,马蹄蟹(Limulus polyphemus)的血细胞(amebocytes)与患者的血清混合。 amebocytes 会对任何内毒素的存在做出反应。 这种反应既可以通过显色性(颜色)观察,也可以通过寻找血清中发生的凝血(凝血反应)来观察。 已经使用的另一种方法是使用抗体检测内毒素的酶联免疫吸附试验(ELISA)。
与内毒素的有毒脂质 A 不同,外毒素是由各种活的致病细菌产生的蛋白质分子。 尽管一些革兰氏阴性病原体会产生外毒素,但大多数是由革兰氏阳性病原体产生的。 表中总结了外毒素在其他几个关键特征上与内毒素的区别\(\PageIndex{3}\)。 与内毒素相比,内毒素在释放时会刺激一般的全身炎症反应,而外毒素的作用和与之相互作用的细胞要具体得多。 每种外毒素都靶向特定细胞上的特定受体,并通过独特的分子机制破坏这些细胞。 内毒素在高温下保持稳定,需要在 121 °C (250 °F) 下加热 45 分钟才能失活。 相比之下,大多数外毒素由于其蛋白质结构而具有耐热性,许多外毒素在高于41°C(106°F)的温度下会变性(失活)。 如前所述,内毒素可以在非常高的浓度下刺激致命的炎症反应,测得的 LD 50 为 0.24 mg/kg。 相比之下,极少浓度的外毒素可能致命。 例如,导致肉毒中毒的肉毒杆菌毒素的 LD 50 为 0.000001 mg/kg(致死性是内毒素的 240,000 倍)。
| 特点 | 内毒素 | 外毒素 |
|---|---|---|
| 来源 | 革兰氏阴性细菌 | 革兰氏阳性(主要)和革兰氏阴性细菌 |
| 构图 | 脂质脂质脂多糖的A成分 | 蛋白质 |
| 对宿主的影响 | 炎症和发烧的一般全身症状 | 对细胞的特异性损伤取决于受体介导的细胞靶向和特定的作用机制 |
| 热稳定性 | 热稳定 | 大多数都不耐热,但有些是热稳定的 |
| LD 50 | 高 | 低 |
外毒素可以根据其靶标分为三类:细胞内靶向、膜干扰和超抗原。 表中\(\PageIndex{4}\)列出了这三个类别中每个类别中特征明确的毒素示例。
| 类别 | 示例 | 病原体 | 机制与疾病 |
|---|---|---|---|
| 细胞内靶向毒素 | 霍乱毒素 | 霍乱弧菌 | 肠道细胞中腺苷酸环化酶的激活,导致环状腺苷一磷酸盐(cAMP)水平升高,细胞内分泌液体和电解质,导致腹泻 |
| 破伤风毒素 | 梭菌 teta ni | 抑制中枢神经系统中抑制性神经递质的释放,导致痉挛性麻痹 | |
| 肉毒毒素 | 肉毒梭菌 | 抑制神经元释放神经递质乙酰胆碱,导致松弛性麻痹 | |
| 白喉毒素 | 白喉棒状杆菌 | 抑制蛋白质合成,导致细胞死亡 | |
| 破坏膜的毒素 | 链球菌溶素 | 化脓性链球菌 | 在细胞膜中聚集成孔隙的蛋白质,破坏其功能并杀死细胞 |
| Pneumolysin | 肺炎链球菌 | ||
| α-毒素 | 金黄色葡萄球菌 | ||
| α-毒素 | 产气荚膜梭菌 | 降解细胞膜磷脂、破坏膜功能和杀死细胞的磷脂酶 | |
| 磷脂酶 C | 铜绿假单胞菌 | ||
| β毒素 | 金黄色葡萄球菌 | ||
| 超抗原 | 毒性休克综合征毒素 | 金黄色葡萄球菌 | 刺激免疫系统细胞的过度激活和免疫系统细胞释放细胞因子(化学介质)。 结果是危及生命的发烧、炎症和休克。 |
| 链球菌有丝分裂外毒素 | 化脓性链球菌 | ||
| 链球菌热原毒素 | 化脓性链球菌 |
细胞内靶向毒素包括两个成分:A代表活性,B用于结合。 因此,这些类型的毒素被称为 A-B 外毒素(图\(\PageIndex{5}\))。 B 成分负责毒素的细胞特异性,介导毒素与特定细胞表面受体的初始附着。 一旦 A-B 毒素与宿主细胞结合,就会通过内吞作用将其带入细胞并被液泡困住。 随着液泡酸化,A 和 B 亚基分离。 然后,A 亚单位进入细胞质并干扰其靶向的特定内部细胞功能。
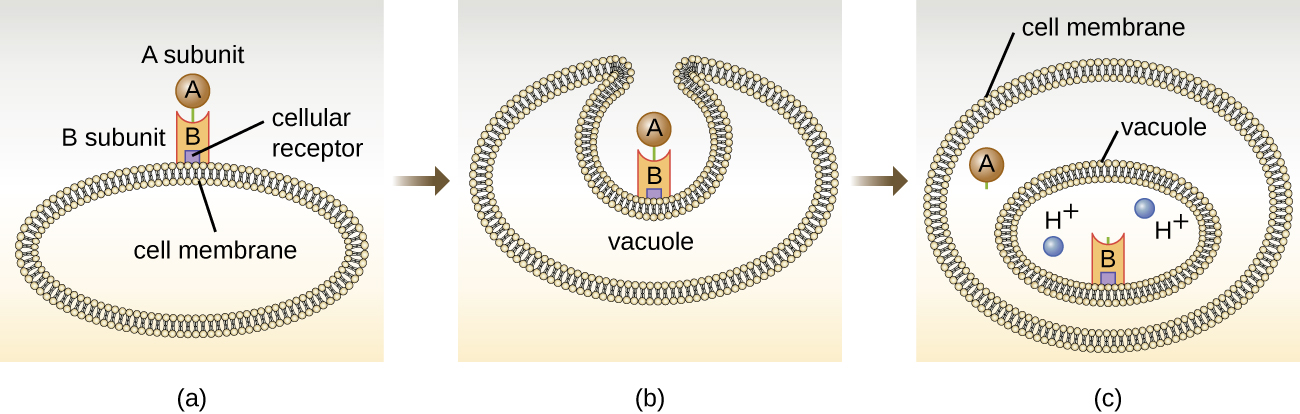
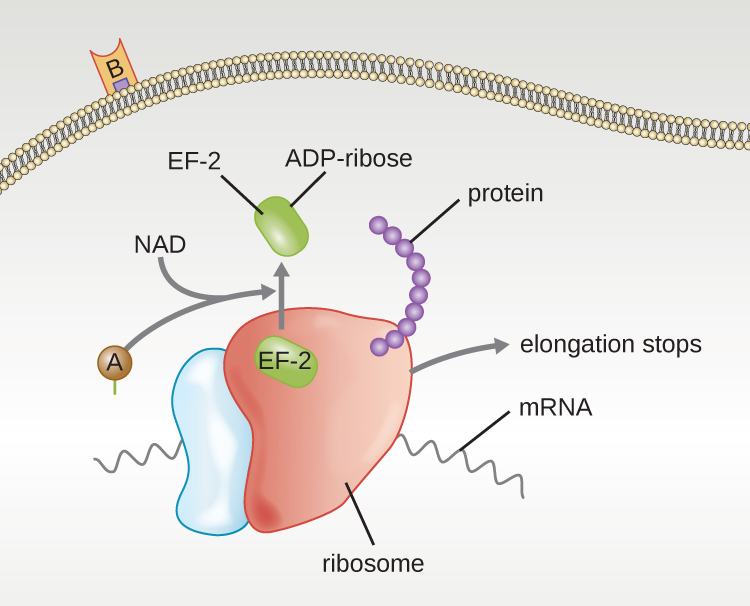
A-B 毒素的四个独特例子是白喉、霍乱、肉毒杆菌和破伤风毒素。 白喉毒素由革兰氏阳性细菌 Corynebacterium diphtheriae 产生,它是鼻咽和皮肤白喉的病原体。 在白喉毒素的A亚单位分离并获得细胞质途径后,它促进二磷酸腺苷(ADP)-核糖转移到蛋白质合成所需的伸长因子蛋白(EF-2)上。 因此,白喉毒素抑制宿主细胞中的蛋白质合成,最终杀死细胞(图\(\PageIndex{6}\))。
霍乱毒素是由革兰氏阴性细菌霍乱弧菌产生的肠毒素,由一个 A 亚单位和五个 B 亚单位组成。 霍乱毒素的作用机制很复杂。 B 亚单位与小肠肠上皮细胞上的受体结合。 进入上皮细胞的细胞质后,A 亚单位激活细胞内 G 蛋白。 反过来,活化的G蛋白会导致腺苷环化酶的激活,该酶开始增加环AMP(一种次要信使分子)的浓度。 cAMP 的增加破坏了肠道上皮细胞的正常生理,导致它们向肠道内腔分泌过量的液体和电解质,从而导致霍乱特有的严重 “水稻粪便” 腹泻。
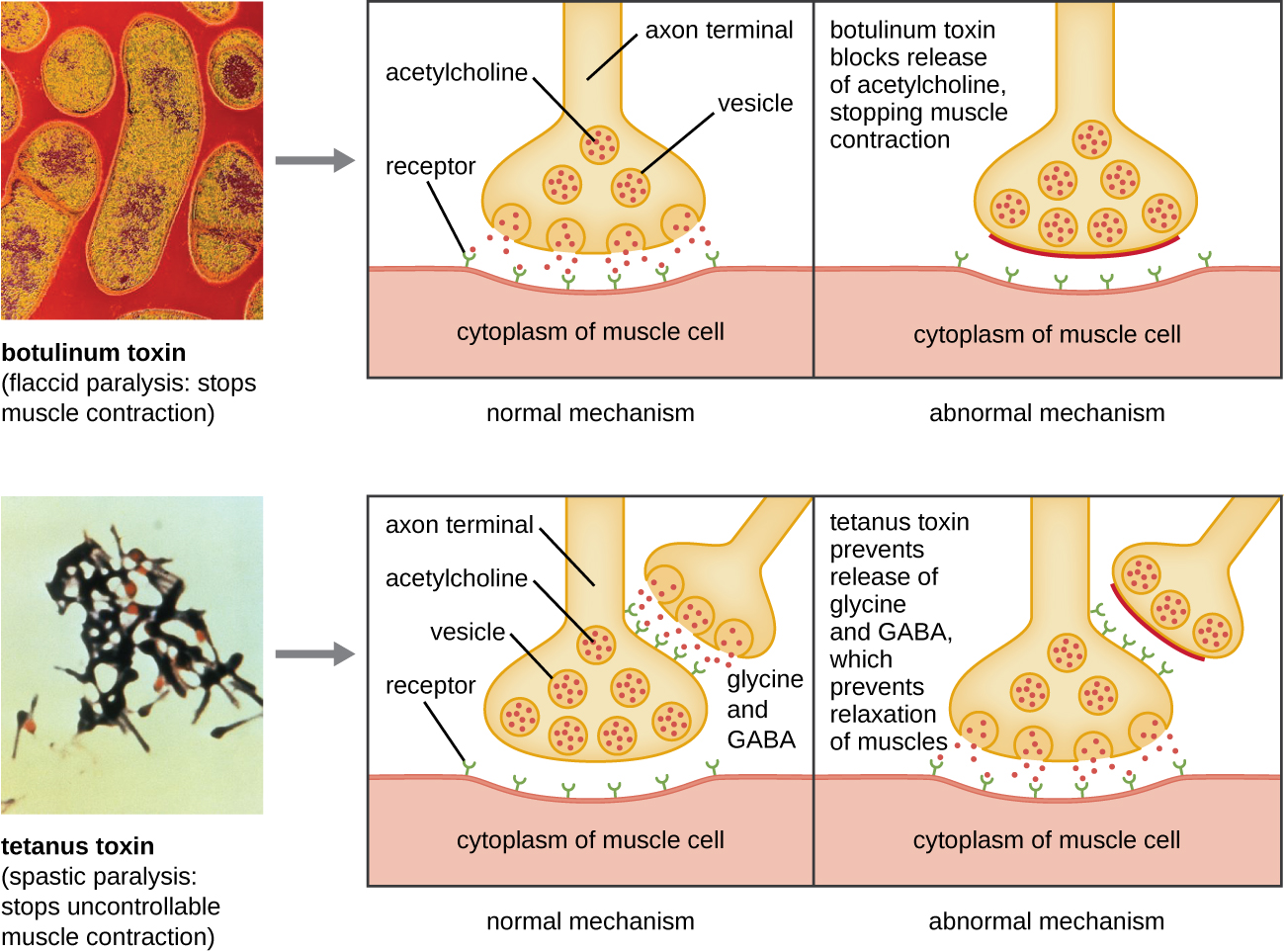
肉毒杆菌毒素(也称为肉毒杆菌毒素)是由革兰氏阳性细菌肉毒梭菌产生的神经毒素。 它是迄今为止已知最剧毒的物质。 毒素由轻 A 亚单位和重蛋白链 B 亚单位组成。 B 亚单位与神经元结合,允许肉毒杆菌毒素进入神经肌肉交界处的神经元。 A 亚单位充当蛋白酶,分解参与神经元释放神经递质分子乙酰胆碱的蛋白质。 通常,神经元释放乙酰胆碱以诱导肌肉纤维收缩。 毒素阻断乙酰胆碱释放的能力会抑制肌肉收缩,从而导致肌肉松弛。 这有可能停止呼吸并导致死亡。 由于其作用,低浓度的肉毒杆菌毒素用于美容和医疗手术,包括去除皱纹和治疗膀胱过度活跃。
另一种神经毒素是破伤风毒素,它由革兰氏阳性细菌破伤风梭状芽孢杆菌产生。 这种毒素还具有轻A亚基和重蛋白链B亚单位。 与肉毒杆菌毒素不同,破伤风毒素与抑制性中间神经元结合,后者负责释放抑制性神经递质甘氨酸和γ-氨基丁酸(GABA)。 通常,这些神经递质与神经肌肉交界处的神经元结合,从而抑制乙酰胆碱的释放。 破伤风毒素抑制中间神经元释放甘氨酸和GABA,导致肌肉永久收缩。 第一个症状通常是下巴僵硬(下巴锁紧)。 随之而来的是身体其他部位的剧烈肌肉痉挛,通常最终导致呼吸衰竭和死亡。 图\(\PageIndex{7}\)显示了肉毒杆菌和破伤风毒素的作用。
破坏膜的毒素通过形成毛孔或破坏宿主细胞膜中的磷脂双层来影响细胞膜功能。 两种破坏膜的外毒素是溶血素和白细胞杀素,它们在细胞膜中形成毛孔,导致细胞质内容物泄漏和细胞裂解。 这些毒素最初被认为分别靶向红细胞(红细胞)和白细胞(白细胞),但我们现在知道它们也可以影响其他细胞。 革兰氏阳性细菌化脓性链球菌产生链球菌溶血素,即水溶性溶血素,与宿主细胞膜中的胆固醇部分结合形成毛孔。 两种类型的链球溶素 O 和 S 根据它们在缺氧或存在氧气的情况下引起红细胞溶血的能力进行分类。 链球菌溶素O在有氧的情况下不活跃,而链球菌溶解素S在有氧气的情况下是活性的。 其他重要的气孔形成膜干扰毒素包括金黄色葡萄球菌的α毒素和肺炎链球菌的肺溶素。
细菌磷脂酶是破坏膜的毒素,它会降解细胞膜的磷脂双层,而不是形成毛孔。 我们已经讨论了与炭疽杆菌、嗜肺杆菌和立克次体物种相关的磷脂酶,这些磷脂酶使这些细菌能够起到吞噬体的裂解作用。 同样的磷脂酶也是溶血素。 其他起溶血素作用的磷脂酶包括产气荚膜梭菌的α毒素、铜绿杆菌的磷脂酶C和金黄色葡萄球菌的β毒素。
一些金黄色葡萄球菌菌株还会产生一种叫做 Panton-Valentine leukocidin(PVL)的白杀素。 PVL 由两个亚基组成,即 S 和 F。S 成分的作用类似于 A-B 外毒素的 B 亚单位,因为它与动物细胞外质膜上的糖脂结合。 F 成分的作用类似于 A-B 外毒素的 A 亚单位,具有酶活性。 毒素会插入并组装到膜的孔隙中。 编码 PVL 的基因更常见于引起皮肤感染和肺炎的金黄色葡萄球菌菌株中。 1 PVL 通过引起水肿、红斑(血管扩张导致皮肤变红)和皮肤坏死来促进皮肤感染。 PVL 也被证明会导致坏死性肺炎。 PVL 促进对肺泡白细胞的促炎和细胞毒性作用。 这会导致酶从白细胞中释放,这反过来又会对肺组织造成损害。
第三类外毒素是超抗原。 这些外毒素会引发免疫细胞的过度非特异性刺激,从而分泌细胞因子(化学信使)。 细胞因子的过量产生,通常被称为细胞因子风暴,会引起强烈的免疫和炎症反应,可能导致危及生命的高热、低血压、多器官衰竭、休克和死亡。 原型超抗原是金黄色葡萄球菌的毒性休克综合征毒素。 大多数中毒性休克综合征病例与月经期女性产生毒素的金黄色葡萄球菌的阴道定植有关;但是,也可能发生其他身体部位的定植。 一些化脓性链球菌菌株也会产生超抗原;它们被称为链球菌有丝分裂外毒素和链球菌热原毒素。
练习\(\PageIndex{2}\)
- 描述外酶如何促进细菌入侵。
- 解释外毒素和内毒素的区别。
- 命名三类外毒素。
影响宿主存活和免疫逃避的毒力因子
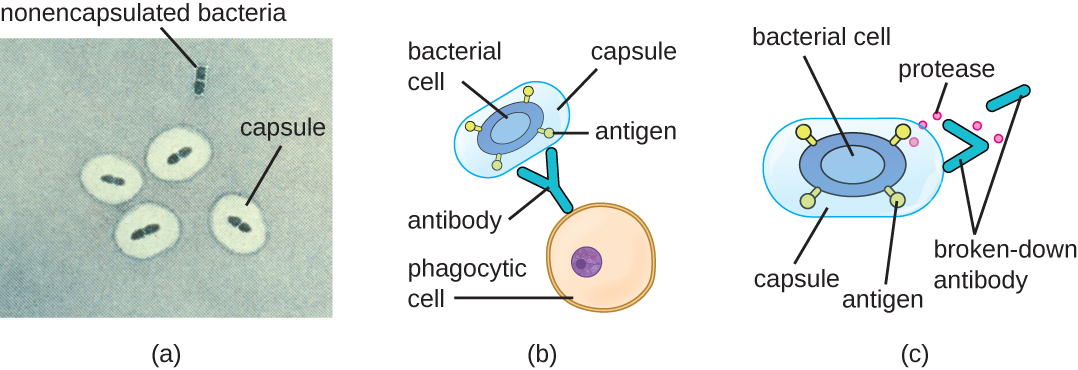
逃避免疫系统对侵入性也很重要。 细菌使用各种毒力因子来逃避免疫系统细胞的吞噬作用。 例如,许多细菌会产生胶囊,这些胶囊用于粘附,但也可以通过防止吞噬细胞摄入来帮助逃避免疫。 胶囊的成分阻止免疫细胞粘附然后吞噬细胞。 此外,胶囊会使细菌细胞变大,使免疫细胞更难吞没病原体(图\(\PageIndex{8}\))。 一种值得注意的产生胶囊的细菌是革兰氏阳性病原体肺炎链球菌,它会导致肺炎球菌肺炎、脑膜炎、败血症和其他呼吸道感染。 封装的肺炎球菌菌株比未封装的菌株毒性更强,更有可能侵入血液并引起败血症和脑膜炎。
一些病原体还可以产生蛋白酶来保护自己免受吞噬作用。 如适应性特异性宿主防御中所述,人体免疫系统产生的抗体与特定细菌(例如胶囊、纤维、鞭毛、脂多糖)上发现的表面分子结合。 这种结合启动吞噬作用和其他抗菌杀死和清除机制。 蛋白酶通过攻击和消化抗体分子来对抗抗体介导的杀伤和清除(图\(\PageIndex{8}\))。
除了胶囊和蛋白酶外,一些细菌病原体还会产生其他毒力因子,使它们能够逃避免疫系统。 某些种类的链球菌的纤维含有 M 蛋白,它会改变链球菌的表面,通过阻断帮助吞噬细胞摄入细菌病原体的补体分子的结合来抑制吞噬作用。 耐酸细菌结核分枝杆菌(结核病的病原体)在其细胞包膜中产生一种称为霉菌酸的蜡状物质。 当细菌被肺中的吞噬细胞吞没时,保护性的霉菌酸涂层使细菌能够抵抗吞噬体内的某些杀伤机制。
一些细菌会产生毒性因子,通过利用宿主自然产生的分子来促进感染。 例如,大多数金黄色葡萄球菌菌株会产生外酶凝固酶,该酶利用血液凝固的自然机制逃避免疫系统。 通常,血液凝固是由于血管损伤而触发的;血小板开始堵塞血块,然后发生一系列反应,其中纤维蛋白原(一种由肝脏产生的可溶性蛋白)被分解成纤维蛋白。 纤维蛋白是一种不溶性的线状蛋白,它与血小板结合,交联并收缩形成结块的血小板和红细胞网。 由此产生的血块可防止受损血管进一步流失血液。 但是,如果细菌将凝血酶释放到血液中,则会在没有血管损伤的情况下触发纤维蛋白原到纤维蛋白的级联。 由此产生的血块将细菌覆盖在纤维蛋白中,保护细菌免受血液中循环的吞噬免疫细胞的暴露。
凝血酶会导致血液凝结,而激酶的作用恰恰相反,它会触发纤溶酶原转化为纤溶酶,而纤溶酶参与纤维蛋白凝块的消化。 通过消化血块,激酶允许被困在血块中的病原体逃脱和传播,类似于胶原酶、透明质酸酶和脱氧核糖核酸酶促进感染传播的方式。 激酶的例子包括葡萄球菌和链激酶,分别由金黄色葡萄球菌和化脓性链球菌产生。 有趣的是,金黄色葡萄球菌既可以产生促进凝血的凝血酶,也可以产生刺激血块消化的葡萄球激酶。 凝血酶的作用为免疫系统提供了重要的保护屏障,但是当营养供应减少或其他情况表明病原体需要逃脱和传播时,葡萄糖激酶的产生可以启动这一过程。
病原体可以用来保护自己免受免疫系统侵害的最后一种机制称为抗原变异,即表面蛋白质的改变,使宿主的免疫系统不再识别病原体。 例如,Borr elia burgdorferi 细菌是莱姆病的病原体,它含有一种称为VLSE的表面脂蛋白。 由于 DNA 复制和修复过程中的基因重组,这种细菌蛋白会经历抗原变异。 每次发烧时,B. burgdorferi 中的 vLSE 蛋白差异很大,以至于针对先前 vLSE 序列的抗体无效。 据信,vLSE 的这种变异促成了 B. burgdorferi 引起慢性病的能力。 另一种使用抗原变异来避开免疫系统的重要人类细菌病原体是淋病奈瑟菌,它会导致性传播疾病淋病。 众所周知,这种细菌能够经受IV型pili的抗原变异以避免免疫防御。
练习\(\PageIndex{3}\)
- 列举胶囊提供免疫系统保护的至少两种方式。
- 除了胶囊之外,还要列举细菌用来逃避免疫系统的另外两种毒力因子。
临床重点:分辨率
根据迈克尔报告的脖子僵硬和偏瘫的症状,医生怀疑感染可能已经扩散到他的神经系统。 医生决定下令使用脊柱抽水器来寻找任何可能侵入脑膜和脑脊液(CSF)的细菌,这些细菌通常是无菌的。 为了进行脊柱抽打,用碘消毒剂擦拭迈克尔的下背部,然后用无菌床单覆盖。 临床医生戴着手套的双手将针头无菌地从制造商的密封塑料包装中取出。 插入针头,少量液体被吸入连接的样品管中。 管子被拆下,盖上盖子,并在上面贴上带有迈克尔数据的准备好的标签。 该STAT(需要紧急或立即分析)标本分为三个独立的无菌管,每根含有 1 mL 的脑脊液。 这些试管立即被送到医院的实验室,在临床化学、血液学和微生物学部门进行分析。 所有三个科室的初步结果都表明发生了脑脊液感染,微生物学部门报告说,迈克尔脑脊液中存在革兰氏阳性棒。
这些结果证实了他的医生的怀疑:迈克尔的新症状是脑膜炎的结果,脑膜炎是保护大脑和脊髓的膜急性炎症。 由于脑膜炎可能危及生命,并且由于第一种抗生素疗法无法有效防止感染传播,迈克尔开了两种抗生素(氨苄青霉素和庆大霉素)的激进疗程,通过静脉注射。 迈克尔在医院待了好几天,接受支持性护理和观察。 一周后,他被允许回家卧床休息和口服抗生素。 经过3周的治疗,他完全康复。
病毒毒力
尽管病毒病原体在结构上与细菌病原体不相似,但促成其毒力的某些特性是相似的。 病毒使用粘附素来促进对宿主细胞的粘附,而某些包膜病毒则依赖抗原变异来避免宿主的免疫防御。 以下各节将更详细地讨论这些毒性因素。
病毒粘附剂
任何病毒感染的第一步是将病毒粘附到细胞表面的特定受体上。 这个过程由作为病毒衣壳或膜包膜一部分的粘附素介导。 病毒粘附素与特定细胞受体的相互作用决定了病毒对体内特定细胞、组织和器官的向性(优先靶向)。 流感病毒上发现的刺突蛋白血凝素是病毒粘附素的一个例子;它允许病毒与宿主呼吸道和肠道细胞膜上的唾液酸结合。 另一种病毒粘附素是HIV上发现的糖蛋白gp20。 要使HIV感染免疫系统的细胞,它必须与细胞表面的两种受体相互作用。 第一种相互作用涉及gp120与一些基本免疫系统细胞中发现的CD4细胞标志物之间的结合。 但是,在病毒进入细胞之前,gp120 与两种趋化因子受体之一(CCR5 和 CXCR4)之间必须发生第二次相互作用。 表中\(\PageIndex{5}\)列出了一些常见病毒病原体的粘附素以及这些粘附素允许病毒附着的特定部位。
| 病原体 | 疾病 | 粘附素 | 附件网站 |
|---|---|---|---|
| 流感病毒 | 流感 | 血凝素 | 呼吸道和肠道细胞中的唾液酸 |
| 单纯疱疹病毒 I 或 II | 口腔疱疹、生殖器疱疹 | 糖蛋白 gB、gC、gD | 口腔粘膜表面和生殖器上的硫酸肝素 |
| 人类免疫缺陷病毒 | 艾滋病毒/艾滋病 | 糖蛋白 gp120 | 免疫系统细胞的 CD4 和 CCR5 或 CXCR4 |
病毒的抗原变异
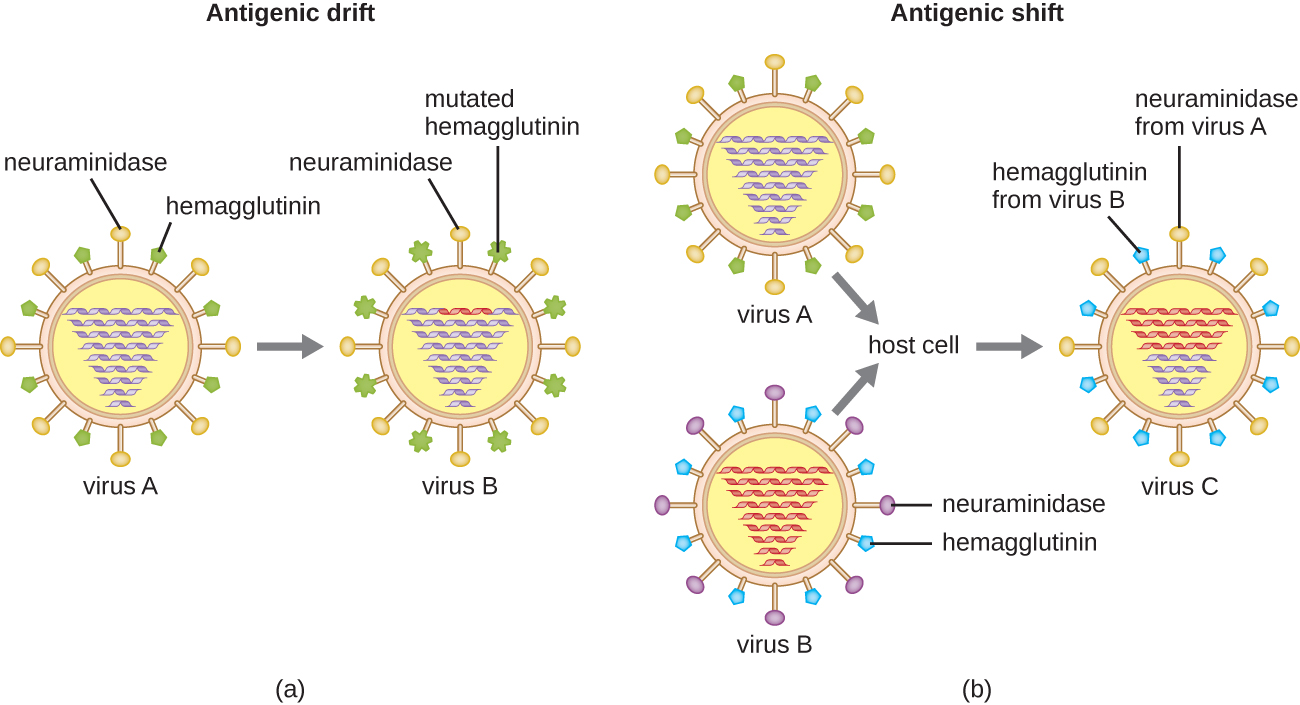
抗原变异也出现在某些类型的包膜病毒中,包括流感病毒,它们表现出两种形式的抗原变异:抗原漂移和抗原移动(图\(\PageIndex{9}\))。 抗原漂移是点突变导致尖峰蛋白血凝素(H)和神经氨酸酶(N)发生轻微变化的结果。 另一方面,抗原转移是由于基因重组导致的刺突蛋白的重大变化。 这种抗原转移的重组通常发生在两种不同的流感病毒感染同一个宿主时。
流感病毒的抗原变异率非常高,这使得免疫系统难以识别流感病毒的许多不同菌株。 尽管人体可能通过自然暴露或疫苗接种对一种菌株产生免疫力,但抗原变异会导致免疫系统无法识别的新菌株不断出现。 这是必须每年接种流感病毒疫苗的主要原因。 每年的流感疫苗都能针对当年最流行的菌株提供保护,但新的或不同的菌株在第二年可能会更流行。
有关抗原移位和漂移如何发生的另一种解释,请观看此视频。
练习\(\PageIndex{4}\)
- 描述粘附素在病毒向性中的作用。
- 解释抗原漂移和抗原移位之间的区别。
关键概念和摘要
毒力因子有助于病原体引起疾病的能力。 外酶和毒素允许病原体侵入宿主组织并造成组织损伤。 外酶根据其靶向的大分子进行分类,而外毒素则根据其作用机制进行分类。 细菌毒素包括内毒素和外毒素。 内毒素是革兰氏阴性细胞包膜脂多糖的脂质A成分。 外毒素是主要由革兰氏阳性细菌分泌的蛋白质,但也由革兰氏阴性细菌分泌。 细菌病原体可能通过产生胶囊以避免吞噬作用、在吞噬细胞的细胞内环境中存活、降解抗体或通过抗原变异来逃避宿主的免疫反应。 病毒病原体使用粘附素引发感染,使用抗原变异来避免免疫防御。 流感病毒同时使用抗原漂移和抗原转移来避免被免疫系统识别。
脚注
- 1 V. Meka。 “Panton-Valentine Leukocidin。” http://www.antimicrobe.org/h04c.file...L-S-aureus.asp


