6.2: 病毒生命周期
- Page ID
- 200059
学习目标
- 描述裂解和溶解生命周期
- 描述动物病毒的复制过程
- 描述逆转录病毒和潜伏病毒的独特特征
- 讨论人类病毒及其病毒与宿主细胞的相互作用
- 解释转导过程
- 描述植物病毒的复制过程
所有病毒都依赖细胞进行繁殖和代谢过程。 病毒本身并不能对病毒复制所需的所有酶进行编码。 但是在宿主细胞内,病毒可以占用细胞机制来产生更多的病毒颗粒。 噬菌体只能在细胞质中复制,因为原核细胞没有细胞核或细胞器。 在真核细胞中,大多数DNA病毒都可以在细胞核内复制,但可以在细胞质中复制的大型DNA病毒(例如痘病毒)中观察到例外。 感染动物细胞的 RNA 病毒通常在细胞质中复制。
带有原核生物宿主的病毒的生命周期
噬菌体的生命周期一直是了解病毒如何影响其感染细胞的好模型,因为已经观察到真核病毒的类似过程,真核病毒可能立即导致细胞死亡或形成潜伏或慢性感染。 毒性噬菌体通常通过细胞裂解导致细胞死亡。 另一方面,温带噬菌体可以成为宿主染色体的一部分,并与细胞基因组一起复制,直到它们被诱导制造出新组装的病毒或后代病毒。
Lytic Cycle
在毒噬菌体的裂解周期中,噬菌体接管细胞,繁殖新的噬菌体并摧毁细胞。 T-even 噬菌体就是一类特征明确的毒性噬菌体的一个很好的例子。 噬菌体溶解周期分为五个阶段(见图\(\PageIndex{1}\))。 附着是感染过程中的第一阶段,在这个阶段中,噬菌体与特定的细菌表面受体(例如宿主表面的脂多糖和 OmpC 蛋白)相互作用。 大多数噬菌体的宿主范围很窄,可能会感染一种细菌或一个物种中的一种菌株。 这种独特的识别可用于通过噬菌体疗法对细菌感染进行靶向治疗,或用于噬菌体分型以识别独特的细菌亚种或菌株。 感染的第二阶段是进入或渗透。 这是通过尾鞘收缩而发生的,尾鞘就像皮下注射针头一样,通过细胞壁和膜注射病毒基因组。 噬菌体头和剩余成分残留在细菌之外。
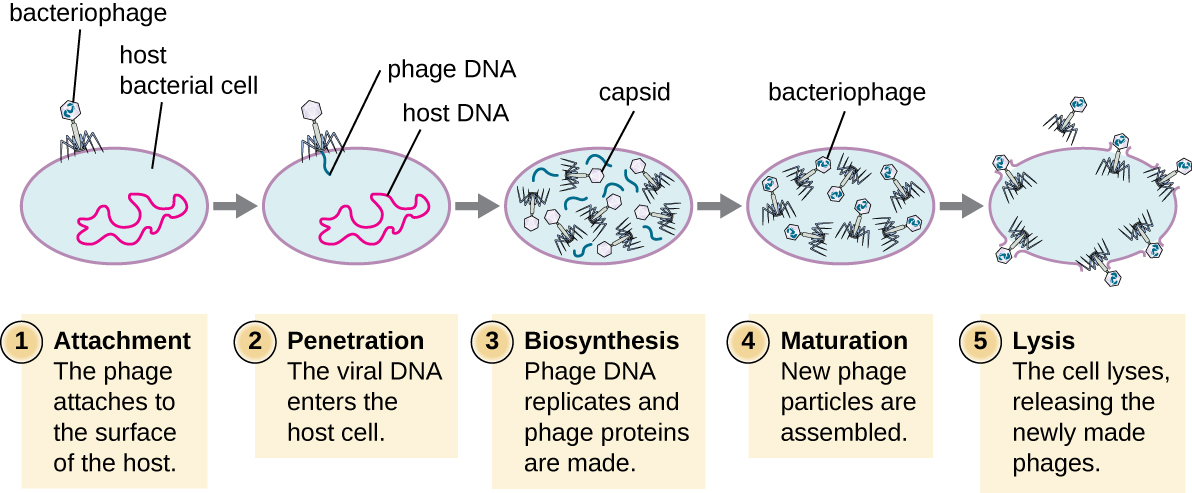
感染的第三阶段是新病毒成分的生物合成。 进入宿主细胞后,病毒合成病毒编码的内切核酸酶以降解细菌染色体。 然后,它劫持宿主细胞,以复制、转录和翻译组装新病毒所需的病毒成分(capsomeres、鞘层、基板、尾纤维和病毒酶)。 聚合酶基因通常在周期的早期表达,而衣壳和尾蛋白则在晚些时候表达。 在成熟阶段,会产生新的病毒体。 为了释放游离的噬菌体,细菌细胞壁会被噬菌体蛋白(如霍林或溶菌酶)破坏。 最后阶段是发布。 成熟病毒通过一种称为裂解的过程从宿主细胞中爆发,后代病毒被释放到环境中以感染新细胞。
溶解循环
在溶解循环中,噬菌体基因组也通过附着和渗透进入细胞。 具有这种生命周期的噬菌体的一个典型例子是 lambda 噬菌体。 在溶解循环中,噬菌体基因组不是杀死宿主,而是整合到细菌染色体中并成为宿主的一部分。 整合的噬菌体基因组被称为预言。 带有预言的细菌宿主被称为溶菌原。 细菌被温带噬菌体感染的过程称为溶菌发育。 温带噬菌体通常在细胞内处于潜伏状态或不活跃状态。 当细菌复制其染色体时,它还会复制噬菌体的DNA,并在繁殖过程中将其传递给新的子细胞。 噬菌体的存在可能会改变细菌的表型,因为它可以带来额外的基因(例如,可以增加细菌毒力的毒素基因)。 宿主表型的这种变化称为溶原转化或噬菌体转化。 有些细菌,例如霍乱弧菌和肉毒梭菌,在没有预言的情况下,毒性会降低。 感染这些细菌的噬菌体携带其基因组中的毒素基因,并在毒素基因表达时增强宿主的毒力。 就霍乱杆菌而言,噬菌体编码的毒素可导致严重腹泻;在肉毒杆菌中,毒素可导致麻痹。 在溶菌发育过程中,预言将在宿主染色体中持续存在,直到诱导,这会导致病毒基因组从宿主染色体中切除。 诱导发生后,温带噬菌体可以经历裂解周期,然后在新感染的细胞中进行溶菌发育(见图\(\PageIndex{2}\))。
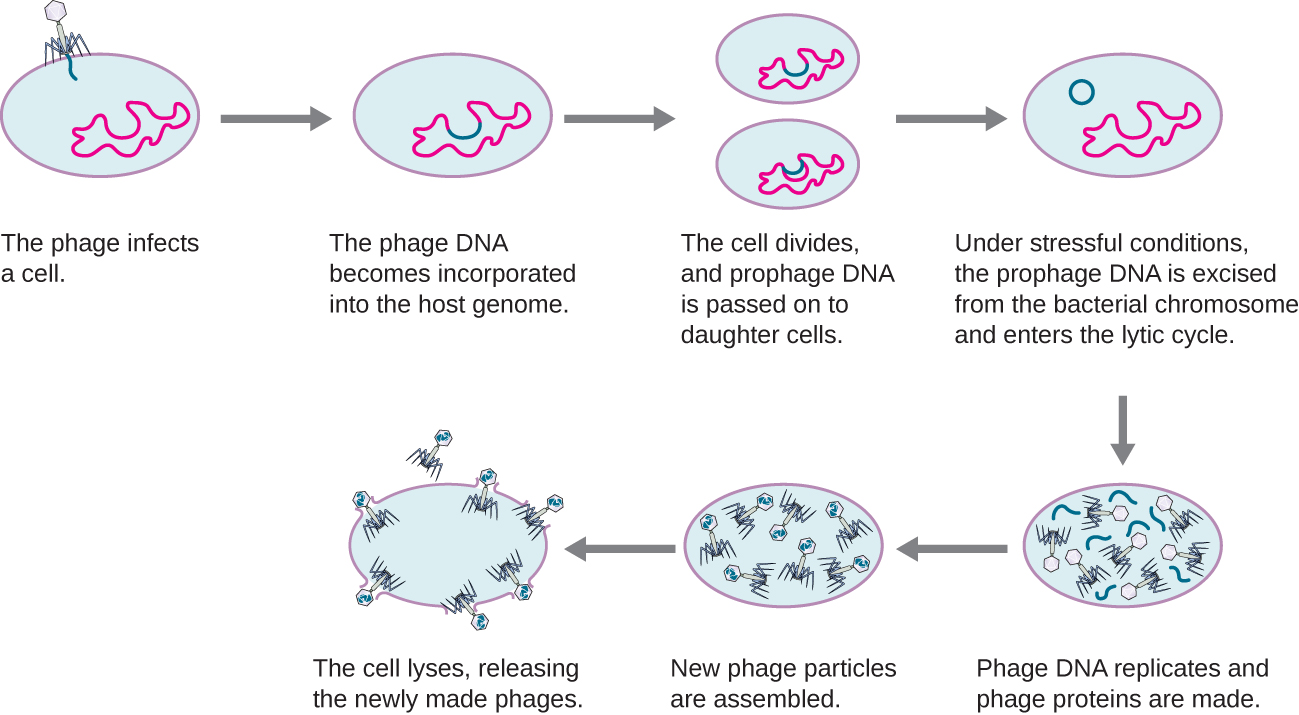
该视频说明了噬菌体溶解生命周期的各个阶段以及向裂解阶段的过渡。
练习\(\PageIndex{1}\)
在细菌中无法检测到潜在的噬菌体吗?
转导
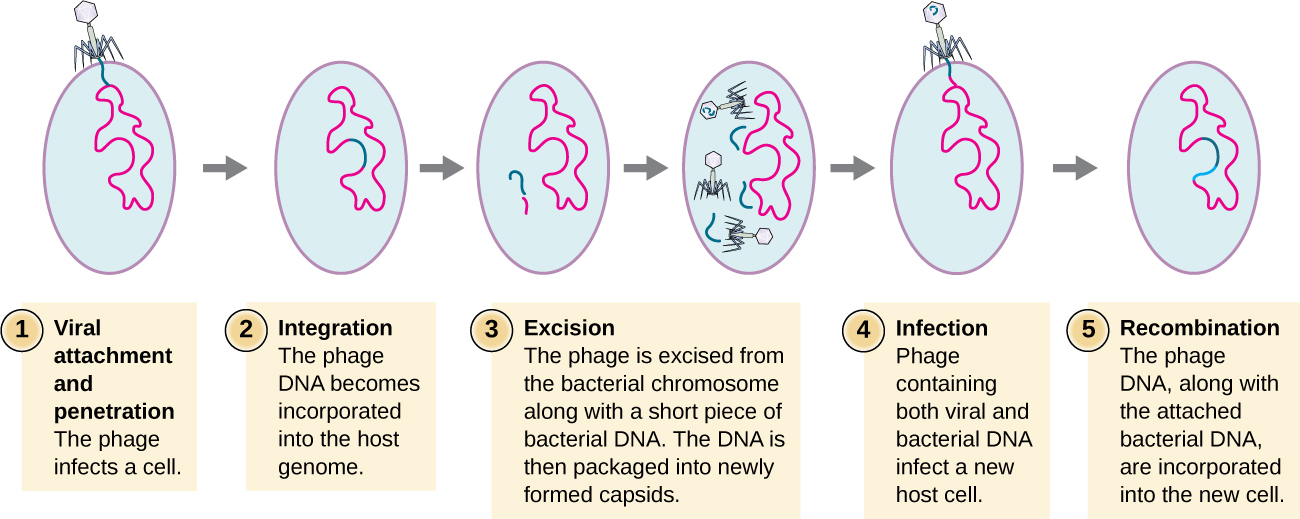
当噬菌体在连续感染期间将细菌 DNA 从一种细菌转移到另一种细菌时,就会发生转导。 转导有两种类型:广义转导和特殊转导。 在病毒复制的裂解周期中,病毒劫持宿主细胞,降解宿主染色体并产生更多的病毒基因组。 当它将 DNA 组装并封装到噬菌体头部时,包装偶尔会出错。 它不是包装病毒 DNA,而是随机抽取一片宿主 DNA 并将其插入衣壳中。 一旦释放,该病毒体就会将前宿主的DNA注入新感染的宿主中。 遗传信息的无性转移可以实现DNA重组,从而为新宿主提供新基因(例如,抗生素耐药基因或糖代谢基因)。 当噬菌体在裂解周期中随机转移细菌染色体 DNA 片段时,就会发生全身转导。 特殊转导发生在溶原周期结束时,预言被切除,噬菌体进入裂解周期。 由于噬菌体已整合到宿主基因组中,因此预言者可以作为宿主的一部分进行复制。 但是,某些条件(例如紫外线照射或化学暴露)会刺激预言者接受诱导,导致噬菌体从基因组中切除,进入裂解周期,并产生新的噬菌体离开宿主细胞。 在切除宿主染色体的过程中,噬菌体偶尔会去除病毒整合部位附近的一些细菌 DNA。 来自整合位点一端或两端的噬菌体和宿主 DNA 被封装在衣壳内,然后转移到新的受感染宿主。 由于噬菌体转移的DNA不是随机包装的,而是整合部位附近的特定DNA片段,因此这种基因转移机制被称为特殊转导(见图\(\PageIndex{3}\))。 然后,DNA可以与宿主染色体重组,赋予后者新的特征。 转导似乎在细菌的进化过程中起着重要作用,为细菌提供了一种无性交换遗传信息的机制。
练习\(\PageIndex{2}\)
哪个噬菌体生命周期与哪种形式的转导有关?
带有动物宿主的病毒的生命周期
裂解性动物病毒的感染阶段与噬菌体相似:附着、渗透、生物合成、成熟和释放(见图\(\PageIndex{4}\))。 但是,细菌和动物病毒的渗透、核酸生物合成和释放机制不同。 与宿主受体结合后,动物病毒通过内吞作用(被宿主细胞吞没)或膜融合(病毒包膜与宿主细胞膜)进入。 许多病毒是宿主特异性的,这意味着它们只感染某种类型的宿主;大多数病毒只感染组织内的某些类型的细胞。 这种特异性被称为组织向性。 这方面的例子包括脊髓灰质炎病毒,它对大脑和脊髓组织表现出向性,或者流感病毒,后者对呼吸道具有主要向性。
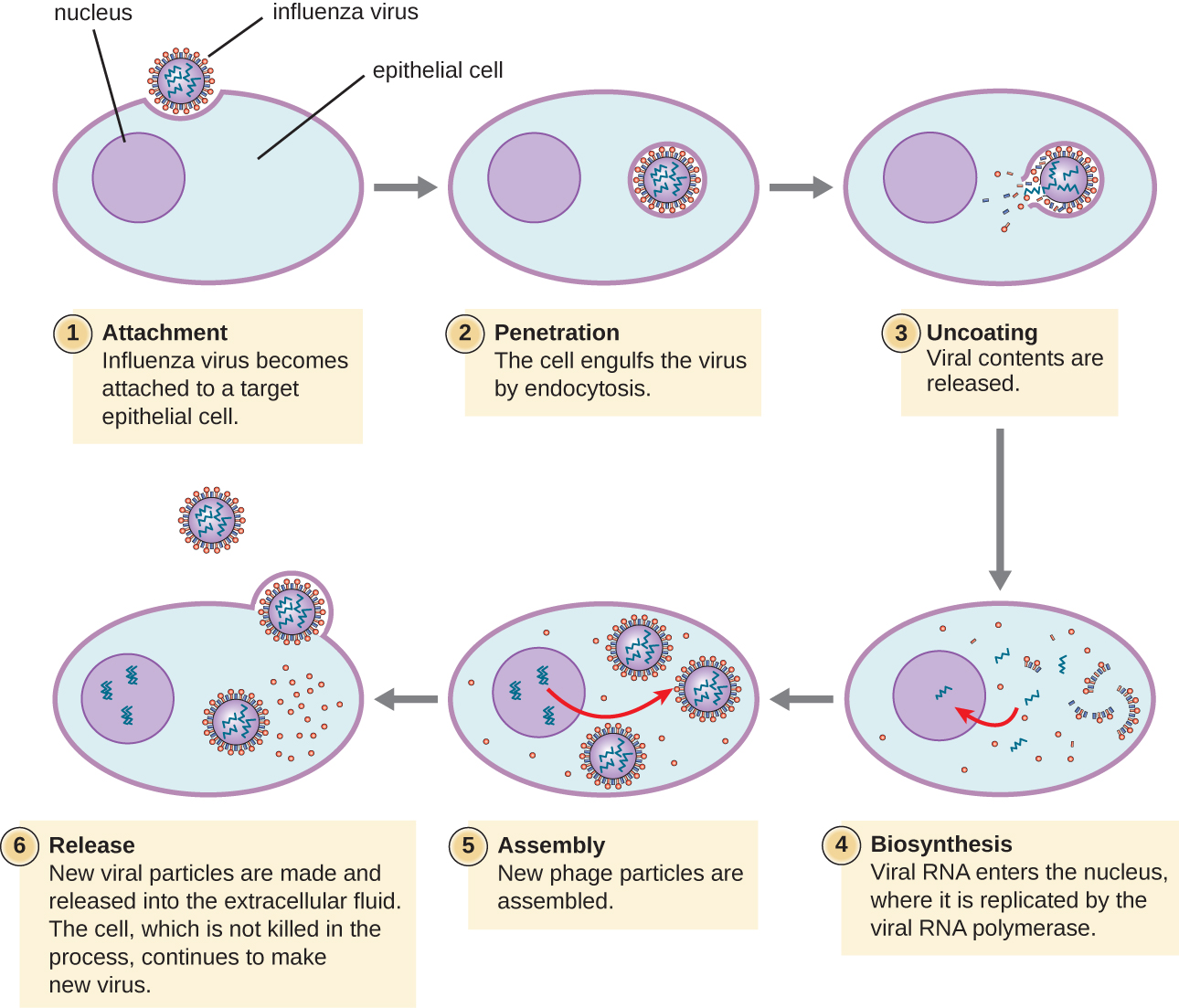
动物病毒并不总是使用正常的遗传信息流来表达其基因,从DNA到RNA再到蛋白质。 有些病毒具有像细胞生物一样的 dsDNA 基因组,可以遵循正常流动。 但是,其他人可能有 ssDNA、dsRNA 或 ssRNA 基因组。 基因组的性质决定了基因组如何被复制并以病毒蛋白的形式表达。 如果基因组是 ssDNA,则宿主酶将用于合成与基因组链互补的第二条链,从而产生 dsDNA。 dsDNA 现在可以像宿主 DNA 一样复制、转录和翻译。
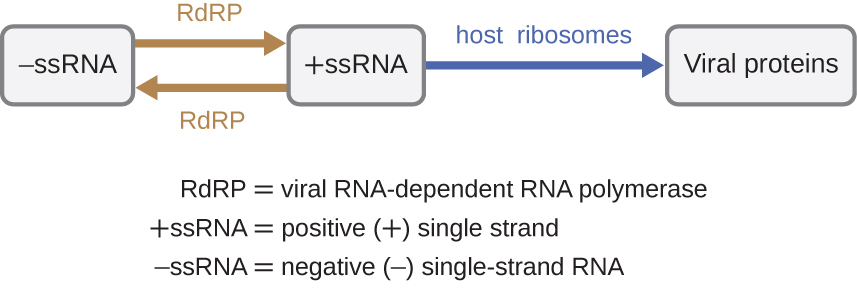
如果病毒基因组是RNA,则必须使用不同的机制。 RNA 基因组有三种类型:dsRNA、阳性(+)单链(+ssRNA)或阴性(−)单链 RNA(−ssRNA)。 如果病毒有 +ssRNA 基因组,则可以直接将其转化为病毒蛋白。 病毒基因组 +ssRNA 的作用类似于细胞 mRNA。 但是,如果病毒含有 −ssRNA 基因组,则在病毒 RNA 依赖性 RNA 聚合酶 (rdRP) 将 −ssRNA 复制为 +ssRNA 之前,宿主核糖体无法将其转化(见图\(\PageIndex{5}\))。 rdRP 由病毒带入,可用于从最初的 −ssRNA 基因组中制作 +ssRNA。 rdRP 也是复制 dsRNA 病毒的重要酶,因为它使用双链基因组的负链作为模板来创建 +ssRNA。 然后,新合成的 +ssRNA 拷贝可以由细胞核糖体翻译。
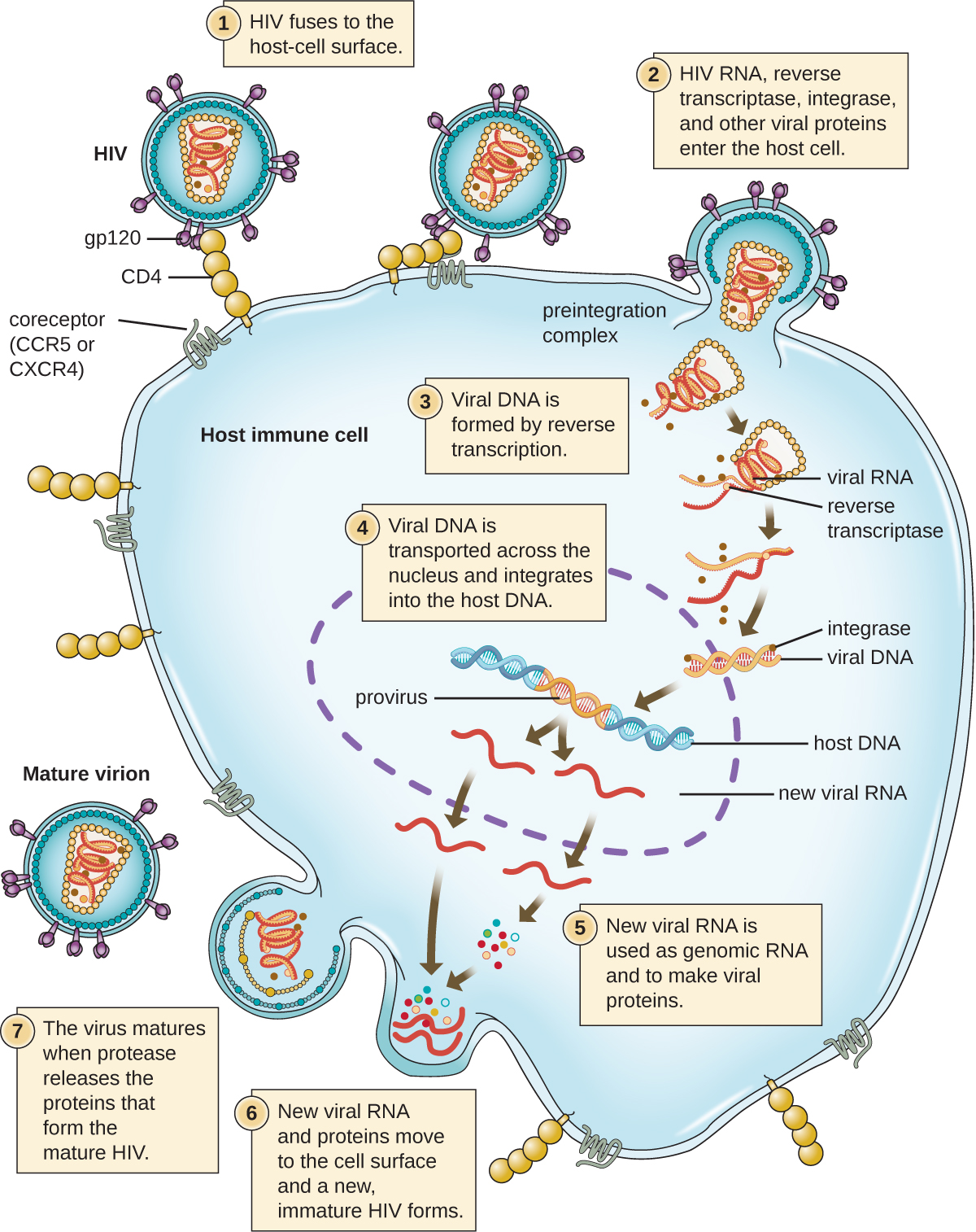
在逆转录病毒 es 中观察到病毒核酸合成的另一种机制,即 +ssRNA 病毒(见图\(\PageIndex{6}\))。 诸如HIV之类的单链RNA病毒在衣壳内携带一种称为逆转录酶的特殊酶,该酶使用+ssRNA基因组作为模板合成互补的ssDNA(cDNA)拷贝。 然后 ssDNA 被制成 dsDNA,它可以整合到宿主染色体中,成为宿主的永久组成部分。 整合的病毒基因组被称为原病毒。 现在,病毒可以在宿主中停留很长时间,从而形成慢性感染。 provirus 阶段类似于溶原周期中细菌感染的预言阶段。 但是,与预言不同,原病毒在拼接到基因组后不会被切除。
练习\(\PageIndex{3}\)
依赖于 RNA 的 RNA 聚合酶是由病毒基因还是宿主基因制成?
持续感染
当病毒没有从宿主系统中完全清除,而是停留在感染者的某些组织或器官中时,就会发生持续感染。 病毒可以保持沉默或发生生产性感染,而不会严重伤害或杀死宿主。 持续感染的机制可能涉及病毒或宿主基因表达的调节或宿主免疫反应的改变。 持续感染的两个主要类别是潜伏感染和慢性感染。 引起潜伏感染的病毒的例子包括单纯疱疹病毒(口腔和生殖器疱疹)、水痘带状疱疹病毒(水痘和带状疱疹)和爱泼斯坦-巴尔病毒(单核细胞增多症)。 丙型肝炎病毒和艾滋病毒是导致长期慢性感染的病毒的两个例子。
潜伏感染
并非所有动物病毒都会通过裂解周期复制。 有些病毒能够在称为潜伏期的过程中在细胞内保持隐藏或休眠状态。 这些类型的病毒被称为潜伏病毒,可能导致潜伏感染。 具有潜伏期的病毒最初可能在进入休眠状态之前引起急性感染。
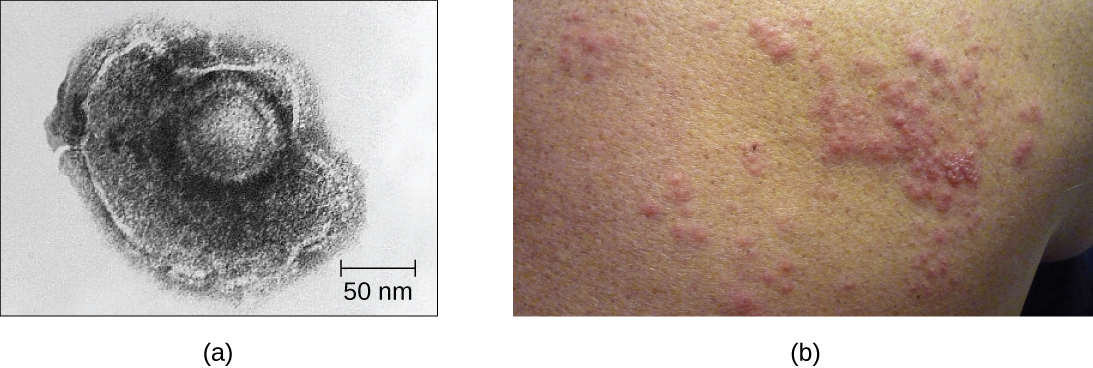
例如,水痘带状疱疹病毒感染全身的许多细胞并引起水痘,其特征是皮肤上有水泡皮疹。 感染后大约 10 到 12 天,病情消退,病毒进入休眠状态,在神经细胞神经节中存活多年。 在此期间,病毒不会杀死神经细胞或继续复制。 目前尚不清楚为什么病毒停止在神经细胞内复制,表达的病毒蛋白很少,但在某些情况下,通常在休眠多年之后,病毒会重新激活并导致一种称为带状疱疹的新疾病(图\(\PageIndex{7}\))。 尽管水痘会影响全身的许多区域,但带状疱疹是一种神经细胞特异性疾病,源于病毒处于休眠状态的神经节。
潜伏病毒可能因在宿主染色体之外以循环病毒基因组分子的形式存在而保持休眠状态。 其他病毒则通过整合到宿主基因组而成为病毒。 在休眠期间,病毒不会引起任何疾病症状,可能难以发现。 除非进行了病毒诊断测试,否则患者可能不知道自己携带了病毒。
慢性感染
慢性感染是一种症状在很长一段时间内反复出现或持续的疾病。 如果人体无法消灭病毒,则某些病毒感染可能是慢性的。 HIV是病毒的一个例子,这种病毒通常是在潜伏期很长一段时间后才会产生慢性感染。 一旦一个人感染了艾滋病毒,此后可以在组织中持续检测到病毒,但未经治疗的患者通常多年没有出现任何症状。 但是,该病毒通过多种干扰免疫功能的机制保持长期持续存在,包括阻止病毒抗原在受感染细胞表面的表达、改变免疫细胞本身、限制病毒基因的表达以及通过以下方式快速改变病毒抗原突变。 最终,对免疫系统的损害会导致疾病的进展,从而导致获得性免疫缺陷综合症(AIDS)。 艾滋病毒为避免被免疫系统清除而使用的各种机制也被其他慢性感染病毒(包括丙型肝炎病毒)所使用。
练习\(\PageIndex{4}\)
病毒可以通过哪两种方式维持持续感染?
带有植物宿主的病毒的生命周期
与噬菌体相比,植物病毒与动物病毒更相似。 植物病毒可能是包膜病毒或非包膜病毒。 像许多动物病毒一样,植物病毒可以具有 DNA 或 RNA 基因组,可以是单链或双链。 但是,大多数植物病毒没有DNA基因组;大多数具有+ssRNA基因组,其作用类似于信使RNA(mRNA)。 只有少数植物病毒具有其他类型的基因组。
植物病毒的宿主范围可能狭窄或广泛。 例如,柑橘 tristeza 病毒仅感染几株柑橘属植物,而黄瓜花叶病毒感染成千上万种不同植物家族的植物。 大多数植物病毒通过植物之间的接触传播,或者通过充当机械媒介的真菌、线虫、昆虫或其他节肢动物传播。 但是,有些病毒只能通过特定类型的昆虫媒介传播;例如,特定病毒可能由蚜虫传播,但不能通过粉虱传播。 在某些情况下,病毒也可能通过伤口进入健康的植物,这可能是由于修剪或天气破坏而发生的。
感染植物的病毒被视为生物养性寄生虫,这意味着它们可以在不杀死宿主的情况下建立感染,类似于在噬菌体的溶解性生命周期中观察到的情况。 病毒感染可能无症状(潜伏),也可能导致细胞死亡(裂解感染)。 生命周期从病毒渗透到宿主细胞开始。 接下来,当衣壳被移除后,病毒在细胞质内被解除涂层。 根据核酸的类型,细胞成分用于复制病毒基因组和合成用于组装新病毒体的病毒蛋白。 要确定全身性感染,病毒必须进入植物血管系统的一部分,例如韧皮。 全身感染所需的时间可能从几天到几周不等,具体取决于病毒、植物种类和环境条件。 当病毒从受感染的植物传播到健康的植物时,其生命周期即告完成。
练习\(\PageIndex{5}\)
典型植物病毒的结构和基因组是什么?
病毒生长曲线
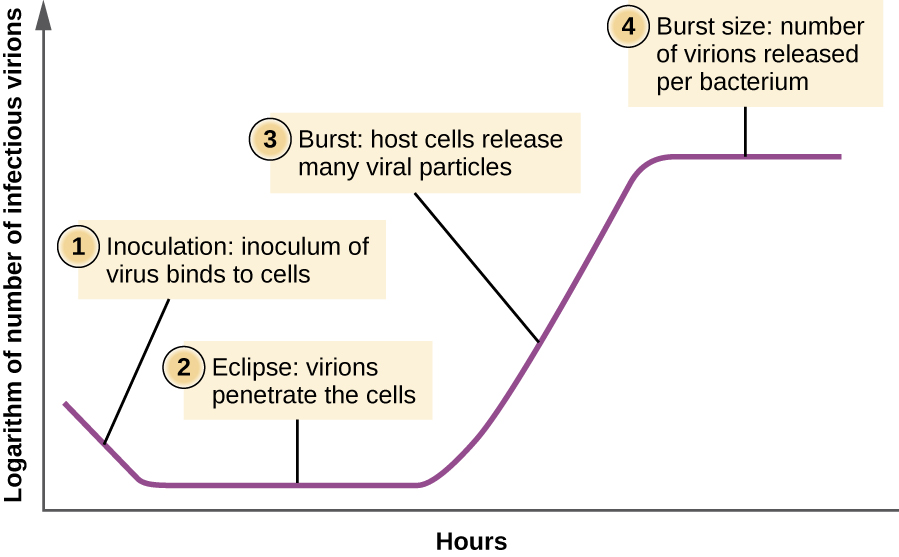
与细菌群体的生长曲线不同,病毒种群在其生命周期内的生长曲线不遵循乙状曲线。 在初始阶段,接种病毒会导致感染。 在日食阶段,病毒结合并穿透细胞,培养基中没有检测到病毒体。 与细菌生长曲线相比,病毒生长曲线接下来出现的主要区别在于病毒体同时从裂解的宿主细胞中释放出来。 这种情况被称为爆发,每种细菌释放的病毒体数量被描述为爆发大小。 在噬菌体的一步增殖曲线中,宿主细胞裂解,向培养基释放许多病毒颗粒,这导致病毒滴度(单位体积的病毒体数)急剧上升。 如果没有存活的宿主细胞残留,则病毒颗粒在培养物衰退期间开始降解(见图\(\PageIndex{8}\))。
练习\(\PageIndex{6}\)
病毒生命周期的哪个方面会导致生长曲线的突然增加?
未注册的治疗
埃博拉是无法治愈的,也是致命的。 2014 年在西非爆发的疫情是前所未有的,在死亡率方面使其他人类埃博拉疫情相形见绌。 在报告的24,666例疑似或确诊病例中,有10,179人死亡。 1
目前尚无经批准的埃博拉治疗方法或疫苗。 尽管一些药物在实验室研究和动物模型中已显示出潜力,但尚未在人体中进行安全性和有效性测试。 这些药物不仅未经测试或未注册,而且供不应求。
鉴于巨大的痛苦和高死亡率,可以公平地问一下,未注册和未经测试的药物是否总比没有好。 鉴于这些药品的供应极为有限,是否应该分发?如果是,谁应该收到这些药物? 在埃博拉患者身上治疗未经测试的药物是否合乎道德? 另一方面,不向垂死的患者提供可能挽救生命的药物是否合乎道德? 还是应该将药物留给致力于控制这种疾病的医疗保健提供者?
2014年8月,两名受感染的美国援助人员和一名西班牙牧师接受了ZmApp的治疗,ZmApp是一种未注册的药物,曾在猴子身上进行过测试,但未在人体中进行过测试。 两名美国援助人员康复了,但牧师死了。 当月晚些时候,世卫组织发布了一份关于用该药物治疗患者的伦理学的报告。 由于埃博拉往往是致命的,专家小组认为,提供未注册药物是合乎道德的,出于安全考虑而扣留这些药物是不道德的。 这种情况是在完善的疗法监管和治理体系之外进行 “富有同情心的使用” 的一个例子。
美国的埃博拉
2014 年 9 月 24 日,托马斯·埃里克·邓肯来到达拉斯的德克萨斯健康长老会医院,抱怨发烧、头痛、呕吐和腹泻,这些症状常见于感冒或流感患者。 检查后,一名急诊科医生诊断他患有鼻窦炎,开了一些抗生素处方,然后将他送回家。 两天后,邓肯乘救护车返回医院。 他的病情恶化了,额外的血液检查证实他感染了埃博拉病毒。
进一步的调查显示,邓肯刚刚从利比里亚返回,利比里亚是埃博拉疫情严重的国家之一。 9月15日,邓肯在到达拉斯医院就诊前九天,他曾帮助将一名受埃博拉影响的邻居送往利比里亚的一家医院。 医院继续治疗邓肯,但他在住院几天后死亡。
邓肯病例的时间表表明了埃博拉病毒的生命周期。 埃博拉的潜伏时间从2天到21天不等。 从邓肯接触病毒感染到出现症状之间已经过去了九天。 这在一定程度上对应于病毒种群增长的日食期。 在日食阶段,邓肯本来无法将这种疾病传播给他人。 但是,一旦感染者开始出现症状,这种疾病就会变得非常具有传染性。 埃博拉病毒通过直接接触唾液、血液和呕吐物等体液飞沫传播。 可以想象,邓肯在开始出现症状后的任何时候都可能将这种疾病传播给他人,大概是在他到达拉斯医院之前的某个时候。 一旦医院发现像邓肯这样的患者感染了埃博拉病毒,该患者就会立即被隔离,公共卫生官员开始回溯以查明像邓肯这样的患者在出现症状期间可能与之互动的所有人。
公共卫生官员找到了10名高危人群(邓肯的家庭成员)和50名低风险人群,以监测他们的感染迹象。 没有人感染这种疾病。 但是,一名负责邓肯护理的护士确实被感染了。 这再加上邓肯最初的误诊,清楚地表明,美国医院需要为医务人员提供额外培训,以防止可能在美国爆发埃博拉疫情。
练习\(\PageIndex{7}\)
- 哪些类型的培训可以使卫生专业人员做好准备,以遏制新出现的流行病,例如2014年的埃博拉疫情?
- 传染性病原体和传染性病原体有什么区别?

有关埃博拉的更多信息,请访问 CDC 网站。
摘要
- 许多病毒以特定的宿主或组织为目标。 有些可能有多个主机。
- 许多病毒要经过几个阶段感染宿主细胞。 这些阶段包括附着、渗透、脱皮、生物合成、成熟和释放。
- 噬菌体具有裂解或溶解循环。 裂解周期导致宿主死亡,而溶解循环导致噬菌体整合到宿主基因组中。
- 噬菌体将 DNA 注入宿主细胞,而动物病毒则通过内吞作用或膜融合进入。
- 动物病毒可以经历潜伏期,类似于噬菌体的溶菌发育。
- 大多数植物病毒是正链 ssRNA,可以发生潜伏期、慢性或裂解感染,正如动物病毒所观察到的那样。
- 与细菌生长曲线相比,噬菌体群体的生长曲线是一条单步乘法曲线,而不是乙状曲线。
- 噬菌体使用广义或特殊转导在宿主之间传递遗传信息。
脚注
- 1 世界卫生组织。 “世卫组织埃博拉数据和统计数据。” 2005 年 3 月 18 日。 http://apps.who.int/gho/data/view.eb...150318? lang=en


