6.3: 病毒的分离、培养和鉴定
- Page ID
- 200067
学习目标
- 讨论为什么最初将病毒描述为可过滤剂
- 描述病毒的培养以及标本的收集和处理
- 比较用于培养病毒的体内和体外技术
在本章开头,我们描述了如何使用孔隙小到允许病毒通过的钱伯兰瓷过滤器来发现 TMV。 如今,陶瓷过滤器已被膜过滤器和其他用于分离和识别病毒的设备所取代。
病毒隔离
与细菌不同,细菌中有许多可以在人工营养培养基上生长,而病毒需要活宿主细胞才能复制。 可以培养和培养受感染的宿主细胞(真核生物或原核细胞),然后收获生长培养基作为病毒来源。 液体介质中的病毒体可以通过离心或过滤与宿主细胞分离。 过滤器可以物理去除溶液中存在的任何大于病毒体的东西;然后可以在滤液中收集病毒(图\(\PageIndex{1}\))。
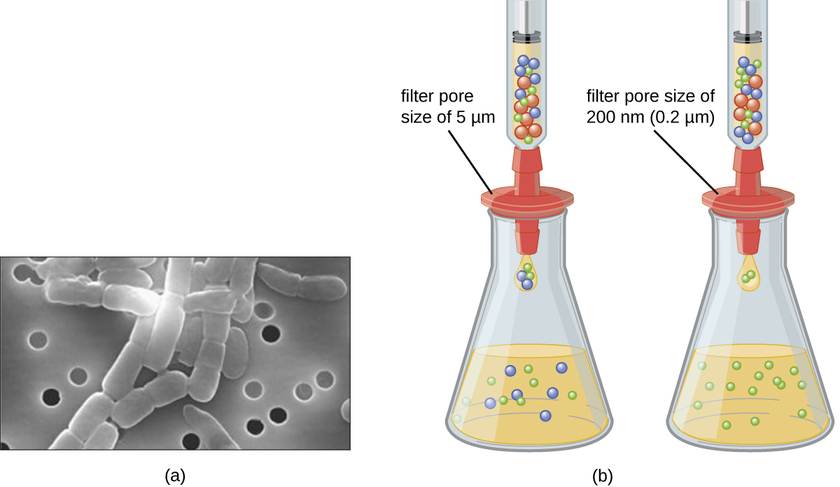
练习\(\PageIndex{1}\)
收集病毒需要多大尺寸的过滤孔?
培养病毒
病毒可以在体内(在整个活生物体、植物或动物内)或体外(在活生物体外,在人工环境中的细胞中生长,例如试管、细胞培养瓶或琼脂板)。 噬菌体可以在培养皿或扁平(水平)烧瓶中生长在 0.7% 软琼脂中的致密细菌层(也称为细菌草坪)的情况下生长(图\(\PageIndex{2a}\))。 琼脂浓度从通常用于培养细菌的1.5%有所降低。 柔软的 0.7% 琼脂使噬菌体能够轻松地通过培养基扩散。 对于裂解噬菌体,当检测到称为斑块的空白区域时,可以很容易地观察到细菌宿主的裂解(图\(\PageIndex{1b}\))。 当噬菌体杀死细菌时,在浑浊的细菌草坪上观察到许多斑块。
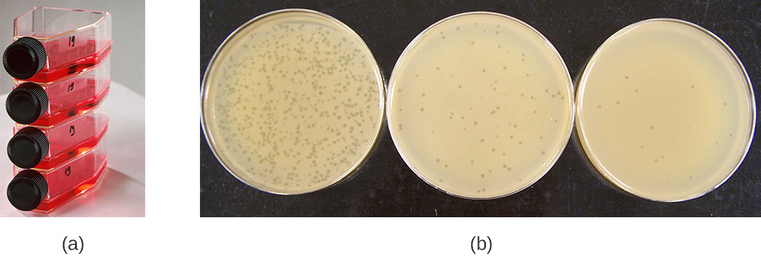
动物病毒需要宿主动物内的细胞或源自动物的组织培养细胞。 动物病毒培养对于 1) 鉴定和诊断临床标本中的致病病毒,2) 疫苗的生产以及 3) 基础研究很重要。 体内宿主来源可以是胚胎鸟蛋(例如鸡、火鸡)中的发育胚胎或整只动物。 例如,为年度流感疫苗接种计划生产的大多数流感疫苗都是在母鸡卵中培养的。
胚胎或宿主动物充当病毒复制的孵化器(图\(\PageIndex{3}\))。 在胚胎或宿主动物内的位置很重要。 许多病毒具有组织向性,因此必须将其引入特定的生长部位。 在胚胎内,靶位点包括羊膜腔、绒毛膜尿囊或卵黄囊。 病毒感染可能破坏组织膜,产生称为痘的病变;破坏胚胎发育;或导致胚胎死亡。
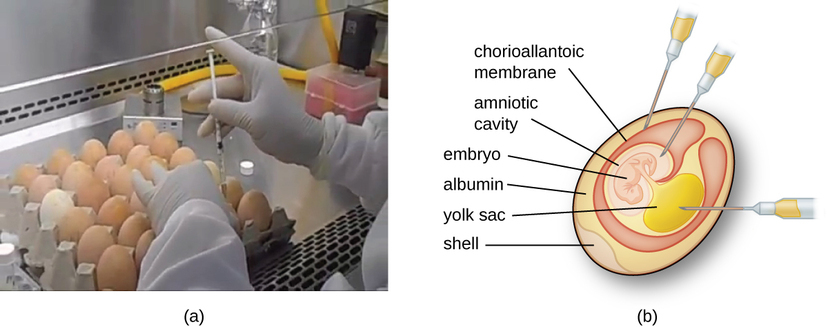
对于体外研究,可以使用各种类型的细胞来支持病毒的生长。 原代细胞培养物是用动物器官或组织新鲜制成的。 通过机械刮擦或切碎从组织中提取细胞以释放细胞,或者通过使用胰蛋白酶或胶原酶的酶法分解组织并将单个细胞释放到悬浮液中。 由于对锚固依赖性的要求,原代细胞培养需要在培养皿或组织培养瓶中使用液体培养基,这样细胞就具有固体表面,例如玻璃或塑料,用于附着和生长。 初级文化的寿命通常有限。 当原代培养物中的细胞经历有丝分裂并产生足够密度的细胞时,细胞就会与其他细胞接触。 当这种细胞间的接触发生时,会触发有丝分裂停止。 这称为接触抑制,它可以防止细胞的密度变得过高。 为了防止接触抑制,必须将来自原代细胞培养物的细胞转移到另一个装有新鲜生长培养基的容器中。 这称为二次细胞培养。 必须定期通过倒掉一些细胞并添加新鲜培养基来降低细胞密度,为维持细胞生长提供空间和营养。 与原代细胞培养不同的是,通常源自转化细胞或肿瘤的连续细胞系通常能够进行多次亚培养,甚至无限期生长(在这种情况下,它们被称为不朽)。 连续细胞系可能不表现出锚固依赖性(它们将在悬浮状态下生长),并且可能已经失去了接触抑制作用。 因此,连续的细胞系可以成堆或肿块生长,类似于小肿瘤的生长(图\(\PageIndex{4}\))。
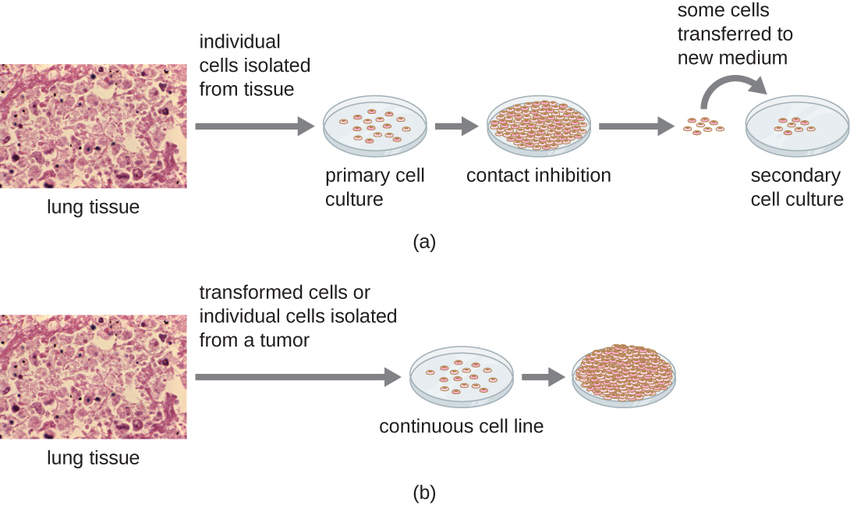
不朽细胞系的一个例子是HeLa细胞系,它最初是从亨丽埃塔·拉克斯(Henrietta Lacks)获得的肿瘤细胞中培养出来的,亨丽埃塔·拉克斯是一名于1951年死于宫颈癌的患者。 HeLa 细胞是第一个连续组织培养细胞系,用于建立组织培养,将其作为细胞生物学、病毒学和医学研究的重要技术。 在发现 HeLa 细胞之前,科学家们无法建立任何可靠或稳定的组织培养物。 六十多年后,这种细胞系仍然存活并被用于医学研究。 参见Henrietta Lacks的不朽细胞系,详细了解这个重要的细胞系以及获得它的有争议的方式。
练习\(\PageIndex{2}\)
细胞的哪些特性使得必须定期稀释原代细胞培养物?
亨丽埃塔·拉克斯的不朽细胞系
1951年1月,来自巴尔的摩的30岁非洲裔美国妇女亨丽埃塔·拉克斯在约翰·霍普金斯医院被诊断出患有宫颈癌。 我们现在知道她的癌症是由人乳头瘤病毒(HPV)引起的。 病毒的细胞病变效应在一个称为转化的过程中改变了她的细胞的特征,这使细胞能够持续分裂。 当然,这种能力导致了癌性肿瘤,最终在10月杀死了拉克斯夫人,享年31岁。 在她去世之前,她的癌细胞样本是在她不知情或未经允许的情况下采集的。 这些样本最终由约翰·霍普金斯大学的生物医学研究员乔治·盖伊博士拥有。 Gey 能够从 Lacks 的样本中培育出一些细胞,从而创造出今天所谓的不朽的 HeLa 细胞系。 这些细胞具有无限期存活和生长的能力,即使在今天,它们仍被广泛用于许多研究领域。
据拉克斯的丈夫说,亨丽埃塔和家人都没有允许医院采集她的组织标本。 事实上,直到拉克斯去世20年后,家人才意识到她的牢房还活着,并被积极用于商业和研究目的。 然而,HeLa细胞在与脊髓灰质炎、癌症和艾滋病等疾病相关的众多研究发现中发挥了关键作用。 这些细胞也已商业化,尽管它们本身从未获得过专利。 尽管如此,亨丽埃塔·拉克斯的财产从未从细胞的使用中受益,尽管在2013年,拉克斯家族获得了公布其细胞遗传序列的控制权。
该案例引发了围绕患者知情同意和知情权的几个生物伦理问题。 在提取拉克斯的组织时,没有关于知情同意的法律或指导方针。 这是否意味着她当时受到了公平的对待? 当然,按照今天的标准,答案是否定的。 未经同意从垂死的患者身上摘取组织或器官不仅被认为是不道德的,而且是非法的,无论这种行为能否挽救其他患者的生命。 那么,尽管按照当今的标准,拉克斯的组织是非法获得的,但科学家继续使用拉克斯的组织进行研究是否合乎道德?
不管是否合乎道德,如今,拉克斯的细胞被广泛用于许多用途,因此不可能将它们全部列出。 在这种情况下,目的是否证明手段是合理的? Lacks会高兴得知她对科学的贡献以及数百万受益的人吗? 她想让家人因使用她的细胞开发的商业产品而获得补偿吗? 还是她会觉得自己受到未经她同意就占用她身体一部分的研究人员的侵犯和剥削? 因为从来没有人问过她,所以我们永远不会知道。
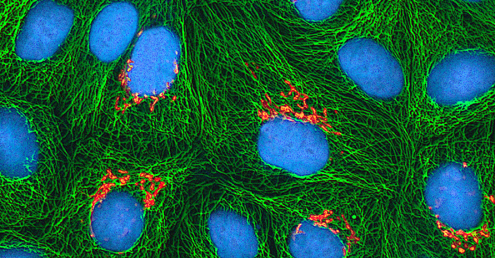
检测病毒
无论采用何种培养方法,一旦病毒被引入整个宿主生物、胚胎或组织培养细胞,就可以从受感染的宿主、胚胎或细胞系中制备样本,以便在明场、电子或荧光显微镜下进行进一步分析。 细胞病变效应(CPE)是病毒感染引起的明显可观察到的细胞异常。 CPE 可能包括失去对容器表面的粘附力、细胞形状从扁平变为圆形、细胞核收缩、细胞质中的液泡、细胞质膜融合和多核合胞的形成、细胞核或细胞质中的包涵体以及细胞完全裂解(见图\(\PageIndex{6}\))。
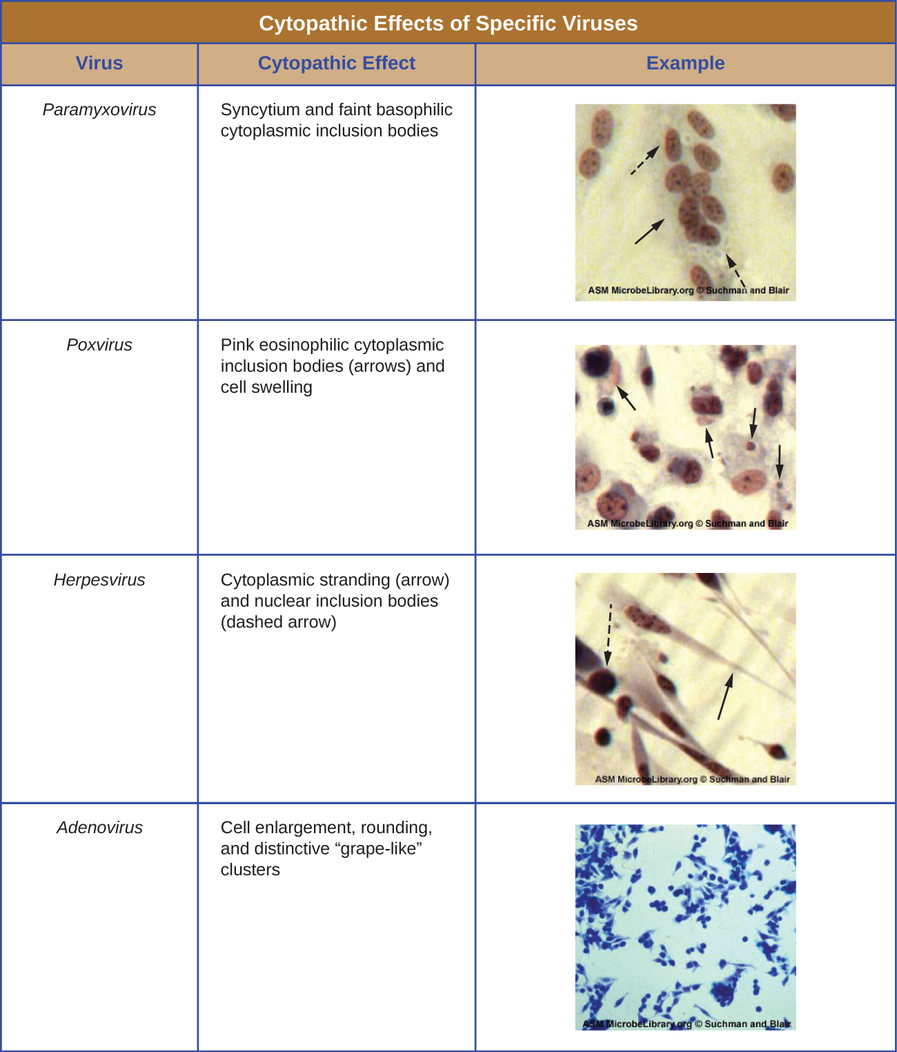
进一步的病理变化包括病毒破坏宿主基因组和将正常细胞转化为转化细胞,这些细胞是与癌症和肉瘤相关的细胞类型。 CPE 的类型或严重性取决于所涉及的病毒类型。 图中\(\PageIndex{6}\)列出了针对特定病毒的 CPE。
观看此视频,了解病毒对细胞的影响。
血凝试验
血清学检测用于检测患者血清中是否存在某些类型的病毒。 血清是血浆中的稻草色液体部分,从中去除了凝血因子。 血清可用于称为血凝测定的直接检测,以检测患者样本中的特定类型的病毒。 血凝是红细胞(红细胞)的凝集(结块)。 许多病毒会产生称为血凝素的表面蛋白质或尖峰,它们可以与红细胞膜上的受体结合并导致细胞凝集。 无需使用显微镜即可观察到血凝作用,但是这种方法并不总是区分传染性和非传染性病毒颗粒,因为两者都可以凝集红细胞。
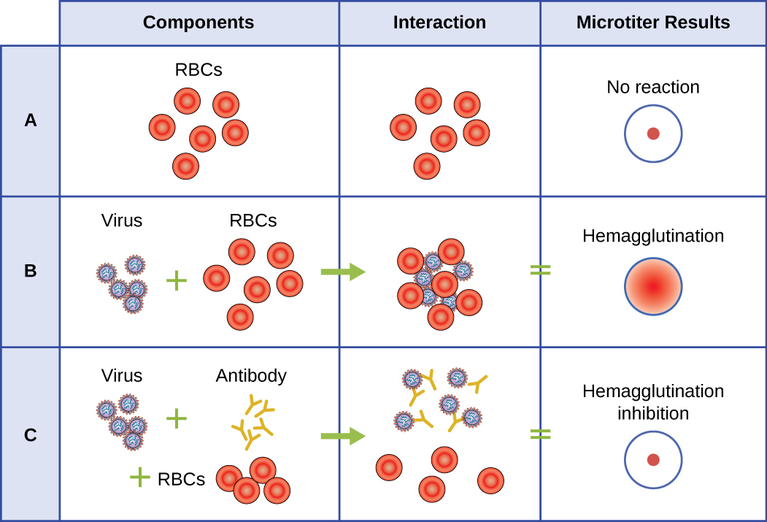
要使用血凝剂识别特定的致病病毒,我们必须使用间接方法。 称为抗体的蛋白质由患者的免疫系统生成,用于对抗特定病毒,可用于与特定类型病毒独特相关的血凝素等成分结合。 抗体与病毒上发现的血凝素的结合随后会阻止红细胞直接与病毒相互作用。 因此,当将红细胞添加到抗体包衣病毒中时,不会出现凝集现象;凝集受到抑制。 我们将这些类型的间接检测称为病毒特异性抗体血凝抑制(HAI)测定。 HAI 可用于检测是否存在针对许多类型病毒的特异性抗体,这些抗体可能在患者感染数月或数年后引起或已经引起感染(见图\(\PageIndex{7}\))。 凝集测定中对该测定进行了更详细的描述。
练习\(\PageIndex{3}\)
HIA 检测呈阳性的结果如何?
核酸扩增试验
核酸扩增试验 (NAAT) 在分子生物学中用于检测患者样本中独特的病毒核酸序列。 聚合酶链反应(PCR)是一种NAAT,用于检测患者组织或体液样本中是否存在病毒 DNA。 聚合酶链反应是一种扩增(即合成许多拷贝)感兴趣的病毒 DNA 片段的技术。 使用聚合酶链反应,称为引物的短核苷酸序列与病毒 DNA 的特定序列结合,从而能够鉴定病毒。
逆转录聚合酶链反应(RT-PCR)是一种用于检测 RNA 病毒存在的 NAAT。 逆转录聚合酶链反应与聚合酶链反应的不同之处在于,逆转录酶 (RT) 酶用于从样本中的少量病毒 RNA 中制成 cDNA。 然后可以通过聚合酶链反应扩增cDNA。 聚合酶链反应和逆转录聚合酶链反应均用于检测和确认患者标本中是否存在病毒核酸。
HPV 恐慌
21岁的护理专业学生米歇尔来到大学诊所时担心自己可能感染了性传播疾病(STD)。 她的性伴侣最近在他的阴茎底部出现了几处肿块。 他推迟去看医生,但米歇尔怀疑这是由HPV引起的尖锐湿疣。 她特别担心,因为她知道HPV不仅会导致疣,而且是宫颈癌的主要原因。 她和她的伴侣总是使用避孕套进行避孕,但她不相信这种预防措施能保护她免受HPV的侵害。
米歇尔的医生没有发现尖锐湿疣或任何其他性传播疾病的体征,但建议米歇尔在进行HPV检测的同时进行子宫颈抹片检查。 子宫颈抹片检查将筛查异常的宫颈细胞和与HPV相关的CPE;HPV 测试将检测病毒的存在。 如果两项检测结果均为阴性,米歇尔可以更放心,她很可能没有感染HPV。 但是,她的医生认为,米歇尔接种HPV疫苗可能是明智的,以保护自己免受将来可能的接触。
练习\(\PageIndex{4}\)
为什么 Michelle 的医生下令进行两种不同的检查,而不是依赖其中一种或另一种?
酶免疫测定
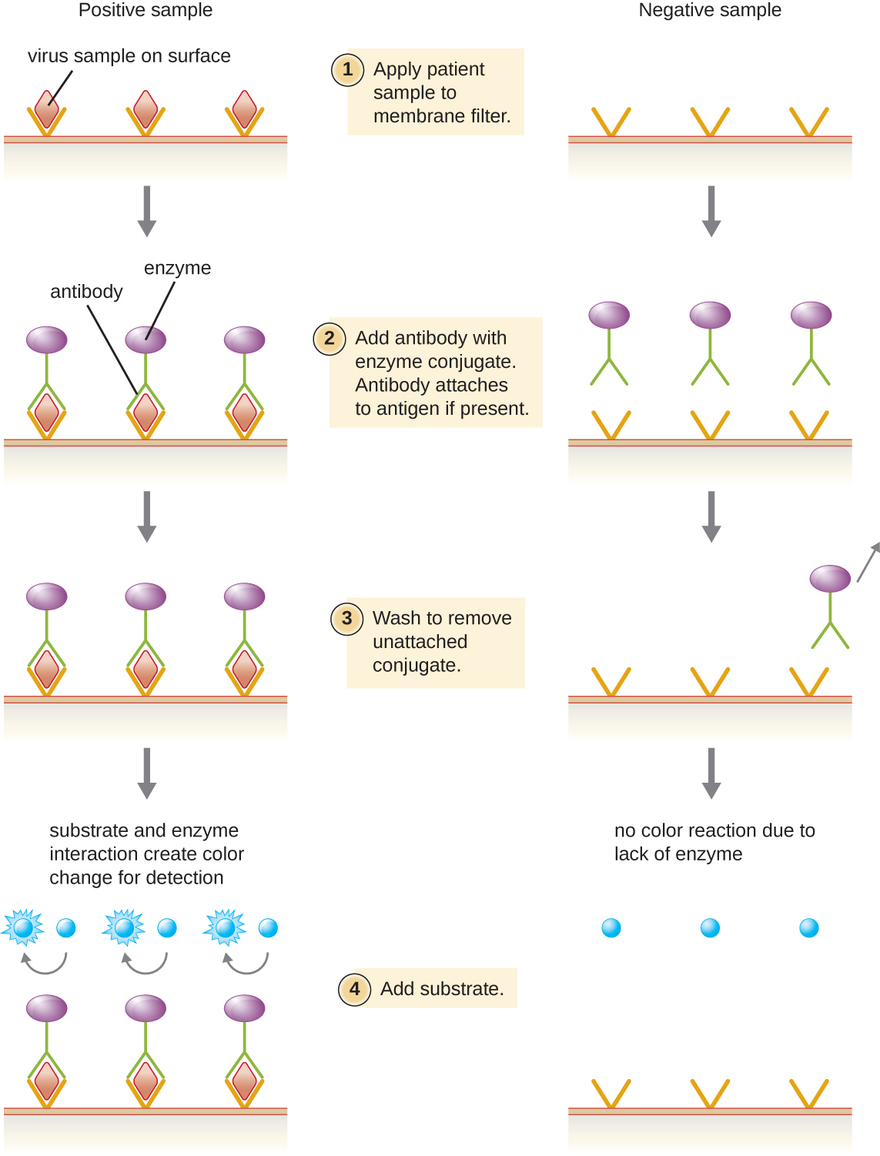
酶免疫测定(EIA)依赖于抗体检测和附着在称为抗原的特定生物分子上的能力。 检测抗体在可能是复杂的生物分子混合物中以高度的特异性附着在靶抗原上。 这种类型的测定中还包括附着在检测抗体上的无色酶。 该酶充当检测抗体上的标签,可以与无色底物相互作用,从而产生彩色的最终产物。 EIA 通常依靠多层抗体来捕获抗原并与之发生反应,所有这些抗原都附着在膜过滤器上(见图\(\PageIndex{8}\))。 病毒抗原的环境影响评估通常用作初步筛查测试。 如果结果为阳性,则需要进行更高灵敏度的检测,例如免疫印迹或NAAT。 环境影响评估和 ELISA 中对环境影响评估进行了更详细的讨论。
练习\(\PageIndex{5}\)
什么通常表示EIA测试呈阳性?
临床重点:第 3 部分
除了逆转录聚合酶链反应分析外,还收集了大卫的唾液用于病毒培养。 总的来说,没有单一的诊断测试足以进行死前诊断,因为结果将取决于测定的灵敏度、测试时存在的病毒体数量以及测定时间,因为唾液中病毒体的释放可能会有所不同。 事实证明,唾液中病毒培养的结果为阴性。 这对于大卫的医生来说并不奇怪,因为一个阴性结果并不能绝对表明没有感染。 可能是因为采样时唾液中的病毒体数量很少。 每隔一段时间重复测试以增加检测到更高病毒载量的机会并不少见。
练习\(\PageIndex{6}\)
大卫的医生是否应该根据这些测试结果修改他的治疗方案?
摘要
- 病毒培养需要存在某种形式的宿主细胞(全生物体、胚胎或细胞培养)。
- 病毒可以通过过滤从样本中分离出来。
- 病毒滤液是释放的病毒体的丰富来源。
- 噬菌体是通过细菌草坪上存在透明斑块来检测的。
- 动植物病毒是通过细胞病变效应、分子技术(PCR、RT-PCR)、酶免疫测定和血清学检测(血凝试验、血凝抑制试验)来检测的。


