5.5: 光谱线的形成
- Page ID
- 202536
学习目标
在本节结束时,您将能够:
- 解释发射线光谱和吸收线光谱是如何形成的
- 描述什么是离子以及它们是如何形成的
- 解释气体中的光谱线和电离水平如何帮助我们确定其温度
我们可以使用玻尔的原子模型来了解光谱线是如何形成的。 原子中电子轨道能级的概念自然可以解释为什么原子只吸收或发射特定的能量或光波长。
氢光谱
让我们从玻尔模型的角度来看氢原子。 假设一束白光(由所有可见波长的光子组成)通过原子氢气体照射。 波长为656纳米的光子具有恰到好处的能量,可以将氢原子中的电子从第二个轨道提升到第三个轨道。 因此,当所有具有不同能量(或波长或颜色)的光子都由氢原子流过时,具有这种特定波长的光子可以被那些电子在第二层运行的原子吸收。 当它们被吸收时,第二层的电子将移动到第三级,而普通白光流中将缺少许多具有这种波长和能量的光子。
其他光子将有合适的能量将电子从第二个轨道提升到第四个轨道,或者从第一个轨道提升到第五个轨道,依此类推。 只有具有这些精确能量的光子才能被吸收。 所有其他光子将原封不动地流过原子。 因此,氢原子仅吸收特定波长的光,并在我们看到的光谱中的这些波长处产生黑线。
假设我们有一个氢气容器,一系列光子正在通过这个容器,允许许多电子向上移动到更高的水平。 当我们关闭光源时,这些电子会从较大的轨道向下 “掉落” 并发射光子,但同样,只会发出与允许轨道之间能量差相对应的能量或波长的光。 产生某些光谱线的氢电子的轨道变化如图所示\(\PageIndex{1}\)。
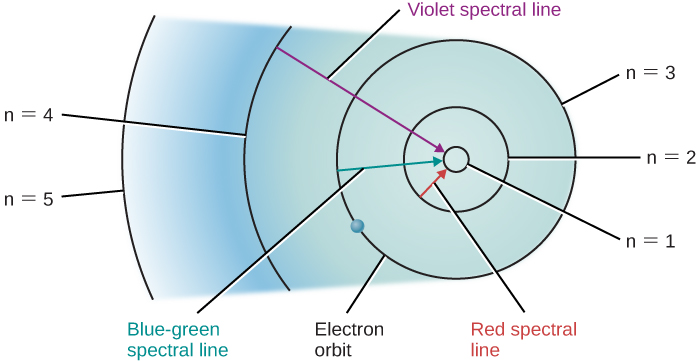
可以为氢以外的原子绘制类似的图片。 但是,由于这些其他原子通常各有多个电子,因此它们的电子轨道要复杂得多,光谱也更加复杂。 出于我们的目的,关键结论是:每种类型的原子都有自己独特的电子轨道模式,没有两组轨道是完全相同的。 这意味着每种类型的原子都显示出自己独特的光谱线集,这些光谱线是由电子在其独特的轨道组之间移动产生的。
天文学家和物理学家通过研究地球实验室中原子吸收和发射光的方式,努力了解每种元素的界限。 然后他们可以利用这些知识来识别天体中的元素。 通过这种方式,我们现在不仅知道了任何恒星的化学成分,甚至还知道了遥远的恒星星系,以至于它们的光在地球形成之前很久就开始传向我们。
能量水平和激励
玻尔的氢原子模型是我们在理解原子方面向前迈出的一大步。 但是,我们今天知道原子无法用这么简单的图片来表示。 例如,明确定义的电子轨道的概念并不正确;但是,在本入门课程的层面上,原子只允许某些离散能量的概念非常有用。 我们一直在讨论的能量水平可以看作代表了电子可能的轨道与原子核之间的某些平均距离。
通常,原子处于能量尽可能低的状态,即其基态。 在玻尔氢原子的模型中,基态对应于处于最内层轨道的电子。 原子可以吸收能量,从而将其提高到更高的能量水平(在简单的玻尔图中,相当于电子向更大轨道的移动)——这被称为激发。 然后据说原子处于激发状态。 通常,原子仅在很短的时间内保持激发状态。 在短暂的间隔(通常为一亿分之一秒左右)之后,它会自发地恢复到基态,同时发射光。 原子可能会在一次跳跃中恢复到最低状态,也可以分两次或更多次跳跃进行过渡,在向下时停在中间水平。 每次跳跃时,它都会发射一个波长的光子,该光子对应于该跳跃开始和结束时水平之间的能量差。
氢原子的能级图和几种可能的原子转变如图所示\(\PageIndex{2}\)。 当我们测量原子在水平之间跳跃时所涉及的能量时,我们发现向基态或从基态(称为莱曼系列线)的过渡会导致紫外光子的发射或吸收。 但是,进入或从第一个激发态(图(a)部分标记为 n = 2)(称为 Balmer 系列\(\PageIndex{2}\))的过渡会在可见光下产生发射或吸收。 实际上,正是为了解释这个巴尔默系列,玻尔首先提出了他的原子模型。
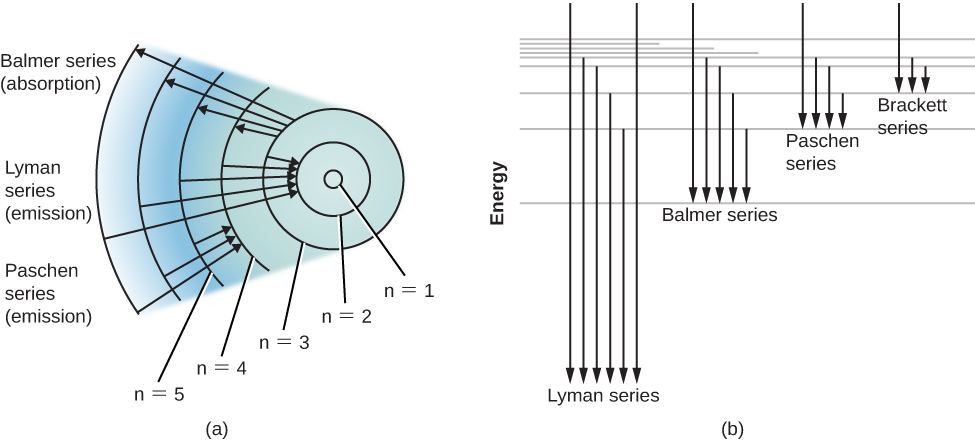
从经过的白光束中吸收特定光子并因此被激发的原子通常会自身解激并在很短的时间内再次发射该光。 那么,你可能想知道为什么会产生暗光谱线。 换句话说,为什么这种重新发射的光不能快速 “填充” 较暗的吸收线?
想象一下,一束白光通过一些较冷的气体向你射来。 有些重新发射的光实际上会返回到你看到的白光束中,但这只会稍微填充吸收线。 原因是气体中的原子向各个方向发光,而重新发射的光中只有一小部分朝向原始光束的方向(朝向你)。 在恒星中,大部分重新发射的光实际上是朝着通向恒星的方向流动,这对恒星以外的观察者没有任何好处。
图中\(\PageIndex{3}\)总结了我们讨论的不同类型的光谱。 白炽灯泡产生连续光谱。 当通过较薄的气体云观察该连续光谱时,可以看到吸收线光谱叠加在连续光谱上。 如果我们只看一团激发的气体原子(背后看不到连续的来源),就会发现激发的原子会发出发射线光谱。
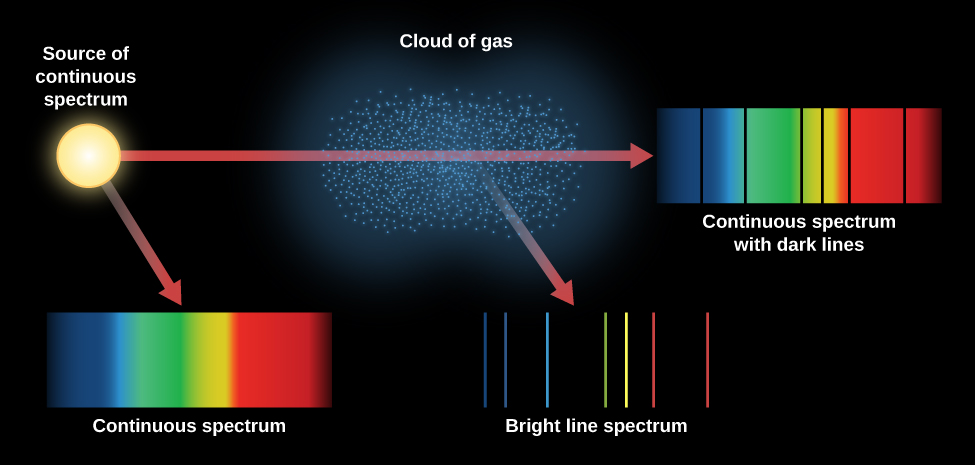
热气中的原子正在高速移动,并且不断相互碰撞,并与任何松散的电子碰撞。 它们可以通过这些碰撞以及吸收和发射光来激发(电子移动到更高的水平)和去激发(电子移动到较低的水平)。 气体中原子的速度取决于温度。 当温度升高时,碰撞的速度和能量也会升高。 因此,气体越热,电子占据最外层轨道的可能性就越大,这与最高的能量水平相对应。 这意味着电子在气体中开始向上跳跃的水平可以作为该气体有多热的指标。 通过这种方式,光谱中的吸收线为天文学家提供了有关吸收线起源区域温度的信息。
使用这个模拟来玩氢原子,看看当电子移动到更高的水平然后在进入较低水平时发出光子时会发生什么。
电离
我们已经描述了原子如何吸收一定数量的离散能量,将其提升到激发态并将其一个电子移动到离原子核更远的地方。 如果吸收了足够的能量,电子就可以从原子中完全移除——这就是所谓的电离。 然后说原子被电离了。 从处于基态的原子中移除一个电子所需的最小能量称为其电离能。
现在电离的原子(称为离子)必须吸收更多的能量才能移除原子结构更深处的额外电子。 要从原子中移除第三、第四、第五等电子,依此类推,需要更多的能量。 如果有足够的能量可用,原子就会完全电离,失去所有电子。 只有一个电子可以丢失的氢原子只能被电离一次;氦原子可以被电离两次;氧原子最多可以被电离八次。 当我们研究宇宙中存在大量高能辐射的区域时,例如最近形成的炙手可热的年轻恒星的社区,我们会看到大量的电离正在发生。
已经被正电离的原子失去了负电荷(缺失的电子),因此留下了净正电荷。 因此,它对任何自由电子都有很强的吸引力。 最终,一个或多个电子将被捕获,原子将再次变为中性(或电离到少一度)。 在电子捕获过程中,原子发射一个或多个光子。 发射哪些光子取决于电子是立即被捕获到原子的最低能量水平,还是在达到最低可用水平的途中停在一个或多个中间水平。
正如原子的激发可能是由与另一个原子、离子或电子的碰撞引起的(与电子的碰撞通常是最重要的)一样,电离也是如此。 这种碰撞电离的发生速率取决于原子的速度,因此也取决于气体的温度——气体越热,其原子被电离的次数就越多。
离子和电子重组的速率还取决于它们的相对速度,即温度。 此外,这取决于气体的密度:密度越高,回收的机会就越大,因为不同种类的颗粒会更紧密地挤在一起。 根据对气体温度和密度的了解,可以计算出被电离一次、两次等的原子的比例。 例如,在太阳中,我们发现其大气中的大多数氢原子和氦原子是中性的,而大多数钙原子以及许多其他较重的原子被电离过一次。
当电离原子处于中性状态时,其能级与同一个原子的能级完全不同。 每当电子从原子中移除时,离子的能量水平以及它可以产生的光谱线的波长都会发生变化。 这有助于天文学家区分给定元素的离子。 没有电子的电离氢不能产生吸收线。
关键概念和摘要
当电子从较高的能量水平移动到较低的能级时,会发射光子,并且在光谱中可以看到发射线。 当电子吸收光子并移动到更高的能量水平时,就会看到吸收线。 由于每个原子都有自己的特征能级集,因此每个原子都与独特的光谱线模式相关联。 这使天文学家能够确定恒星中以及恒星之间的气体和尘埃云中存在哪些元素。 能量水平最低的原子处于基态。 如果电子处于能量最低的轨道以外的轨道上,则该原子被认为是被激发的。 如果一个原子失去了一个或多个电子,它就被称为离子,据说是电离的。 不同离子的光谱看起来不同,可以告诉天文学家他们正在观测的光源的温度。
词汇表
- 激励
- 赋予原子或离子的能量大于其处于最低能量(基)状态的能量的过程
- 基态
- 原子的最低能量状态
- 离子
- 由于一个或多个电子的添加或丢失而带电的原子
- 电离化
- 原子获得或失去电子的过程


