26.3: الأمراض اللاخلوية المسببة للأمراض في الجهاز العصبي
- Page ID
- 195241
أهداف التعلم
- حدد مسببات الأمراض غير الخلوية الأكثر شيوعًا التي يمكن أن تسبب التهابات الجهاز العصبي
- قارن الخصائص الرئيسية لأمراض فيروسية محددة تؤثر على الجهاز العصبي
يمكن أن يسبب عدد من الفيروسات المختلفة والجسيمات دون الفيروسية أمراضًا تؤثر على الجهاز العصبي. تميل الأمراض الفيروسية إلى أن تكون أكثر شيوعًا من الالتهابات البكتيرية للجهاز العصبي اليوم. لحسن الحظ، تكون العدوى الفيروسية عمومًا أكثر اعتدالًا من نظيراتها البكتيرية وغالبًا ما تختفي تلقائيًا. تم وصف بعض مسببات الأمراض اللاخلوية الأكثر أهمية في الجهاز العصبي في هذا القسم.
التهاب السحايا الفيروسي
على الرغم من أنه أكثر شيوعًا من التهاب السحايا البكتيري، إلا أن التهاب السحايا الفيروسي عادة ما يكون أقل حدة. يمكن أن تؤدي العديد من الفيروسات المختلفة إلى التهاب السحايا كنتيجة للعدوى الأولية، بما في ذلك تلك التي تسبب الهربس والأنفلونزا والحصبة والنكاف. تزول معظم حالات التهاب السحايا الفيروسي تلقائيًا، ولكن تحدث حالات شديدة.
التهاب الدماغ بالفيروسات الشجرية
يمكن أن تسبب عدة أنواع من الفيروسات التي تنقلها الحشرات التهاب الدماغ. يشار إلى هذه الفيروسات مجتمعة باسم فيروسات أربوفيروس (لأنها عبارة عن ثروبو-بو رين)، وتُوصف الأمراض التي تسببها بالتهاب الدماغ بالفيروسات الجرثومية. معظم فيروسات أربو متوطنة في مناطق جغرافية محددة. تشمل أمراض التهاب الدماغ بالفيروسات الشجرية الموجودة في الولايات المتحدة التهاب الدماغ الخيلي الشرقي (EEE) والتهاب الدماغ الخيلي الغربي (WEE) والتهاب الدماغ في سانت لويس والتهاب الدماغ في غرب النيل (WNE). يحدث أحيانًا توسع فيروسات أربوفيروس خارج مناطقها الموبوءة، بشكل عام نتيجة للتغيرات البيئية المواتية للفيروس أو ناقله. كما سمحت زيادة سفر البشر أو الحيوانات أو النواقل المصابة بالفيروسات الأربوفيروسات بالانتشار إلى مناطق جديدة.
في معظم الحالات، تكون العدوى بالفيروسات الشجرية بدون أعراض أو تؤدي إلى مرض خفيف. ومع ذلك، عند ظهور الأعراض، فإنها تشمل ارتفاع درجة الحرارة والقشعريرة والصداع والقيء والإسهال والأرق. في المرضى المسنين، يمكن أن يؤدي التهاب الدماغ الشديد بالفيروسات الشجرية بسرعة إلى التشنجات والغيبوبة والموت.
البعوض هو الناقل البيولوجي الأكثر شيوعًا لفيروسات أربوفيروس، والتي تميل إلى أن تكون فيروسات ssRNA مغلفة. وبالتالي، فإن أفضل طريقة للوقاية من العدوى بالفيروسات الشجرية هي تجنب البعوض - باستخدام طارد الحشرات، وارتداء السراويل الطويلة والأكمام، والنوم في غرف يتم فحصها جيدًا، واستخدام الناموسيات، وما إلى ذلك.
يعتمد تشخيص التهاب الدماغ بالفيروسات الشجرية على الأعراض السريرية والاختبارات المصلية للمصل أو CSF. لا توجد أدوية مضادة للفيروسات لعلاج أي من هذه الأمراض الفيروسية، لذلك يتكون العلاج من الرعاية الداعمة وإدارة الأعراض.
يحدث التهاب الدماغ الخيلي الشرقي (EEE) بسبب فيروس التهاب الدماغ الخيلي الشرقي (EEEV)، والذي يمكن أن يسبب مرضًا شديدًا في الخيول والبشر. الطيور عبارة عن مستودعات لـ EEEV مع انتقال عرضي إلى الخيول والبشر عن طريق أنواع البعوض الزاعجة وCoquillettidia و Culex. لا تعمل الخيول ولا البشر كخزانات. EEE هو الأكثر شيوعًا في ساحل الخليج الأمريكي والولايات الأطلسية. يعد EEE أحد أكثر الأمراض التي تنتقل عن طريق البعوض خطورة في الولايات المتحدة، ولكن لحسن الحظ، إنه مرض نادر جدًا في الولايات المتحدة (الشكل\(\PageIndex{1}\)). 1 2
يحدث التهاب الدماغ الخيلي الغربي (WEE) بسبب فيروس التهاب الدماغ الخيلي الغربي (WEEV). عادة ما ينتقل WEEV إلى الخيول والبشر عن طريق بعوض Culex tarsalis، وقد تسبب في العقد الماضي في حالات قليلة جدًا من التهاب الدماغ لدى البشر في الولايات المتحدة. في البشر، تكون أعراض WEE أقل حدة من EEE وتشمل الحمى والقشعريرة والقيء، بمعدل وفيات يتراوح بين 3 و 4٪. مثل EEEV، تعتبر الطيور الخزان الطبيعي لـ WEEV. بشكل دوري، ولأسباب غير محددة، حدثت أوبئة في الحالات البشرية في أمريكا الشمالية في الماضي. كانت أكبر حالة مسجلة في عام 1941، مع أكثر من 3400 حالة. 3
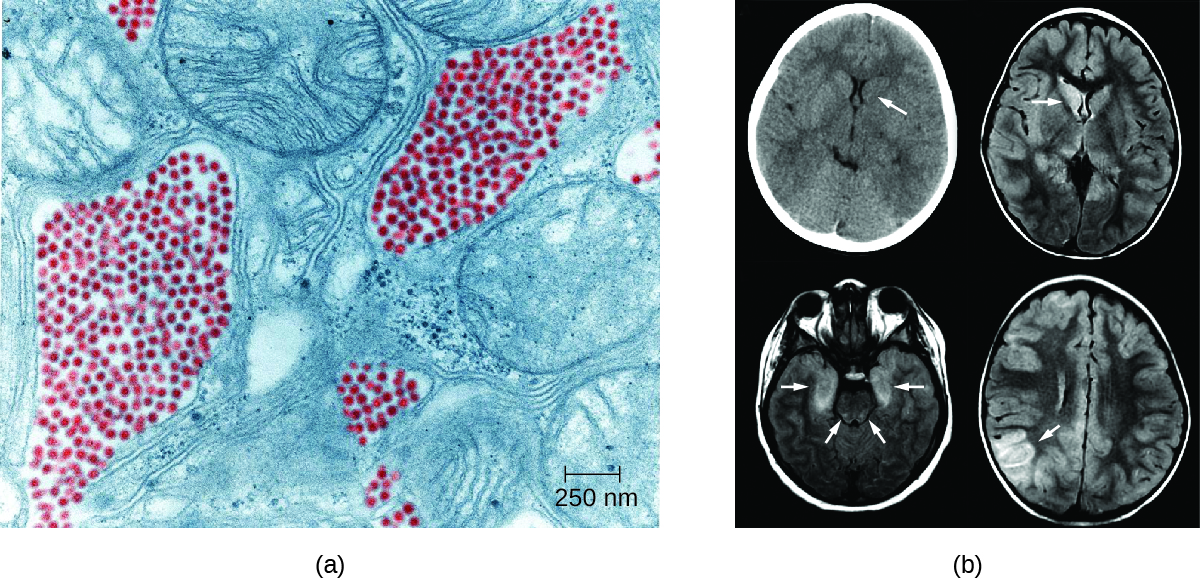
التهاب الدماغ في سانت لويس (SLE)، الناجم عن فيروس التهاب الدماغ في سانت لويس (SLEV)، هو شكل نادر من التهاب الدماغ مع ظهور الأعراض في أقل من 1٪ من المرضى المصابين. الخزانات الطبيعية لـ SLEV هي الطيور. غالبًا ما توجد SLEV في حوض نهر أوهايو - ميسيسيبي بوسط الولايات المتحدة وتم تسميتها بعد تفشي المرض الشديد في ولاية ميسوري في عام 1934. حدث أسوأ تفشي لالتهاب الدماغ في سانت لويس في عام 1975، حيث تم الإبلاغ عن أكثر من 2000 حالة. (4) يُصاب البشر بالعدوى عندما يلدغهم بعوض C. tarsalis أو C. quiefasciatus أو C. pipiens الذي يحمل معظم المرضى لا تظهر عليهم أعراض، ولكن في عدد قليل من الأفراد، تتراوح الأعراض من متلازمات خفيفة تشبه الإنفلونزا إلى التهاب الدماغ القاتل. معدل الوفيات الإجمالي للمرضى الذين يعانون من أعراض هو 5-15٪. 5
يعد التهاب الدماغ الياباني، الذي يسببه فيروس التهاب الدماغ الياباني (JEV)، السبب الرئيسي لالتهاب الدماغ الذي يمكن الوقاية منه بالتطعيم لدى البشر وهو مستوطن في بعض البلدان الأكثر اكتظاظًا بالسكان في العالم، بما في ذلك الصين والهند واليابان وجميع دول جنوب شرق آسيا. ينتقل فيروس JEV إلى البشر عن طريق بعوض Culex، الذي عادة ما يكون من النوع C. tritaeniorhynchus. تشمل الخزانات البيولوجية لـ JEV الخنازير والطيور الخواضة. معظم المرضى الذين يعانون من عدوى JEV لا تظهر عليهم أعراض، مع ظهور الأعراض في أقل من 1٪ من الأفراد المصابين. ومع ذلك، يموت حوالي 25٪ من أولئك الذين يصابون بالتهاب الدماغ، ومن بين أولئك الذين يتعافون، يعاني 30-50٪ من ضعف نفسي أو عصبي أو إدراكي. 6 لحسن الحظ، هناك لقاح فعال يمكن أن يمنع العدوى بـ JEV. توصي مراكز مكافحة الأمراض والوقاية منها (CDC) بهذا اللقاح للمسافرين الذين يتوقعون قضاء أكثر من شهر في المناطق الموبوءة.
كما يوحي الاسم، لم ينشأ فيروس غرب النيل (WNV) والمرض المرتبط به، التهاب الدماغ غرب النيل (WNE)، في أمريكا الشمالية. حتى عام 1999، كان المرض متوطنًا في الشرق الأوسط وأفريقيا وآسيا؛ ومع ذلك، تم تحديد الحالات الأمريكية الأولى في نيويورك في عام 1999، وبحلول عام 2004، انتشر الفيروس في جميع أنحاء قارة الولايات المتحدة. تم تأكيد أكثر من 35000 حالة، بما في ذلك 1400 حالة وفاة، في فترة الخمس سنوات بين عامي 1999 و 2004. لا تزال عدوى WNV قابلة للإبلاغ إلى CDC.
وينتقل فيروس غرب النيل إلى البشر عن طريق بعوض Culex من مستودعه الطبيعي والطيور المصابة، ولا يعاني 70 إلى 80% من المرضى المصابين من أي أعراض. تتضمن معظم حالات الأعراض أعراضًا خفيفة تشبه أعراض الأنفلونزا فقط، ولكن أقل من 1٪ من الأشخاص المصابين يصابون بالتهاب الدماغ أو التهاب السحايا الوخيم والمميت أحيانًا. يبلغ معدل الوفيات في مرضى WNV الذين يصابون بمرض عصبي حوالي 10٪. يمكن العثور على مزيد من المعلومات حول فيروس غرب النيل في طرق انتقال الأمراض.
تحدد هذه الخريطة التفاعلية حالات العديد من أمراض الفيروسات الشجرية في البشر وأنواع الخزانات حسب الولاية والسنة في الولايات المتحدة.
التمارين\(\PageIndex{1}\)
- لماذا من غير المحتمل أن يتم القضاء على فيروسات التهاب الدماغ بالمفصليات في المستقبل؟
- ما هو الشكل الأكثر شيوعًا لالتهاب الدماغ الفيروسي في الولايات المتحدة؟
التركيز السريري: الجزء 2
ليفوفلوكساسين هو مضاد حيوي من الكينولون يوصف غالبًا لعلاج الالتهابات البكتيرية في الجهاز التنفسي، بما في ذلك الالتهاب الرئوي والتهاب الشعب الهوائية. ولكن بعد تناول الدواء لمدة أسبوع، عاد ديفيد إلى طبيبه أكثر مرضًا من ذي قبل. وادعى أن المضاد الحيوي لم يكن له أي تأثير على أعراضه السابقة. بالإضافة إلى ذلك، يعاني الآن من الصداع وتيبس الرقبة وصعوبة التركيز في العمل. كما أظهر للطبيب طفح جلدي ظهر على ذراعيه خلال الأسبوع الماضي. بدأ طبيبه، الذي أصبح أكثر قلقًا الآن، يسأل عن أنشطة ديفيد خلال الأسبوعين الماضيين.
أوضح ديفيد أنه كان يعمل مؤخرًا على مشروع لتفكيك حظيرة قديمة. قام طبيبه بجمع عينات البلغم والخدوش من طفح ديفيد للثقافات. كما تم إجراء البزل الشوكي لفحص السائل النخاعي لديفيد. كشف الفحص المجهري لسائل CSF الخاص به عن خلايا خميرة مغلفة. وبناءً على هذه النتيجة، وصف الطبيب علاجًا جديدًا مضادًا للميكروبات باستخدام الأمفوتريسين B والفلوسيتوزين.
التمارين\(\PageIndex{2}\)
- لماذا كان العلاج الأصلي غير فعال؟
- لماذا يعتبر وجود الكبسولة مهمًا سريريًا؟
عدوى فيروس زيكا
عدوى فيروس زيكا هي مرض فيروسي ناشئ مرتبط بأمراض بشرية في أفريقيا وجنوب شرق آسيا وأمريكا الجنوبية والوسطى؛ ومع ذلك، فإن نطاقه يتوسع نتيجة للنطاق الواسع لناقلات البعوض. تم الإبلاغ عن الحالات الأولى التي نشأت في الولايات المتحدة في عام 2016. تم وصف فيروس زيكا في البداية في عام 1947 من القرود في غابة زيكا في أوغندا من خلال شبكة تراقب الحمى الصفراء. لم يُعتَبَر الفيروس من العوامل الممرضة البشرية الخطيرة حتى حدثت أولى حالات تفشي المرض على نطاق واسع في ميكرونيزيا في عام 2007؛ 7 ومع ذلك، اكتسب الفيروس شهرة كبيرة على مدى العقد الماضي، حيث ظهر كسبب لأعراض مشابهة لأعراض العدوى الأخرى بالفيروسات الشجرية التي تشمل الحمى والطفح الجلدي، التهاب الملتحمة وآلام العضلات والمفاصل والشعور بالضيق والصداع. البعوض من جنس الزاعجة هو الناقل الأساسي، على الرغم من أن الفيروس يمكن أن ينتقل أيضًا جنسيًا، من الأم إلى الطفل أثناء الحمل، أو من خلال نقل الدم.
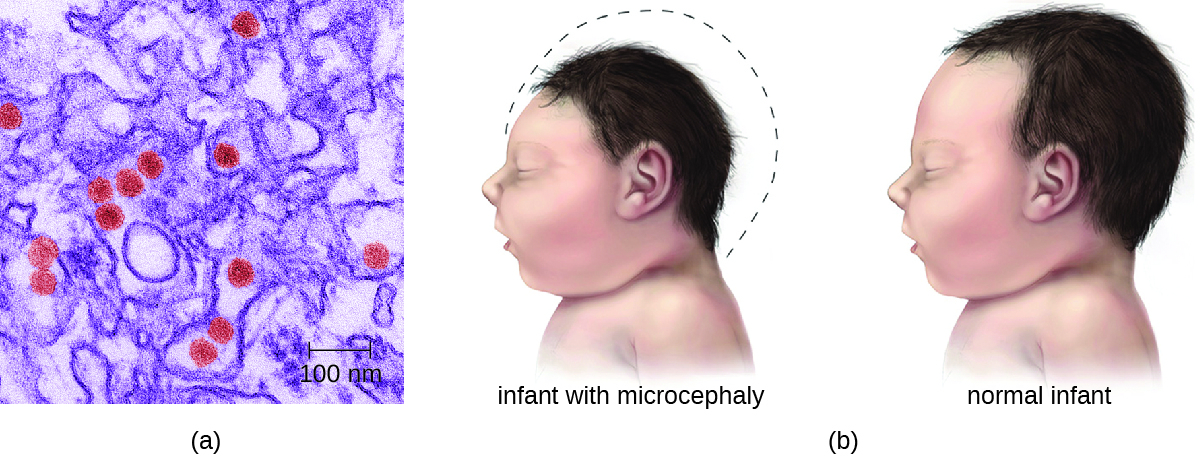
تؤدي معظم حالات العدوى بفيروس زيكا إلى أعراض خفيفة مثل الحمى أو الطفح الجلدي الطفيف أو التهاب الملتحمة. ومع ذلك، يمكن أن تؤثر العدوى عند النساء الحوامل سلبًا على الجنين النامي. تشير التقارير في عام 2015 إلى أن التهابات الجنين يمكن أن تؤدي إلى تلف الدماغ، بما في ذلك عيب خلقي خطير يسمى صغر الرأس، حيث يولد الطفل برأس صغير بشكل غير طبيعي (الشكل\(\PageIndex{2}\)). 8
يعتمد تشخيص زيكا بشكل أساسي على الأعراض السريرية. ومع ذلك، سمحت إدارة الغذاء والدواء الأمريكية مؤخرًا باستخدام مقايسة الحمض النووي الريبي لفيروس زيكا، و Trioplex RT-PCR، و Zika MAC-ELISA لاختبار دم المريض وبوله للتأكد من مرض فيروس زيكا. لا توجد حاليًا علاجات مضادة للفيروسات أو لقاحات لفيروس زيكا، ويقتصر العلاج على الرعاية الداعمة.
التمارين\(\PageIndex{3}\)
- ما هي علامات وأعراض عدوى فيروس زيكا لدى البالغين؟
- لماذا تعتبر عدوى فيروس زيكا تهديدًا خطيرًا للصحة العامة؟
داء الكلب
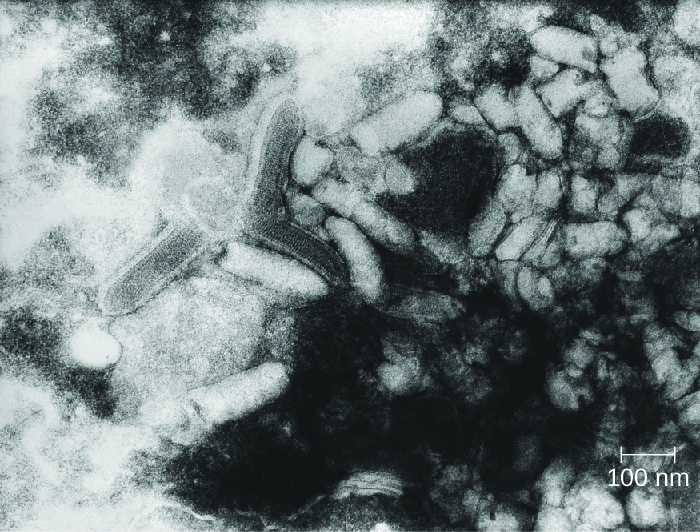
داء الكلب هو مرض حيواني مميت معروف منذ العصور القديمة. يحدث المرض بسبب فيروس داء الكلب (RV)، وهو أحد أفراد عائلة Rhabdoviridae، وينتقل المرض بشكل أساسي من خلال لدغة حيوان ثديي مصاب. Rhabdoviridae هي فيروسات RNA مغلفة لها شكل رصاصة مميزة (الشكل\(\PageIndex{3}\))؛ تمت دراستها لأول مرة من قبل لويس باستور، الذي حصل على فيروس داء الكلب من الكلاب المسعورة وزرع الفيروس في الأرانب. لقد نجح في إعداد لقاح داء الكلب باستخدام الأنسجة العصبية المجففة من الحيوانات المصابة. تم استخدام هذا اللقاح لعلاج الإنسان المصاب لأول مرة في عام 1885.
أكثر الخزانات شيوعًا في الولايات المتحدة هي الحيوانات البرية مثل الراكون (30.2٪ من جميع حالات الحيوانات خلال عام 2014) والخفافيش (29.1٪) والظربان (26.3٪) والثعالب (4.1٪)؛ بشكل جماعي، كانت هذه الحيوانات مسؤولة عن إجمالي 92.6٪ من حالات داء الكلب الحيواني في الولايات المتحدة في عام 2014. كانت نسبة 7.4٪ المتبقية من الحالات في ذلك العام في الحيوانات الأليفة مثل الكلاب والقطط والخيول والبغال والأغنام والماعز واللاما. 9 في حين أن هناك عادة حالة أو حالتين فقط من حالات الإصابة البشرية سنويًا في الولايات المتحدة، إلا أن داء الكلب لا يزال يتسبب في عشرات الآلاف من الوفيات البشرية سنويًا في جميع أنحاء العالم، وخاصة في آسيا وأفريقيا.
يرجع انخفاض معدل الإصابة بداء الكلب في الولايات المتحدة في المقام الأول إلى التطعيم الواسع النطاق للكلاب والقطط. يستخدم اللقاح الفموي أيضًا لحماية الحيوانات البرية، مثل الراكون والثعالب، من العدوى. تميل برامج اللقاح الفموي إلى التركيز على المناطق الجغرافية حيث يتوطن داء الكلب. 10 عادة ما يتم تسليم اللقاح الفموي في عبوة من الطُعم يتم إسقاطها بالطائرة، على الرغم من أن الاصطياد في المناطق الحضرية يتم يدويًا لتحقيق أقصى قدر من السلامة. 11 تتطلب العديد من البلدان الحجر الصحي أو إثبات التطعيم ضد داء الكلب للحيوانات الأليفة المنزلية التي يتم إحضارها إلى البلاد. هذه الإجراءات صارمة بشكل خاص في الدول الجزرية حيث لا يوجد داء الكلب بعد، مثل أستراليا.
يمكن أن تكون فترة حضانة داء الكلب طويلة، تتراوح من عدة أسابيع أو أشهر إلى أكثر من عام. عندما يتكاثر الفيروس، ينتقل من موقع اللدغة إلى المحاور الحركية والحسية للأعصاب الطرفية وينتشر من عصب إلى آخر باستخدام عملية تسمى النقل الرجعي، وفي النهاية يشق طريقه إلى الجهاز العصبي المركزي عبر العقد الشوكية. بمجرد وصول فيروس داء الكلب إلى الدماغ، تؤدي العدوى إلى التهاب الدماغ الناجم عن تعطيل وظيفة الناقل العصبي الطبيعية، مما يؤدي إلى الأعراض المرتبطة بداء الكلب. تعمل الفيروسات في المساحات المشبكية كمنافسين لمجموعة متنوعة من الناقلات العصبية لمستقبلات الأسيتيل كولين و GABA والجليسين. وبالتالي، فإن عمل فيروس داء الكلب سام للأعصاب وليس سامًا للخلايا. بعد أن يصيب فيروس داء الكلب الدماغ، يمكن أن يستمر في الانتشار عبر مسارات عصبية أخرى، وينتقل من الجهاز العصبي المركزي إلى أنسجة مثل الغدد اللعابية، حيث يمكن إطلاق الفيروس. ونتيجة لذلك، مع تقدم المرض، يمكن العثور على الفيروس في العديد من الأنسجة الأخرى، بما في ذلك الغدد اللعابية وبراعم التذوق وتجويف الأنف والدموع.
تشمل الأعراض المبكرة لداء الكلب عدم الراحة في مكان اللدغة والحمى والصداع. بمجرد وصول الفيروس إلى الدماغ وظهور الأعراض لاحقًا، يكون المرض دائمًا مميتًا. يمكن أن تنتهي حالات داء الكلب النهائية بإحدى طريقتين: داء الكلب الغاضب أو الشللي. يصبح الأفراد المصابون بداء الكلب الغاضب في حالة من الانزعاج الشديد والنشاط المفرط. يعد رهاب الماء (الخوف من الماء) شائعًا في المرضى الذين يعانون من داء الكلب الغاضب، والذي يحدث بسبب التشنجات العضلية في الحلق عند البلع أو التفكير في الماء. يمكن أن يؤدي إفراز اللعاب الزائد والرغبة في العض إلى رغوة الفم. تعمل هذه السلوكيات على تعزيز احتمالية انتقال الفيروس، على الرغم من أن ملامسة الإفرازات المصابة مثل اللعاب أو الدموع وحدها كافية للعدوى. يبلغ المرض ذروته بعد بضعة أيام فقط من الرعب والارتباك، يليه توقف القلب والأوعية الدموية والجهاز التنفسي. في المقابل، يتبع الأفراد المصابون بداء الكلب الشللي عمومًا مسارًا أطول من المرض. تصاب العضلات في موقع الإصابة بالشلل. على مدى فترة من الزمن، ينتشر الشلل ببطء في جميع أنحاء الجسم. هذا الشكل المشلول من المرض يبلغ ذروته في الغيبوبة والموت.
قبل توفر طرق التشخيص الحالية، تم تشخيص داء الكلب باستخدام تاريخ الحالة السريرية والفحص النسيجي للخزعة أو أنسجة التشريح، بحثًا عن وجود أجسام نيجري. نحن نعلم الآن أن هذه التغييرات النسيجية لا يمكن استخدامها لتأكيد تشخيص داء الكلب. لا توجد اختبارات يمكنها اكتشاف فيروس داء الكلب لدى البشر في وقت اللدغة أو بعد ذلك بوقت قصير. بمجرد أن يبدأ الفيروس في التكاثر (ولكن قبل ظهور الأعراض السريرية)، يمكن اكتشاف الفيروس باستخدام اختبار الفلورة المناعية على الأعصاب الجلدية الموجودة في قاعدة بصيلات الشعر. يمكن أيضًا اختبار اللعاب بحثًا عن المواد الوراثية الفيروسية عن طريق النسخ العكسي متبوعًا بتفاعل البوليميراز المتسلسل (RT-PCR). حتى عند إجراء هذه الاختبارات، يتم التعامل مع معظم حالات العدوى المشتبه بها على أنها إيجابية في حالة عدم وجود أدلة مخالفة. من الأفضل أن يخضع المرضى للعلاج غير الضروري بسبب نتيجة إيجابية كاذبة، بدلاً من الموت نتيجة نتيجة سلبية كاذبة.
يتم علاج العدوى البشرية بداء الكلب عن طريق التحصين بجرعات متعددة من اللقاح الموهن لتطوير مناعة نشطة لدى المريض (انظر ميزة التركيز السريري في الفصل الخاص بمسببات الأمراض اللاخلوية). يمكن أن ينجح تطعيم شخص مصاب بالفعل بسبب التقدم البطيء للمرض، مما يتيح الوقت لجهاز المناعة لدى المريض لتطوير أجسام مضادة ضد الفيروس. يمكن أيضًا علاج المرضى بالجلوبيولين المناعي لداء الكلب البشري (الأجسام المضادة لفيروس داء الكلب) لتشجيع المناعة السلبية. ستقوم هذه الأجسام المضادة بتحييد أي جزيئات فيروسية حرة. على الرغم من أن عدوى داء الكلب تتطور ببطء في الأنسجة الطرفية، إلا أن المرضى لا يستطيعون عادة تكوين استجابة مناعية وقائية من تلقاء أنفسهم.
التمارين\(\PageIndex{4}\)
- كيف تنقل لدغة حيوان مصاب داء الكلب؟
- ما هو الهدف من برامج تطعيم الحياة البرية لداء الكلب؟
- كيف يتم علاج داء الكلب في الإنسان؟
شلل الأطفال
شلل الأطفال (شلل الأطفال)، الذي يسببه فيروس شلل الأطفال، هو مرض معوي في المقام الأول ينتقل، في نسبة صغيرة من الحالات، إلى الجهاز العصبي، مما يسبب الشلل وربما الموت. فيروس شلل الأطفال مرض شديد العدوى، حيث يحدث انتقاله عن طريق البراز - الفم أو عن طريق الرذاذ أو الرذاذ أو الرذاذ. ما يقرب من 72٪ من جميع حالات عدوى فيروس شلل الأطفال لا تظهر عليها أعراض؛ وتؤدي 25٪ أخرى فقط إلى مرض معوي خفيف، مما يؤدي إلى الغثيان والحمى والصداع. 12 ومع ذلك، حتى في غياب الأعراض، يمكن للمرضى المصابين بالفيروس التخلص منه في البراز والإفرازات الفموية، مما قد ينقل الفيروس إلى الآخرين. في حوالي حالة واحدة من كل 200، يؤثر فيروس شلل الأطفال على الخلايا في الجهاز العصبي المركزي. 13
بعد دخوله عن طريق الفم، يحدث التكاثر الأولي لفيروس شلل الأطفال في موقع الزرع في البلعوم والجهاز الهضمي. مع تقدم العدوى، عادة ما يكون فيروس شلل الأطفال موجودًا في الحلق وفي البراز قبل ظهور الأعراض. بعد أسبوع واحد من ظهور الأعراض، يقل عدد فيروسات شلل الأطفال في الحلق، ولكن لعدة أسابيع، يستمر إفراز فيروس شلل الأطفال في البراز. يغزو فيروس شلل الأطفال الأنسجة اللمفاوية المحلية، ويدخل مجرى الدم، ومن ثم قد يصيب خلايا الجهاز العصبي المركزي. يؤدي تكرار فيروس شلل الأطفال في الخلايا العصبية الحركية لخلايا القرن الأمامي في الحبل الشوكي أو جذع الدماغ أو القشرة الحركية إلى تدمير الخلايا ويؤدي إلى الشلل الرخو. في الحالات الشديدة، يمكن أن يشمل ذلك الجهاز التنفسي، مما يؤدي إلى الوفاة. يتم علاج المرضى الذين يعانون من اختلال وظائف الجهاز التنفسي باستخدام أنظمة التهوية ذات الضغط الإيجابي. في الماضي، كان المرضى يقتصرون أحيانًا على أجهزة تنفس إيمرسون، والمعروفة أيضًا باسم الرئتين الحديدية (الشكل\(\PageIndex{4}\)).
يمكن الكشف المباشر عن فيروس شلل الأطفال من الحلق أو البراز باستخدام النسخ العكسي PCR (RT-PCR) أو التسلسل الجيني لتحديد النمط الجيني لفيروس شلل الأطفال الذي يصيب المريض. يمكن استخدام الاختبارات المصلية لتحديد ما إذا كان المريض قد تم تطعيمه مسبقًا. لا توجد تدابير علاجية لشلل الأطفال؛ ويقتصر العلاج على تدابير داعمة مختلفة. يشمل ذلك مسكنات الألم والراحة والعلاج الحراري لتخفيف التشنجات العضلية والعلاج الطبيعي والأقواس التصحيحية إذا لزم الأمر للمساعدة في المشي والتهوية الميكانيكية للمساعدة في التنفس إذا لزم الأمر.

تم إدخال لقاحين مختلفين في الخمسينيات من القرن الماضي مما أدى إلى انخفاض كبير في شلل الأطفال في جميع أنحاء العالم (الشكل\(\PageIndex{5}\)). لقاح سالك هو فيروس شلل الأطفال المعطل الذي تم تقديمه لأول مرة في عام 1955. يتم تسليم هذا اللقاح عن طريق الحقن العضلي. لقاح سابين هو لقاح شلل الأطفال الفموي الذي يحتوي على فيروس موهن؛ وقد تم ترخيصه للاستخدام في عام 1962. هناك ثلاثة أنماط مصلية لفيروس شلل الأطفال تسبب المرض لدى البشر؛ حيث يعتبر كل من لقاحي سالك وسابين فعّالين ضد جميع هذه الأنواع الثلاثة.
يتم إلقاء الفيروسات الموهنة من لقاح سابين في براز الأفراد المحصنين وبالتالي لديها القدرة على إصابة الأفراد غير المحصنين. بحلول أواخر التسعينيات، يمكن إرجاع حالات شلل الأطفال القليلة التي نشأت في الولايات المتحدة إلى لقاح سابين. في هذه الحالات، من المحتمل أن تكون طفرات الفيروس الموهن بعد التطعيم قد سمحت للميكروب بالعودة إلى شكله الخبيث. لهذا السبب، تحولت الولايات المتحدة حصريًا إلى لقاح سالك في عام 2000. نظرًا لأن لقاح سالك يحتوي على فيروس معطل، فلا يوجد خطر الانتقال إلى الآخرين (انظر اللقاحات). يوصى حاليًا بأربع جرعات من اللقاح للأطفال: في عمر 2 و 4 و 6 إلى 18 شهرًا وفي عمر 4-6 سنوات.
في عام 1988، أطلقت منظمة الصحة العالمية المبادرة العالمية لاستئصال شلل الأطفال بهدف القضاء على شلل الأطفال في جميع أنحاء العالم من خلال التحصين. هذا الهدف قريب من التحقيق الآن. أصبح شلل الأطفال متوطنًا الآن في عدد قليل من البلدان فقط، بما في ذلك أفغانستان وباكستان ونيجيريا، حيث تعطلت جهود التطعيم بسبب الصراع العسكري أو عدم الاستقرار السياسي.

إرهاب شلل الأطفال
في السنوات التي أعقبت الحرب العالمية الثانية، دخلت الولايات المتحدة والاتحاد السوفيتي فترة تعرف باسم الحرب الباردة. على الرغم من عدم وجود صراع مسلح، إلا أن القوتين العظميين كانتا معزولتين دبلوماسيًا واقتصاديًا عن بعضهما البعض، كما يتضح من ما يسمى بالستار الحديدي بين الاتحاد السوفيتي وبقية العالم. بعد عام 1950، كانت الهجرة أو السفر خارج الاتحاد السوفيتي صعبة للغاية، وكان من الصعب أيضًا على الأجانب دخول الاتحاد السوفيتي. كما وضعت الولايات المتحدة قيودًا صارمة على دخول السوفييت إلى البلاد. خلال إدارة أيزنهاور، لم يُسمح إلا لـ 20 طالبًا من طلاب الدراسات العليا من الاتحاد السوفيتي بالحضور للدراسة في الولايات المتحدة سنويًا.
لكن حتى الستار الحديدي لم يكن مناسبًا لشلل الأطفال. أصبح لقاح سالك متاحًا على نطاق واسع في الغرب في عام 1955، وبحلول الوقت الذي كان فيه لقاح سابين جاهزًا للتجارب السريرية، كان معظم السكان المعرضين للإصابة في الولايات المتحدة وكندا قد تم تطعيمهم بالفعل ضد شلل الأطفال. احتاج سابين إلى البحث في مكان آخر عن المشاركين في الدراسة. في ذروة الحرب الباردة، سُمح لميخائيل تشوماكوف بالقدوم إلى الولايات المتحدة لدراسة أعمال سابين. وبالمثل، سُمح لسابين، عالم الأحياء الدقيقة الأمريكي، بالسفر إلى الاتحاد السوفيتي لبدء التجارب السريرية. نظم Chumakov الإنتاج السوفيتي وأدار التجارب التجريبية لاختبار اللقاح الجديد في الاتحاد السوفيتي. بحلول عام 1959، تم علاج أكثر من عشرة ملايين طفل سوفيتي بأمان بلقاح سابين.
نتيجة لحملة التطعيم العالمية بلقاح سابين، انخفض المعدل الإجمالي لشلل الأطفال بشكل كبير. اليوم، تم القضاء على شلل الأطفال تقريبًا في جميع أنحاء العالم ونادرًا ما يظهر في الولايات المتحدة. ربما سيصبح شلل الأطفال قريبًا ثالث مرض ميكروبي يتم استئصاله من عامة السكان [الجدري الصغير وطاعون الماشية (سبب طاعون الماشية) هما المرضان الأولان].
التمارين\(\PageIndex{5}\)
- كيف ينتقل فيروس شلل الأطفال؟
- قارن بين إيجابيات وسلبيات كل من لقاحي شلل الأطفال.
اعتلالات الدماغ الإسفنجية السارية
العوامل المعدية اللاخلوية التي تسمى البريونات مسؤولة عن مجموعة من الأمراض ذات الصلة المعروفة باسم اعتلالات الدماغ الإسفنجية القابلة للانتقال (TSEs) التي تحدث في البشر والحيوانات الأخرى (انظر الفيروسات والفيروسات والبريونات). جميع الأمراض المنقولة بالاتصال الجنسي هي أمراض عصبية تنكسية مميتة تحدث عندما تصاب أنسجة المخ بالبريونات. تبدأ هذه الأمراض ببطء؛ فقد لا تظهر الأعراض إلا بعد فترة حضانة تمتد لسنوات وربما عقود، لكن الوفاة تحدث عادة في غضون أشهر إلى بضع سنوات بعد ظهور الأعراض الأولى.
تشمل الأمراض المنقولة بالاتصال الجنسي (TSEs) في الحيوانات سكرابي، وهو مرض يصيب الأغنام معروف منذ القرن الثامن عشر، ومرض الهزال المزمن، وهو مرض يصيب الغزلان والأيائل في الولايات المتحدة وكندا. يظهر مرض جنون البقر في الماشية ويمكن أن ينتقل إلى البشر من خلال استهلاك الأنسجة العصبية المصابة. تشمل أمراض البريون البشرية مرض كروتزفيلدت-جاكوب والكورو، وهو مرض نادر مستوطن في بابوا غينيا الجديدة.
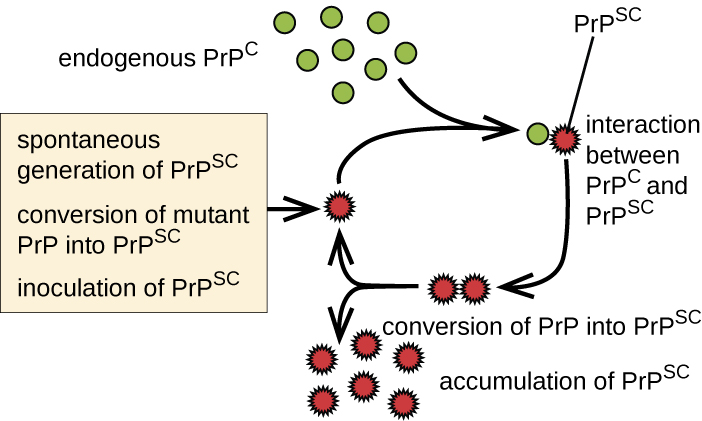
البريونات هي جزيئات بروتينية معدية ليست فيروسات ولا تحتوي على حمض نووي. عادة ما تنتقل عن طريق التعرض لأنسجة الجهاز العصبي المصابة وابتلاعها، وزرع الأنسجة، ونقل الدم، أو الفوميتات الملوثة. توجد بروتينات البريون عادة في أنسجة المخ السليمة في شكل يسمى PrP C. ومع ذلك، إذا تم خلط هذا البروتين في شكل مشوه (PrP Sc)، فقد يسبب المرض. على الرغم من أن الوظيفة الدقيقة لـ PrP C ليست مفهومة حاليًا، فإن البروتين يتحول في الغالب إلى حلزون ألفا ويربط النحاس. من ناحية أخرى، يتحول البروتين المارق في الغالب إلى صفائح مطوية ببيتا وهو مقاوم للتحلل البروتيني. بالإضافة إلى ذلك، يمكن لـ PrP Sc أن يحفز PrP C على أن يصبح مطويًا وينتج المزيد من البروتين المارق (الشكل\(\PageIndex{6}\)).
عندما يتراكم PrP Sc، فإنه يتجمع ويشكل الألياف داخل الخلايا العصبية. تتسبب مركبات البروتين هذه في نهاية المطاف في موت الخلايا. ونتيجة لذلك، تشكل أنسجة المخ للأفراد المصابين كتلًا من التشابك الليفي العصبي واللوحات النشوانية التي تعطي الدماغ مظهرًا إسفنجيًا، وهذا هو سبب تسمية هذه الأمراض باعتلال الدماغ الإسفنجي (الشكل 6.4.3). يؤدي تلف أنسجة المخ إلى مجموعة متنوعة من الأعراض العصبية. في الغالب، يعاني الأفراد المصابون من فقدان الذاكرة وتغيرات الشخصية وعدم وضوح الرؤية والحركات غير المنسقة والأرق. تتفاقم هذه الأعراض تدريجيًا بمرور الوقت وتبلغ ذروتها في الغيبوبة والموت.
المعيار الذهبي لتشخيص TSE هو الفحص النسيجي لخزعات الدماغ لوجود لويحات الأميلويد المميزة والفجوات وبروتينات البريون. يجب على الأطباء توخي الحذر الشديد عند التعامل مع المواد المشتبه في إصابتها بالبريون لتجنب الإصابة بأنفسهم. تبحث فحوصات الأنسجة الأخرى عن وجود بروتين 14-3-3، وهو علامة لأمراض البريون مثل مرض كروتزفيلدت-جاكوب. توفر الاختبارات الجديدة، مثل RT-Quic (التحويل الناجم عن الزلازل في الوقت الفعلي)، أملاً جديدًا للكشف الفعال عن بروتينات البريون غير الطبيعية في الأنسجة في وقت مبكر من مسار العدوى. لا يمكن علاج أمراض البريون. ومع ذلك، قد تساعد بعض الأدوية في إبطاء تقدمها. يركز الدعم الطبي على إبقاء المرضى مرتاحين قدر الإمكان على الرغم من الأعراض التدريجية والمنهكة.
نظرًا لأن المواد الملوثة بالبريون هي مصادر محتملة للعدوى للعلماء والأطباء السريريين، توفر كل من منظمة الصحة العالمية ومراكز مكافحة الأمراض والوقاية منها معلومات لإعلام وتثقيف وتقليل مخاطر العدوى بسبب البريونات.
التمارين\(\PageIndex{6}\)
- هل تتكاثر البريونات بالمعنى التقليدي؟
- ما العلاقة بين البريونات وإزالة المنتجات الثانوية الحيوانية من طعام حيوانات المزرعة؟
الالتهابات اللاخلوية للجهاز العصبي
العواقب الخطيرة هي الخيط المشترك بين هذه الأمراض العصبية. يتسبب العديد منها في الإصابة بالشلل المنهك، وبعضها، مثل داء كروتزفيلد جاكوب وداء الكلب، يكون دائمًا أو تقريبًا مميتًا. ونظراً لقلة الأدوية المتاحة لمكافحة هذه العدوى، فإن مكافحة النواقل والتطعيم أمران حاسمان للوقاية والاحتواء. \(\PageIndex{7}\)يلخص الشكل بعض الالتهابات الفيروسية والبريونية المهمة للجهاز العصبي.
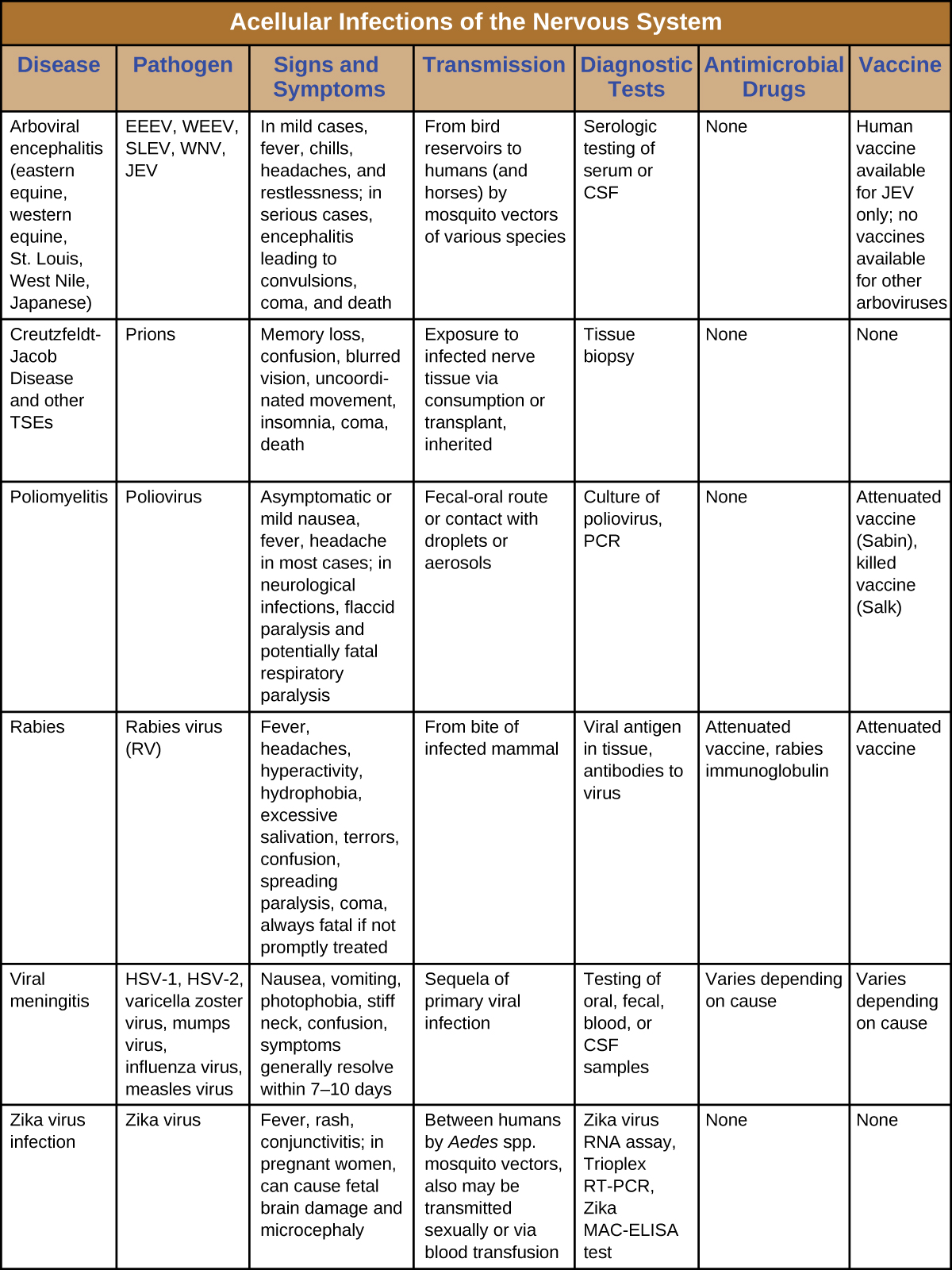
المفاهيم الأساسية والملخص
- يعد التهاب السحايا الفيروسي أكثر شيوعًا وأقل حدة بشكل عام من التهاب السحايا الجرثومي. يمكن أن ينتج عن عقابيل ثانوية للعديد من الفيروسات أو أن يكون ناتجًا عن عدوى فيروسات أربوفيروس.
- تتركز أنواع مختلفة من التهاب الدماغ بالفيروسات الشجرية في مواقع جغرافية معينة في جميع أنحاء العالم. عادةً ما تكون هذه العدوى الفيروسية التي ينقلها البعوض في الجهاز العصبي خفيفة، ولكنها قد تكون مهددة للحياة في بعض الحالات.
- فيروس زيكا هو عدوى فيروسية ناشئة ذات أعراض خفيفة بشكل عام في معظم الأفراد، ولكن عدوى النساء الحوامل يمكن أن تسبب صغر الرأس الناجم عن العيب الخلقي.
- عادةً ما يكون شلل الأطفال عدوى معوية خفيفة ولكن يمكن أن يكون ضارًا أو مميتًا إذا تطور إلى مرض عصبي.
- داء الكلب دائمًا ما يكون مميتًا عند عدم علاجه ويظل مشكلة كبيرة في جميع أنحاء العالم.
- تحدث الاعتلالات الدماغية الإسفنجية السارية مثل مرض كروتزفيلد جاكوب والكورو بسبب البريونات. هذه الأمراض غير قابلة للعلاج ومميتة في نهاية المطاف. توجد أمراض بريون مماثلة في الحيوانات.
الحواشي
- 1 المراكز الأمريكية لمكافحة الأمراض والوقاية منها، «حالات ووفيات مرض فيروس التهاب الدماغ الخيلي الشرقي المبلغ عنها إلى مراكز مكافحة الأمراض والوقاية منها حسب السنة والعرض السريري، 2004-2013"، 2014. www.cdc.gov/Easternequineence... _2004-2013.pdf.
- 2 مراكز أمريكية لمكافحة الأمراض والوقاية منها، «التهاب الدماغ الخيلي الشرقي، الأعراض والعلاج، 2016"، تم الوصول إليه في 29 يونيو 2016. https://www.cdc.gov/easternequineenc... /symptoms.html.
- 3 مراكز الولايات المتحدة لمكافحة الأمراض والوقاية منها، «التهاب الدماغ الخيلي الغربي - الولايات المتحدة وكندا، 1987"، التقرير الأسبوعي للمراضة والوفيات 36، رقم 39 (1987): 655.
- 4 مراكز أمريكية لمكافحة الأمراض والوقاية منها، «التهاب الدماغ في سانت لويس، علم الأوبئة والتوزيع الجغرافي»، تم الوصول إليها في 30 يونيو 2016. http://www.cdc.gov/sle/technical/epi.html.
- 5 مراكز أمريكية لمكافحة الأمراض والوقاية منها، «التهاب الدماغ في سانت لويس، الأعراض والعلاج»، تم الوصول إليها في 30 يونيو 2016. http://www.cdc.gov/sle/technical/symptoms.html.
- 6 مراكز أمريكية لمكافحة الأمراض والوقاية منها، «التهاب الدماغ الياباني والأعراض والعلاج»، تم الوصول إليها في 30 يونيو 2016. www.cdc.gov/japaneseenephali... oms/index.html.
- (7) سيكا، وفيرونيكا، وفيجاي كومار تشاتو، وراج ك. بوبلي، وساغار سي غالوانكار، وداناشري كيلكار، وستانلي جي. ساويكي، وستانيسلاف بي ستاويكي، وتوماس جيه باباديموس، «ظهور فيروس زيكا كتهديد للأمن الصحي العالمي: مراجعة وبيان توافقي لفريق العمل المشترك التابع للاتحاد الدولي للدفاع عن حقوق الإنسان،» مجلة الأمراض المعدية العالمية 8، العدد 1 (2016): 3.
- 8 ملاكار، جيرنيج، ميسا كورفا، ناتاشا تول، مارا بوبوفيتش، ماتيا بوليشاك - بريجاتيلج، جيريكا مراز، ماركو كولينك وآخرون، «فيروس زيكا المرتبط بصغر الرأس»، مجلة نيو إنجلاند للطب 374، رقم 10 (2016): 951-8.
- 9 مراكز أمريكية لمكافحة الأمراض والوقاية منها، «داء الكلب، الحيوانات البرية»، 2016. تم الوصول إليه في 13 سبتمبر 2016. www.cdc.gov/rabies/location/u... d_animals.html.
- 10 سليت، دينيس، تشارلز إي روبريخت، جين أ. روني، دينيس دونوفان، دونالد إتش لين، وريتشارد بي تشيبمان، «حالة التطعيم الفموي ضد داء الكلب في الحيوانات آكلة اللحوم البرية في الولايات المتحدة»، أبحاث الفيروسات 111، رقم 1 (2005): 68-76.
- (11) فينيغان، كريستوفر جيه، شارون إم بروكس، نيكولاس جونسون، جيما سميث، كارين إل مانسفيلد، فيكتوريا إل كين، لورين م. ماكيلهيني، وأنتوني آر فوكس، «داء الكلب في أمريكا الشمالية وأوروبا»، مجلة الجمعية الملكية للطب 95، رقم 1 (2002): 9-13. www.ncbi.nlm.nih.gov/pmC/المقالات/PMC1279140/.
- 12 مركزًا أمريكيًا لمكافحة الأمراض والوقاية منها، «الصحة العالمية - شلل الأطفال»، 2014. تم الوصول إليه في 30 يونيو 2016. http://www.cdc.gov/polio/about/index.htm.
- 13 مركزًا أمريكيًا لمكافحة الأمراض والوقاية منها، «الصحة العالمية - شلل الأطفال»، 2014. تم الوصول إليه في 30 يونيو 2016. http://www.cdc.gov/polio/about/index.htm.


