8.2: هدم الكربوهيدرات
- Page ID
- 194791
أهداف التعلم
- وصف سبب عدم اعتماد تحلل السكر على الأكسجين
- حدد ووصف العائد الصافي لجزيئات الكربون الثلاثة و ATP و NADH من تحلل السكر
- اشرح كيف يتم تحويل جزيئات البيروفات ثلاثية الكربون إلى مجموعات أسيتيل ثنائية الكربون يمكن توجيهها إلى دورة كريبس.
- تحديد ووصف العائد الصافي لثاني أكسيد الكربون و GTP/ATP و FADH 2 و NADH من دورة كريبس
- اشرح كيف يمكن استخدام جزيئات الكربون الوسيطة لدورة كريبس في الخلية
توجد مسارات إنزيمية واسعة النطاق لتكسير الكربوهيدرات لالتقاط الطاقة في روابط ATP. بالإضافة إلى ذلك، تنتج العديد من المسارات التقويضية جزيئات وسيطة تستخدم أيضًا ككتل بناء لعملية الأيض. إن فهم هذه العمليات مهم لعدة أسباب. أولاً، نظرًا لأن عمليات التمثيل الغذائي الرئيسية المعنية شائعة في مجموعة واسعة من كائنات التغذية الكيميائية، يمكننا أن نتعلم الكثير عن التمثيل الغذائي البشري من خلال دراسة التمثيل الغذائي في البكتيريا التي يسهل معالجتها مثل E. coli. ثانيًا، نظرًا لأن مسببات الأمراض الحيوانية والبشرية هي أيضًا كائنات كيميائية متغيرة، فإن التعرف على تفاصيل التمثيل الغذائي في هذه البكتيريا، بما في ذلك الاختلافات المحتملة بين المسارات البكتيرية والبشرية، مفيد لتشخيص مسببات الأمراض وكذلك لاكتشاف العلاجات المضادة للميكروبات التي تستهدف مسببات أمراض محددة. أخيرًا، يعد التعلم تحديدًا حول المسارات التي ينطوي عليها التمثيل الغذائي الكيميائي أيضًا بمثابة أساس لمقارنة استراتيجيات التمثيل الغذائي الأخرى الأكثر غرابة التي تستخدمها الميكروبات. على الرغم من أن المصدر الكيميائي للإلكترونات التي تبدأ نقل الإلكترون يختلف بين الكيمياء المتجانسة والكيميائية، إلا أن العديد من العمليات المماثلة تستخدم في كلا النوعين من الكائنات الحية.
المثال النموذجي المستخدم لتقديم مفاهيم التمثيل الغذائي للطلاب هو هدم الكربوهيدرات. بالنسبة للمواد الكيميائية المتغايرة، تبدأ أمثلة التمثيل الغذائي لدينا بهدم السكريات مثل الجليكوجين أو النشا أو السليلوز. يمكن أن تتسبب الإنزيمات مثل الأميليز، الذي يكسر الجليكوجين أو النشا، والسليولاز، التي تكسر السليلوز، في التحلل المائي للروابط الغليكوزيدية بين مونومرات الجلوكوز في هذه البوليمرات، مما يؤدي إلى إطلاق الجلوكوز لمزيد من الهدم.
تحلل السكر
بالنسبة للبكتيريا وحقيقيات النوى ومعظم الأركيا، فإن تحلل السكر هو المسار الأكثر شيوعًا لتقويض الجلوكوز؛ فهو ينتج الطاقة ويقلل من حاملات الإلكترون والجزيئات الأولية لعملية التمثيل الغذائي الخلوي. يقوم كل كائن حي بنوع من تحلل السكر، مما يشير إلى أن هذه الآلية هي عملية استقلابية عالمية قديمة. لا تستخدم العملية نفسها الأكسجين؛ ومع ذلك، يمكن أن يقترن تحلل السكر بعمليات أيضية إضافية إما هوائية أو لاهوائية. يحدث تحلل السكر في السيتوبلازم للخلايا بدائية النواة وخلايا حقيقية النواة. يبدأ بجزيء جلوكوز واحد من ستة كربون وينتهي بجزيئين من سكر ثلاثي الكربون يسمى البيروفات. قد يتحلل البيروفات أكثر بعد تحلل السكر لتسخير المزيد من الطاقة من خلال التنفس الهوائي أو اللاهوائي، ولكن العديد من الكائنات الحية، بما في ذلك العديد من الميكروبات، قد تكون غير قادرة على التنفس؛ بالنسبة لهذه الكائنات، قد يكون تحلل السكر هو المصدر الوحيد لتوليد ATP.
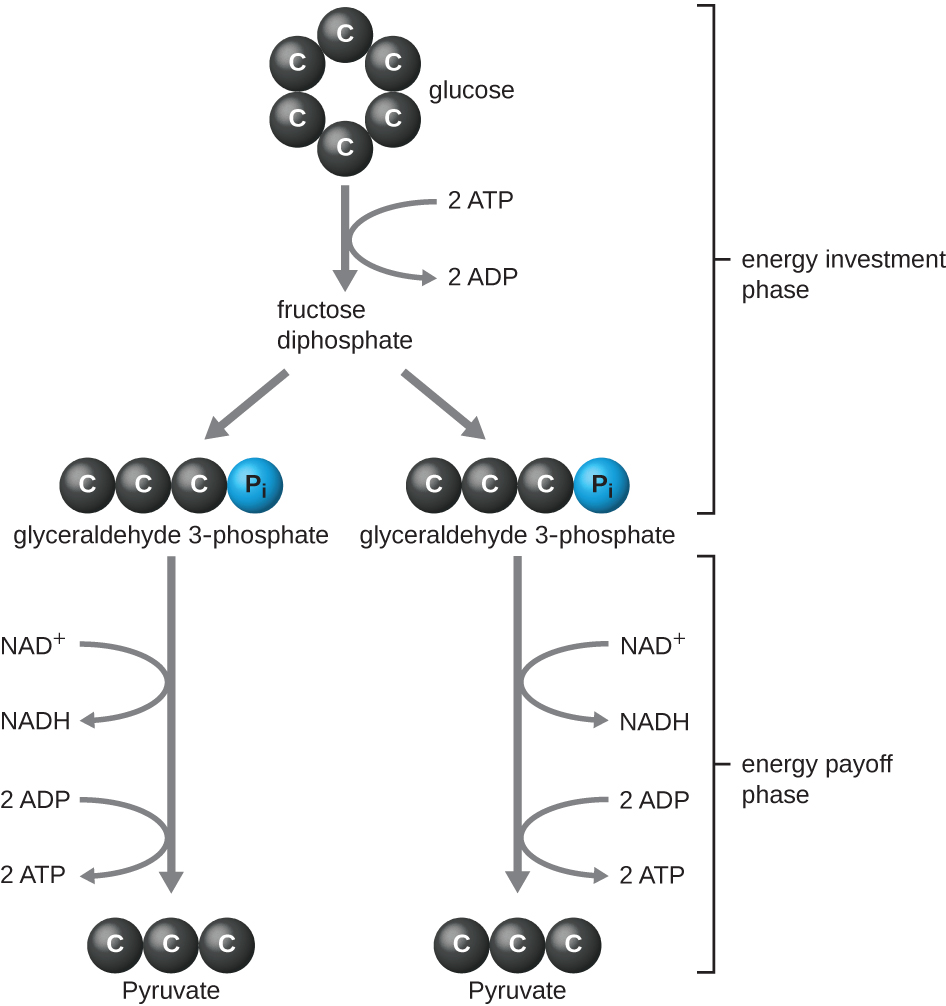
نوع تحلل السكر الموجود في الحيوانات والأكثر شيوعًا في الميكروبات هو مسار Embend-Meyerhof-Parnas (EMP)، الذي سمي على اسم غوستاف إمبدن (1874-1933) وأوتو مايرهوف (1884-1951) وجاكوب بارناس (1884—1949). يتكون تحلل السكر باستخدام مسار EMP من مرحلتين متميزتين (الشكل\(\PageIndex{1}\)). يستخدم الجزء الأول من المسار، الذي يُطلق عليه مرحلة استثمار الطاقة، الطاقة من جزيئين من ATP لتعديل جزيء الجلوكوز بحيث يمكن تقسيم جزيء السكر المكون من ستة كربون بالتساوي إلى جزيئين فوسفوريين ثلاثي الكربون يسمى الجلسرين ثلاثي الفوسفات (G3P). يستخرج الجزء الثاني من المسار، المسمى بمرحلة مكافأة الطاقة، الطاقة عن طريق أكسدة G3P إلى البيروفات، وإنتاج أربعة جزيئات ATP وتقليل جزيئين من NAD+ إلى جزيئين من NADH، باستخدام الإلكترونات التي نشأت من الجلوكوز. (تظهر مناقشة وتوضيح لمسار EMP الكامل مع الهياكل الكيميائية وأسماء الإنزيمات في الملحق C.)
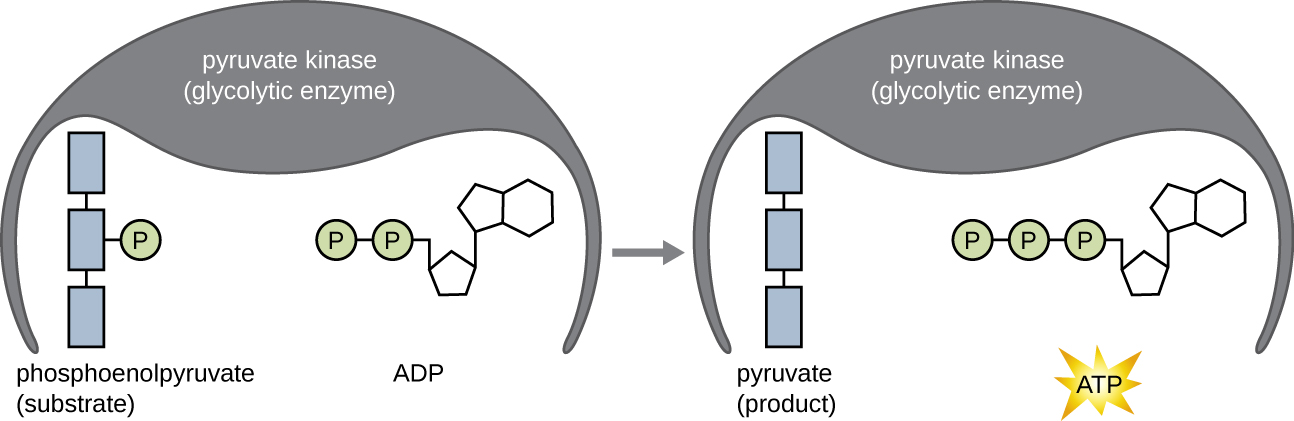
تتكون جزيئات ATP المنتجة خلال مرحلة مردود الطاقة لتحلل السكر عن طريق الفسفرة على مستوى الركيزة (الشكل\(\PageIndex{1}\))، وهي إحدى آليتين لإنتاج ATP. في الفسفرة على مستوى الركيزة، تتم إزالة مجموعة الفوسفات من الجزيء العضوي ويتم نقلها مباشرة إلى جزيء ADP المتاح، مما ينتج ATP. أثناء تحلل السكر، تتم إضافة مجموعات الفوسفات عالية الطاقة من الجزيئات الوسيطة إلى ADP لصنع ATP.
بشكل عام، في عملية تحلل السكر هذه، يكون الربح الصافي من انهيار جزيء جلوكوز واحد هو:
- جزيئان ATP
- اثنين من جزيئات NADH، و
- جزيئان من البيروفات.
مسارات تحلل السكر الأخرى
عندما نشير إلى تحلل السكر، ما لم يُذكر خلاف ذلك، فإننا نشير إلى مسار EMP الذي تستخدمه الحيوانات والعديد من البكتيريا. ومع ذلك، تستخدم بعض بدائيات النواة مسارات بديلة للجلوكليتيك. أحد البدائل المهمة هو مسار Entner-Doudoroff (ED)، الذي سمي على اسم مكتشفيه ناثان إنتنر ومايكل دودوروف (1911-1975). على الرغم من أن بعض البكتيريا، بما في ذلك العامل الممرض الانتهازي السلبي للجرام Pseudomonas aeruginosa، تحتوي فقط على مسار الضعف الجنسي لتحلل السكر، فإن البكتيريا الأخرى، مثل E. coli، لديها القدرة على استخدام مسار الضعف الجنسي أو مسار EMP.
النوع الثالث من مسار تحلل السكر الذي يحدث في جميع الخلايا، والذي يختلف تمامًا عن المسارين السابقين، هو مسار فوسفات البنتوس (PPP) الذي يُطلق عليه أيضًا مسار الفوسفوغلوكونات أو تحويلة سداسي الفوسفات أحادي الفوسفات. تشير الأدلة إلى أن PPP قد يكون أقدم مسار سكري عالمي. يتم استخدام المواد الوسيطة من PPP للتخليق الحيوي للنيوكليوتيدات والأحماض الأمينية. لذلك، قد يكون هذا المسار الجليكلي مفضلًا عندما تحتاج الخلية إلى الحمض النووي و/أو تخليق البروتين، على التوالي. تظهر مناقشة وتوضيح لمسار ED الكامل و PPP مع الهياكل الكيميائية وأسماء الإنزيمات في الملحق C.
التمارين\(\PageIndex{1}\)
متى يمكن للكائن الحي استخدام مسار الضعف الجنسي أو PPP لتحلل السكر؟
التفاعل الانتقالي والإنزيم المساعد A ودورة كريبس
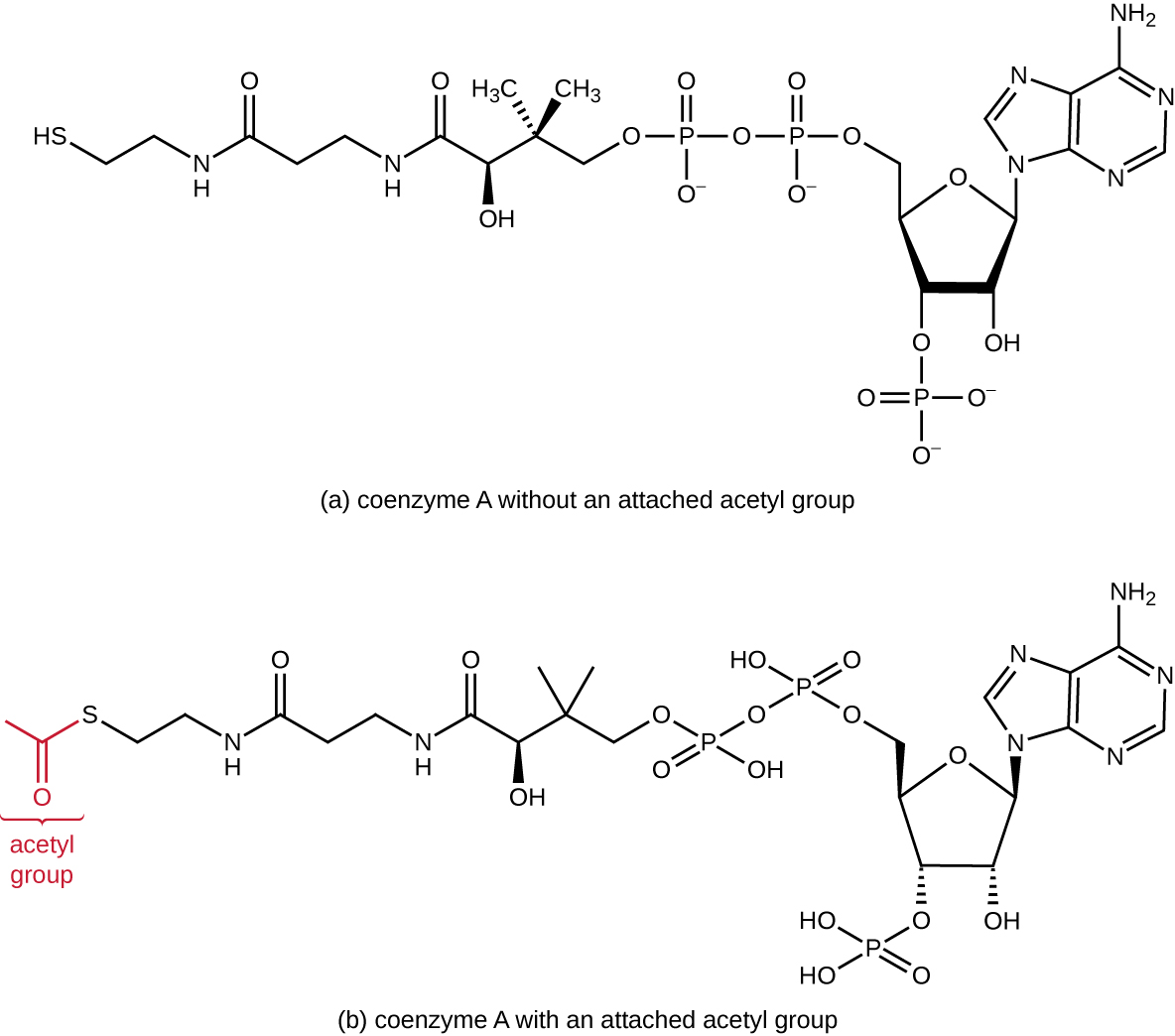
ينتج تحلل السكر البيروفات، والتي يمكن أن تتأكسد أكثر لالتقاط المزيد من الطاقة. لكي يدخل البيروفات في المسار التأكسدي التالي، يجب أولاً نزع الكربوكسيل بواسطة مركب الإنزيم ثنائي هيدروجينيز البيروفات إلى مجموعة أسيتيل ثنائية الكربون في التفاعل الانتقالي، وتسمى أيضًا تفاعل الجسر (انظر الملحق C والشكل\(\PageIndex{3}\)). في التفاعل الانتقالي، يتم نقل الإلكترونات أيضًا إلى NAD+ لتشكيل NADH. للانتقال إلى المرحلة التالية من عملية التمثيل الغذائي هذه، يجب ربط الأسيتيل الصغير نسبيًا ثنائي الكربون بمركب حامل كبير جدًا يسمى الإنزيم المساعد A (CoA). يحدث التفاعل الانتقالي في مصفوفة الميتوكوندريا لحقيقيات النوى؛ وفي بدائيات النواة، يحدث في السيتوبلازم لأن بدائيات النواة تفتقر إلى العضيات المغلقة بالغشاء.
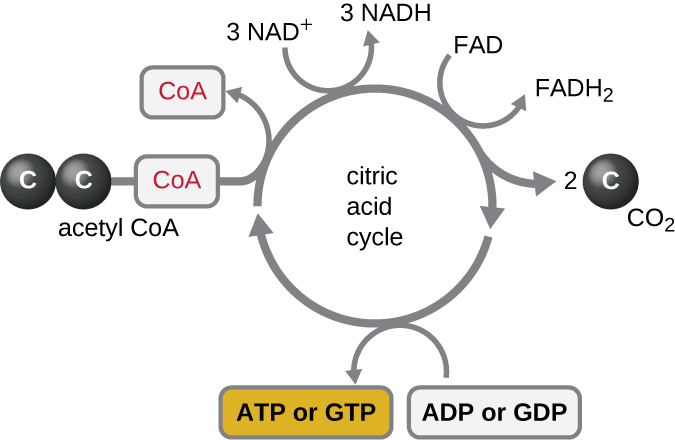
تقوم دورة كريبس بنقل الإلكترونات المتبقية من مجموعة الأسيتيل المنتجة أثناء التفاعل الانتقالي إلى جزيئات حامل الإلكترون، وبالتالي تقليلها. تحدث دورة كريبس أيضًا في سيتوبلازم بدائيات النواة جنبًا إلى جنب مع تحلل السكر والتفاعل الانتقالي، ولكنها تحدث في مصفوفة الميتوكوندريا للخلايا حقيقية النواة حيث يحدث التفاعل الانتقالي أيضًا. تمت تسمية دورة كريبس على اسم مكتشفها، العالم البريطاني هانز أدولف كريبس (1900-1981) وتسمى أيضًا دورة حمض الستريك، أو دورة حمض التريكاربوكسيليك (TCA) لأن حمض الستريك يحتوي على ثلاث مجموعات من الكربوكسيل في تركيبته. على عكس تحلل السكر، فإن دورة كريبس عبارة عن حلقة مغلقة: الجزء الأخير من المسار يجدد المركب المستخدم في الخطوة الأولى (الشكل\(\PageIndex{4}\)). الخطوات الثماني للدورة هي سلسلة من التفاعلات الكيميائية التي تلتقط مجموعة الأسيتيل ثنائي الكربون (لا يدخل حامل CoA دورة كريبس) من تفاعل الانتقال، والذي يتم إضافته إلى وسيط رباعي الكربون في دورة كريبس، مما ينتج حمض الستريك الوسيط المكون من ستة كربون (يعطي اسم بديل لهذه الدورة). عندما تعود دورة واحدة من الدورة إلى نقطة البداية للوسيط رباعي الكربون، تنتج الدورة جزيئين من ثاني أكسيد الكربون، وجزيء ATP واحد (أو ما يعادله، مثل جوانوزين ثلاثي الفوسفات [GTP]) ينتج عن الفسفرة على مستوى الركيزة، وثلاثة جزيئات من NADH وواحد من FADH 2 . (تظهر مناقشة وتوضيح مفصل لدورة كريبس الكاملة في الملحق C.)
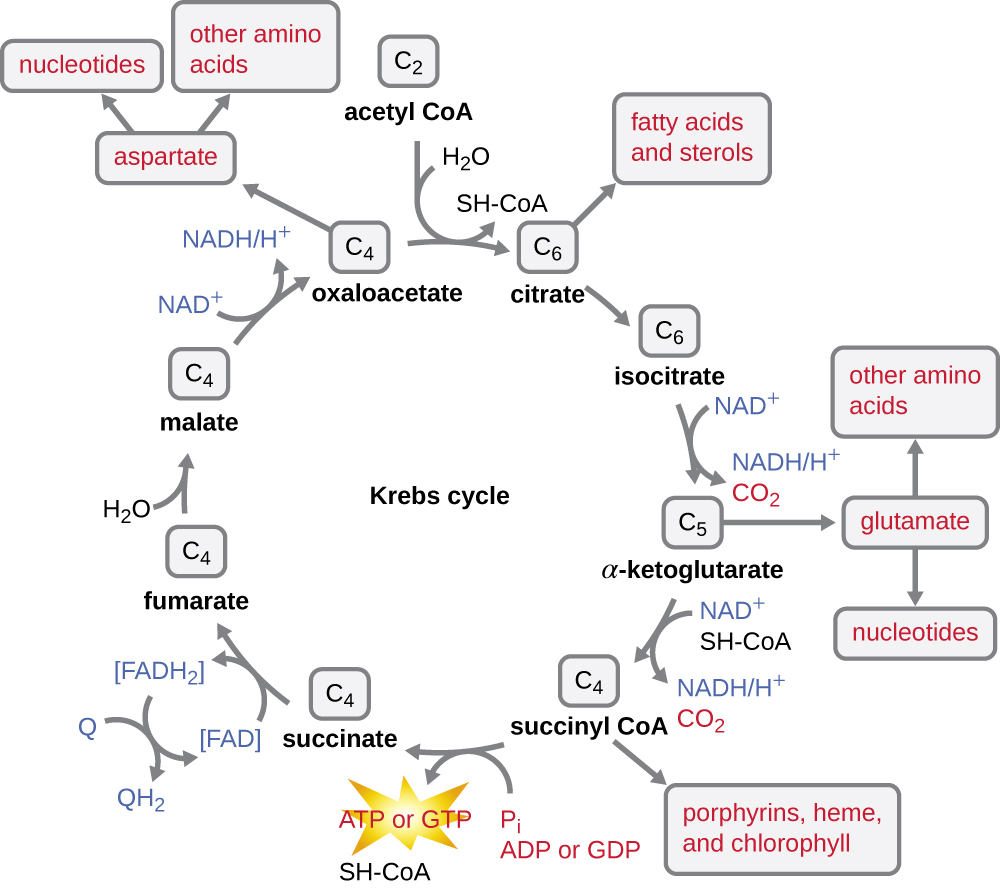
على الرغم من أن العديد من الكائنات الحية تستخدم دورة كريبس كما هو موضح كجزء من استقلاب الجلوكوز، يمكن استخدام العديد من المركبات الوسيطة في دورة كريبس في تركيب مجموعة متنوعة من الجزيئات الخلوية المهمة، بما في ذلك الأحماض الأمينية والكلوروفيل والأحماض الدهنية والنيوكليوتيدات؛ وبالتالي، فإن الدورة هي كل من الابتنائية والتقويضية (الشكل\(\PageIndex{5}\)).
المفاهيم الأساسية والملخص
- تحلل السكر هو الخطوة الأولى في تكسير الجلوكوز، مما يؤدي إلى تكوين ATP، الذي ينتج عن طريق الفسفرة على مستوى الركيزة؛ NADH؛ وجزيئين من البيروفات. لا يستخدم تحلل السكر الأكسجين ولا يعتمد على الأكسجين.
- بعد تحلل السكر، يتم نزع الكربوكسيل من البيروفات ثلاثي الكربون لتشكيل مجموعة أسيتيل ثنائية الكربون، إلى جانب تكوين NADH. ترتبط مجموعة الأسيتيل بمركب حامل كبير يسمى الإنزيم المساعد A.
- بعد الخطوة الانتقالية، ينقل الإنزيم المساعد A الأسيتيل ثنائي الكربون إلى دورة كريبس، حيث يدخل الكربونان الدورة. في كل دورة من الدورة، تتأكسد مجموعة أسيتيل واحدة مشتقة من تحلل السكر بشكل إضافي، وتنتج ثلاثة جزيئات NADH، وواحدة FADH 2، وواحدة ATP عن طريق الفسفرة على مستوى الركيزة، وتطلق جزيئين من ثاني أكسيد الكربون.
- يمكن استخدام دورة Krebs لأغراض أخرى. يتم استخدام العديد من المواد الوسيطة لتجميع الجزيئات الخلوية المهمة، بما في ذلك الأحماض الأمينية والكلوروفيل والأحماض الدهنية والنيوكليوتيدات.


