12.4: إمكانات العمل
- Page ID
- 203212
أهداف التعلم
- وصف مكونات الغشاء التي تحدد إمكانات غشاء الراحة
- وصف التغييرات التي تحدث للغشاء والتي تؤدي إلى إمكانية الفعل
تعتمد وظائف الجهاز العصبي - الإحساس والتكامل والاستجابة - على وظائف الخلايا العصبية الكامنة وراء هذه المسارات. لفهم كيفية قدرة الخلايا العصبية على التواصل، من الضروري وصف دور الغشاء المثير في توليد هذه الإشارات. أساس هذا الاتصال هو إمكانات العمل، والتي توضح كيف يمكن للتغيرات في الغشاء أن تشكل إشارة. يتضمن النظر إلى طريقة عمل هذه الإشارات في ظروف أكثر تنوعًا إلقاء نظرة على الإمكانات المقدرة، والتي سيتم تناولها في القسم التالي.
أغشية الخلايا النشطة كهربائيًا
تستخدم معظم خلايا الجسم الجسيمات المشحونة والأيونات لتكوين شحنة عبر غشاء الخلية. في السابق، ثبت أن هذا جزء من كيفية عمل خلايا العضلات. يتطلب تقلص عضلات الهيكل العظمي، بناءً على الإثارة - اقتران الانقباض، مدخلات من خلية عصبية. تستخدم كلتا الخليتين غشاء الخلية لتنظيم حركة الأيونات بين السائل خارج الخلية والخلوي الخلوي.
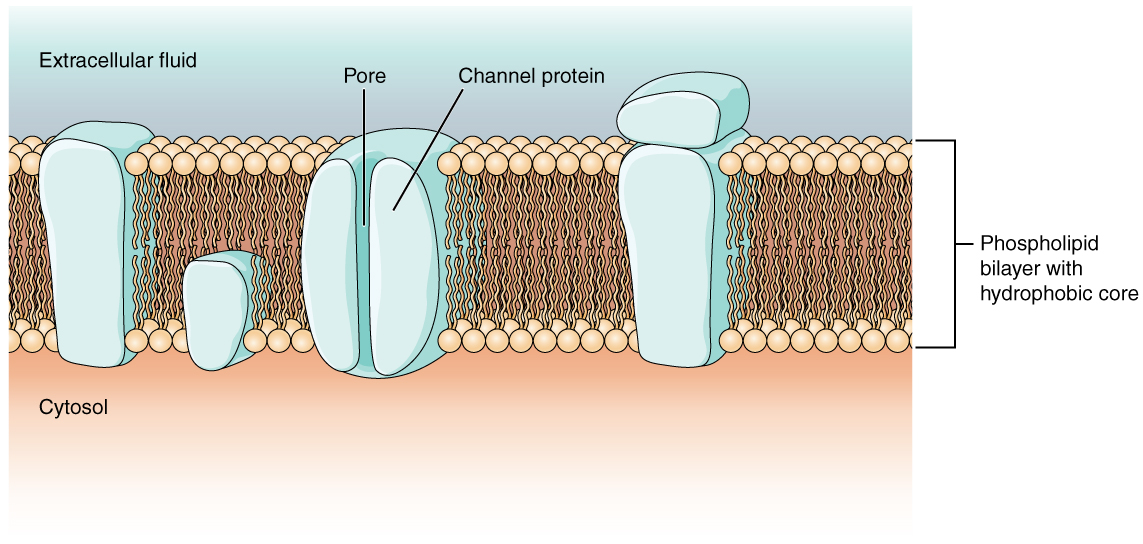
كما تعلمت في الفصل الخاص بالخلايا، فإن غشاء الخلية مسؤول بشكل أساسي عن تنظيم ما يمكن أن يعبر الغشاء وما يبقى على جانب واحد فقط. غشاء الخلية عبارة عن طبقة ثنائية الفسفوليبيد، لذا فإن المواد التي يمكن أن تمر مباشرة عبر النواة الكارهة للماء فقط هي التي يمكن أن تنتشر دون مساعدة. لا يمكن للجسيمات المشحونة، التي هي محبة للماء بحكم تعريفها، أن تمر عبر غشاء الخلية دون مساعدة (الشكل\(\PageIndex{1}\)). تجعل البروتينات عبر الغشاء، وخاصة بروتينات القناة، هذا ممكنًا. تعد العديد من قنوات النقل السلبية، بالإضافة إلى مضخات النقل النشطة، ضرورية لتوليد إمكانات عبر الغشاء وإمكانات العمل. من الأمور ذات الأهمية الخاصة البروتين الناقل الذي يشار إليه بمضخة الصوديوم/البوتاسيوم التي تنقل أيونات الصوديوم (Na +) من الخلية وأيونات البوتاسيوم (K +) إلى الخلية، وبالتالي تنظم تركيز الأيونات على جانبي غشاء الخلية.
تتطلب مضخة الصوديوم/البوتاسيوم طاقة في شكل ثلاثي فوسفات الأدينوزين (ATP)، لذلك يشار إليها أيضًا باسم ATPase. كما هو موضح في فصل الخلية، يكون تركيز Na + أعلى خارج الخلية منه في الداخل، وتركيز K + أعلى داخل الخلية منه في الخارج. وهذا يعني أن هذه المضخة تقوم بتحريك الأيونات مقابل تدرجات تركيز الصوديوم والبوتاسيوم، وهذا هو السبب في أنها تتطلب الطاقة. في الواقع، تحافظ المضخة بشكل أساسي على تدرجات التركيز هذه.
القنوات الأيونية هي مسام تسمح لجزيئات مشحونة معينة بعبور الغشاء استجابة لتدرج التركيز الحالي. البروتينات قادرة على توسيع غشاء الخلية، بما في ذلك جوهرها الكارهة للماء، ويمكن أن تتفاعل مع شحنة الأيونات بسبب الخصائص المتنوعة للأحماض الأمينية الموجودة في مجالات أو مناطق محددة من قناة البروتين. توجد الأحماض الأمينية الكارهة للماء في المجالات التي يتم وضعها على ذيول الهيدروكربون للفوسفوليبيدات. تتعرض الأحماض الأمينية المحبة للماء لبيئات السوائل في السائل خارج الخلية والسيتوسول. بالإضافة إلى ذلك، ستتفاعل الأيونات مع الأحماض الأمينية المحبة للماء، والتي ستكون انتقائية لشحنة الأيون. ستحتوي قنوات الكاتيونات (الأيونات الموجبة) على سلاسل جانبية سالبة الشحنة في المسام. ستحتوي قنوات الأنيونات (الأيونات السالبة) على سلاسل جانبية موجبة الشحنة في المسام. وهذا ما يسمى الاستبعاد الكهروكيميائي، مما يعني أن مسام القناة خاص بالشحنة.
يمكن أيضًا تحديد القنوات الأيونية بقطر المسام. ستكون المسافة بين الأحماض الأمينية محددة لقطر الأيون عندما ينفصل عن جزيئات الماء المحيطة به. نظرًا لجزيئات الماء المحيطة، فإن المسام الكبيرة ليست مثالية للأيونات الصغيرة لأن جزيئات الماء ستتفاعل، عن طريق الروابط الهيدروجينية، بسهولة أكبر من السلاسل الجانبية للأحماض الأمينية. وهذا ما يسمى استبعاد الحجم. بعض القنوات الأيونية انتقائية للشحن ولكن ليس بالضرورة للحجم، وبالتالي تسمى قناة غير محددة. تسمح هذه القنوات غير المحددة للكاتيونات - خاصة Na + و K + و Ca 2+ - بعبور الغشاء، ولكن مع استبعاد الأنيونات.
لا تسمح القنوات الأيونية دائمًا بحرية للأيونات بالانتشار عبر الغشاء. يتم فتح بعضها بأحداث معينة، مما يعني أن القنوات مسورة. لذا فإن الطريقة الأخرى التي يمكن بها تصنيف القنوات هي على أساس كيفية تبويرها. على الرغم من أن هذه الفئات من القنوات الأيونية توجد بشكل أساسي في خلايا الأنسجة العصبية أو العضلية، إلا أنها يمكن العثور عليها أيضًا في خلايا الأنسجة الظهارية والأنسجة الضامة.
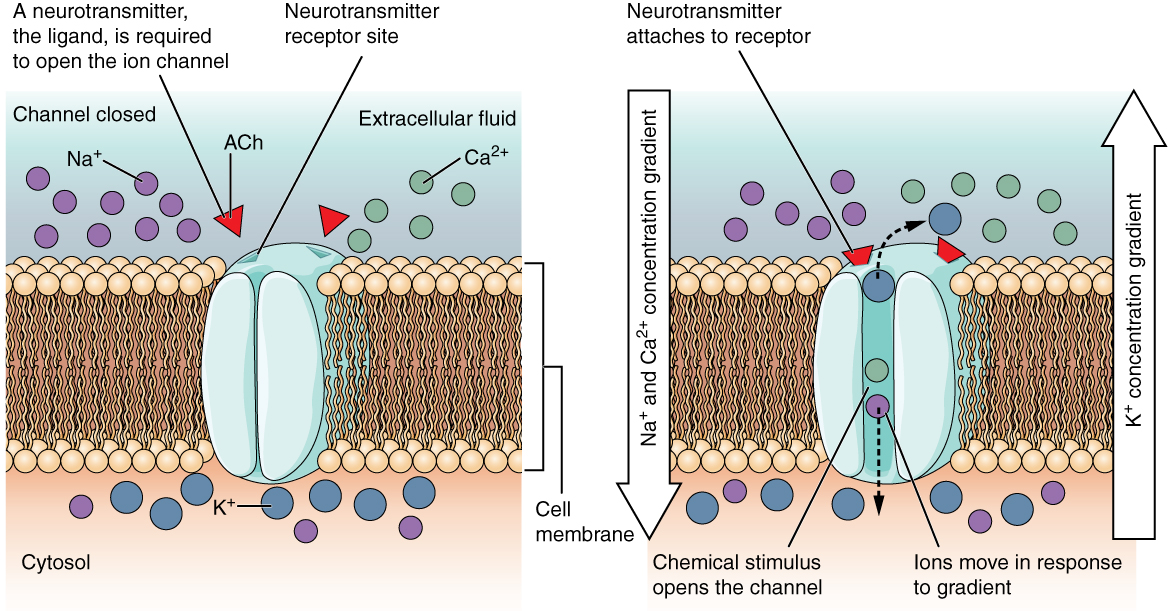
يتم فتح قناة ذات بوابات لولبية لأن جزيء الإشارة، وهو ليجاند، يرتبط بالمنطقة خارج الخلية للقناة. يُعرف هذا النوع من القنوات أيضًا باسم المستقبلات الأيونية لأنه عندما يرتبط الليغند، المعروف باسم الناقل العصبي في الجهاز العصبي، بالبروتين، تعبر الأيونات الغشاء وتغير شحنته (الشكل\(\PageIndex{2}\)).
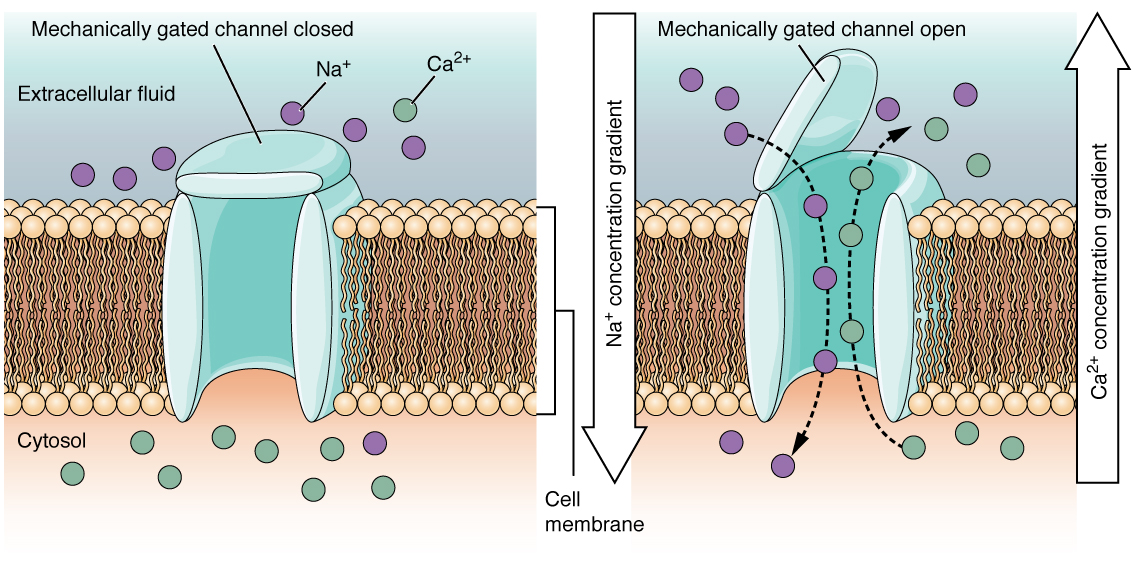
يتم فتح قناة ذات بوابات ميكانيكيًا بسبب التشوه المادي لغشاء الخلية. يتم ربط العديد من القنوات المرتبطة بإحساس اللمس (الإحساس الجسدي) ميكانيكيًا. على سبيل المثال، عند الضغط على الجلد، تفتح هذه القنوات وتسمح للأيونات بالدخول إلى الخلية. على غرار هذا النوع من القنوات، ستكون القناة التي تفتح على أساس التغيرات في درجات الحرارة، كما هو الحال في اختبار الماء في الحمام (الشكل\(\PageIndex{3}\)).
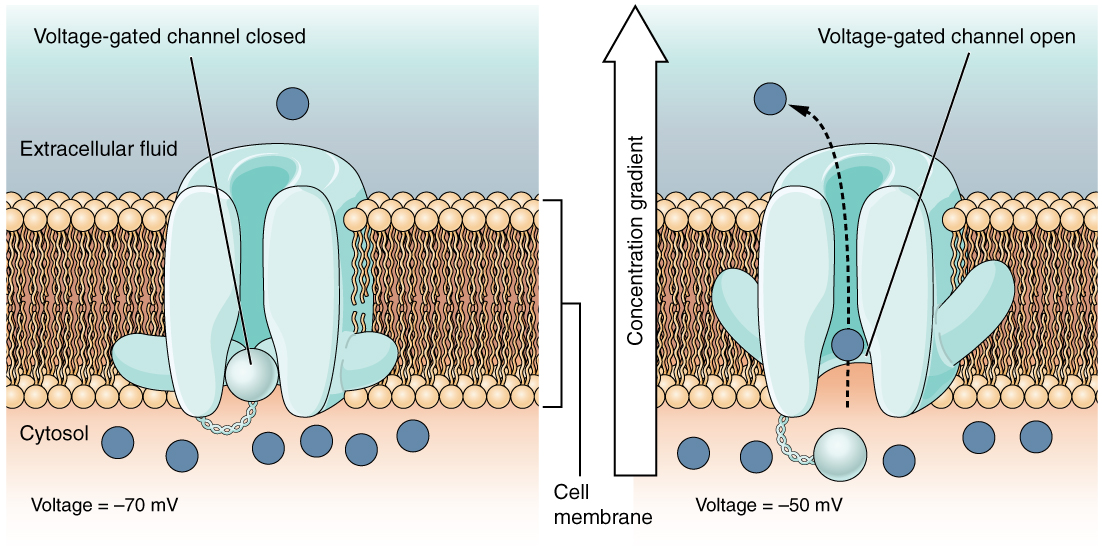
القناة ذات الجهد الكهربائي هي قناة تستجيب للتغيرات في الخواص الكهربائية للغشاء الذي يتم تضمينه فيه. عادةً ما يكون الجزء الداخلي من الغشاء بجهد سالب. عندما يصبح هذا الجهد أقل سالبة، تبدأ القناة في السماح للأيونات بعبور الغشاء (الشكل\(\PageIndex{4}\)).
يتم فتح قناة التسرب بشكل عشوائي، مما يعني أنها تفتح وتغلق بشكل عشوائي، ومن هنا تأتي الإشارة إلى التسرب. لا يوجد حدث فعلي يفتح القناة؛ بدلاً من ذلك، لديها معدل جوهري للتبديل بين الحالات المفتوحة والمغلقة. تساهم قنوات التسرب في الجهد الغشائي المريح للغشاء القابل للإثارة (الشكل\(\PageIndex{5}\)).
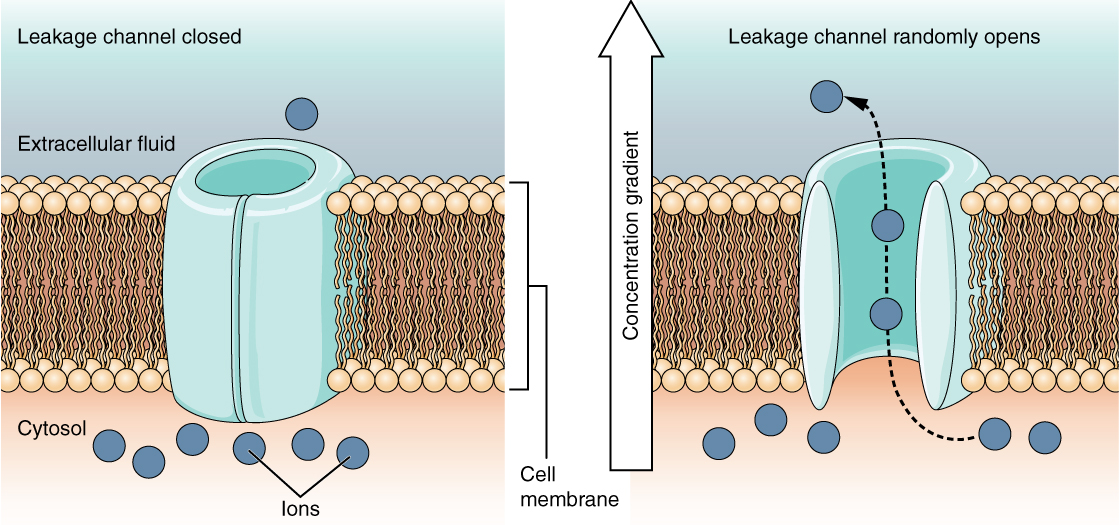
إمكانات الغشاء
يمكن أن تحتوي الحالة الكهربائية لغشاء الخلية على العديد من الاختلافات. هذه كلها اختلافات في إمكانات الغشاء. الاحتمال هو توزيع الشحنة عبر غشاء الخلية، ويتم قياسها بالمليفولت (mV). المعيار هو مقارنة داخل الخلية بالنسبة للخارج، وبالتالي فإن إمكانات الغشاء هي قيمة تمثل الشحنة على الجانب داخل الخلايا من الغشاء استنادًا إلى أن الخارج هو صفر، نسبيًا (الشكل\(\PageIndex{6}\)).
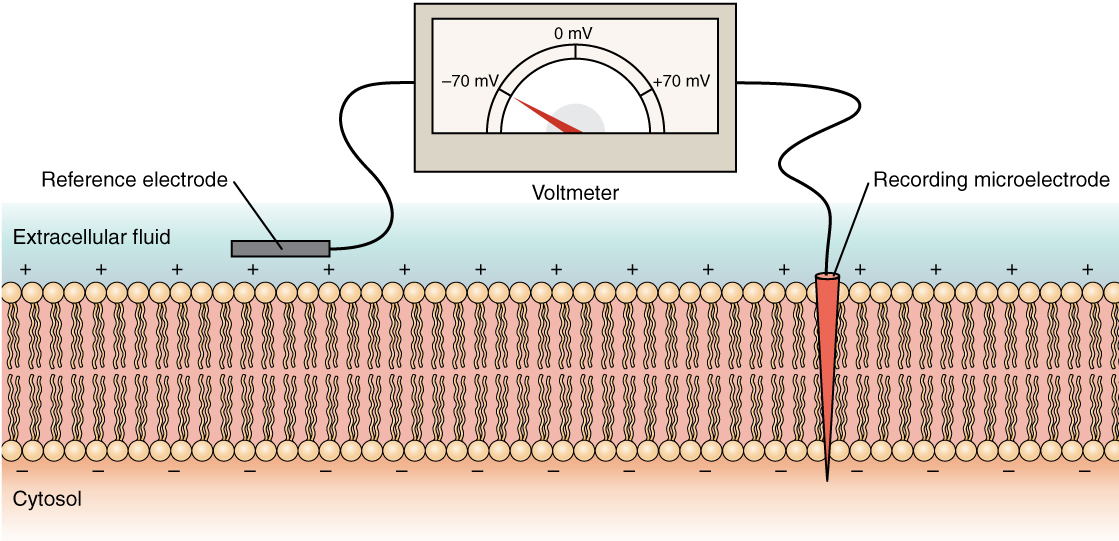
يكون تركيز الأيونات في السوائل خارج الخلية وداخل الخلايا متوازنًا إلى حد كبير، بشحنة صافية محايدة. ومع ذلك، يحدث اختلاف بسيط في الشحنة مباشرة على سطح الغشاء، داخليًا وخارجيًا. إنه الاختلاف في هذه المنطقة المحدودة للغاية التي لديها كل القوة في الخلايا العصبية (وخلايا العضلات) لتوليد إشارات كهربائية، بما في ذلك إمكانات العمل.
قبل وصف هذه الإشارات الكهربائية، يجب شرح حالة الراحة للغشاء. عندما تكون الخلية في حالة راحة، ويتم إغلاق القنوات الأيونية (باستثناء قنوات التسرب التي تفتح عشوائيًا)، يتم توزيع الأيونات عبر الغشاء بطريقة يمكن التنبؤ بها جدًا. تركيز Na + خارج الخلية أكبر بعشر مرات من التركيز في الداخل. كما أن تركيز K + داخل الخلية أكبر من الخارج. يحتوي السيتوسول على نسبة عالية من الأنيونات، في شكل أيونات الفوسفات والبروتينات سالبة الشحنة. الأنيونات الكبيرة هي أحد مكونات غشاء الخلية الداخلية، بما في ذلك الدهون الفوسفورية المتخصصة والبروتينات المرتبطة بالنشرة الداخلية للغشاء (النشرة هي مصطلح يستخدم لجانب واحد من الغشاء ثنائي الطبقة الدهنية). يتم تحديد الشحنة السالبة في الأنيونات الكبيرة.
عند توزيع الأيونات عبر الغشاء بهذه التركيزات، يتم قياس الفرق في الشحنة عند -70 mV، وهي القيمة الموصوفة بقدرة الغشاء الباقي. تختلف القيمة الدقيقة المقاسة لإمكانات غشاء الراحة بين الخلايا، ولكن -70 mV هي الأكثر استخدامًا كقيمة. سيكون هذا الجهد في الواقع أقل بكثير باستثناء مساهمات بعض البروتينات المهمة في الغشاء. تسمح قنوات التسرب لـ Na + بالانتقال ببطء إلى الخلية أو K + بالخروج ببطء، وتستعيدها مضخة Na + /K +. قد يبدو هذا مضيعة للطاقة، ولكن لكل منها دور في الحفاظ على إمكانات الغشاء.
إمكانات العمل
تصف إمكانات الغشاء المستريح الحالة الثابتة للخلية، وهي عملية ديناميكية يتم موازنتها بالتسرب الأيوني وضخ الأيونات. بدون أي تأثير خارجي، لن يتغير. لبدء الإشارة الكهربائية، يجب أن تتغير إمكانات الغشاء.
يبدأ هذا بفتح قناة لـ Na + في الغشاء. نظرًا لأن تركيز Na + أعلى خارج الخلية منه داخل الخلية بعامل 10، فسوف تندفع الأيونات إلى الخلية مدفوعة إلى حد كبير بتدرج التركيز. نظرًا لأن الصوديوم هو أيون ذو شحنة موجبة، فإنه سيغير الجهد النسبي مباشرة داخل الخلية بالنسبة للخارج مباشرة. إمكانات الراحة هي حالة الغشاء بجهد -70 mV، وبالتالي فإن كاتيون الصوديوم الذي يدخل الخلية سيؤدي إلى أن يصبح أقل سلبية. يُعرف هذا باسم إزالة الاستقطاب، مما يعني أن إمكانات الغشاء تتحرك نحو الصفر.
إن تدرج التركيز لـ Na + قوي جدًا لدرجة أنه سيستمر في دخول الخلية حتى بعد أن تصبح إمكانات الغشاء صفرًا، بحيث يبدأ الجهد الموجود حول المسام مباشرة في أن يصبح إيجابيًا. يلعب التدرج الكهربائي أيضًا دورًا، حيث تجذب البروتينات السالبة الموجودة أسفل الغشاء أيون الصوديوم. ستصل إمكانات الغشاء إلى +30 mV بحلول الوقت الذي يدخل فيه الصوديوم الخلية.
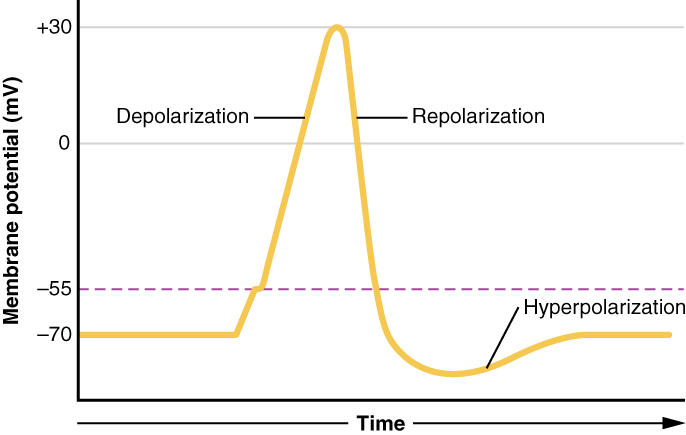
عندما تصل إمكانات الغشاء إلى +30 mV، يتم فتح قنوات أخرى ذات جهد كهربائي في الغشاء. هذه القنوات مخصصة لأيون البوتاسيوم. يعمل تدرج التركيز على K + أيضًا. عندما تبدأ K + في مغادرة الخلية، مع أخذ شحنة موجبة معها، تبدأ إمكانات الغشاء في العودة نحو جهد الراحة. وهذا ما يسمى بإعادة الاستقطاب، مما يعني أن جهد الغشاء يتحرك مرة أخرى نحو قيمة -70 mV لإمكانات الغشاء المستريح.
تقوم إعادة الاستقطاب بإرجاع إمكانات الغشاء إلى قيمة -70 mV التي تشير إلى إمكانات الراحة، ولكنها في الواقع تتجاوز هذه القيمة. تصل أيونات البوتاسيوم إلى التوازن عندما يكون جهد الغشاء أقل من -70 mV، لذلك تحدث فترة من فرط الاستقطاب أثناء فتح قنوات K +. تأخرت قنوات K + هذه قليلاً في الإغلاق، وهو ما يمثل هذا التجاوز القصير.
ما تم وصفه هنا هو جهد الفعل، والذي يتم تقديمه كرسم بياني للجهد بمرور الوقت في الشكل\(\PageIndex{6}\). إنها الإشارة الكهربائية التي تولدها الأنسجة العصبية للتواصل. التغيير في جهد الغشاء من -70 mV عند الراحة إلى +30 mV في نهاية إزالة الاستقطاب هو تغيير 100 mV. يمكن كتابة ذلك أيضًا كتغيير 0.1-V. لوضع هذه القيمة في منظورها الصحيح، فكر في البطارية. من الواضح أن بطارية AA التي قد تجدها في جهاز التحكم عن بُعد في التلفزيون بجهد 1.5 فولت، أو بطارية 9 فولت (البطارية المستطيلة ذات عمودين في أحد طرفيها) هي 9 فولت. التغيير الملحوظ في إمكانات الحركة أقل بمقدار واحد أو مرتين من الشحن في هذه البطاريات. في الواقع، يمكن وصف إمكانات الغشاء بأنها بطارية. يتم تخزين الشحنة عبر الغشاء الذي يمكن إطلاقه في ظل الظروف الصحيحة. قامت بطارية في جهاز التحكم عن بُعد بتخزين شحنة «تم تحريرها» عند الضغط على زر.
التمارين\(\PageIndex{1}\)
ما يحدث عبر غشاء الخلية النشطة كهربائيًا هو عملية ديناميكية يصعب تصورها بالصور الثابتة أو من خلال الأوصاف النصية. شاهد هذه الرسوم المتحركة لمعرفة المزيد حول هذه العملية. ما الفرق بين القوة الدافعة لـ Na+ و K+؟ وما الذي يشبه حركة هذين الأيونين؟
السؤال هو، الآن، ما الذي يبدأ إمكانات العمل؟ يتطرق الوصف أعلاه بشكل ملائم إلى هذه النقطة. ولكن من الضروري فهم ما يحدث. ستبقى إمكانات الغشاء عند جهد الراحة حتى يتغير شيء ما. الوصف أعلاه يقول فقط أن قناة Na + تفتح. الآن، إن قول «قناة تفتح» لا يعني أن بروتينًا واحدًا عبر الغشاء يتغير. بدلاً من ذلك، فهذا يعني فتح نوع واحد من القنوات. هناك عدة أنواع مختلفة من القنوات التي تسمح لـ Na + بعبور الغشاء. ستفتح قناة Na + ذات البوابات المربوطة عندما يرتبط بها ناقل عصبي وستفتح قناة Na + ذات البوابات ميكانيكيًا عندما يؤثر التحفيز المادي على مستقبل حسي (مثل الضغط المطبق على الجلد الذي يضغط على مستقبل اللمس). سواء كان ناقلًا عصبيًا مرتبطًا ببروتين مستقبله أو محفزًا حسيًا ينشط خلية مستقبلية حسية، فإن بعض التحفيز يؤدي إلى بدء العملية. يبدأ الصوديوم في دخول الخلية ويصبح الغشاء أقل سلبية.
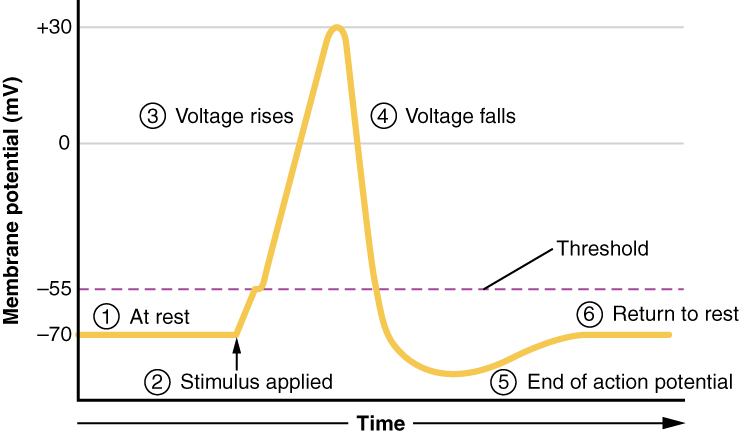
النوع الثالث من القنوات التي تعد جزءًا مهمًا من إزالة الاستقطاب في إمكانات العمل هو قناة Na + ذات الجهد. تساعد القنوات التي تبدأ في إزالة استقطاب الغشاء بسبب التحفيز الخلية على إزالة الاستقطاب من -70 mV إلى -55 mV. بمجرد وصول الغشاء إلى هذا الجهد، يتم فتح قنوات Na + ذات الجهد. هذا هو ما يعرف بالعتبة. أي إزالة للاستقطاب لا تغير إمكانات الغشاء إلى -55 mV أو أعلى لن تصل إلى الحد الأدنى وبالتالي لن تؤدي إلى إمكانية العمل. أيضًا، فإن أي حافز يعمل على إزالة الاستقطاب من الغشاء إلى -55 mV أو أكثر سيؤدي إلى فتح عدد كبير من القنوات وبدء إمكانية العمل.
بسبب الحد الأدنى، يمكن تشبيه إمكانية الإجراء بحدث رقمي - إما أن يحدث أو لا يحدث. إذا لم يتم الوصول إلى الحد الأدنى، فلن يحدث أي إجراء محتمل. إذا وصلت إزالة الاستقطاب إلى -55 mV، فستستمر إمكانات الفعل وتمتد حتى +30 mV، حيث يتسبب K + في إعادة الاستقطاب، بما في ذلك التجاوز المفرط للاستقطاب. كما أن هذه التغييرات هي نفسها لكل إجراء محتمل، مما يعني أنه بمجرد الوصول إلى الحد الأدنى، يحدث نفس الشيء بالضبط. إن التحفيز الأقوى، الذي قد يزيل الاستقطاب عن الغشاء بعد الحد الأقصى، لن يؤدي إلى إمكانات عمل «أكبر». إمكانات العمل هي «الكل أو لا شيء». إما أن يصل الغشاء إلى العتبة ويحدث كل شيء كما هو موضح أعلاه، أو لا يصل الغشاء إلى العتبة ولا يحدث أي شيء آخر. تبلغ جميع إمكانات الحركة ذروتها عند نفس الجهد (+30 mV)، لذا فإن إمكانات إجراء واحد ليست أكبر من الأخرى. ستعمل المنبهات الأقوى على إطلاق إمكانات عمل متعددة بسرعة أكبر، لكن الإشارات الفردية ليست أكبر. وبالتالي، على سبيل المثال، لن تشعر بإحساس أكبر بالألم، أو ستصاب بانقباض عضلي أقوى، بسبب حجم إمكانات الحركة لأنها ليست بأحجام مختلفة.
كما رأينا، يعتمد إلغاء الاستقطاب وإعادة استقطاب إمكانات العمل على نوعين من القنوات (قناة Na + ذات الجهد وقناة K + ذات الجهد). تحتوي قناة Na + ذات الجهد بالفعل على بوابتين. الأولى هي بوابة التنشيط، التي تفتح عندما تتقاطع إمكانات الغشاء مع -55 mV. أما البوابة الأخرى فهي بوابة التعطيل، التي تغلق بعد فترة زمنية محددة - في حدود جزء من المللي ثانية. عندما تكون الخلية في حالة راحة، يتم إغلاق بوابة التنشيط وتكون بوابة التعطيل مفتوحة. ومع ذلك، عند الوصول إلى الحد الأدنى، يتم فتح بوابة التنشيط، مما يسمح لـ Na + بالاندفاع إلى الخلية. يتم إغلاق بوابة التعطيل في الوقت الذي تبلغ فيه ذروة إزالة الاستقطاب. أثناء إعادة الاستقطاب، لا يمكن أن يدخل المزيد من الصوديوم إلى الخلية. عندما تمر إمكانات الغشاء -55 mV مرة أخرى، يتم إغلاق بوابة التنشيط. بعد ذلك، يتم إعادة فتح بوابة التعطيل، مما يجعل القناة جاهزة لبدء العملية بأكملها مرة أخرى.
تحتوي قناة K + ذات الجهد على بوابة واحدة فقط، وهي حساسة لجهد غشائي يبلغ -50 mV. ومع ذلك، فإنه لا يفتح بالسرعة التي تفتح بها قناة Na + ذات الجهد. قد يستغرق الأمر جزءًا من ميلي ثانية حتى تفتح القناة بمجرد الوصول إلى هذا الجهد. يتزامن توقيت ذلك تمامًا مع الوقت الذي يبلغ فيه تدفق Na + ذروته، لذلك يتم فتح قنوات K + ذات الجهد تمامًا كما يتم تعطيل قنوات Na + ذات الجهد. مع إعادة استقطاب إمكانات الغشاء وتجاوز الجهد -50 mV مرة أخرى، يتم إغلاق القناة - مرة أخرى، مع القليل من التأخير. يستمر البوتاسيوم في مغادرة الخلية لفترة قصيرة وتصبح إمكانات الغشاء أكثر سلبية، مما يؤدي إلى فرط الاستقطاب. ثم يتم إغلاق القناة مرة أخرى ويمكن للغشاء العودة إلى إمكانات الراحة بسبب النشاط المستمر للقنوات غير المسورة ومضخة Na + /K +.
كل هذا يحدث في غضون 2 مللي ثانية تقريبًا (الشكل\(\PageIndex{7}\)). في حين أن إمكانات العمل قيد التقدم، لا يمكن بدء واحدة أخرى. يشار إلى هذا التأثير باسم فترة المقاومة. هناك مرحلتان من فترة المقاومة: فترة المقاومة المطلقة وفترة المقاومة النسبية. خلال المرحلة المطلقة، لن تبدأ إمكانات عمل أخرى. هذا بسبب بوابة التعطيل لقناة Na + ذات الجهد. بمجرد عودة هذه القناة إلى شكلها المريح (أقل من -55 mV)، يمكن بدء إمكانات عمل جديدة، ولكن فقط من خلال حافز أقوى من ذلك الذي بدأ إمكانات العمل الحالية. هذا بسبب تدفق K + خارج الخلية. نظرًا لأن هذا الأيون يندفع للخارج، فإن أي Na + يحاول الدخول لن يؤدي إلى إزالة الاستقطاب من الخلية، ولكنه سيمنع الخلية فقط من الاستقطاب المفرط.
نشر إمكانات العمل
تبدأ إمكانات العمل في بداية المحور، عند ما يسمى بالمقطع الأولي. هناك كثافة عالية من قنوات Na + ذات الجهد بحيث يمكن إزالة الاستقطاب السريع هنا. وبالنزول إلى طول المحور، يتم نشر إمكانات الحركة نظرًا لفتح المزيد من قنوات Na + ذات الجهد مع انتشار إزالة الاستقطاب. يحدث هذا الانتشار لأن Na + يدخل عبر القناة ويتحرك على طول الجزء الداخلي من غشاء الخلية. عندما تتحرك Na + أو تتدفق لمسافة قصيرة على طول غشاء الخلية، تعمل شحنتها الموجبة على إزالة الاستقطاب قليلاً من غشاء الخلية. ومع انتشار إزالة الاستقطاب هذه، تفتح قنوات Na + الجديدة ذات الجهد وتندفع المزيد من الأيونات إلى الخلية، مما يؤدي إلى نشر إزالة الاستقطاب إلى مسافة أبعد قليلاً.
نظرًا لأن قنوات Na + ذات الجهد يتم تعطيلها في ذروة إزالة الاستقطاب، فلا يمكن فتحها مرة أخرى لفترة وجيزة - فترة المقاومة المطلقة. ولهذا السبب، فإن إزالة الاستقطاب التي تنتشر مرة أخرى نحو القنوات المفتوحة سابقًا ليس لها أي تأثير. يجب أن تنتشر إمكانات الفعل باتجاه أطراف المحور؛ ونتيجة لذلك، يتم الحفاظ على قطبية الخلايا العصبية، كما هو مذكور أعلاه.
ينطبق الانتشار، كما هو موضح أعلاه، على المحاور العصبية غير الميلانية. عند وجود الميالين، تنتشر إمكانات الفعل بشكل مختلف. تبدأ أيونات الصوديوم التي تدخل الخلية في الجزء الأولي بالانتشار على طول مقطع المحور، ولكن لا توجد قنوات Na + ذات جهد حتى العقدة الأولى من Ranvier. نظرًا لعدم وجود فتح مستمر لهذه القنوات على طول مقطع المحور، تنتشر إزالة الاستقطاب بسرعة مثالية. المسافة بين العقد هي المسافة المثلى للحفاظ على بقاء الغشاء غير مستقطب فوق الحد عند العقدة التالية. عندما تنتشر Na + على طول الجزء الداخلي من غشاء مقطع المحور، تبدأ الشحنة في التبدد. إذا كانت العقدة أبعد من المحور، فإن إزالة الاستقطاب هذه ستنخفض كثيرًا بحيث لا يمكن تنشيط قنوات Na + ذات الجهد في العقدة التالية من Ranvier. إذا كانت العقد أقرب من بعضها البعض، فستكون سرعة الانتشار أبطأ.
ويُشار إلى الانتشار على طول محور عصبي غير ميالين بالتوصيل المستمر؛ وهو عبارة عن توصيل ملحي بطول محور عصبي ميالين. يكون التوصيل المستمر بطيئًا نظرًا لوجود قنوات Na + ذات الجهد دائمًا مفتوحة، ويندفع المزيد والمزيد من Na + إلى الخلية. يكون التوصيل الملحي أسرع لأن إمكانات الحركة تقفز أساسًا من عقدة إلى أخرى (saltare = «to leap»)، ويجدد التدفق الجديد لـ Na + الغشاء غير المستقطب. إلى جانب الميالين في المحور، يمكن أن يؤثر قطر المحور على سرعة التوصيل. فبقدر ما تجري المياه بشكل أسرع في النهر الواسع مقارنة بالخور الضيق، فإن إزالة الاستقطاب القائمة على Na + تنتشر بشكل أسرع في محور عصبي عريض بدلاً من انتشاره في محور ضيق. يُعرف هذا المفهوم بالمقاومة وينطبق بشكل عام على الأسلاك الكهربائية أو السباكة، تمامًا كما هو الحال بالنسبة للمحاور، على الرغم من اختلاف الظروف المحددة على مقاييس الإلكترونات أو الأيونات مقابل الماء في النهر.
اختلالات التوازن: تركيز البوتاسيوم
الخلايا الدبقية، وخاصة الخلايا النجمية، مسؤولة عن الحفاظ على البيئة الكيميائية لأنسجة الجهاز العصبي المركزي. إن تركيزات الأيونات في السائل خارج الخلية هي الأساس لكيفية إنشاء إمكانات الغشاء والتغيرات في الإشارات الكهروكيميائية. في حالة اختلال توازن الأيونات، من الممكن تحقيق نتائج جذرية.
عادةً ما يكون تركيز K+ أعلى داخل الخلية العصبية منه في الخارج. بعد مرحلة إعادة الاستقطاب لإمكانات الحركة، تضمن قنوات التسرب K+ ومضخة Na+/K+ عودة الأيونات إلى مواقعها الأصلية. بعد السكتة الدماغية أو أي حدث إقفاري آخر، ترتفع مستويات K+ خارج الخلية. تم تجهيز الخلايا النجمية في المنطقة لإزالة فائض K+ لمساعدة المضخة. ولكن عندما يكون المستوى بعيدًا عن التوازن، يمكن أن تكون التأثيرات لا رجعة فيها.
يمكن أن تتفاعل الخلايا النجمية في مثل هذه الحالات، مما يضعف قدرتها على الحفاظ على البيئة الكيميائية المحلية. تتضخم الخلايا الدبقية وتتضخم عملياتها. تفقد قدرتها على التخزين المؤقت لـ K+ وتتأثر وظيفة المضخة أو حتى تنعكس. واحدة من العلامات المبكرة لأمراض الخلايا هي «تسرب» أيونات الصوديوم إلى خلايا الجسم. يؤثر اختلال توازن الصوديوم/البوتاسيوم سلبًا على الكيمياء الداخلية للخلايا، مما يمنعها من العمل بشكل طبيعي.
قم بزيارة هذا الموقع لمشاهدة مختبر الفيزيولوجيا العصبية الافتراضي، ولمراقبة عمليات الفيزيولوجيا الكهربية في الجهاز العصبي، حيث يقيس العلماء بشكل مباشر الإشارات الكهربائية التي تنتجها الخلايا العصبية. غالبًا ما تحدث إمكانات الحركة بسرعة كبيرة بحيث لا يكون من المفيد مشاهدة الشاشة لرؤيتها. يتم تشغيل مكبر الصوت من خلال الإشارات المسجلة من الخلايا العصبية ويتم «إطلاقه» في كل مرة تطلق فيها الخلية العصبية إمكانات عمل. يتم إطلاق إمكانات الحركة هذه بسرعة كبيرة بحيث تبدو ثابتة على الراديو. يمكن لعلماء الفيزيولوجيا الكهربائية التعرف على الأنماط داخل هذا الثابت لفهم ما يحدث. لماذا يستخدم نموذج العلقة لقياس النشاط الكهربائي للخلايا العصبية بدلاً من استخدام البشر؟
مراجعة
يتميز الجهاز العصبي بإشارات كهربائية يتم إرسالها من منطقة إلى أخرى. سواء كانت هذه المناطق قريبة أو بعيدة جدًا، يجب أن تنتقل الإشارة على طول محور عصبي. أساس الإشارة الكهربائية هو التوزيع المتحكم فيه للأيونات عبر الغشاء. تنظم القنوات الأيونية عبر الغشاء الوقت الذي يمكن فيه للأيونات أن تتحرك داخل الخلية أو خارجها، بحيث يتم إنشاء إشارة دقيقة. هذه الإشارة هي إمكانات العمل التي لها شكل مميز للغاية يعتمد على تغيرات الجهد عبر الغشاء في فترة زمنية معينة.
عادة ما يكون الغشاء في حالة سكون بتركيزات Na + و K + الثابتة على كلا الجانبين. سيبدأ التحفيز في إزالة استقطاب الغشاء، وستؤدي القنوات ذات الجهد الكهربائي إلى مزيد من إزالة الاستقطاب متبوعًا بإعادة استقطاب الغشاء. يمثل التجاوز الطفيف للاستقطاب المفرط نهاية إمكانات الحركة. في حين أن إمكانات العمل قيد التقدم، لا يمكن إنشاء عمل آخر في ظل نفس الظروف. في حين أن قناة Na + ذات الجهد معطلة، لا يمكن توليد أي إمكانات عمل على الإطلاق. بمجرد عودة هذه القناة إلى حالة الراحة، تصبح إمكانية الحركة الجديدة ممكنة، ولكن يجب أن تبدأ بحافز أقوى نسبيًا للتغلب على K + الذي يغادر الخلية.
تنتقل إمكانات الحركة إلى أسفل المحور حيث يتم فتح القنوات الأيونية ذات الجهد من خلال إزالة الاستقطاب المنتشر. في المحاور العصبية غير الميالين، يحدث هذا بشكل مستمر بسبب وجود قنوات ذات جهد في جميع أنحاء الغشاء. في المحاور الميالينية، يوصف الانتشار بأنه مملح لأن القنوات ذات الجهد الكهربائي لا توجد إلا في عقد رانفير ويبدو أن الأحداث الكهربائية «تقفز» من عقدة إلى أخرى. يكون التوصيل الملحي أسرع من التوصيل المستمر، مما يعني أن المحاور الميلينية تنشر إشاراتها بشكل أسرع. يُحدث قطر المحور أيضًا فرقًا لأن الأيونات المنتشرة داخل الخلية تتمتع بمقاومة أقل في مساحة أوسع.
أسئلة الرابط التفاعلي
ما يحدث عبر غشاء الخلية النشطة كهربائيًا هو عملية ديناميكية يصعب تصورها بالصور الثابتة أو من خلال الأوصاف النصية. شاهد هذه الرسوم المتحركة لفهم العملية حقًا. ما الفرق بين القوة الدافعة لـ Na + و K +؟ وما الذي يشبه حركة هذين الأيونين؟
الإجابة: ينتقل الصوديوم إلى الخلية بسبب تدرج التركيز الهائل، في حين أن البوتاسيوم يخرج بسبب إزالة الاستقطاب الذي يسببه الصوديوم. ومع ذلك، يتحرك كلاهما لأسفل تدرجات كل منهما، نحو التوازن.
قم بزيارة هذا الموقع لمشاهدة مختبر الفيزيولوجيا العصبية الافتراضي، ولمراقبة عمليات الفيزيولوجيا الكهربية في الجهاز العصبي، حيث يقيس العلماء بشكل مباشر الإشارات الكهربائية التي تنتجها الخلايا العصبية. غالبًا ما تحدث إمكانات الحركة بسرعة كبيرة بحيث لا يكون من المفيد مشاهدة الشاشة لرؤيتها. يتم تشغيل مكبر الصوت من خلال الإشارات المسجلة من الخلايا العصبية ويتم «إطلاقه» في كل مرة تطلق فيها الخلية العصبية إمكانات عمل. يتم إطلاق إمكانات الحركة هذه بسرعة كبيرة بحيث تبدو ثابتة على الراديو. يمكن لعلماء الفيزيولوجيا الكهربائية التعرف على الأنماط داخل هذا الثابت لفهم ما يحدث. لماذا يستخدم نموذج العلقة لقياس النشاط الكهربائي للخلايا العصبية بدلاً من استخدام البشر؟
الإجابة: خصائص الفيزيولوجيا الكهربائية شائعة في جميع الحيوانات، لذا فإن استخدام العلقة هو نهج أسهل وأكثر إنسانية لدراسة خصائص هذه الخلايا. هناك اختلافات بين الأجهزة العصبية للافقاريات (مثل العلقة) والفقاريات، ولكن ليس من أجل ما تدرسه هذه التجارب.
مراجعة الأسئلة
س: ما الأيون الذي يدخل الخلية العصبية مسببًا إزالة الاستقطاب من غشاء الخلية؟
أ. صوديوم
كلوريد ب.
C. البوتاسيوم
د. الفوسفات
الإجابة: أ
س: يتم فتح قنوات Na + ذات الجهد عند الوصول إلى أي ولاية؟
أ. إمكانات الاختبار
باء - العتبة
جيم - إعادة الاستقطاب
د. التجاوز
الإجابة: ب
س: ما الذي تتطلبه القناة ذات البوابات من أجل فتحها؟
أ. زيادة تركيز أيونات Na +
ب. ربط الناقل العصبي
C. زيادة تركيز أيونات K +
د. إزالة الاستقطاب للغشاء
الإجابة: ب
س: ما الذي تستجيب له القناة ذات البوابات ميكانيكيًا؟
أ. التحفيز البدني
ب. التحفيز الكيميائي
C. زيادة المقاومة
D. انخفاض المقاومة
الإجابة: أ
س: أي من الفولتات التالية من المرجح أن يتم قياسها خلال فترة المقاومة النسبية؟
أ. +30 فولت
ب. 0 ميجا فولت
درجة مئوية -45 فولت
د. -80 مللي فولت
الإجابة: د
س: أي مما يلي من المحتمل أن ينشر إمكانات العمل بشكل أسرع؟
أ. محور عصبي رقيق غير ميالين
B. محور عصبي رقيق يحتوي على الميالين
ج. محور عصبي سميك غير ميالين
د. محور عصبي سميك مصنوع من الميالين
الإجابة: د
أسئلة التفكير النقدي
س: ماذا يعني أن يكون الإجراء المحتمل حدثًا «الكل أو لا شيء»؟
ج: يجب أن يصل غشاء الخلية إلى العتبة قبل فتح قنوات Na + ذات الجهد. إذا لم يتم الوصول إلى الحد الأدنى، فلن تفتح هذه القنوات، ولا تحدث مرحلة إزالة الاستقطاب من إمكانات الفعل، وسيعود غشاء الخلية إلى حالة الراحة.
س: غالبًا ما يتأخر الإدراك الواعي للألم بسبب الوقت الذي تستغرقه الأحاسيس للوصول إلى القشرة الدماغية. لماذا سيكون هذا هو الحال بناءً على انتشار إمكانات المحور العصبي؟
ج: إن محاور الخلايا العصبية الحسية التي تستشعر الألم رقيقة وغير مملوءة بالميالين بحيث يستغرق الأمر وقتًا أطول حتى يصل هذا الإحساس إلى الدماغ مقارنة بالأحاسيس الأخرى.
مسرد المصطلحات
- فترة مقاومة مطلقة
- الوقت خلال فترة العمل التي لا يمكن فيها توليد إمكانية عمل أخرى بسبب تعطيل قناة Na + ذات الجهد
- بوابة التنشيط
- جزء من قناة Na + ذات الجهد الكهربائي والتي تفتح عندما يصل جهد الغشاء إلى الحد
- التوصيل المستمر
- الانتشار البطيء لإمكانات الفعل على طول محور عصبي غير ميالين بسبب قنوات Na + ذات الجهد الموجودة على طول غشاء الخلية بالكامل
- إزالة الاستقطاب
- تغير في إمكانات غشاء الخلية من السكون نحو الصفر
- استبعاد كهروكيميائي
- مبدأ السماح الانتقائي للأيونات عبر القناة على أساس شحنتها
- غشاء قابل للإثارة
- غشاء الخلية الذي ينظم حركة الأيونات بحيث يمكن توليد إشارة كهربائية
- بوابات
- خاصية القناة التي تحدد كيفية فتحها في ظل ظروف محددة، مثل تغيير الجهد أو التشوه المادي
- بوابة التعطيل
- جزء من قناة Na + ذات الجهد والتي يتم إغلاقها عندما تصل إمكانات الغشاء إلى +30 mV
- مستقبلات أيونوتروبيك
- مستقبل الناقل العصبي الذي يعمل كبوابة قناة أيونية، ويفتح عن طريق ربط الناقل العصبي
- قناة التسرب
- قناة أيونية تفتح بشكل عشوائي ولا يتم ربطها بحدث معين، والمعروفة أيضًا باسم القناة غير المسورة
- قنوات مسننة
- اسم آخر لمستقبلات أيونية يكون الناقل العصبي لها هو الليغند
- قناة مسورة ميكانيكيًا
- قناة أيونية تفتح عندما يؤثر حدث مادي بشكل مباشر على بنية البروتين
- إمكانات الغشاء
- توزيع الشحنة عبر غشاء الخلية، بناءً على شحنات الأيونات
- قناة غير محددة
- قناة غير خاصة بأيون فوق آخر، مثل قناة الكاتيونات غير المحددة التي تسمح لأي أيون ذي شحنة موجبة عبر الغشاء
- فترة المقاومة
- الوقت بعد بدء إمكانية الإجراء عندما لا يمكن إنشاء إمكانية عمل أخرى
- فترة المقاومة النسبية
- الوقت خلال الفترة المقاومة للحرارة عندما لا يمكن بدء إمكانات عمل جديدة إلا من خلال حافز أقوى من إمكانات العمل الحالية لأن قنوات K + ذات الجهد غير مغلقة
- إعادة الاستقطاب
- عودة إمكانات الغشاء إلى جهده السلبي الطبيعي في نهاية إمكانات الفعل
- مقاومة
- خاصية المحور العصبي التي تتعلق بقدرة الجسيمات على الانتشار من خلال السيتوبلازم؛ وهذا يتناسب عكسياً مع قطر الألياف
- إمكانات غشاء الراحة
- الفرق في الجهد المقاس عبر غشاء الخلية في ظل ظروف الحالة المستقرة، عادةً -70 mV
- التوصيل الملحي
- الانتشار السريع لإمكانات العمل على طول محور عصبي ميالين بسبب وجود قنوات Na + ذات الجهد فقط في عقد Ranvier
- استبعاد الحجم
- مبدأ السماح الانتقائي للأيونات عبر القناة على أساس حجمها النسبي
- قناة مسورة الجهد
- قناة أيونية تفتح بسبب تغيير الشحنة الموزعة عبر الغشاء الذي توجد فيه


