11.2: סחר בחלבונים
- Page ID
- 208573
הרעיון שלרצפי פרופפטיד יש תפקידים חשובים בהבשלת חלבון מעבר רק למנוע מהם להיות פעילים אינו בלעדי להרכבה. מחלקה מרכזית של רצפי פפטידים מבוקעים היא פפטידי אותות. פפטידי אות מכוונים את החלבון מהציטופלזמה לתא סלולרי מסוים. במקרה של פרוקריוטים, זה בעצם אומר קרום התא, אבל עבור אוקריוטים, ישנם פפטידי אות ספציפיים שיכולים לכוון את החלבון לגרעין, למיטוכונדריה, לרטיקולום האנדופלזמי ולאברונים תאיים אחרים. הפפטידים מוכרים במיוחד על ידי קולטנים על הממברנות של תאים מסוימים, אשר לאחר מכן מסייעים להנחות את החדרת החלבון לתוך או דרך הממברנה. כמעט כל סינתזת החלבון באאוקריוטים מתבצעת בציטופלזמה (למעט כמה חלבונים בכלורופלסטים ובמיטוכונדריה), כך שחלבונים שנמצאו בכל תא אחר או מוטבעים בכל קרום חייבים להיות ממוקדים ומועברים לתא זה על ידי רצף האותות שלו.
למרות שזה נחשב בעיקר לתהליך אוקריוטי בהתחשב בכך שיש כל כך הרבה מטרות פוטנציאליות, לפרוקריוטים יש חלבוני ממברנה (למעשה, כ -800 שונים ב אי - קולי המהווים ~ 20% מסך החלבון), והם ממוקמים שם בעזרת אנזימי אינסרטאז כגון YiDC ומתחמים כגון טרנסלוקאז Sec. הטרנסלוקאז Sec משתמש בחלקיק זיהוי אותות (SRP) בדומה לזה באיקריוטים, ויידון בהמשך פרק זה כאשר ה-SRP יוצג. YidC, שיש לו הומולוגים אוקריוטיים (למשל Oxa1 במיטוכונדריה), הוא חלבון טרנסממברני של 61 kDa המוצב בממברנה באמצעות מנגנון טרנסלוקאז SRP-sec. כשהם שם, YIDC מקיים אינטראקציה עם פוליפפטידים המתהווים (ברגע שהם מגיעים לאורך ~ 70 חומצות אמינו) שהחלו לקיים אינטראקציה עם השומנים של קרום התא, ודוחף את החלבון לתוך/דרך הממברנה.
הגרעין הוא תא אחד כזה, ודוגמאות לחלבונים המצויים בתוכו כוללות פולימראזות DNA ו- RNA, גורמי שעתוק והיסטונים. לחלבונים גרעיניים אלה ואחרים יש רצף אותות N-טרמינלי המכונה NLS, או אות לוקליזציה גרעינית. זהו מסלול נחקר היטב הכולל קבוצה של חלבוני מתאם יבואן וקומפלקס הנקבוביות הגרעיניות (איור). \(\PageIndex{3}\) ההובלה לגרעין מאתגרת במיוחד מכיוון שיש לה קרום כפול (זכרו שהיא רציפה עם קרום הרשת האנדופלזמית. למרות שישנם מנגנונים נוספים לייצור חלבונים המוטבעים בממברנה הגרעינית, המנגנון העיקרי לייבוא וייצוא של מולקולות גדולות אל תוך הגרעין עצמו ומחוצה לו הוא קומפלקס הנקבוביות הגרעיניות. המתחם גדול מאוד ויכול להיות עשוי ממעל 50 חלבונים שונים (נוקלאופורינים, הנקראים לפעמים nups). הנוקליאופורינים מורכבים לנקבובית מתומנת פתוחה גדולה דרך הממברנות הגרעיניות. כפי \(\PageIndex{3}\) שמעיד האיור, ישנם סיבים דמויי אנטנה על הפנים הציטופלזמיים, ואלה עוזרים להנחות חלבונים ממוצאם בציטופלזמה אל הנקבובית הגרעינית, ובצד הגרעיני יש מבנה סל. כמובן, לא כל החלבונים מורשים להיכנס לגרעין, והמנגנון להבחנה בין מטרות מתאימות הוא פשוט. החלבון חייב לשאת אות לוקליזציה גרעינית (NLS). בעודו בציטופלזמה, חלבון importin-α נקשר ל-NLS של חלבון גרעיני, וגם נקשר ל-importin-β. הייבוא-β מזוהה ונקשר על ידי קומפלקס הנקבוביות הגרעיניות. הפרטים של מנגנון ההובלה עכורים, אך סבורים כי חזרות פנילאלנין-גליצין בתת-יחידות הנוקלאופורין (FG-NUPs) מעורבות.
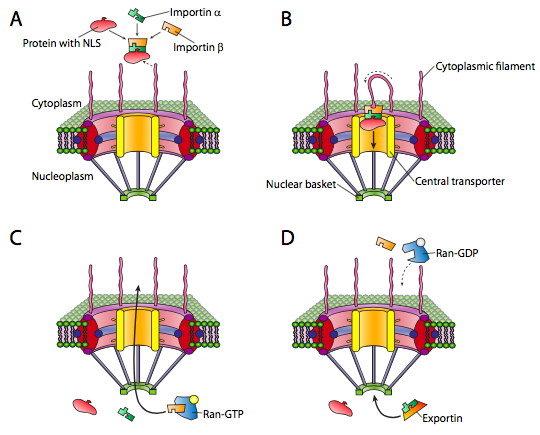
ברגע שאגרגט הנוקלאופרוטאין-אימפורטין מועבר לגרעין, Ran-GTP, GTPase קטן, גורם לצבירה להתנתק (איור ג). \(\PageIndex{3}\) החלבון המיובא משתחרר בגרעין. היבואנים משתחררים גם בגרעין, אך הם מיוצאים שוב החוצה כדי לעשות בהם שימוש חוזר עם חלבון אחר המיועד לגרעין.
המנגנונים של הפעלת GTPase קטנה של תהליכים אחרים יידונו שוב בפירוט רב יותר בפרקים מאוחרים יותר (ציטוסקלטון, איתות). המפתח להבנת המנגנון הוא לזכור שה-GTPase מבצע הידרוליזה של GTP לתוצר, אך עדיין מחזיק בתוצר. למרות שה-GTPase יעשה הידרוליזה של GTP באופן ספונטני, החלבון המפעיל GTPase, GAP (או RAN-gap במקרה זה) מאיץ מאוד את קצב ההידרוליזה. על מנת להחזיר את המערכת ל- GTP, התוצר אינו מזורחן מחדש: הוא מוחלף ל- GTP חדש. ההחלפה מקלה מאוד על ידי פעולתו של חלבון אביזר, גורם חילופי הנוקלאוטידים של גואנין (GEF), במקרה הספציפי הזה, Ran-GEF.
ייצוא מהגרעין לציטופלזמה מתרחש גם דרך הנקבובית הגרעינית. ה-Ran-GTP הוא גם חלק ממכלול הייצוא (איור \(\PageIndex{3}\) ד), ובשילוב עם חלבון יצואטין וכל מה שיש לייצא, מועבר אל מחוץ לגרעין דרך הנקבובית הגרעינית. פעם אחת בציטופלזמה, ההידרוליזה של GTP ל-GDP על ידי רן (מופעל על ידי Ran-GAP, חלבון ציטופלזמי) מספק את האנרגיה לנתק את המטען (למשל mRNA) ממולקולות ההובלה המייצאות. לאחר מכן, ה- Ran-GDP נקשר לייבואנים, נכנס מחדש לגרעין, והתמ"ג מוחלף ל- GTP.
הנקבובית הגרעינית היא מתחם ההובלה היחיד המשתרע על פני שכבות קרום כפולות, אם כי ישנם זוגות מתואמים של מתחמי הובלה באברונים בעלי קרום כפול כגון מיטוכונדריה. חלבוני ההובלה בממברנה המיטוכונדריאלית החיצונית מתחברים לחלבוני הובלה בקרום המיטוכונדריאלי הפנימי כדי להעביר חלבונים הקשורים למטריצה (למשל אלה המעורבים במחזור TCA) פנימה מהציטופלזמה. הקומפלקסים המעבירים חלבונים על פני הממברנה החיצונית מורכבים ממשפחת החלבונים של טום (הממברנה החיצונית של טרנסלוקטור). חלק מהחלבונים יישארו מוטבעים בקרום החיצוני: הם מעובדים על ידי קומפלקס SAM (מכונות מיון והרכבה) המוטמע גם בקרום החיצוני). בינתיים, אחרים ממשיכים לחלבוני טים (הממברנה הפנימית של טרנסלוקטור) שמעבירים אותם על פני הממברנה הפנימית. בדומה לחלבונים הגרעיניים, קיים רצף אותות קונצנזוס על חלבונים מיטוכונדריאליים הקשור למלווים ציטוזוליים המביאים אותם לטרנספורטרים של טום. כפי שמוצג בטבלה שלהלן, ישנם רצפי אותיות/פרופפטידים המכוונים חלבונים למספר תאים אחרים.
חשיבות מיוחדת להמשך פרק זה, היא הרצף המכוון חלבונים לרטיקולום האנדופלזמי, ובהרחבה, כל חלבונים המיועדים ל-ER, מנגנון גולגי, קרום התא, שלפוחיות ותאים שמקורם בשלפוחית, והפרשה מחוץ לתא. כאן, בנוסף לרצף אותות N-טרמינלי, המיקום של רצפי אותות פנימיים משניים (הנקראים לפעמים תיקוני אותות) עוזר לקבוע את הנטייה של החלבון כשהוא נכנס ל-ER.
ההכנסה הראשונית דורשת זיהוי של רצף האותות על ידי SRP, חלבון זיהוי האות. ה- SRP הוא חלבון G ומחליף את התוצר הקשור שלו ל- GTP עם קישור לרצף האותות של חלבון. ה- SRP עם החלבון המחובר שלו עוגן לאחר מכן לקולטן (הנקרא קולטן SRP, באופן מדהים מספיק) המוטמע בקרום ה- ER ומשתרע לתוך הציטופלזמה. ה-SRP נקשר בדרך כלל ברגע שרצף האותות זמין, וכאשר הוא עושה זאת, הוא עוצר את התרגום עד שהוא מעוגן לקרום ה-ER. אגב, זהו מקורו של הרטיקולום האנדופלזמי "המחוספס": הריבוזומים החוטפים את ה-ER מחוברים למשטח הציטופלזמי ER על ידי הפוליפפטיד המתהווה שהוא מייצר ו-SRP. קולטן ה- SRP יכול להתקיים בכוחות עצמו או בשיתוף עם טרנסלוקון, שהוא ערוץ טרנסלוקציה דו -צדדי. קולטן ה- SRP (SR) הוא גם GTPase, ובדרך כלל נושא מולקולת GDP כאשר הוא אינו קשור. עם זאת, בשיתוף עם הטרנסלוקון היא מחליפה את התוצר שלה עבור GTP. GTP אלה חשובים מכיוון שכאשר ה-SRP נקשר ל-SR, שתי פעילויות ה-GTPase מופעלות ושחרור האנרגיה המתקבל מתנתק הן מהטרנסלוקון והן מהפוליפפטיד המתהווה. זה מקל על החסימה בתרגום שהוטל על ידי ה-SRP, והחלבון החדש נדחף דרך הטרנסלוקון בזמן שהוא מסונתז. לאחר שרצף האותות נכנס לחלוטין לומן של ה-ER, הוא חושף אתר זיהוי לפפטידאז האות, אנזים הידרוליטי השוכן בלומן ER ומטרתו לגזור את פפטיד האות.
פרוקריוטים משתמשים גם בהומולוג SRP. ב אי - קולי, ה-SRP פשוט, מורכב מתת-יחידת חלבון אחת (Ffh) ו-4.5S RNA קטן. לשם השוואה, לכמה אוקריוטים גבוהים יותר יש SRP המורכב משש יחידות משנה שונות של חלבונים ו-7S RNA. באופן דומה, יש הומולוג פרוקריוטי פשוט לקולטן SRP, FtsY. הבדל מעניין הוא ש- FtsY בדרך כלל אינו מקיים אינטראקציה עם חלבונים מיוצאים, ונראה שהוא נחוץ רק לחלבונים המוטבעים בממברנה. אחרת, ישנם קווי דמיון רבים במנגנון להחדרה מבוססת SRP של חלבוני ממברנה במינים אוקריוטיים ופרוקריוטים, כולל תלות ב- GTP, והשלמת המנגנון על ידי טרנסלוקאז (SecYEG ב אי - קולי).
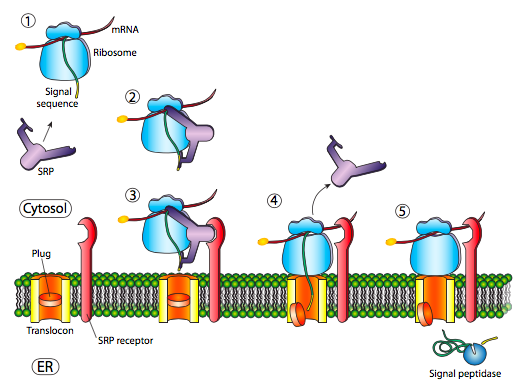
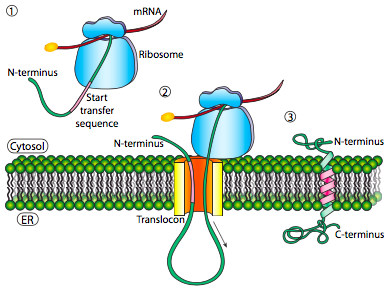
אם זה היה רצף האותות היחיד בחלבון, שאר החלבון מסונתז ונדחף דרך הטרנסלוקון וחלבון מסיס מופקד בלומן ER, כפי שמוצג באיור. \(\PageIndex{4}\) מה לגבי חלבונים המוטבעים בממברנה? לחלבונים טרנסממברניים יש רצפי אותות פנימיים (הנקראים לפעמים תיקוני אות). בהתאם למיקומם היחסי, הם עשויים להיחשב לרצף התחלה-העברה או עצירה -העברה, כאשר "העברה" מתייחסת לטרנסלוקציה של הפפטיד דרך הטרנסלוקון. זה הכי קל להבין על ידי התייחסות איור\(\PageIndex{5}\).
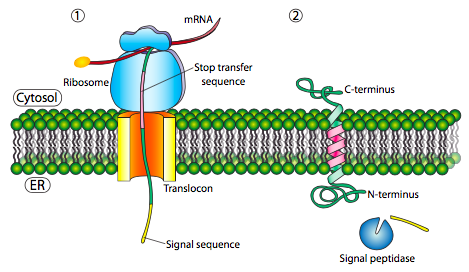
אם יש קטע משמעותי של שאריות הידרופוביות ללא הפרעה, זה ייחשב לאות עצירת העברה, מכיוון שחלק זה של החלבון יכול להיתקע בטרנסלוקון (ולאחר מכן בממברנת ER) ולאלץ את שארית החלבון להישאר מחוץ למיון. זה ייצור חלבון שחודר לממברנה פעם אחת, עם קצה ה-N שלו בלומן ER וקצה ה-C בציטופלזמה. בחלבון טרנסממברני רב-מעבר, יכולים להיות מספר תיקוני אות הידרופוביים של התחלה ועצירה.
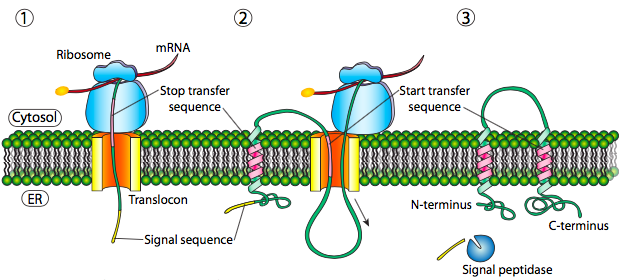
בהתבסס על דוגמת המעבר היחיד, אם היה תיקון אות נוסף לאחר רצף העצירה, הוא ישמש כרצף התחלה-העברה, מתחבר לטרנסלוקון ומאפשר להעביר את שארית החלבון למיון. התוצאה היא חלבון עם N- ו- C- termini בלומן ER, עובר דרך קרום ה- ER פעמיים, ועם לולאה ציטופלזמית בולטת החוצה. כמובן, מסוף ה- N יכול להיות בצד השני. עבור מסוף N ציטופלזמי, לחלבון לא יכול להיות רצף אותות N-טרמינלי (איור). \(\PageIndex{7}\) במקום זאת יש לו תיקון אות פנימי. זה ממלא בעצם את אותו תפקיד, אבל הכיוון של התיקון אומר שה-N-terminal נשאר ציטופלסמי. הפוליפפטיד מתורגם לאחר הזנת התיקון למיון. ובדיוק כמו בדוגמה האחרונה, רצפי עצירה והתחלה מרובים יכולים להכניס מחדש את החלבון לממברנה ולשנות את הפנים של החלק הבא.