8.4: עיבוד פוסט-תעתיק של RNA
- Page ID
- 208469
הראשון מהאירועים שלאחר התעתיק הוא מכסת קצה 5'. ברגע שקצה 5 'של RNA המתהווה משתרע ללא RNAP II בערך 20-30 nt, הוא מוכן להיות מכוסה על ידי מבנה 7-מתילגואנוסין. "כובע" 5 'זה משמש כאתר זיהוי להובלת ה- mRNA שהושלם אל מחוץ לגרעין ואל הציטופלזמה.
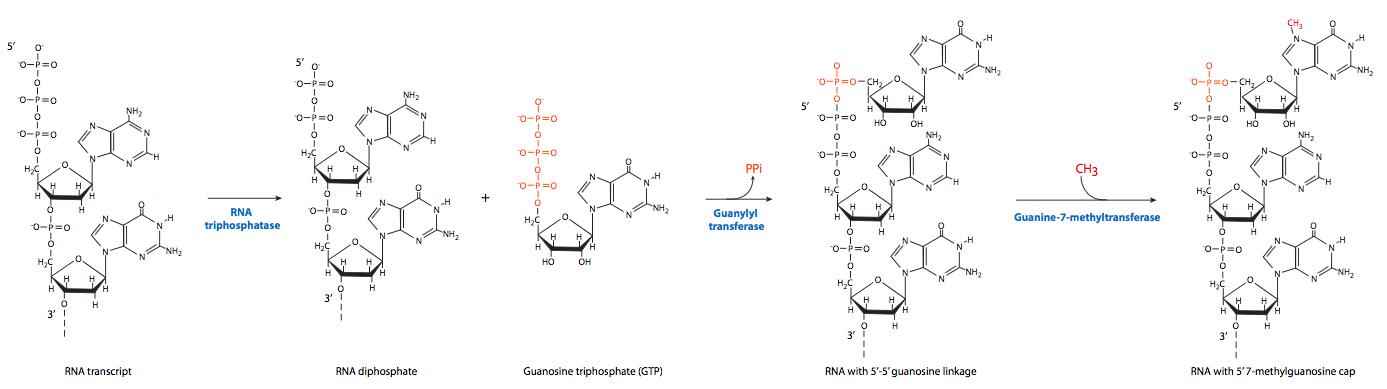
התהליך כולל למעשה שלושה שלבים. ראשית, RNA טריפוספטאז מסיר את קבוצת הטריפוספט 5'-טרמינלית. גואנילציה על ידי GTP מזורזת על ידי אנזים מכסה, ויוצרת קשר יוצא דופן 5'-5' "לאחור" בין הגואנין החדש לנוקלאוטיד הראשון של תמליל ה- RNA. לבסוף, גואנין-7-מתילטרנספראז מתילט את הגואנין החדש המחובר.
בקצה הנגדי של ה-RNA, ב-3'-OH החופשי, מתרחשת פוליאדנילציה. כפי שצוין קודם לכן, קומפלקס אנזים העוגן לאתר בזנב CTD של RNAP II מבקע חלק מקצה 3 'ליד רצף זיהוי AAUAAA ולאחר מכן מוסיף באופן סדרתי מספר רב של שאריות אדנין. זנב הפולי (A) אינו נדרש לתרגום, אך יש לו השפעה על יציבות התמלילים בציטופלזמה. ככל שמולקולות mRNA נשארות בציטופלזמה זמן רב יותר, זנב הפולי (A) מוסר בהדרגה. ברגע שזנב הפולי (A) ייעלם, ה-mRNA ייהרס בקרוב. מולקולות mRNA עם זנבות פולי (A) ארוכים יותר בדרך כלל ארוכות יותר בציטופלזמה מאלו עם זנבות קצרים יותר, אך כרגע אין עדות להשפעה פרופורציונלית ישירה.
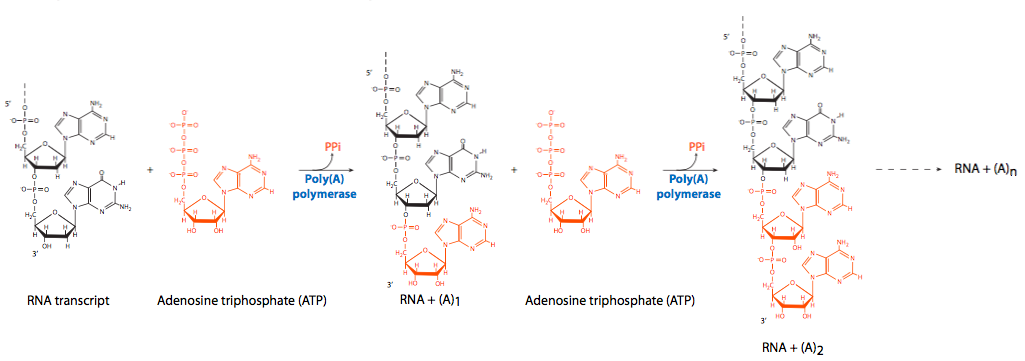
למרות שהאנזים שמבקע את התמליל העיקרי כהכנה לפוליאדנילציה לא זוהה, שני גורמים לא אנזימטיים, גורם המחשוף I (CFI) בעל השם המרגש וגורם המחשוף II (CFII) היו מעורבים. האדנילציה הסדרתית מגיעה מפעילות פולי (A) פולימראז (PAP) בשילוב עם CPSF (מחשוף ופוליאדנילציה speci city factor), הנקשר ל-RNA. ל- PAP עצמו יש זיקה ירודה יחסית ל- RNA. כמו בפולימראזות אחרות של חומצות גרעין, הוא מוסיף נוקלאוטידים חדשים ל-3'-OH החופשי של השרשרת הקיימת. כדי לעודד תהליכים (פילמור רציף) חלבון קושר פולי (A) II (PABII) מצטרף לקומפלקס הפוליאדנילציה, ומעורב בשליטה באורך הסופי של זנב הפולי (A). יש לציין כי PABII הוא חלבון גרעיני ואין לבלבל אותו עם חלבון מחייב PABP (פולי (A)) הנקשר למולקולות mRNA בציטופלזמה וממלא תפקיד בהגנה עליהן מפני התקפת נוקלאז.
השינוי השלישי והמסובך ביותר ל-RNA אוקריוטי שהועתק לאחרונה הוא שחבור. בניגוד ל-RNA פרוקריוטי, שהוא אזור קידוד הניתן לתרגום רציף מיד כשהוא יוצא מה-RNA פולימראז, רוב ה-RNA האוקריוטי קטעו את אזורי הקידוד. שחבור הוא התהליך שבו מוסרים האזורים הלא מקודדים, המכונים אינטרונים, ואזורי הקידוד, המכונים אקסונים, מחוברים זה לזה. בחלק מה-RNA זה יכול לקרות באופן אוטונומי, כאשר חלק מה-RNA פועל כזרז אנזימטי לתהליך. זה דורש של-RNA יהיה מבנה משני ושלישוני ספציפי, המקרב את שני האקסונים זה לזה תוך לולאה החוצה של האינטרון. זה היה המחקר של תופעה זו שהוביל לגילוי ריבוזימים, שהם אנזימים עשויים RNA.
עד לגילוי הריבוזימים, ההנחה הייתה שרק האנזימים יכולים להיווצר רק עם מגוון המבנים האפשריים עם חומצות האמינו בחלבונים.
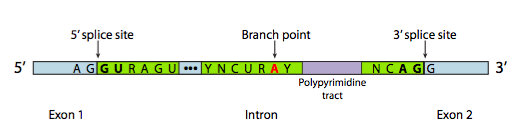
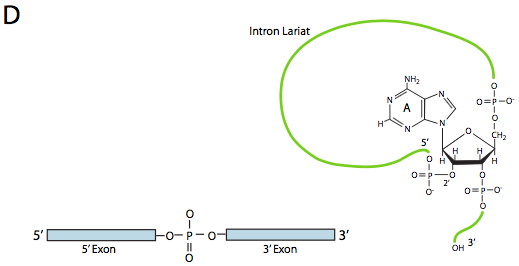
אולם ברוב המקרים, השחבור מתבצע על ידי קומפלקס חלבון מרובה יחידות המכונה הספליזוזום. בין אם זה שחבור עצמי או על ידי spliceosome, ישנם שלושה מרכיבי רצף עיקריים הדרושים להגדרת אינטרון שעומד להיות מחולק (איור). \(\PageIndex{8}\) יש אתר אחוי 5' עם רצף הקונצנזוס AG|GUAAGU. יש אתר שחבור של 3 'שמתחיל במערכת פוליפירימידין של 11 נוקלאוטידים ואחריו NCAG | G. ואיפשהו בין השניים, יש אדנין מסועף, בדרך כלל בתוך רצף YNCURAY (Y הוא פירמידין, N הוא כל נוקלאוטיד, R הוא פורין). שחבור הוא למעשה קבוצה של שתי תגובות טרנס-אסטריפיקציה רציפות, ודורש קרבה פיזית של האתרים התגובתיים על ידי כיפוף ולולאה של ה- RNA, באופן אוטונומי או סביב גורמי חלבון המכונים snRNPs (מבוטא "snurps"). snRNPs הוא ראשי תיבות של ריבונוקלאופרוטאינים גרעיניים קטנים. הם מכילים גם חלבון וגם רכיב RNA גרעיני קטן (snRNA); האחרון מסייע בזיהוי רצף. בחינת המבנה של חלק ה-snRNA של snRNPs spliceosome אלה מראה שהם דומים מאוד לצורות שנלקחו על ידי תמליל ה-RNA עצמו במקרים של שחבור עצמי. אם ניקח זאת בחשבון, חלק גדול מהתיאור הבא של שחבור בתיווך spliceosome מתרחש גם בשחבור עצמי.
למרות שה-snRNPs הם המרכיבים העיקריים של הספליזוזום, גם מגוון גורמי שחבור אחרים ממלאים תפקיד. הבולטים ביותר הם U2AF (גורם הקשור ל-U2, הנקשר למערכת הפוליפירימידין, ו-SF1 (גורם שחבור 1, המכונה חלבון נקודת ענף BPP) הנקשר לרצף קונצנזוס ליד נקודת הענף. יחד הם עוזרים למקם כראוי את U2 snRNP. ישנם גם מגוון גורמי שחבור אחרים שנחקרו פחות ממשפחת חלבוני SR (מוטיב מחייב סרין-ארגינין מסוף C) ומשפחות hnRNP (ריבונוקליאו-חלבון גרעיני הטרוגני) הפועלות לגיוס החברים העיקריים של הספליזוזום למיקומם הנכון.
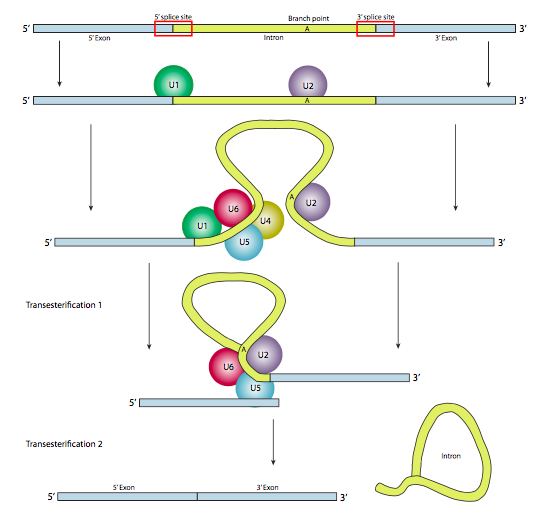
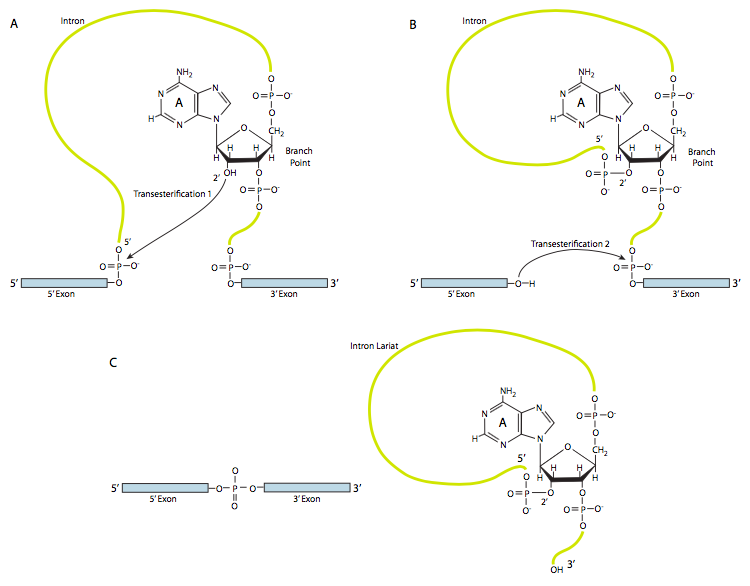
בשלב הראשון, ה-U1 snRNP נקשר לחלק האינטרוני של אתר השחבור 5'. לאחר מכן, U2 snRNP נקשר לאתר הקונצנזוס סביב נקודת הסניף, אך חשוב מכך, אין זיווג בסיס לנקודת הסניף A עצמה. במקום זאת, עקב זיווג בסיסי של U2 עם הרצף שמסביב, נקודת הענף A נאלצת לבלוט החוצה משאר ה- RNA באזור זה. U4, U5 ו-U6 מחברים את הספליזוזום יחד, אך בעוד U5 נקשר לאקסון 5', ו-U6 עוקר את U1 באתר השחבור 5', U4 מחובר רק באופן זמני וגם נופל מהספליזוזום לפני תגובת הטרנססטריפיקציה הראשונה. כפי שמראה האיור, בתגובה זו, ה-2'-OH של נקודת הענף A תוקף באופן נוקלאופילי את ה-5'-פוספט של נוקלאוטיד האינטרון הראשון ויוצר מבנה לריאט שבו קצה 5' של האינטרון מחובר לנקודת הענף באמצעות קשר 2',5'-פוספודיסטר. זה משחרר את האקסון 5' (ואת כל מחצית ה-5' של ה-RNA לצורך העניין), אך הוא נשמר בסמיכות לאקסון 3' (ולשאר ה-RNA) על ידי U5, שמתחבר לשני האקסונים. זה מאפשר להתרחש הטרנססטריפיקציה השנייה, שבה ה-3'- OH של האקסון הראשון תוקף את הפוספט 5' בתחילת האקסון השני, ובכך מפרק בו זמנית את הקשר בין האינטרון לאקסון השני, וגם מחבר את שני האקסונים באמצעות קשר 3',5'-פוספודיסטר קונבנציונאלי. האינטרון, בצורת לריאט, משתחרר כך ויהיה מושפל במהירות.
שחבור הוא דרך יעילה (ביחס לגודל הגנום) ליצירת מגוון חלבונים. בחבור חלופי, כמה אינטרונים פוטנציאליים עשויים להיות מחולקים בנסיבות מסוימות אך להישאר כרצף קידוד בנסיבות אחרות. נזכיר שאתרי השחבור מזוהים על ידי זיווג בסיסים ולכן, יכולים להיות אתרי שחבור חזקים וחלשים יותר, תלוי עד כמה הם קרובים לקונצנזוס ולרצף המשלים ב-snRNPs. לכן, בגן עם מספר אינטרונים פוטנציאליים עשויים להיות כל האינטרונים שחוברו 80% מהזמן, אבל ב -20% האחרים של הזמן, אולי רק אינטרונים אחד או שניים מחולקים החוצה. הוספת שונות, ישנם גורמי שחבור שעשויים להיקשר ליד אתרי שחבור ויכולים להפוך אותם לזיהוי קל יותר, או כמעט מוסתרים.
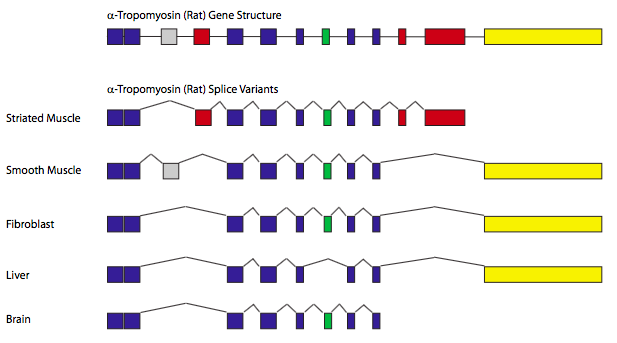
הדוגמה הקלאסית לשחבור חלופי היא הגן המקודד α-tropomyosin (איור). \(\PageIndex{11}\) על ידי שחבור פנימה/החוצה שילובים שונים של אקסונים, גן בודד יכול ליצור שבעה חלבונים שונים, בהתאם לסוג הרקמה. במקרים אלה, סוגים מסוימים של תאים או רקמות מכילים שילובים ספציפיים של גורמי שחבור, ולכן שולטים בזיהוי אתרי שחבור ספציפיים, מה שמוביל לדפוסי השחבור השונים.
למרות שזה מסיים את הדיון במנגנונים בסיסיים של שעתוק, הפרק הבא הוא באמת המשך של זה: שליטה בביטוי הגנים בצורתו הפשוטה ביותר היא ויסות ההכרה ברצף פרומטור על ידי פולימראז RNA.