15.2: כיצד פתוגנים גורמים למחלות
- Page ID
- 208941
מטרות למידה
- סכמו את ההנחות של קוך ואת ההנחות המולקולריות של קוך, בהתאמה, והסבירו את משמעותן ומגבלותיהן
- הסבר את מושג הפתוגניות (ארסיות) במונחים של מינון זיהומי וקטלני
- להבחין בין פתוגנים ראשוניים לאופורטוניסטיים ולזהות דוגמאות ספציפיות לכל אחד מהם
- לסכם את שלבי הפתוגנזה
- הסבירו את תפקידי פורטלי הכניסה והיציאה בהעברת מחלות וזיהו דוגמאות ספציפיות לפורטלים אלה
עבור רוב המחלות הזיהומיות, היכולת לזהות במדויק את הפתוגן הסיבתי היא צעד קריטי במציאת או מרשם של טיפולים יעילים. הרופאים, המטופלים והחוקרים של ימינו חייבים חוב ניכר לרופא רוברט קוך (1843—1910), שהמציא גישה שיטתית לאישור קשרים סיבתיים בין מחלות ופתוגנים ספציפיים.
ההנחות של קוך
בשנת 1884 פרסם קוך ארבע הנחות שסיכמו את שיטתו לקביעת האם מיקרואורגניזם מסוים הוא הגורם למחלה מסוימת. כל אחת מההנחות של קוך מייצגת קריטריון שיש לעמוד בו לפני שניתן יהיה לקשר באופן חיובי מחלה עם פתוגן. על מנת לקבוע אם הקריטריונים מתקיימים, מבוצעות בדיקות על חיות מעבדה ומשווים תרבויות מבעלי חיים בריאים וחולים (איור\(\PageIndex{1}\)).
ההנחות של קוך
- יש למצוא את הפתוגן החשוד בכל מקרה של מחלה ולא להימצא אצל אנשים בריאים.
- ניתן לבודד את הפתוגן החשוד ולגדל אותו בתרבות טהורה.
- נבדק בריא שנדבק בפתוגן החשוד חייב לפתח את אותם סימנים ותסמינים של מחלה כפי שניתן לראות בפוסטולאט
- הפתוגן חייב להיות מבודד מחדש מהמארח החדש וחייב להיות זהה לפתוגן מפוסטולציה 2.
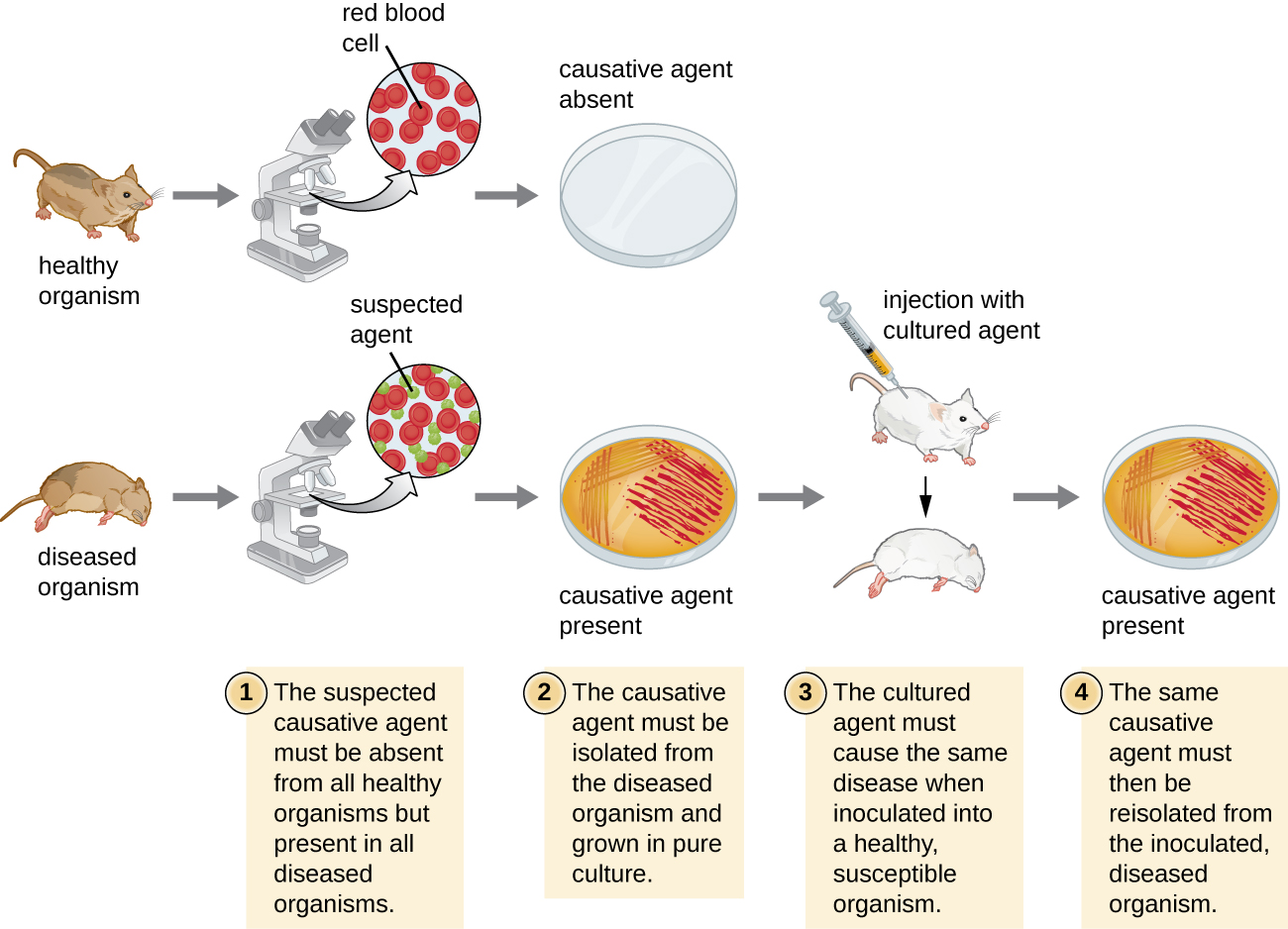
במובנים רבים, ההנחות של קוך עדיין מרכזיות בהבנתנו הנוכחית את הגורמים למחלות. עם זאת, ההתקדמות במיקרוביולוגיה חשפה כמה מגבלות חשובות בקריטריונים של קוך. קוך הניח כמה הנחות שאנו יודעים כיום שאינן נכונות במקרים רבים. הראשון מתייחס לתנוחה 1, המניחה כי פתוגנים נמצאים רק אצל אנשים חולים, לא בריאים. זה לא נכון לגבי פתוגנים רבים. לדוגמה, הליקובקטר פילורי, שתואר מוקדם יותר בפרק זה כפתוגן הגורם לדלקת קיבה כרונית, הוא גם חלק מהמיקרוביוטה התקינה של הקיבה בבני אדם בריאים רבים שלעולם אינם מפתחים דלקת קיבה. ההערכה היא כי למעלה מ -50% מאוכלוסיית האדם רוכשת הליקובקטר פילורי בשלב מוקדם של החיים, כאשר רובם שומרים עליו כחלק מהמיקרוביוטה הרגילה למשך שארית חייהם מבלי לפתח מחלה.
ההנחה השגויה השנייה של קוך הייתה שכל נבדקי הבדיקה הבריאים רגישים באותה מידה למחלות. כעת אנו יודעים כי אנשים אינם רגישים באותה מידה למחלות. אנשים ייחודיים מבחינת המיקרוביוטה שלהם ומצב המערכת החיסונית שלהם בכל זמן נתון. הרכב המיקרוביוטה התושבת יכול להשפיע על רגישותו של האדם לזיהום. חברי המיקרוביוטה הרגילה ממלאים תפקיד חשוב בחסינות על ידי עיכוב צמיחתם של פתוגנים חולפים. במקרים מסוימים, המיקרוביוטה עשויה למנוע מפתוגן לבסס זיהום; באחרים, זה לא יכול למנוע זיהום לחלוטין אך עשוי להשפיע על חומרת או סוג הסימנים והתסמינים. כתוצאה מכך, שני אנשים עם אותה מחלה עשויים לא תמיד להופיע עם אותם סימנים ותסמינים. בנוסף, יש אנשים שיש להם מערכת חיסונית חזקה יותר מאחרים. אנשים עם מערכת חיסונית מוחלשת על ידי גיל או מחלה לא קשורה הם הרבה יותר רגישים לזיהומים מסוימים מאשר אנשים עם מערכת חיסונית חזקה.
קוך גם הניח שכל הפתוגנים הם מיקרואורגניזמים שניתן לגדל בתרבית טהורה (הנחה 2) וכי בעלי חיים יכולים לשמש מודלים אמינים למחלות אנושיות. עם זאת, אנו יודעים כעת שלא ניתן לגדל את כל הפתוגנים בתרבות טהורה, ולא ניתן לשכפל באופן מהימן מחלות אנושיות רבות במארחים של בעלי חיים. וירוסים וחיידקים מסוימים, כולל ריקטסיה וכלמידיה, הם פתוגנים תאיים מחייבים שיכולים לצמוח רק כאשר הם נמצאים בתוך תא מארח. אם לא ניתן לתרבות חיידק, חוקר אינו יכול לעבור את ההנחה 2. באופן דומה, ללא מארח לא אנושי מתאים, חוקר אינו יכול להעריך את ההנחה 2 מבלי להדביק בני אדם בכוונה, מה שמציג חששות אתיים ברורים. איידס הוא דוגמה למחלה כזו מכיוון שנגיף הכשל החיסוני האנושי (HIV) גורם רק למחלות אצל בני אדם.
תרגיל \(\PageIndex{1}\)
סכם בקצרה את מגבלות ההנחות של קוך.
ההנחות המולקולריות של קוך
בשנת 1988 הציע סטנלי פאלקוב (1934—) צורה מתוקנת של ההנחות של קוך המכונה הנחות מולקולריות של קוך. אלה מפורטים בעמודה השמאלית של טבלה\(\PageIndex{1}\). הנחת היסוד של ההנחות המולקולריות של קוך אינה ביכולת לבודד פתוגן מסוים אלא לזהות גן שעלול לגרום לאורגניזם להיות פתוגני.
השינויים של פאלקוב בהנחות המקוריות של קוך מסבירים לא רק זיהומים הנגרמים על ידי פתוגנים תוך תאיים אלא גם את קיומם של זנים פתוגניים של אורגניזמים שהם בדרך כלל לא פתוגניים. לדוגמה, הצורה השולטת של החיידק Escherichia coli היא חברה במיקרוביוטה הרגילה של המעי האנושי ונחשבת בדרך כלל לא מזיקה. עם זאת, ישנם זנים פתוגניים של אי - קולי כגון אי - קולי אנטרוטוקסיגני (ETEC) ו אי - קולי אנטרו-המורגי (O157: H7) (EHEC). כעת אנו יודעים כי ETEC ו- EHEC קיימים בגלל רכישת גנים חדשים על ידי ה - E. coli שלא היה מזיק בעבר, אשר בצורה של זנים פתוגניים אלה מסוגל כעת לייצר רעלים ולגרום למחלות. הצורות הפתוגניות נבעו משינויים גנטיים קלים. העמודה הימנית של הטבלה \(\PageIndex{1}\) ממחישה כיצד ניתן ליישם את ההנחות המולקולריות של קוך לזיהוי EHEC כחיידק פתוגני.
| ההנחות המולקולריות של קוך | בקשה ל- EHEC |
|---|---|
| (1) הפנוטיפ (סימן או סימפטום של מחלה) צריך להיות קשור רק לזנים פתוגניים של מין. | EHEC גורם לדלקת מעיים ושלשולים, ואילו זנים לא פתוגניים של E. coli לא. |
| (2) השבתת הגנים החשודים הקשורים לפתוגניות אמורה לגרום לאובדן מדיד של פתוגניות. | אחד הגנים ב- EHEC מקודד לרעלן שיגה, רעלן חיידקי (רעל) המעכב את סינתזת החלבון. השבתת גן זה מפחיתה את יכולתו של החיידק לגרום למחלות. |
| (3) היפוך הגן הלא פעיל אמור לשחזר את הפנוטיפ של המחלה. | על ידי הוספת הגן המקודד את הרעלן בחזרה לגנום (למשל, עם פאג או פלסמיד), היכולת של EHEC לגרום למחלה משוחזרת. |
בדומה להנחות המקוריות של קוך, להנחות המולקולריות של קוך יש מגבלות. לדוגמה, מניפולציה גנטית של כמה פתוגנים אינה אפשרית בשיטות הנוכחיות של גנטיקה מולקולרית. ברוח דומה, למחלות מסוימות אין מודלים מתאימים של בעלי חיים, מה שמגביל את התועלת של ההנחות המקוריות והמולקולריות כאחד.
תרגיל \(\PageIndex{2}\)
הסבר את ההבדלים בין ההנחות המקוריות של קוך לבין ההנחות המולקולריות של קוך.
פתוגניות וארסיות
היכולת של גורם מיקרוביאלי לגרום למחלות נקראת פתוגניות, והמידה שבה אורגניזם פתוגני נקראת ארסיות. ארסיות היא רצף. בקצה אחד של הספקטרום נמצאים אורגניזמים שהם אוויריים (לא מזיקים) ומצד שני אורגניזמים ארסיים ביותר. פתוגנים ארסיים מאוד יובילו כמעט תמיד למצב מחלה כאשר הם מוצגים לגוף, וחלקם אף עלולים לגרום לכשל רב-איברים ומערכת הגוף אצל אנשים בריאים. פתוגנים פחות ארסיים עלולים לגרום לזיהום ראשוני, אך לא תמיד עלולים לגרום למחלה קשה. סביר יותר שפתוגנים עם ארסיות נמוכה יגרמו לסימנים ותסמינים קלים של מחלה, כגון חום בדרגה נמוכה, כאבי ראש או כאבי שרירים. אנשים מסוימים עשויים אפילו להיות אסימפטומטיים.
דוגמה למיקרואורגניזם ארסי ביותר הוא Bacillus anthracis, הפתוגן האחראי לאנתרקס. B. anthracis יכול לייצר צורות שונות של מחלה, בהתאם למסלול ההעברה (למשל, הזרקה עורית, שאיפה, בליעה). הצורה החמורה ביותר של אנתרקס היא אנתרקס שאיפה. לאחר שאיפה של נבגי B. anthracis, הם נובטים. מתפתח זיהום פעיל והחיידקים משחררים רעלים חזקים הגורמים לבצקת (הצטברות נוזלים ברקמות), היפוקסיה (מצב המונע חמצן להגיע לרקמות) ונמק (מוות תאים ודלקת). הסימנים והתסמינים של אנתרקס שאיפה כוללים חום גבוה, קשיי נשימה, הקאות ושיעול דם וכאבים חזקים בחזה המרמזים על התקף לב. עם אנתרקס שאיפה, הרעלים והחיידקים נכנסים לזרם הדם, מה שעלול להוביל לכשל רב-איברים ומוות של המטופל. אם גן (או גנים) המעורבים בפתוגנזה אינו פעיל, החיידקים הופכים פחות ארסיים או לא פתוגניים.
ניתן לכמת ארסיות של פתוגן באמצעות ניסויים מבוקרים עם חיות מעבדה. שני אינדיקטורים חשובים לארסיות הם המינון הזיהומי החציוני (ID 50) והמינון הקטלני החציוני (LD 50), שניהם נקבעים בדרך כלל בניסוי באמצעות מודלים של בעלי חיים. מזהה 50 הוא מספר תאי הפתוגן או הנגיפים הנדרשים כדי לגרום לזיהום פעיל ב -50% מבעלי החיים המחוסנים. LD 50 הוא מספר התאים הפתוגניים, הווירונים או כמות הרעלן הנדרשת כדי להרוג 50% מבעלי החיים הנגועים. כדי לחשב ערכים אלה, כל קבוצת בעלי חיים מחוסנת באחד ממגוון המספרים הידועים של תאי פתוגן או וירוסים. בגרפים כמו זה שמוצג באיור\(\PageIndex{2}\), אחוז בעלי החיים שנדבקו (עבור מזהה 50) או נהרגו (עבור LD 50) משורטט כנגד ריכוז הפתוגן שחוסן. האיור \(\PageIndex{2}\) מייצג נתונים בתרשים מניסוי היפותטי המודד את LD 50 של פתוגן. פרשנות הנתונים מגרף זה מצביעה על כך שה-LD 50 של הפתוגן עבור חיות הניסוי הוא 10 4 תאי פתוגן או ויריון (תלוי בפתוגן שנחקר).
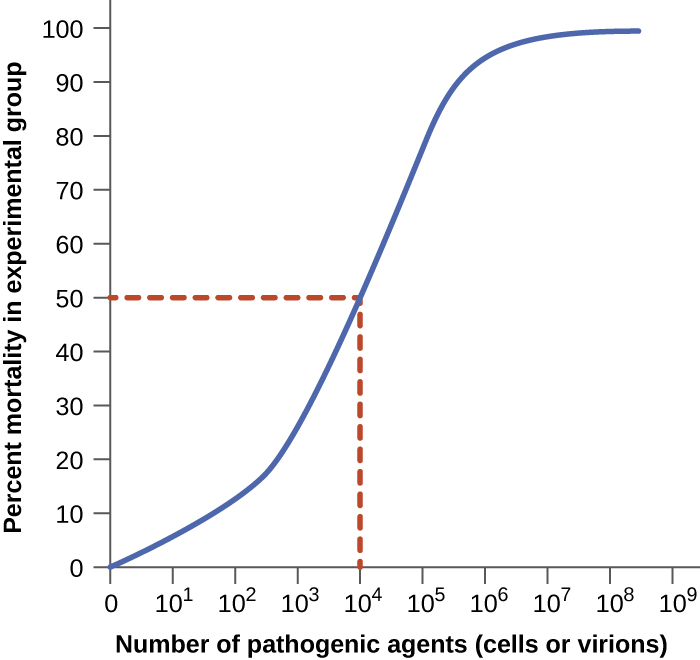
הטבלה \(\PageIndex{2}\) מפרטת פתוגנים נבחרים הנישאים במזון וערכי ID 50 שלהם בבני אדם (כפי שנקבע מנתונים אפידמיולוגיים ומחקרים על מתנדבים אנושיים). זכור כי אלה הם ערכים חציוניים. המינון הזיהומי בפועל לאדם יכול להשתנות במידה רבה, בהתאם לגורמים כמו דרך הכניסה; הגיל, הבריאות ומצב החיסון של המארח; וגורמים סביבתיים וספציפיים לפתוגן כגון רגישות ל- pH החומצי של הקיבה. כמו כן, חשוב לציין כי מינון זיהומי של פתוגן אינו בהכרח מתאם לחומרת המחלה. לדוגמה, רק תא בודד של סלמונלה אנטריקה סרוטיפ Typhimurium יכול לגרום לזיהום פעיל. המחלה המתקבלת, סלמונלה גסטרואנטריטיס או סלמונלוזיס, עלולה לגרום לבחילות, הקאות ושלשולים, אך שיעור התמותה שלה נמוך מ -1% בקרב מבוגרים בריאים. לעומת זאת, S. enterica סרוטיפ לטיפי יש מזהה 50 גבוה בהרבה, בדרך כלל דורש עד 1,000 תאים כדי לייצר זיהום. עם זאת, סרוטיפ זה גורם לחום בטיפוס, מחלה מערכתית וחמורה הרבה יותר שיש לה שיעור תמותה גבוה עד 10% בקרב אנשים לא מטופלים.
| פתוגן | תעודת זהות 50 |
|---|---|
| וירוסים | |
| וירוס הפטיטיס A | 10—100 |
| נורובירוס | 1—10 |
| וירוס רוטבי | 10—100 |
| חיידקים | |
| אי קולי, אנטרודימורגי (EHEC, סרוטיפ O157) | 10—100 |
| אי - קולי, אנטרו-פולשני (EIEC) | 200—5,000 |
| אי - קולי, אנטרופתוגני (EPEC) | 10,000,000—10,000,000,000 |
| אי - קולי, אנטרוטוקסיגני (ETEC) | 10,000,000—10,000,000,000 |
| סלמונלה אנטריקה סרובר Typhi | <1,000 |
| S. enterica סרובר טיפימוריום | ≥1 |
| שיגלה דיזנטריה | 10—200 |
| ויבריו כולרה (סרוטיפים O139, O1) | 1,000,000 |
| V. פרהמוליטיקוס | 100,000,000 |
| פרוטוזואה | |
| ג'יארדיה למבליה | 1 |
| קריפטוספורידיום פרוום | 10—100 |
תרגיל \(\PageIndex{3}\)
- מה ההבדל בין מינון זיהומי של פתוגן למינון קטלני?
- מה קשור יותר לחומרת המחלה?
פתוגנים ראשוניים לעומת פתוגנים אופורטוניסטיים
ניתן לסווג פתוגנים כפתוגנים ראשוניים או פתוגנים אופורטוניסטיים. פתוגן ראשוני יכול לגרום למחלות במארח ללא קשר למיקרוביוטה או למערכת החיסון של המארח. פתוגן אופורטוניסטי, לעומת זאת, יכול לגרום למחלות רק במצבים המסכנים את ההגנה של המארח, כגון מחסומי ההגנה של הגוף, מערכת החיסון או מיקרוביוטה רגילה. אנשים הרגישים לזיהומים אופורטוניסטיים כוללים את הצעירים מאוד, קשישים, נשים בהריון, חולים שעברו כימותרפיה, אנשים עם ליקויים חיסוניים (כגון תסמונת כשל חיסוני נרכש [איידס]), חולים המחלימים מניתוח ואלו שעברו הפרה של מחסומי הגנה (כגון פצע קשה או כוויה).
דוגמה לפתוגן ראשוני הוא enterohemorrhagic E. coli (EHEC), המייצר גורם ארסיות המכונה רעלן שיגה. רעלן זה מעכב את סינתזת החלבון, מה שמוביל לשלשול חמור ועקוב מדם, דלקת ואי ספיקת כליות, אפילו בחולים עם מערכת חיסון בריאה. סטפילוקוקוס אפידרמידיס, לעומת זאת, הוא פתוגן אופורטוניסטי שהוא בין הגורמים השכיחים ביותר למחלות נוזוקומיאליות. 2 S. epidermidis הוא חבר במיקרוביוטה הרגילה של העור, שם הוא בדרך כלל אווירולנטי. עם זאת, בבתי חולים הוא יכול לצמוח גם בביופילמים הנוצרים על צנתרים, שתלים או מכשירים אחרים המוחדרים לגוף במהלך ניתוחים. ברגע שנכנס לגוף, S. epidermidis יכול לגרום לזיהומים חמורים כמו אנדוקרדיטיס, והוא מייצר גורמי ארסיות המקדמים את ההתמדה של זיהומים כאלה.
חברים אחרים במיקרוביוטה הרגילה יכולים גם לגרום לזיהומים אופורטוניסטיים בתנאים מסוימים. זה קורה לעתים קרובות כאשר חיידקים השוכנים באופן לא מזיק במיקום גוף אחד מגיעים למערכת גוף אחרת, שם הם גורמים למחלות. לדוגמה, E. coli שנמצא בדרך כלל במעי הגס יכול לגרום לזיהום בדרכי השתן אם הוא נכנס לשלפוחית השתן. זהו הגורם המוביל לדלקות בדרכי השתן בקרב נשים.
חברי המיקרוביוטה הרגילה עלולים גם לגרום למחלות כאשר שינוי בסביבת הגוף מוביל לצמיחת יתר של מיקרואורגניזם מסוים. לדוגמה, השמרים קנדידה היא חלק מהמיקרוביוטה הרגילה של העור, הפה, המעי והנרתיק, אך אוכלוסייתה נשמרת על ידי אורגניזמים אחרים של המיקרוביוטה. עם זאת, אם אדם נוטל תרופות אנטיבקטריאליות, ניתן להרוג חיידקים שבדרך כלל יעכבו את צמיחת הקנדידה, מה שמוביל לגידול פתאומי באוכלוסיית הקנדידה, שאינה מושפעת מתרופות אנטיבקטריאליות מכיוון שמדובר בפטרייה. צמיחת יתר של קנדידה יכולה להתבטא כקיכלי פה (צמיחה בפה, בגרון ובלשון), זיהום שמרים בנרתיק או קנדידיזיס עורית. תרחישים אחרים יכולים גם לספק הזדמנויות לזיהומים בקנדידה. סוכרת לא מטופלת עלולה לגרום לריכוז גבוה של גלוקוז ברוק, המספק סביבה אופטימלית לצמיחת קנדידה, וכתוצאה מכך קיכלי. ליקויים חיסוניים כמו אלה הנראים בחולים עם HIV, איידס וסרטן מובילים גם לשכיחות גבוהה יותר של קיכלי. דלקות שמרים בנרתיק יכולות לנבוע מירידה ברמות האסטרוגן במהלך הווסת או גיל המעבר. כמות הגליקוגן הזמינה ללקטובצילי בנרתיק נשלטת על ידי רמות האסטרוגן; כאשר רמות האסטרוגן נמוכות, לקטובצילים מייצרים פחות חומצה לקטית. העלייה המתקבלת ב- pH בנרתיק מאפשרת צמיחת יתר של קנדידה בנרתיק.
תרגיל \(\PageIndex{4}\)
- הסבר את ההבדל בין פתוגן ראשוני לפתוגן אופורטוניסטי.
- תאר כמה תנאים שבהם זיהום אופורטוניסטי יכול להתרחש.
שלבי פתוגנזה
כדי לגרום למחלה, פתוגן חייב להשיג בהצלחה ארבעה שלבים או שלבים של פתוגנזה: חשיפה (מגע), הידבקות (קולוניזציה), פלישה וזיהום. הפתוגן חייב להיות מסוגל להיכנס למארח, לנסוע למקום בו הוא יכול לבסס זיהום, להתחמק או להתגבר על התגובה החיסונית של המארח ולגרום נזק (כלומר, מחלה) למארח. במקרים רבים, המחזור מסתיים כאשר הפתוגן יוצא מהמארח ומועבר למארח חדש.
חשיפה
מפגש עם פתוגן פוטנציאלי מכונה חשיפה או מגע. האוכל שאנו אוכלים והחפצים שאנו מטפלים בהם הם כל הדרכים בהן אנו יכולים לבוא במגע עם פתוגנים פוטנציאליים. עם זאת, לא כל אנשי הקשר גורמים לזיהום ומחלות. כדי שפתוגן יגרום למחלה, הוא צריך להיות מסוגל לקבל גישה לרקמת המארח. אתר אנטומי שדרכו פתוגנים יכולים לעבור לרקמת המארח נקרא פורטל כניסה. אלו הם מיקומים שבהם התאים המארחים נמצאים במגע ישיר עם הסביבה החיצונית. פורטלי כניסה עיקריים מזוהים באיור \(\PageIndex{3}\) וכוללים את העור, הריריות והנתיבים הפרנטרליים.
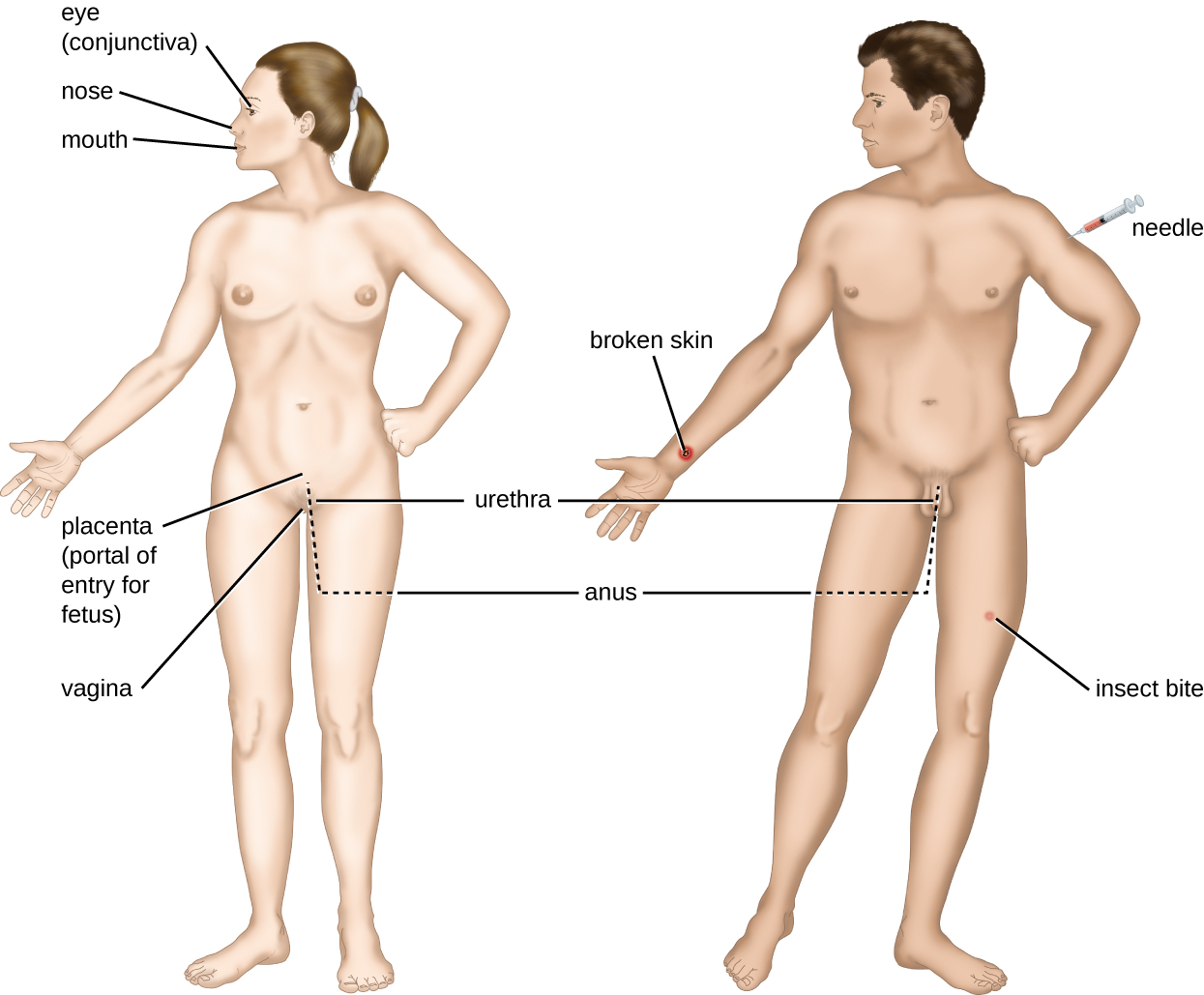
משטחים ריריים הם פורטלי הכניסה החשובים ביותר לחיידקים; אלה כוללים את הריריות של דרכי הנשימה, דרכי העיכול ודרכי השתן. למרות שרוב משטחי הרירית נמצאים בחלק הפנימי של הגוף, חלקם צמודים לעור החיצוני בפתחי גוף שונים, כולל העיניים, האף, הפה, השופכה ופי הטבעת.
רוב הפתוגנים מתאימים לפורטל כניסה מסוים. סגוליות הפורטל של פתוגן נקבעת על ידי ההתאמות הסביבתיות של האורגניזם ועל ידי האנזימים והרעלים שהם מפרישים. דרכי הנשימה והמעיים הם פורטלי כניסה פגיעים במיוחד מכיוון שחלקיקים הכוללים מיקרואורגניזמים נשאפים או נבלעים ללא הרף, בהתאמה.
פתוגנים יכולים גם להיכנס דרך הפרה של מחסומי המגן של העור ואת רירית הממברנות. פתוגנים הנכנסים לגוף בדרך זו אמורים להיכנס בדרך הפרנטרלית. לדוגמא, העור מהווה מחסום טבעי טוב לפתוגנים, אך שבירות בעור (למשל פצעים, עקיצות חרקים, עקיצות בעלי חיים, דקירות מחט) יכולות לספק פורטל כניסה פרנטרלי למיקרואורגניזמים.
אצל נשים הרות, השליה מונעת בדרך כלל ממיקרואורגניזמים לעבור מהאם לעובר. עם זאת, כמה פתוגנים מסוגלים לחצות את מחסום הדם-שליה. החיידק החיובי לגרם ליסטריה מונוציטוגנים, הגורם למחלת המזון ליסטריוזיס, הוא דוגמא אחת המהווה סיכון רציני לעובר ולעיתים יכולה להוביל להפלה ספונטנית. פתוגנים אחרים שיכולים לעבור את מחסום השליה כדי להדביק את העובר ידועים ביחד על ידי ראשי התיבות TORCH (טבלה\(\PageIndex{3}\)).
העברת מחלות זיהומיות מאם לתינוק מהווה גם דאגה בזמן הלידה כאשר התינוק עובר בתעלת הלידה. תינוקות שאמהותיהם סובלות מדלקות כלמידיה או זיבה פעילים עלולים להיחשף לפתוגנים הסיבתיים בנרתיק, מה שעלול לגרום לדלקות עיניים המובילות לעיוורון. כדי למנוע זאת, מקובל לתת טיפות אנטיביוטיות לעיני התינוקות זמן קצר לאחר הלידה.
| מחלה | פתוגן | |
|---|---|---|
| T | טוקסופלזמוזיס | טוקסופלזמה גונדי (פרוטוזואן) |
| O 3 |
עגבת אבעבועות רוח הפטיטיס B HIV מחלה חמישית (אריתמה אינקטוסום) |
טרפונמה פלידיום (חיידק) וירוס אבעבועות רוח (וירוס הרפס אנושי 3) נגיף הפטיטיס B (הפדנאווירוס) רטרווירוס פרבווירוס B19 |
| R | אדמת (חצבת גרמנית) | נגיף טוגה |
| ג | ציטומגלווירוס | הרפס ווירוס אנושי 5 |
| H | הרפס | נגיפי הרפס סימפלקס (HSV) 1 ו -2 |
מיקוד קליני: חלק 2
במרפאה רופא מוריד את ההיסטוריה הרפואית של מייקל ושואל על פעילותו ותזונתו במהלך השבוע האחרון. לאחר שנודע לו שמייקל חלה יום לאחר המסיבה, הרופא מזמין בדיקת דם לבדיקת פתוגנים הקשורים למחלות הנישאות במזון. לאחר שבדיקות מאשרות את נוכחותו של מוט חיובי גרם בדמו של מייקל, הוא מקבל זריקה של אנטיביוטיקה רחבת טווח ונשלח לבית חולים סמוך, שם הוא אושפז כחולה. שם הוא אמור לקבל טיפול אנטיביוטי תוך ורידי נוסף ונוזלים.
תרגיל \(\PageIndex{5}\)
- האם החיידק הזה בדמו של מייקל הוא חלק ממיקרוביוטה רגילה?
- באיזה פורטל כניסה השתמשו החיידקים כדי לגרום לזיהום זה?
הדבקה
לאחר החשיפה הראשונית, הפתוגן דבק בפורטל הכניסה. המונח הידבקות מתייחס ליכולתם של חיידקים פתוגניים להיצמד לתאי הגוף באמצעות גורמי הדבקה, ופתוגנים שונים משתמשים במנגנונים שונים כדי להיצמד לתאי הרקמות המארחות.
מולקולות (חלבונים או פחמימות) הנקראות אדהזינים נמצאות על פני השטח של פתוגנים מסוימים ונקשרות לקולטנים ספציפיים (גליקופרוטאינים) בתאי המארח. אדזינים קיימים על פימבריה ודגלים של חיידקים, ציציות הפרוטוזואה והקפסידים או הממברנות של נגיפים. פרוטוזואנים יכולים גם להשתמש בווים ודוקרנים להדבקה; חלבוני ספייק על וירוסים גם משפרים את ההידבקות הנגיפית. ייצור גליקוקליסים (שכבות רפש וכמוסות) (איור\(\PageIndex{4}\)), עם תכולת הסוכר והחלבון הגבוהה שלהם, יכול גם לאפשר לפתוגנים חיידקיים מסוימים להיצמד לתאים.
גידול ביופילם יכול לשמש גם כגורם הדבקה. ביופילם הוא קהילה של חיידקים המייצרים גליקוקליקס, המכונה חומר אקסטרפולימרי (EPS), המאפשר לביופילם להיצמד למשטח. זיהומים מתמשכים של Pseudomonas aeruginosa שכיחים בחולים הסובלים מסיסטיק פיברוזיס, פצעי כוויות ודלקות באוזן התיכונה (דלקת אוזן תיכונה) מכיוון P. aeruginosa מייצר ביופילם. ה-EPS מאפשר לחיידקים להיצמד לתאי המארח ומקשה על המארח להסיר פיזית את הפתוגן. ה-EPS לא רק מאפשר התקשרות אלא מספק הגנה מפני המערכת החיסונית וטיפולים אנטיביוטיים, ומונע מאנטיביוטיקה להגיע לתאי החיידק בתוך הביופילם. בנוסף, לא כל החיידקים בביופילם גדלים במהירות; חלקם נמצאים בשלב נייח. מכיוון שאנטיביוטיקה יעילה ביותר נגד חיידקים הגדלים במהירות, חלקים של חיידקים בביופילם מוגנים מפני אנטיביוטיקה. 4
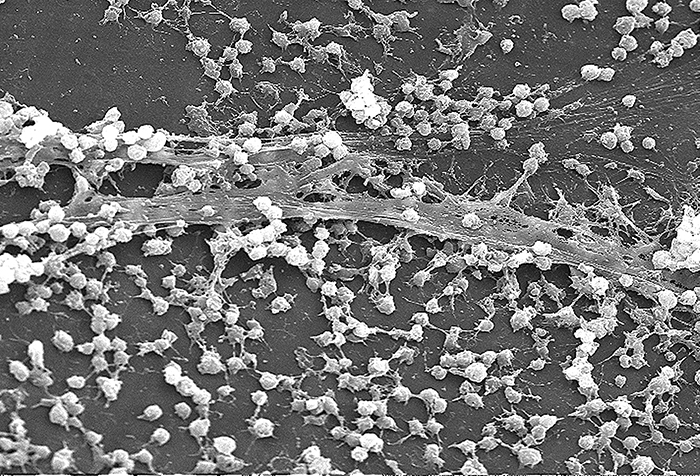
פלישה
ברגע שההדבקה מוצלחת, הפלישה יכולה להמשיך. הפלישה כוללת הפצת פתוגן בכל הרקמות המקומיות או בגוף. פתוגנים עשויים לייצר אקסואנזימים או רעלים, המשמשים כגורמי ארסיות המאפשרים להם להתיישב ולפגוע ברקמות המארח כשהם מתפשטים עמוק יותר לתוך הגוף. פתוגנים עשויים גם לייצר גורמי ארסיות המגנים עליהם מפני הגנות מערכת החיסון. גורמי הארסיות הספציפיים של הפתוגן קובעים את מידת הנזק לרקמות המתרחש. איור \(\PageIndex{5}\) מראה את הפלישה של הליקובקטר פילורי לרקמות הקיבה, וגורם נזק ככל שהוא מתקדם.
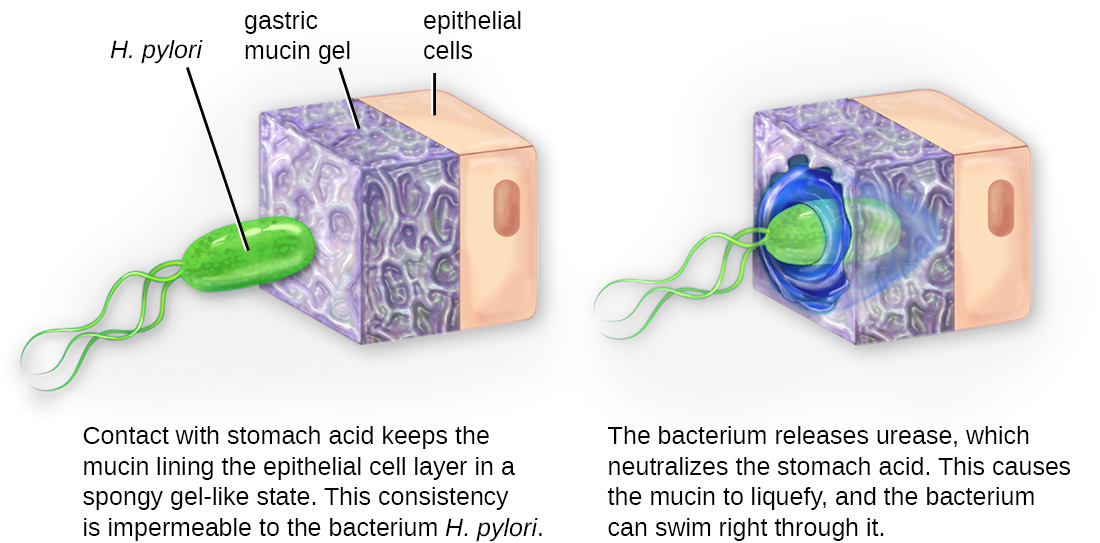
פתוגנים תוך תאיים משיגים פלישה על ידי כניסה לתאי המארח והתרבות. חלקם פתוגנים תוך תאיים מחייבים (כלומר הם יכולים להתרבות רק בתוך תאי מארח) ואחרים הם פתוגנים תאיים פקולטטיביים (כלומר הם יכולים להתרבות בתוך או מחוץ לתאי המארח). על ידי כניסה לתאי המארח, פתוגנים תוך תאיים מסוגלים להתחמק ממנגנונים מסוימים של מערכת החיסון תוך ניצול החומרים המזינים בתא המארח.
כניסה לתא יכולה להתרחש על ידי אנדוציטוזיס. עבור רוב סוגי התאים המארחים, פתוגנים משתמשים באחד משני מנגנונים שונים לאנדוציטוזה וכניסה. מנגנון אחד מסתמך על חלבוני אפקטור המופרשים על ידי הפתוגן; חלבוני אפקטור אלה מעוררים כניסה לתא המארח. זוהי השיטה בה משתמשים סלמונלה ושיגלה בעת פלישה לתאי אפיתל במעי. כאשר פתוגנים אלה באים במגע עם תאי אפיתל במעי, הם מפרישים מולקולות אפקטור הגורמות לבליטות של סלסולי קרום המביאים את התא החיידקי פנימה. תהליך זה נקרא פרע ממברנה. המנגנון השני מסתמך על חלבוני פני השטח המתבטאים על הפתוגן הנקשרים לקולטנים בתא המארח, וכתוצאה מכך כניסה. לדוגמה, Yersinia pseudotuberculosis מייצר חלבון פני השטח המכונה invasin הנקשר לאינטגרינים בטא -1 המתבטאים על פני השטח של תאי המארח.
חלק מהתאים המארחים, כגון תאי דם לבנים ופגוציטים אחרים של מערכת החיסון, אנדוציטוזים פעילים בתהליך הנקרא פגוציטוזיס. למרות שפגוציטוזיס מאפשרת לפתוגן להיכנס לתא המארח, ברוב המקרים, התא המארח הורג ומפרק את הפתוגן באמצעות אנזימי עיכול. בדרך כלל, כאשר פתוגן נבלע על ידי פגוציט, הוא סגור בתוך פגוזום בציטופלזמה; הפגוזום מתמזג עם ליזוזום ליצירת פגוליסוזום, שבו אנזימי עיכול הורגים את הפתוגן (ראה זיהוי פתוגן ופגוציטוזיס). עם זאת, לחלק מהפתוגנים התוך-תאיים יש את היכולת לשרוד ולהתרבות בתוך פגוציטים. דוגמאות לכך כוללות ליסטריה מונוציטוגנים ושיגלה; חיידקים אלה מייצרים חלבונים המסלקים את הפגוזום לפני שהוא מתמזג עם הליזוזום, ומאפשרים לחיידקים לברוח לציטופלזמה של הפגוציט שם הם יכולים להתרבות. חיידקים כגון Mycobacterium tuberculosis, Legionella pneumophila ומיני סלמונלה משתמשים במנגנון שונה במקצת כדי להתחמק מעיכול על ידי הפגוציט. חיידקים אלה מונעים את היתוך הפגוזום עם הליזוזום, ובכך נשארים בחיים ומתחלקים בתוך הפגוזום.
זיהום
לאחר הפלישה, כפל מוצלח של הפתוגן מוביל לזיהום. ניתן לתאר זיהומים כמקומיים, מוקדים או מערכתיים, תלוי במידת הזיהום. זיהום מקומי מוגבל לאזור קטן בגוף, בדרך כלל בסמוך לפורטל הכניסה. לדוגמה, זקיק שיער הנגוע בזיהום Staphylococcus aureus עלול לגרום לרתיחה סביב מקום ההדבקה, אך החיידק מכיל במידה רבה את המיקום הקטן הזה. דוגמאות נוספות לזיהומים מקומיים הכרוכים במעורבות רקמות נרחבת יותר כוללות דלקות בדרכי השתן המוגבלות לשלפוחית השתן או דלקת ריאות המוגבלת לריאות.
בזיהום מוקד, פתוגן מקומי, או הרעלים שהוא מייצר, יכולים להתפשט למקום משני. לדוגמא, שיננית שמנקרת את המסטיק בכלי חד יכולה להוביל לזיהום מקומי בחניכיים על ידי חיידקי סטרפטוקוקוס של המיקרוביוטה האוראלית הרגילה. סטרפטוקוקוס spp. לאחר מכן עשויים לקבל גישה לזרם הדם ולעשות את דרכם למקומות אחרים בגוף, וכתוצאה מכך זיהום משני.
כאשר זיהום מופץ בכל הגוף, אנו קוראים לזה זיהום מערכתי. לדוגמה, זיהום בנגיף varicella-zoster בדרך כלל מקבל כניסה דרך קרום רירי של מערכת הנשימה העליונה. לאחר מכן הוא מתפשט בכל הגוף, וכתוצאה מכך נגעי העור האדומים הקלאסיים הקשורים לאבעבועות רוח. מאז נגעים אלה אינם אתרים של זיהום ראשוני, הם סימנים של זיהום מערכתי.
לפעמים זיהום ראשוני, הזיהום הראשוני הנגרם על ידי פתוגן אחד, יכול להוביל לזיהום משני על ידי פתוגן אחר. לדוגמה, המערכת החיסונית של חולה עם זיהום ראשוני על ידי HIV נפגעת, מה שהופך את המטופל לרגיש יותר למחלות משניות כמו קיכלי פה ואחרים הנגרמים על ידי פתוגנים אופורטוניסטיים. באופן דומה, זיהום ראשוני על ידי נגיף השפעת פוגע ומקטין את מנגנוני ההגנה של הריאות, מה שהופך את החולים לרגישים יותר לדלקת ריאות משנית על ידי פתוגן חיידקי כמו Haemophilus influenzae או Streptococcus pneumoniae. כמה זיהומים משניים יכולים אף להתפתח כתוצאה מטיפול בזיהום ראשוני. טיפול אנטיביוטי המכוון לפתוגן העיקרי עלול לגרום לנזק נלווה למיקרוביוטה הרגילה, וליצור פתח לפתוגנים אופורטוניסטיים (ראה מקרה בנקודה: זיהום שמרים משני להלן).
זיהום שמרים משני
אניטה, אם לשלושה בת 36, הולכת למרכז טיפול דחוף ומתלוננת על לחץ באגן, השתנה תכופה וכואבת, התכווצויות בטן ושתן מדי פעם עם גוון דם. בחשד לדלקת בדרכי השתן (UTI), הרופא מבקש דגימת שתן ושולח אותה למעבדה לצורך בדיקת שתן. מאז זה ייקח בערך 24 שעות כדי לקבל את התוצאות של התרבות, הרופא מיד מתחיל אניטה על אנטיביוטיקה ciprofloxacin. למחרת, המעבדה למיקרוביולוגיה מאשרת את נוכחותו של E. coli בשתן של אניטה, אשר עולה בקנה אחד עם האבחנה המשוערת. עם זאת, בדיקת הרגישות לאנטי-מיקרוביאלית מצביעה על כך שציפרופלוקסצין לא יטפל ביעילות ב- UTI של אניטה, ולכן הרופא רושם אנטיביוטיקה אחרת.
לאחר נטילת האנטיביוטיקה שלה במשך שבוע, אניטה חוזרת למרפאה ומתלוננת כי המרשם אינו פועל. למרות שההשתנה הכואבת שככה, היא חווה כעת גירוד בנרתיק, צריבה ופריקה. לאחר בדיקה קצרה, הרופא מסביר לאניטה כי ככל הנראה האנטיביוטיקה הצליחה להרוג את ה- E. coli האחראי ל- UTI שלה; עם זאת, תוך כדי כך הם גם מחקו רבים מהחיידקים ה"טובים "במיקרוביוטה הרגילה של אניטה. התסמינים החדשים עליהם דיווחה אניטה תואמים זיהום שמרים משני על ידי קנדידה אלביקנס, פטרייה אופורטוניסטית השוכנת בדרך כלל בנרתיק אך מעוכבת על ידי החיידקים השוכנים בדרך כלל באותה סביבה.
כדי לאשר אבחנה זו, שקופית מיקרוסקופ של כתם נרתיקי ישיר מוכן מן הפרשות כדי לבדוק את נוכחותם של שמרים. מדגם של הפריקה מלווה שקופית זו למעבדה למיקרוביולוגיה כדי לקבוע אם חלה עלייה באוכלוסיית השמרים הגורמת לדלקת הנרתיק. לאחר שהמעבדה למיקרוביולוגיה מאשרת את האבחנה, הרופא רושם תרופה נגד פטריות לאניטה לשימוש בכדי לחסל את זיהום השמרים המשני שלה.
תרגיל \(\PageIndex{6}\)
- מדוע קנדידה לא נהרגה על ידי האנטיביוטיקה שנקבעה ל- UTI?
- ציין שלושה מצבים שעלולים להוביל לזיהום משני.
העברת מחלות
כדי שפתוגן יימשך, עליו לשים את עצמו במצב שיועבר למארח חדש, ולהשאיר את המארח הנגוע דרך פורטל יציאה (איור\(\PageIndex{6}\)). כמו בפורטלי כניסה, פתוגנים רבים מותאמים לשימוש בפורטל יציאה מסוים. בדומה לפורטלים של כניסה, הפורטלים הנפוצים ביותר של היציאה כוללים את העור ואת דרכי הנשימה, האורגניטל ומערכת העיכול. שיעול והתעטשות יכולים לגרש פתוגנים מדרכי הנשימה. עיטוש בודד יכול לשלוח אלפי חלקיקי וירוס לאוויר. הפרשות והפרשות יכולות להעביר פתוגנים מתוך פורטלי יציאה אחרים. צואה, שתן, זרע, הפרשות בנרתיק, קרעים, זיעה ותאי עור נשירים יכולים לשמש כלי עזר לפתוגן לעזוב את הגוף. פתוגנים המסתמכים על וקטורי חרקים להעברה יוצאים מהגוף בדם המופק על ידי חרק נושך. באופן דומה, חלק מהפתוגנים יוצאים מהגוף בדם המופק על ידי מחטים.
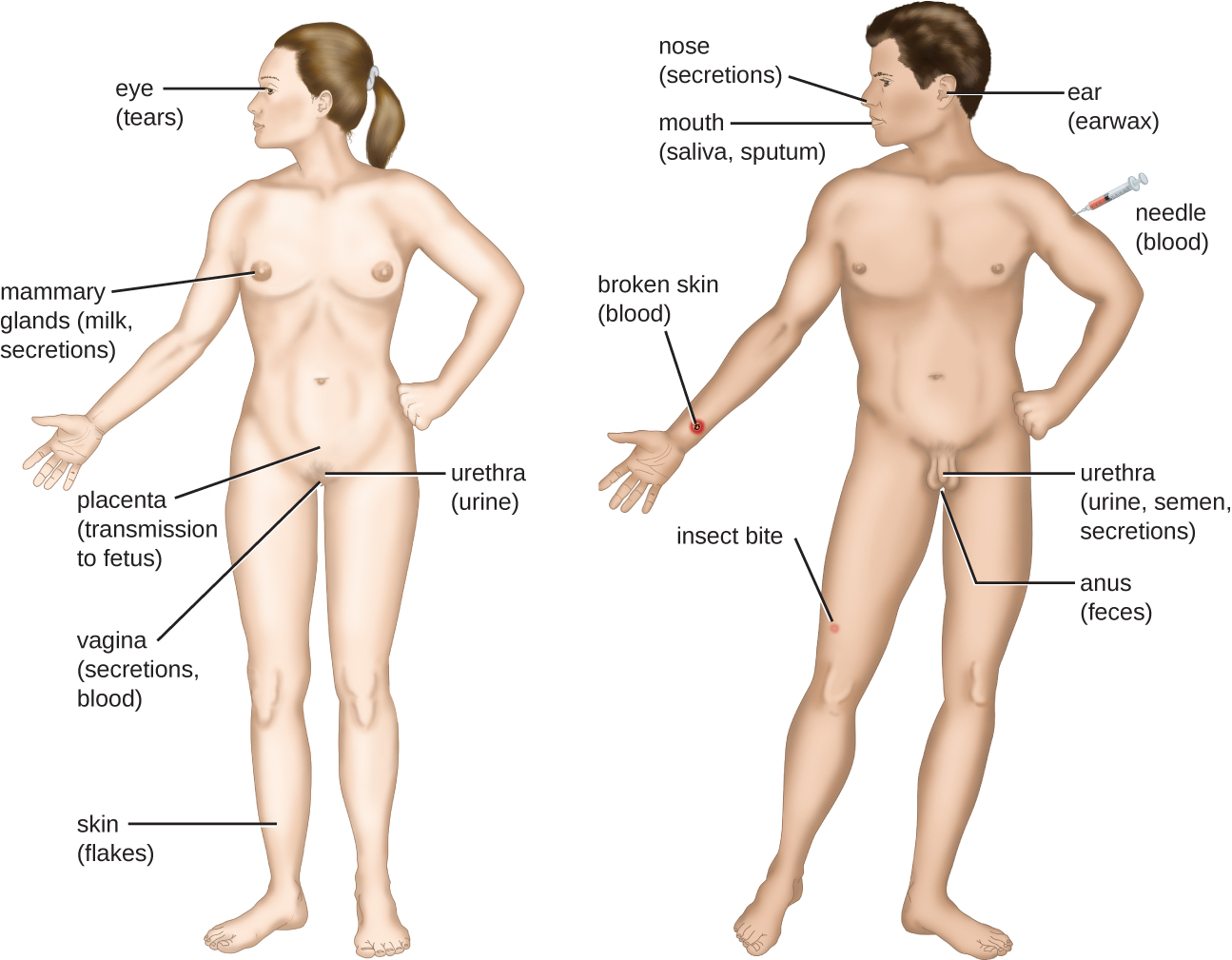
מושגי מפתח וסיכום
- ההנחות של קוך משמשות כדי לקבוע אם מיקרואורגניזם מסוים הוא פתוגן. ההנחות המולקולריות של קוך משמשות כדי לקבוע אילו גנים תורמים ליכולתו של הפתוגן לגרום למחלות.
- ניתן לכמת ארסיות, המידה שבה פתוגן יכול לגרום למחלה, על ידי חישוב מזהה 50 או LD 50 של פתוגן באוכלוסייה נתונה.
- פתוגנים ראשוניים מסוגלים לגרום לשינויים פתולוגיים הקשורים למחלה אצל אדם בריא, בעוד שפתוגנים אופורטוניסטיים יכולים לגרום למחלות רק כאשר האדם נפגע מהפסקה במחסומי הגנה או דיכוי חיסוני.
- זיהומים ומחלות יכולים להיגרם על ידי פתוגנים בסביבה או חיידקים במיקרוביוטה התושבת של הפרט.
- ניתן לסווג זיהומים כמקומיים, מוקדים או מערכתיים בהתאם למידת התפשטות הפתוגן בגוף.
- זיהום משני יכול להתרחש לעיתים לאחר שההגנה של המארח או המיקרוביוטה הרגילה נפגעות על ידי זיהום ראשוני או טיפול אנטיביוטי.
- פתוגנים נכנסים לגוף דרך פורטלי כניסה ויוצאים דרך פורטלי יציאה. שלבי הפתוגנזה כוללים חשיפה, הידבקות, פלישה, זיהום והעברה.
הערות שוליים
- 1 מינהל המזון והתרופות. "ספר באגים רעים, מיקרואורגניזמים פתוגניים הנישאים במזון ורעלים טבעיים." מהדורה שנייה. סילבר ספרינג, MD: מינהל המזון והתרופות האמריקני; 2012.
- 2 מ 'אוטו. "סטפילוקוקוס אפידרמידיס - הפתוגן ה'מקריי'." סקירות טבע מיקרוביולוגיה 7 מס '8 (2009) :555—567.
- 3 ה- O ב- TORCH מייצג "אחר".
- 4 ד 'דייויס. "הבנת עמידות ביופילם לחומרים אנטיבקטריאליים." סקירות טבע גילוי סמים 2 (2003): 114—122.


