10.4: נזכר
- Page ID
- 208222
ריקול - תרופות, תרופות ביולוגיות, מכשירים ומזון
ריקול הוא הסרה מרצון של מוצר על ידי יצרן או לבקשת ה- FDA. זיכרונות הם כמעט תמיד בהתנדבות. ה- FDA יכול להנפיק ריקול רק כאשר יש להם את הכוח המנדט לעשות זאת. ה- FDA אינו יכול להיזכר בתרופה, או ביולוגית, אך יכול להיזכר במכשיר רפואי, כמה קוסמטיקה ומזון. כאשר יש להם סמכות זיכרון, הם יכולים לעשות זאת רק כאשר קיים סיכון משמעותי לבריאות הציבור ובטיחות. https://www.fda.gov/consumers/consumer-updates/fda-101-product-recalls
משאבי זיכרון: https://www.fda.gov/safety/recalls-m...call-resources
אוכל
ה- FDA יכול להנפיק החזרת מזון. בשנת 2011, ה- FDA קיבל סמכות מוגברת בוויסות ותגובה לזיהום מוצרי מזון באמצעות החוק החדש למודרניזציה לבטיחות מזון (FSMA). ה- FSMA מאפשר ל- FDA להשעות את השירותים והייצור של מפיצי מזון אם יש חשד לזיהום. לא צריכה להיות שום הוכחה למקור הזיהום. לקבלת מידע נוסף על FSMA: http://www.foodsafety.gov/news/fsma.html
מכשור רפואי
ה- FDA יכול להנפיק החזרת מכשיר. בשנת 2012 הודיע מינהל המזון והתרופות האמריקני (FDA) כי הוא מבקש ליישם סמכות להחזרת מכשירים רפואיים לפי סעיף 518 (ה) לחוק FD & ampC ופרק 21, סעיף 810 של CFR. רשות הזכירה למכשירים רפואיים תאפשר ל- FDA להורות ליצרנים להפסיק את הפצת המכשיר ולהודיע לאנשי מקצוע בתחום הבריאות אם ה- FDA ימצא סבירות סבירה שהמכשיר יגרום לתגובות בריאותיות שליליות חמורות או למוות (fda.gov). ריקול לא אומר בהכרח שיש להחזיר את המוצר, לפעמים רק צריך להתאים אותו, או לספק הוראות בטיחות הבהרה. 21 CFR 7 מספק הנחיות לביצוע ריקול מרצון יעיל.
דוגמאות לסוגי הפעולות שעשויות להיחשב כזכור מכשיר:
- בדיקת המכשיר עבור בעיות
- תיקון המכשיר
- התאמת הגדרות במכשיר
- תיוג מחדש של המכשיר
- מכשיר השמדת
- הודעה למטופלים על בעיה
- מעקב אחר מטופלים לבעיות בריאות
החזרת מכשיר רפואי היא תיקון או הסרה. תיקון מטפל בבעיה במכשיר רפואי במקום בו הוא נמכר. הסרה מתקרבת לבעיה על ידי הסרת ההתקן מהמקום שבו הוא נמכר. ברוב המקרים, חברה נזכרת מרצון במכשיר בפני עצמה. כאשר החברה הפרה חוק ה- FDA, על החברה להחזיר את המכשיר (תיקון או הסרה) ולהודיע ל- FDA. מבחינה משפטית, ה- FDA יכול לדרוש מחברה להחזיר מכשיר אם ארגון מסרב לעשות זאת תחת 21 CFR 810, רשות החזרת מכשירים רפואיים. 21 CFR 810 מתאר את ההליכים שה- FDA נוקט בהפעלת סמכות החזרת המכשירים הרפואיים שלו לפי סעיף 518 (ה) לחוק FD & ampC.
ריקול אינו כולל משיכת שוק או התאוששות מניות. משיכת שוק היא הסרה או תיקון של חברה של מוצר מבוזר הכרוך בהפרה קלה שלא תהיה כפופה לפעולה משפטית על ידי ה- FDA או שאינה כרוכה בהפרה, למשל, נוהלי סיבוב מניות רגילים, התאמות ציוד שגרתיות ותיקונים (fda.gov). בסופו של דבר, כמעט כל הזיכרונות נערכים בהתנדבות על ידי היצרן. https://www.fda.gov/safety/recalls-market-withdrawals-safety-alerts
חקור!
מאגר זיכרון מכשור רפואי מקיף וניתן לחיפוש: www.accessdata.fda.gov/סקריפטים/CDRH/CFDocs/CFres/Res.cfFM
למידע נוסף על החזרות מכשירים, בקר בדף האינטרנט של זיכרון מכשיר ה- FDA https://www.fda.gov/medicaldevices/safety/listofrecalls/ וגם צפה בסרטון ה- FDA כאן. http://fda.yorkcast.com/webcast/Play/1b95461f64be40ecbe3415195cb394911d
המכשיר נזכר בעקבות אותו הליך זיכרון כללי, כפי שנדון בעבר עבור תרופות. זה כולל סיווג של זיכרון (I, II או III) פיתוח אסטרטגיית זיכרון ומתן ל- FDA דוחות מצב זיכרון.
התראת בטיחות מכשור רפואי: מונפקת במצבים בהם מכשיר רפואי עלול להוות סיכון בלתי סביר לפגיעה משמעותית. במקרים מסוימים, מצבים אלה נחשבים גם כזיכרונות (fda.gov)
נסיגת שוק מתרחשת כאשר למוצר יש הפרה קלה שלא תהיה כפופה לפעולה משפטית של ה- FDA. המשרד מסיר את המוצר מהשוק או מתקן את ההפרה. לדוגמה, מוצר שהוצא מהשוק עקב חבלה, ללא עדות לבעיות ייצור או הפצה יהיה נסיגה בשוק. (fda.gov)
בטיחות וזמינות תרופות
ה- FDA מציע אתרים רבים המתייחסים ספציפית לבטיחות התרופה ולזמינות לתקשורת עם הלקוחות. הנה כמה שאולי תרצה לחקור. https://www.fda.gov/drugs/drug-safety-and-availability
- תקשורת בטיחות סמים: https://www.fda.gov/drugs/drug-safety-and-availability/drug-safety-communications
- בטיחות תרופות לאחר השוק: https://www.fda.gov/drugs/drug-safety-and-availability/postmarket-drug-safety-information-patients-and-providers
- מה חדש — סמים אנושיים: https://www.fda.gov/drugs/news-events-human-drugs
- דיווח על אירועים שליליים: https://www.fda.gov/drugs/surveillance/questions-and-answers-fdas-adverse-event-reporting-system-faers
היזכרות בסמים
החזרת סמים היא פעולה מרצון שננקטה על ידי חברה. www.fda.gov/drugs/תזכורות תרופות/fdas-roledrug-recalls. לא כל הזיכרונות מוכרזים ב- FDA.gov או בתקשורת החדשות. הודעה ציבורית מונפקת בדרך כלל כאשר נזכר מוצר שהופץ באופן נרחב או מהווה סכנה בריאותית חמורה. עם זאת, אם חברה לא תוציא הודעה פומבית על ריקול, ה- FDA עשוי לעשות זאת אם הסוכנות תקבע כי יש צורך להגן על חולים. ה- FDA מעריך את יעילות הריקול על ידי הערכת מאמצי החברה להודיע ללקוחות כראוי ולהסיר את המוצר הפגום מהשוק. אם ייקבע כי ריקול אינו יעיל ה- FDA יבקש מהחברה לנקוט בפעולות נוספות.
דוחות אכיפה: https://www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/enforcement-reports
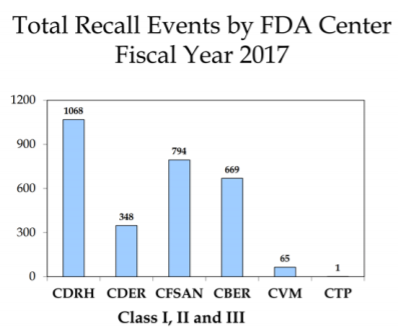
זיכרונות בכיתה I, II ו- III
- סוג I זוכר: "סבירות סבירה שהשימוש במוצר מפר או חשיפה אליו יגרום לתוצאות בריאותיות שליליות חמורות או למוות." (fda.gov)
- נזכיר Class II: "שימוש במוצר מפר או חשיפה אליו עלול לגרום לתוצאות בריאותיות שליליות זמניות או הפיכות מבחינה רפואית או כאשר ההסתברות לתוצאות בריאותיות שליליות חמורות היא רחוקה". (fda.gov)
- נזכיר Class III: "שימוש במוצר מפר או חשיפה אליו אינו צפוי לגרום לתוצאות בריאותיות שליליות." (fda.gov)
בחן את הידע שלך!
קרא את המאמר וצפה בסרטון "FDA 101: החזרת מוצרים - מההתראה הראשונה ועד בדיקות יעילות" וקרא שאלות נפוצות על ה- FDA:
- כיצד ה- FDA לומד לראשונה על בעיה במוצר?
- כיצד מתריע ה- FDA למוצר על החזרת מוצר?
- דון בדוגמה של זיכרון, וציין באיזה סוג זיכרון מדובר ומדוע.
חקור!
פודקאסט בטיחות התרופות של ה- FDA מיוצרים על ידי ה- CDER של ה- FDA ומספקים מידע בטיחותי מתפתח על תרופות בשילוב עם פרסום יועצים לבריאות הציבור ובעיות אחרות בנושא בטיחות תרופות. (fda.gov).


