20.1: יישומים מעשיים של נוגדנים חד שבטיים ופוליקלוניים
- Page ID
- 209063
מטרות למידה
- השווה את שיטת הפיתוח, השימוש והמאפיינים של נוגדנים חד שבטיים ופוליקלוניים
- הסבר את אופי התגובה הצולבת של נוגדנים ומדוע זו פחות בעיה בנוגדנים חד שבטיים
מיקוד קליני: חלק 1
באירוע מצער, עובד בריאות שנאבק בהתמכרות נתפס גונב מזרקים של משככי כאבים ומחליף אותם במזרקים מלאים בחומרים לא ידועים. בית החולים פיטר מיד את העובד ועצר אותו; עם זאת, שני חולים שעבד איתם נבדקו מאוחר יותר חיוביים ל- HIV.
אמנם לא הייתה הוכחה לכך שהזיהומים מקורם במזרקים הנגועים, אך רופא בריאות הציבור של בית החולים נקט בצעדים מיידיים כדי לקבוע אם חולים אחרים היו בסיכון. למרות שהעובד הועסק רק לזמן קצר, נקבע כי בא במגע עם יותר מ 1300 חולים. בית החולים החליט ליצור קשר עם כל החולים הללו ולבדוק אותם ל- HIV.
תרגיל \(\PageIndex{1}\)
- מדוע בית החולים מרגיש שיש צורך לבדוק כל חולה ל- HIV?
- באילו סוגי בדיקות ניתן להשתמש כדי לקבוע אם לחולה יש HIV?
בנוסף להיותם חיוניים לתגובה החיסונית הרגילה שלנו, נוגדנים מספקים כלים רבי עוצמה למטרות מחקר ואבחון. הספציפיות הגבוהה של נוגדנים הופכת אותם לכלי מצוין לאיתור וכימות מגוון רחב של מטרות, מתרופות ועד חלבונים בסרום ועד מיקרואורגניזמים. בעזרת מבחני חוץ גופית, ניתן להשתמש בנוגדנים כדי לזרז אנטיגנים מסיסים, לצבור תאים (גושים), להתיז ולהרוג חיידקים בעזרת משלים ולנטרל תרופות, רעלים ווירוסים.
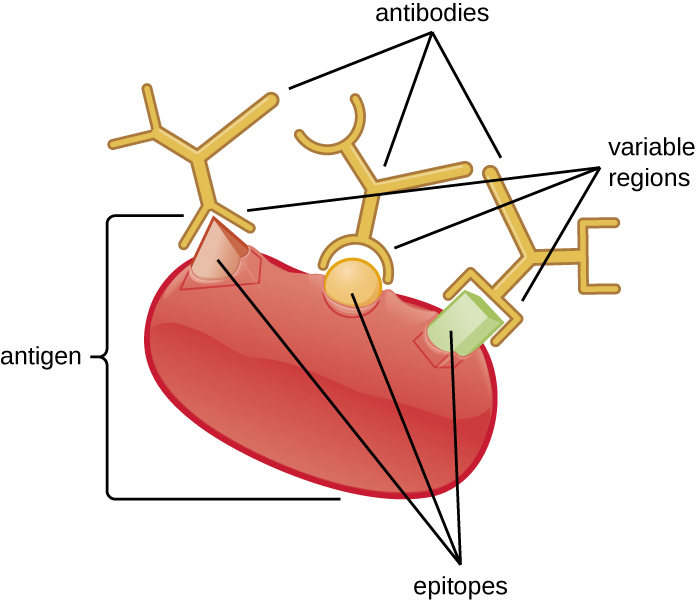
הספציפיות של נוגדן נובעת מאתר קשירת האנטיגן שנוצר בתוך האזורים המשתנים-אזורים של הנוגדן שיש להם דפוסים ייחודיים של חומצות אמינו שיכולות להיקשר רק לאנטיגנים מטרה עם רצף מולקולרי המספק מטענים משלימים וקשרים לא קוולנטיים. עם זאת, ישנן מגבלות לספציפיות הנוגדנים. חלק מהאנטיגנים דומים כל כך כימית עד שמתרחשת תגובתיות צולבת; במילים אחרות, נוגדנים המועלים כנגד אנטיגן אחד נקשרים לאנטיגן דומה מבחינה כימית אך שונה. שקול אנטיגן המורכב מחלבון בודד עם אפיטופים מרובים (איור). \(\PageIndex{1}\) חלבון בודד זה עשוי לעורר ייצור של נוגדנים רבים ושונים, שחלקם עשויים להיקשר לאפיטופים זהים מבחינה כימית על חלבונים אחרים.
סביר יותר שתתרחש תגובתיות צולבת בין נוגדנים לאנטיגנים בעלי זיקה או נטייה נמוכה. זיקה, שניתן לקבוע בניסוי, היא מדד לחוזק הקישור בין אתר הקישור של נוגדן לאפיטופ, ואילו נחישות היא החוזק הכולל של כל האינטראקציות בקומפלקס נוגדן-אנטיגן (שעשוי להיות לו יותר מאתר קשר אחד). ההתלהבות מושפעת מהזיקה כמו גם מהסידורים המבניים של האפיטופ והאזורים המשתנים של הנוגדן. אם לנוגדן יש זיקה/נחישות גבוהה לאנטיגן ספציפי, יש פחות סיכוי שהוא יגיב צולב עם אנטיגן שיש לו זיקה/נטייה נמוכה יותר.
תרגיל \(\PageIndex{2}\)
- איזה מאפיין הופך נוגדנים לשימושיים למחקר ולאבחון קליני?
- מהי תגובתיות צולבת ומדוע היא מתרחשת?
ייצור נוגדנים פוליקלוניים
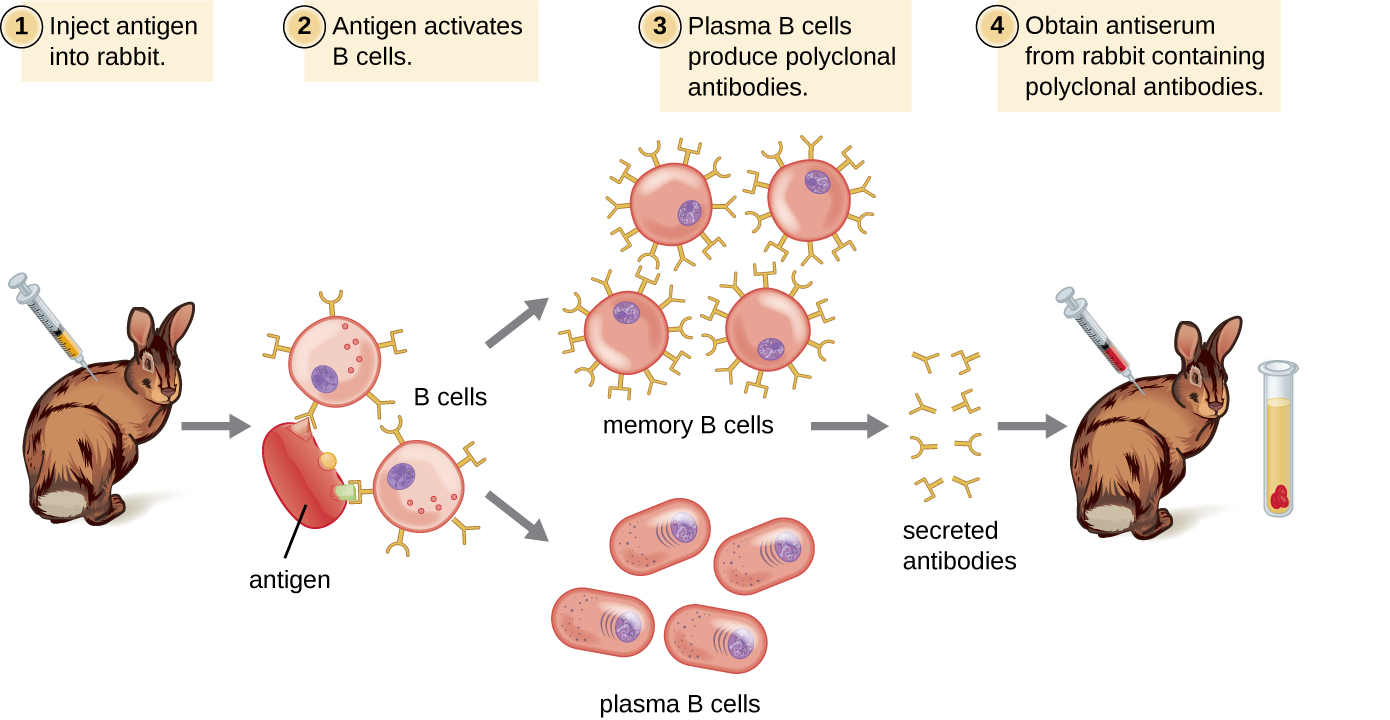
נוגדנים המשמשים למטרות מחקר ואבחון מתקבלים לרוב על ידי הזרקת חיית מעבדה כמו ארנב או עז עם אנטיגן ספציפי. תוך מספר שבועות, המערכת החיסונית של החיה תייצר רמות גבוהות של נוגדנים ספציפיים לאנטיגן. ניתן לקצור נוגדנים אלה באנטי-סרום, שהוא סרום שלם שנאסף מבעל חיים בעקבות חשיפה לאנטיגן. מכיוון שרוב האנטיגנים הם מבנים מורכבים עם אפיטופים מרובים, הם גורמים לייצור נוגדנים מרובים בחיית המעבדה. תגובה זו כביכול של נוגדנים פוליקלוניים אופיינית גם לתגובה לזיהום על ידי מערכת החיסון האנושית. אנטי-סרום שנשאב מבעל חיים יכיל אפוא נוגדנים ממספר שיבוטים של תאי B, כאשר כל תא B יגיב לאפיטופ ספציפי על האנטיגן (איור). \(\PageIndex{2}\)
חיות מעבדה מוזרקות בדרך כלל לפחות פעמיים עם אנטיגן כאשר משתמשים בהן לייצור אנטי-סרום. הזריקה השנייה תפעיל תאי זיכרון היוצרים נוגדנים מסוג IgG כנגד האנטיגן. תאי הזיכרון עוברים גם התבגרות זיקה, וכתוצאה מכך מאגר נוגדנים בעלי זיקה ממוצעת גבוהה יותר. התבגרות זיקה מתרחשת בגלל מוטציות באזורים המשתנים של הגן האימונוגלובולין, וכתוצאה מכך תאי B עם אתרי קשירת אנטיגן שהשתנו מעט. בחשיפה חוזרת לאנטיגן, אותם תאי B המסוגלים לייצר נוגדנים בעלי אתרי קשירת אנטיגן בעלי זיקה גבוהה יותר יעוררו להתרבות ולייצר יותר נוגדנים מאשר עמיתיהם בעלי זיקה נמוכה יותר. אדג'ובנט, שהוא חומר כימי המעורר הפעלה כללית של מערכת החיסון המגרה ייצור נוגדנים גדול יותר, מעורבב לעתים קרובות עם האנטיגן לפני ההזרקה.
אנטי-סרום המתקבל מבעלי חיים לא יכיל רק נוגדנים כנגד האנטיגן שהוכנס באופן מלאכותי במעבדה, אלא הוא יכיל גם נוגדנים לכל אנטיגנים אחרים אליהם נחשפה החיה במהלך חייה. מסיבה זו, תחילה יש "לטהר" אנטיסרה כדי להסיר נוגדנים אחרים לפני השימוש בנוגדנים למחקר או מבחני אבחון.
שימושים קליניים באנטיסרה פוליקלונלית
אנטיסרה פוליקלונלית משמשת בבדיקות קליניות רבות שנועדו לקבוע אם מטופל מייצר נוגדנים בתגובה לפתוגן מסוים. למרות שבדיקות אלה הן בהחלט כלי אבחון רבי עוצמה, יש להן מגבלות, מכיוון שהן אמצעי עקיף לקבוע אם קיים פתוגן מסוים. בדיקות המבוססות על תגובה פוליקלונלית יכולות לפעמים להוביל לתוצאה חיובית כוזבת - במילים אחרות, בדיקה המאשרת את נוכחותו של אנטיגן שלמעשה אינו קיים. בדיקות מבוססות נוגדנים יכולות גם לגרום לתוצאה שלילית כוזבת, המתרחשת כאשר הבדיקה לא מצליחה לזהות נוגדן שנמצא למעשה.
ניתן לתאר את הדיוק של בדיקות נוגדנים במונחים של רגישות לבדיקה וספציפיות הבדיקה. רגישות הבדיקה היא ההסתברות לקבל תוצאת בדיקה חיובית כאשר המטופל אכן נגוע. אם לבדיקה יש רגישות גבוהה, ההסתברות לשלילה כוזבת נמוכה. סגוליות הבדיקה, לעומת זאת, היא ההסתברות לקבל תוצאת בדיקה שלילית כאשר המטופל אינו נגוע. אם לבדיקה יש ספציפיות גבוהה, ההסתברות לחיוב כוזב נמוכה.
תוצאות חיוביות שגויות מתרחשות לעתים קרובות עקב תגובתיות צולבת, שיכולה להתרחש כאשר אפיטופים מפתוגן אחר דומים לאלה שנמצאו על הפתוגן הנבדק. מסיבה זו, בדיקות מבוססות נוגדנים משמשות לרוב רק כבדיקות סקר; אם התוצאות חיוביות, משתמשים בבדיקות אישור אחרות כדי לוודא שהתוצאות לא היו חיוביות כוזבות.
לדוגמה, ניתן לבדוק את דגימת הדם של חולה החשוד כסובל מהפטיטיס C לנגיף באמצעות נוגדנים הנקשרים לאנטיגנים בנגיף הפטיטיס C. אם החולה אכן נגוע בנגיף הפטיטיס C, הנוגדנים ייקשרו לאנטיגנים, ויניבו תוצאת בדיקה חיובית. אם המטופל אינו נגוע בנגיף C הפטיטי, הנוגדנים בדרך כלל לא ייקשרו לשום דבר והבדיקה צריכה להיות שלילית; עם זאת, חיובי כוזב עלול להתרחש אם המטופל נדבק בעבר על ידי כל אחד ממגוון הפתוגנים המעוררים נוגדנים המגיבים צולבים עם אנטיגנים של נגיף הפטיטיס C. לבדיקות נוגדנים להפטיטיס C יש רגישות גבוהה (סבירות נמוכה לשלילה כוזבת) אך ספציפיות נמוכה (סבירות גבוהה לחיוב כוזב). לפיכך, חולים שנבדקים חיוביים חייבים לעבור בדיקת אישור שנייה כדי לשלול אפשרות לחיוב כוזב. בדיקת האישור היא בדיקה יקרה יותר וגוזלת זמן שבודקת ישירות לנוכחות RNA נגיפי הפטיטיס C בדם. רק לאחר שהבדיקה המאשרת חוזרת חיובית, ניתן לאבחן את המטופל באופן סופי עם זיהום בהפטיטיס C. בדיקות מבוססות נוגדנים עלולות לגרום לשלילה כוזבת אם, מסיבה כלשהי, המערכת החיסונית של המטופל לא ייצרה רמות ניתנות לזיהוי של נוגדנים. עבור מחלות מסוימות, ייתכן שיחלפו מספר שבועות לאחר ההדבקה עד שמערכת החיסון מייצרת מספיק נוגדנים כדי לחצות את סף הזיהוי של הבדיקה. בחולים עם פגיעה בחיסון, ייתכן שמערכת החיסון אינה מסוגלת לייצר רמה ניתנת לזיהוי של נוגדנים.
מגבלה נוספת של שימוש בייצור נוגדנים כאינדיקטור למחלה היא שנוגדנים בדם יימשכו זמן רב לאחר ניקוי הזיהום. בהתאם לסוג הזיהום, נוגדנים יהיו נוכחים במשך חודשים רבים; לפעמים, הם עשויים להיות נוכחים למשך שארית חייו של המטופל. לפיכך, בדיקה חיובית המבוססת על נוגדנים פירושה רק שהמטופל נדבק בנקודת זמן מסוימת; זה לא מוכיח שהזיהום פעיל.
בנוסף לתפקידם באבחון, אנטיסרה פוליקלונלית יכולה להפעיל משלים, לזהות נוכחות של חיידקים במסגרות קליניות ותעשיית המזון, ולבצע מגוון רחב של תגובות משקעים שיכולות לזהות ולכמת חלבונים בסרום, וירוסים או אנטיגנים אחרים. עם זאת, עם הספציפיות הרבות של נוגדנים הקיימים באנטי-סרום פוליקלונלי, קיימת סבירות משמעותית שהאנטי -סרום יגיב צולב עם אנטיגנים שאליהם הפרט מעולם לא נחשף. לכן, עלינו תמיד להסביר את האפשרות של תוצאות חיוביות כוזבות בעת עבודה עם antiserum polyclonal.
תרגיל \(\PageIndex{3}\)
- מהו חיובי כוזב ומהן כמה סיבות לכך שמתרחשות חיוביות שגויות?
- מהו שלילי כוזב ומהן כמה סיבות לכך שמתרחשות חיוביות שגויות?
- אם מטופל בודק שלילי בבדיקה רגישה ביותר, מה הסבירות שהאדם נגוע בפתוגן?
ייצור נוגדנים חד שבטיים
סוגים מסוימים של מבחנים דורשים ספציפיות וזיקה טובה יותר של נוגדנים ממה שניתן להשיג באמצעות אנטי-סרום פוליקלוני. כדי להשיג ספציפיות גבוהה זו, כל הנוגדנים חייבים להיקשר בזיקה גבוהה לאפיטופ יחיד. ספציפיות גבוהה זו יכולה להינתן על ידי נוגדנים חד שבטיים (mAbs). הטבלה \(\PageIndex{1}\) משווה כמה מהמאפיינים החשובים של נוגדנים חד שבטיים ופוליקלוניים.
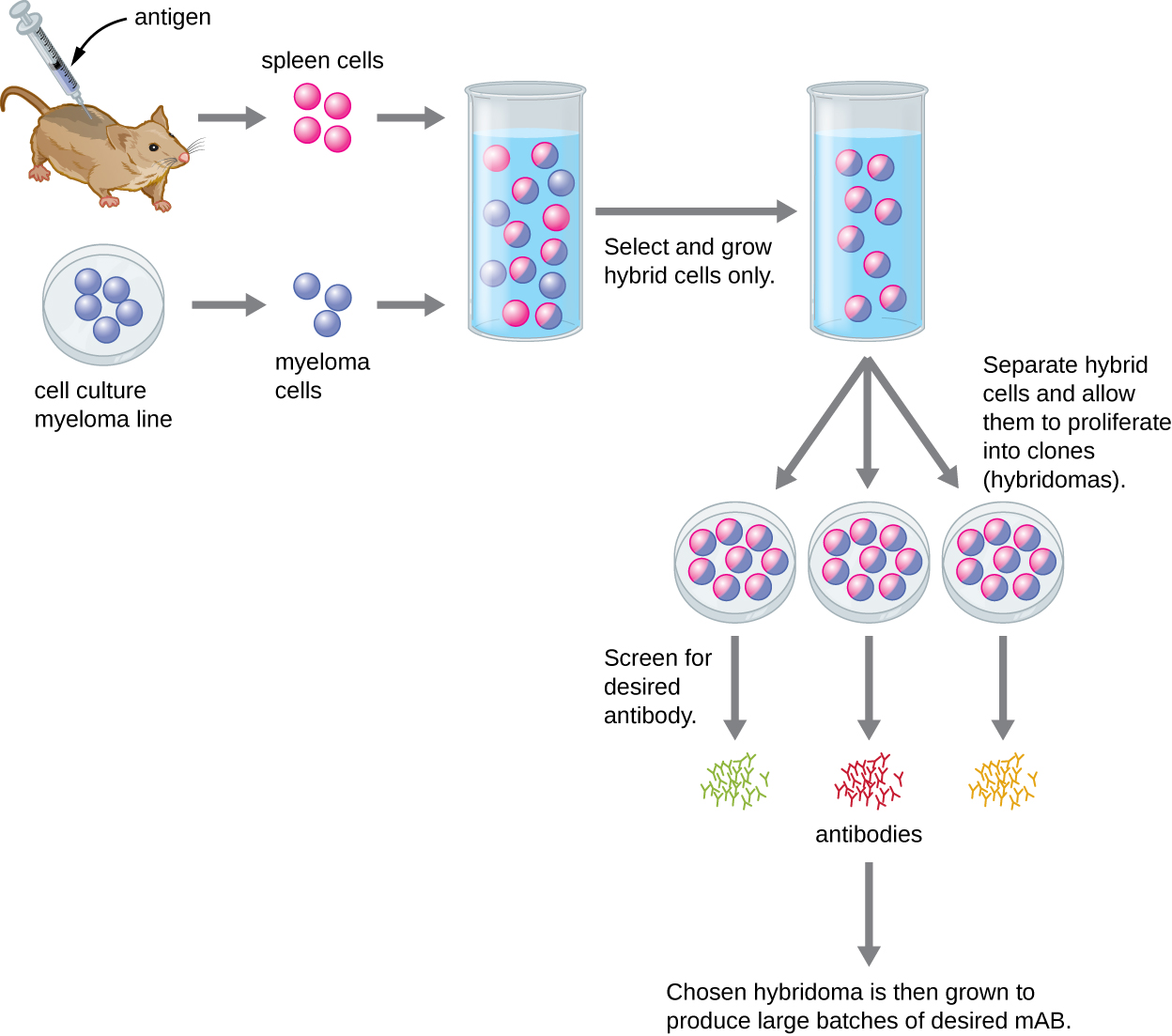
בניגוד לנוגדנים פוליקלוניים, המיוצרים בבעלי חיים חיים, נוגדנים חד שבטיים מיוצרים בַּמַבחֵנָה באמצעות טכניקות תרבית רקמות. mAbs מיוצרים על ידי חיסון בעל חיים, לרוב עכבר, מספר פעמים עם אנטיגן ספציפי. תאי B מהטחול של החיה המחוסנת מוסרים לאחר מכן. מכיוון שתאי B נורמליים אינם מסוגלים להתרבות לנצח, הם מתמזגים עם תאי B סרטניים אלמותיים הנקראים תאי מיאלומה, כדי להניב תאי היברידומה. לאחר מכן כל התאים ממוקמים במדיום סלקטיבי המאפשר רק להיברידומות לצמוח; תאי מיאלומה לא התמזגו אינם יכולים לצמוח, וכל תאי B שאינם מתמזגים מתים. ההיברידומות, המסוגלות לגדול ברציפות בתרבית תוך ייצור נוגדנים, נבדקות לאחר מכן לאיתור ה-mAb הרצוי. אלה המייצרים את ה-mAb הרצוי גדלים בתרבית רקמות; מדיום התרבות נקטף מעת לעת ו-mAbs מטוהרים מהמדיום. זהו תהליך יקר מאוד זמן רב. זה עשוי לקחת שבועות של טיפוח וליטרים רבים של מדיה כדי לספק מספיק mAbs לניסוי או לטיפול בחולה יחיד. mAbs יקרים (איור). \(\PageIndex{3}\)
| נוגדנים חד שבטיים | נוגדנים פוליקלוניים |
|---|---|
| ייצור יקר | ייצור זול |
| זמן ייצור ארוך | ייצור מהיר |
| כמויות גדולות של נוגדנים ספציפיים | כמויות גדולות של נוגדנים לא ספציפיים |
| זיהוי אפיטופ בודד על אנטיגן | זיהוי אפיטופים מרובים על אנטיגן |
| הייצור הוא רציף ואחיד ברגע שההיברידומה נעשית | קבוצות שונות משתנות בהרכב |
שימושים קליניים בנוגדנים חד שבטיים
מכיוון שהשיטות הנפוצות ביותר לייצור נוגדנים חד שבטיים משתמשות בתאי עכבר, יש צורך ליצור נוגדנים חד שבטיים אנושיים לשימוש קליני אנושי. לא ניתן להזריק שוב ושוב נוגדנים לעכברים לבני אדם, מכיוון שמערכת החיסון תזהה אותם כזרים ותגיב אליהם בנוגדנים מנטרלים. ניתן למזער בעיה זו על ידי הנדסה גנטית של הנוגדן בתא B העכבר. האזורים המשתנים של הגנים הקלים והשרשרת הכבדה של העכבר נקשרים לאזורים קבועים אנושיים, ולאחר מכן הגן הכימרי מועבר לתא מארח. זה מאפשר ייצור של mAb שהוא בעיקר "אנושי" כאשר רק האתר המחייב אנטיגן הוא ממוצא עכבר.
mAbs הומניזציה שימשו בהצלחה לטיפול בסרטן עם תופעות לוואי מינימליות. לדוגמה, תרופת הנוגדנים החד שבטיים ההומנית Herceptin הועילה לטיפול בסוגים מסוימים של סרטן השד. היו גם כמה ניסויים ראשוניים של mAb אנושי לטיפול במחלות זיהומיות, אך אף אחד מהטיפולים הללו אינו בשימוש כעת. במקרים מסוימים, mAbs הוכיחו שהם ספציפיים מדי לטיפול במחלות זיהומיות, מכיוון שהם מזהים כמה סרוברים של פתוגן אך לא אחרים. שימוש בקוקטייל של mAbs מרובים המכוונים לזנים שונים של הפתוגן יכול לטפל בבעיה זו. עם זאת, העלות הגדולה הכרוכה בייצור mAb היא אתגר נוסף שמנע מ-mAbs להפוך למעשי לשימוש בטיפול בזיהומים מיקרוביאליים. 1
טכנולוגיה מבטיחה אחת עבור mAbs זולים היא השימוש בצמחים מהונדסים גנטית לייצור נוגדנים (או plantibodies). טכנולוגיה זו הופכת תאי צמחים למפעלי נוגדנים במקום להסתמך על תאי תרבית רקמות, שהם יקרים ותובעניים מבחינה טכנית. במקרים מסוימים, ייתכן אפילו שניתן יהיה לספק נוגדנים אלה על ידי כך שהמטופלים יאכלו את הצמחים ולא על ידי חילוץ והזרקת הנוגדנים. לדוגמה, בשנת 2013, קבוצת מחקר שיבטה גנים של נוגדנים לצמחים שהיו בעלי יכולת לנטרל רעלן חשוב מחיידקים העלולים לגרום למחלות קשות במערכת העיכול. 2 אכילת הצמחים עלולה להעביר את הנוגדנים ישירות לרעלן.
תרגיל \(\PageIndex{4}\)
- כיצד נוצרים נוגדנים חד שבטיים הומניים?
- מה המשמעות של "חד שבטי" של נוגדנים חד שבטיים?
שימוש בנוגדנים חד שבטיים למאבק באבולה
במהלך התפרצות האבולה 2014—2015 במערב אפריקה, כמה חולים נגועים באבולה טופלו ב-ZMapp, תרופה שהוכחה כיעילה בניסויים שנעשו במקקי רזוס רק כמה חודשים לפני כן. 3 ZMapp הוא שילוב של שלושה mAbs המיוצרים על ידי שילוב גני הנוגדנים בצמחי טבק באמצעות וקטור ויראלי. על ידי שימוש בשלושה mAbs, התרופה יעילה על פני זנים מרובים של הנגיף. למרבה הצער, היה מספיק ZMapp לטיפול במספר זעיר של חולים.
בעוד שהטכנולוגיה הנוכחית אינה מספקת לייצור כמויות גדולות של ZMapp, היא אכן מראה שגופי צמחים - MABs המיוצרים על ידי צמחים - אפשריים לשימוש קליני, שעלולים להיות חסכוניים ושווה פיתוח נוסף. בשנים האחרונות נרשמה התפוצצות במספר התרופות החדשות המבוססות על MAB לטיפול בסרטן ומחלות זיהומיות; עם זאת, השימוש הנרחב בתרופות כאלה מעוכב כיום על ידי עלותן המופרזת, במיוחד באזורים לא מפותחים בעולם, שבהם מנה אחת עשויה לעלות יותר מההכנסה לכל החיים של המטופל. פיתוח שיטות לשיבוט גנים של נוגדנים לצמחים יכול להפחית עלויות באופן דרמטי.
מושגי מפתח וסיכום
- נוגדנים נקשרים בספציפיות גבוהה לאנטיגנים המשמשים לאתגר את המערכת החיסונית, אך הם עשויים גם להראות תגובתיות צולבת על ידי קישור לאנטיגנים אחרים החולקים תכונות כימיות עם האנטיגן המקורי.
- הזרקת אנטיגן לבעל חיים תגרום לתגובת נוגדנים פוליקלוניים בה נוצרים נוגדנים שונים המגיבים עם האפיטופים השונים על האנטיגן.
- אנטיסרה פוליקלונלית שימושית עבור סוגים מסוימים של מבחני מעבדה, אך מבחנים אחרים דורשים ספציפיות רבה יותר. בדיקות אבחון המשתמשות באנטיסרה פוליקלונלית משמשות בדרך כלל רק להקרנה בגלל האפשרות לתוצאות חיוביות שגויות ושליליות כוזבות.
- נוגדנים חד שבטיים מספקים ספציפיות גבוהה יותר מאשר אנטיסרה פוליקלונלית מכיוון שהם נקשרים לאפיטופ בודד ובדרך כלל יש להם זיקה גבוהה.
- נוגדנים חד שבטיים מיוצרים בדרך כלל על ידי גידול היברידומות המפרישות נוגדנים שמקורן בעכברים. mAbs משמשים כיום לטיפול בסרטן, אך עלותם המופרזת מנעה מהם שימוש נרחב יותר לטיפול במחלות זיהומיות. ובכל זאת, הפוטנציאל שלהם לשימוש מעבדתי וקליני מניע את הפיתוח של פתרונות חדשים וחסכוניים כגון plantibodies.
הערות שוליים
- 1 סיילור, קרולין, יקטרינה דדחובה וארטורו קסדוואל, "טיפולים מבוססי נוגדנים חד שבטיים למחלות מיקרוביאליות", חיסון 27 (2009): G38-G46.
- 2 נקנישי, קאטסוהירו ואח '., "ייצור של צמחים היברידיים IgG/IgA עם פעילות מנטרלת נגד רעלן שיגה 1", PLoS One 8, מס' 11 (2013): e80712.
- 3 Qiu, Xiangguo et al., "היפוך מחלת נגיף אבולה מתקדמת בפרימטים לא אנושיים עם ZMapp," טבע 514 (2014): 47—53.


