18.1: ארכיטקטורה של מערכת החיסון
- Page ID
- 208869
מטרות למידה
- הגדר זיכרון, תגובה ראשונית, תגובה משנית וספציפיות
- הבחנה בין חסינות הומוריסטית לסלולרית
- להבדיל בין אנטיגנים, אפיטופים והפטנס
- תאר את המבנה והתפקוד של נוגדנים והבחין בין מחלקות הנוגדנים השונות
מיקוד קליני: חלק 1
אוליביה, תינוקת בת שנה, מובאת לחדר המיון על ידי הוריה, המדווחים על הסימפטומים שלה: בכי מוגזם, עצבנות, רגישות לאור, עייפות יוצאת דופן והקאות. רופא מרגיש בלוטות לימפה נפוחות בגרונה ובבתי השחי של אוליביה. בנוסף, אזור הבטן מעל הטחול נפוח ורך.
תרגיל \(\PageIndex{1}\)
- מה הסימפטומים האלה מציעים?
- אילו בדיקות ניתן להזמין כדי לנסות לאבחן את הבעיה?
חסינות מסתגלת מוגדרת על ידי שני מאפיינים חשובים: ספציפיות וזיכרון. ספציפיות מתייחסת ליכולתה של מערכת החיסון ההסתגלותית למקד לפתוגנים ספציפיים, והזיכרון מתייחס ליכולתה להגיב במהירות לפתוגנים שאליהם נחשף בעבר. לדוגמה, כאשר אדם מתאושש מאבעבועות רוח, הגוף מפתח זיכרון של הזיהום שיגן עליו באופן ספציפי מפני הגורם הסיבתי, נגיף הווריצלה-זוסטר, אם הוא נחשף שוב לנגיף מאוחר יותר.
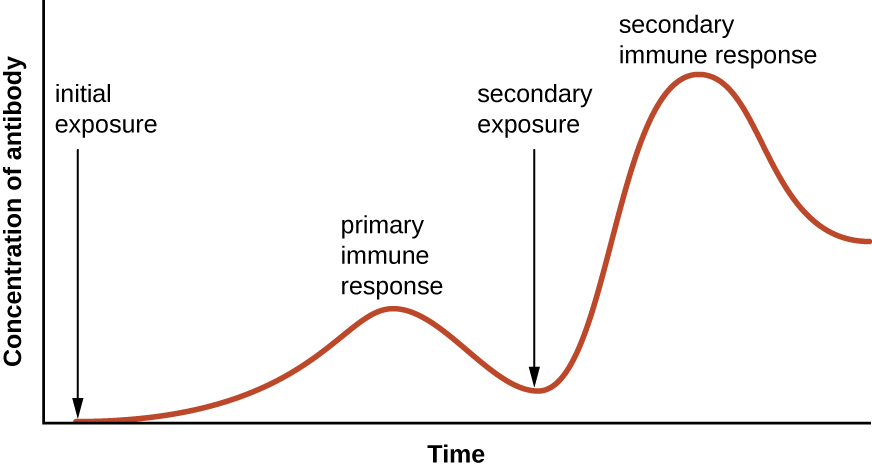
ספציפיות וזיכרון מושגים על ידי תכנות בעצם תאים מסוימים המעורבים בתגובה החיסונית להגיב במהירות לחשיפות הבאות של הפתוגן. תכנות זה מתרחש כתוצאה מהחשיפה הראשונה לפתוגן או לחיסון, מה שמעורר תגובה ראשונית. חשיפות עוקבות גורמות לתגובה משנית מהירה וחזקה יותר כתוצאה מזיכרון הגוף מהחשיפה הראשונה (איור\(\PageIndex{1}\)). תגובה משנית זו, לעומת זאת, היא ספציפית לפתוגן המדובר. לדוגמה, חשיפה לנגיף אחד (למשל, נגיף אבעבועות רוח) לא תספק הגנה מפני מחלות ויראליות אחרות (למשל, חצבת, חזרת או פוליו).
חסינות ספציפית מסתגלת כוללת פעולות של שני סוגי תאים נפרדים: לימפוציטים B (תאי B) ולימפוציטים T (תאי T). למרות שתאי B ותאי T נובעים ממסלול התמיינות נפוץ של תאי גזע המטופואטיים, אתרי ההתבגרות שלהם ותפקידיהם בחסינות הסתגלותית שונים מאוד.
תאי B מתבגרים במח העצם ואחראים לייצור גליקופרוטאינים הנקראים נוגדנים, או אימונוגלובולינים. נוגדנים מעורבים בהגנה של הגוף מפני פתוגנים ורעלים בסביבה החוץ תאית. מנגנונים של חסינות ספציפית אדפטיבית הכוללים תאי B וייצור נוגדנים מכונים חסינות הומורלית. ההתבגרות של תאי T מתרחשת בתימוס. תאי T מתפקדים כמתזמר המרכזי של תגובות חיסוניות מולדות ומסתגלות כאחד. הם אחראים גם להרס של תאים נגועים פתוגנים תאיים. המיקוד וההרס של פתוגנים תוך תאיים על ידי תאי T נקרא חסינות מתווכת תאים, או חסינות תאית.
תרגיל \(\PageIndex{2}\)
- רשום את שני המאפיינים המגדירים של חסינות אדפטיבית.
- הסבר את ההבדל בין תגובה חיסונית ראשונית ומשנית.
- במה שונות החסינות ההומורלית והסלולרית?
אנטיגנים
הפעלת ההגנה החיסונית האדפטיבית מופעלת על ידי מבנים מולקולריים ספציפיים לפתוגן הנקראים אנטיגנים. אנטיגנים דומים לדפוסים המולקולריים הקשורים לפתוגן (PAMPs) הנדונים בזיהוי פתוגנים ופגוציטוזיס; עם זאת, בעוד ש- PAMPs הם מבנים מולקולריים המצויים על פתוגנים רבים, אנטיגנים ייחודיים לפתוגן ספציפי. האנטיגנים המעוררים חסינות אדפטיבית לאבעבועות רוח, למשל, ייחודיים לנגיף הווריצלה-זוסטר אך שונים באופן משמעותי מהאנטיגנים הקשורים לפתוגנים ויראליים אחרים.
המונח אנטיגן שימש בתחילה לתיאור מולקולות המעוררות ייצור נוגדנים; למעשה, המונח בא משילוב של המילים אנטי גוף ו- gen erator, ומולקולה המגרה ייצור נוגדנים אמורה להיות אנטיגנית. עם זאת, תפקידם של אנטיגנים אינו מוגבל לחסינות הומורלית וייצור נוגדנים; לאנטיגנים יש גם תפקיד חיוני בגירוי חסינות התאית, ומסיבה זו מכונים לעיתים אנטיגנים בצורה מדויקת יותר אימונוגנים. עם זאת, בטקסט זה נתייחס אליהם בדרך כלל כאנטיגנים.
פתוגנים יש מגוון של מבנים שעשויים להכיל אנטיגנים. לדוגמה, אנטיגנים מתאי חיידקים עשויים להיות קשורים לכמוסות שלהם, לדפנות התא, לפימבריה, לפללה או לפילי. אנטיגנים חיידקיים עשויים להיות קשורים גם לרעלים חוץ-תאיים ולאנזימים שהם מפרישים. לנגיפים יש מגוון אנטיגנים הקשורים לקפסידים שלהם, למעטפות ולמבני הדוקרנים שהם משתמשים בהם לצורך התקשרות לתאים.
אנטיגנים עשויים להשתייך לכל מספר של מחלקות מולקולריות, כולל פחמימות, שומנים, חומצות גרעין, חלבונים ושילובים של מולקולות אלה. אנטיגנים ממעמדות שונים משתנים ביכולתם לעורר הגנות חיסוניות אדפטיביות וכן בסוג התגובה שהם מעוררים (הומוריסטית או תאית). המורכבות המבנית של מולקולה אנטיגנית היא גורם חשוב בפוטנציאל האנטיגני שלה. באופן כללי, מולקולות מורכבות יותר יעילות יותר כאנטיגנים. לדוגמה, המבנה המורכב התלת מימדי של החלבונים הופך אותם לאנטיגנים היעילים והחזקים ביותר, המסוגלים לעורר חסינות הומורלית ותאית כאחד. לשם השוואה, פחמימות מורכבות פחות במבנה ולכן פחות יעילות כאנטיגנים; הם יכולים רק לעורר הגנות חיסוניות הומורליות. ליפידים וחומצות גרעין הן המולקולות הפחות אנטיגניות, ובמקרים מסוימים עשויות להפוך לאנטיגניות רק בשילוב עם חלבונים או פחמימות ליצירת גליקוליפידים, ליפופרוטאינים או נוקלאופרוטאינים.
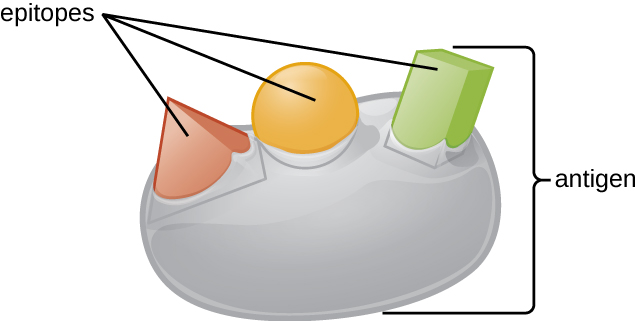
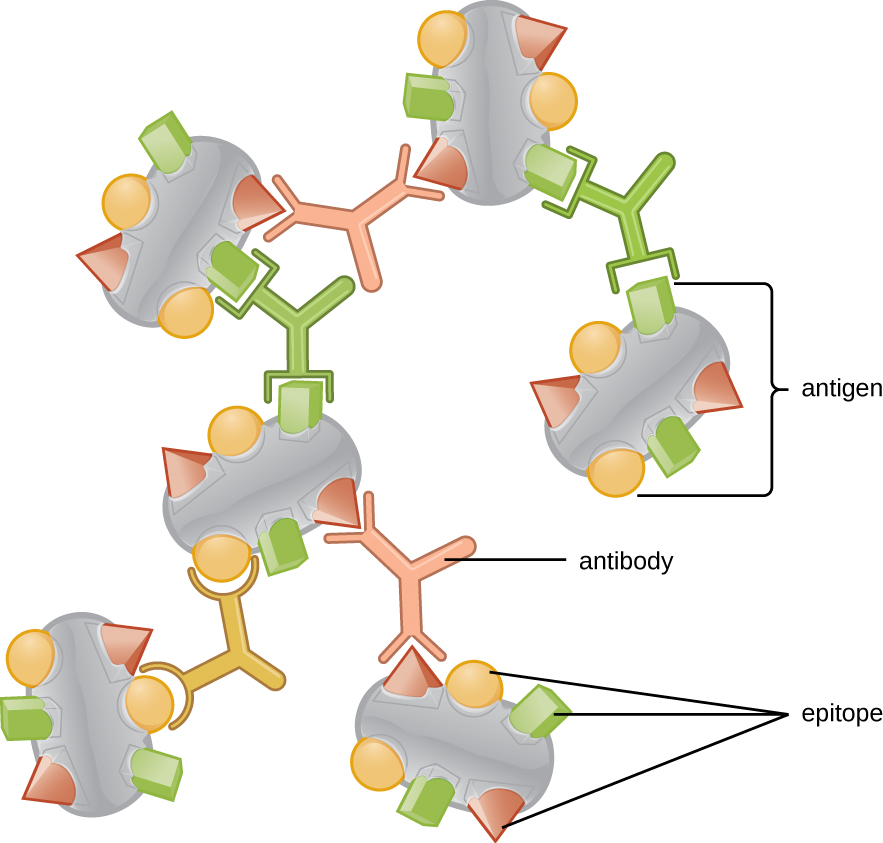
אחת הסיבות שהמורכבות התלת מימדית של אנטיגנים חשובה כל כך היא שנוגדנים ותאי T אינם מזהים ומקיימים אינטראקציה עם אנטיגן שלם אלא עם אזורים חשופים קטנים יותר על פני השטח של אנטיגנים הנקראים אפיטופים. לאנטיגן בודד עשויים להיות מספר אפיטופים שונים (איור\(\PageIndex{2}\)), ונוגדנים שונים עשויים להיקשר לאפיטופים שונים על אותו אנטיגן (איור). \(\PageIndex{3}\) לדוגמה, הדגל החיידקי הוא מבנה חלבון גדול ומורכב שיכול להכיל מאות ואף אלפי אפיטופים בעלי מבנים תלת מימדיים ייחודיים. יתר על כן, דגלים ממיני חיידקים שונים (או אפילו זנים מאותו מין) מכילים אפיטופים ייחודיים שיכולים להיות קשורים רק לנוגדנים ספציפיים.
גודלו של אנטיגן הוא גורם חשוב נוסף בפוטנציאל האנטיגני שלו. בעוד שלמבנים אנטיגניים גדולים כמו דגלים יש אפיטופים מרובים, חלק מהמולקולות קטנות מכדי להיות אנטיגניות מעצמן. מולקולות כאלה, הנקראות haptens, הן בעצם אפיטופים חופשיים שאינם חלק מהמבנה התלת מימדי המורכב של אנטיגן גדול יותר. כדי שהפטן יהפוך לאנטיגני, עליו להתחבר תחילה למולקולת נשא גדולה יותר (בדרך כלל חלבון) כדי לייצר אנטיגן מצומד. הנוגדנים הספציפיים להפטן המיוצרים בתגובה לאנטיגן המצומד מסוגלים לאחר מכן לקיים אינטראקציה עם מולקולות הפטן החופשיות הבלתי מצומדות. לא ידוע כי Haptens קשורים לפתוגנים ספציפיים כלשהם, אך הם אחראים לתגובות אלרגיות מסוימות. לדוגמא, האורושיול ההפטן, מולקולה שנמצאת בשמן של צמחים הגורמים לקיסוס רעיל, גורמת לתגובה חיסונית שעלולה לגרום לפריחה קשה (הנקראת דרמטיטיס במגע). באופן דומה, הפניצילין ההפטן יכול לגרום לתגובות אלרגיות לתרופות במחלקת הפניצילין.
תרגיל \(\PageIndex{3}\)
- מה ההבדל בין אנטיגן לאפיטופ?
- אילו גורמים משפיעים על הפוטנציאל האנטיגני של אנטיגן?
- מדוע הפטנים בדרך כלל אינם אנטיגניים, וכיצד הם הופכים לאנטיגניים?
נוגדנים
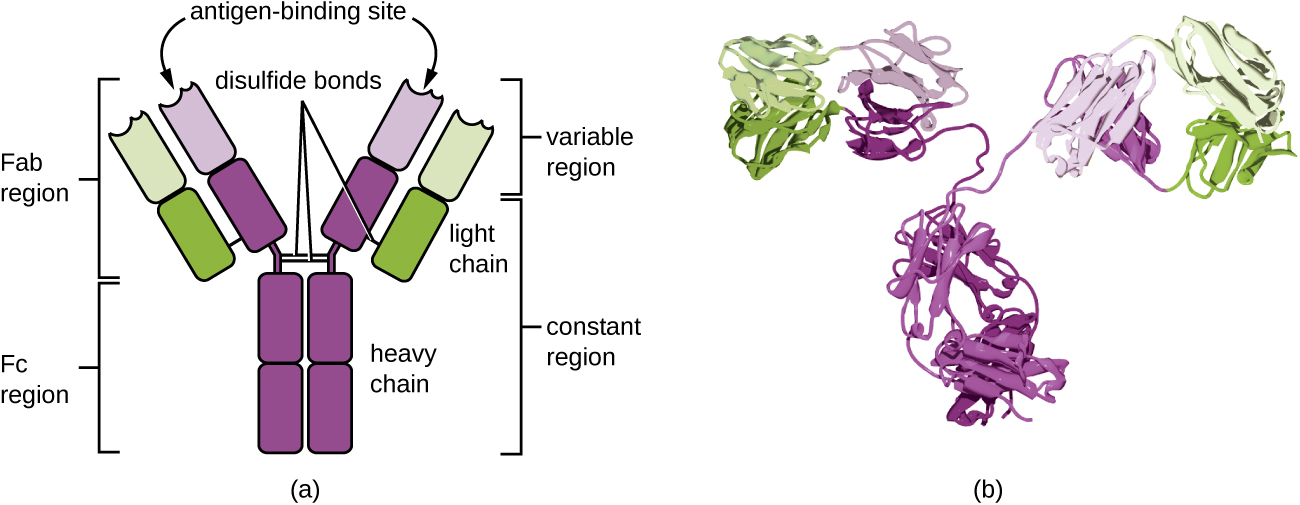
נוגדנים (הנקראים גם אימונוגלובולינים) הם גליקופרוטאינים הנמצאים הן בדם והן בנוזלי הרקמות. המבנה הבסיסי של מונומר נוגדנים מורכב מארבע שרשראות חלבון המוחזקות יחד על ידי קשרי דיסולפיד (איור\(\PageIndex{4}\)). קשר דיסולפיד הוא קשר קוולנטי בין קבוצות הסולפידריל R שנמצאות על שתי חומצות אמינו ציסטאין. שתי השרשראות הגדולות זהות זו לזו ונקראות השרשראות הכבדות. שתי השרשראות הקטנות יותר זהות זו לזו ונקראות שרשראות קלות. יחד, השרשראות הכבדות והקלות יוצרות מבנה בסיסי בצורת Y.
שתי ה'זרועות' של מולקולת הנוגדנים בצורת Y ידועות כאזור Fab, עבור "שבר של קישור אנטיגן". הקצה הרחוק של אזור Fab הוא האזור המשתנה, המשמש כאתר הקישור לאנטיגן. רצף חומצות האמינו באזור המשתנה מכתיב את המבנה התלת מימדי, ובכך את האפיטופ התלת מימדי הספציפי שאליו אזור ה- Fab מסוגל להיקשר. למרות שהספציפיות האפיטופית של אזורי Fab זהה לכל זרוע של מולקולת נוגדנים אחת, אזור זה מציג מידה גבוהה של שונות בין נוגדנים בעלי סגוליות אפיטופים שונות. קשירה לאזור Fab נחוצה לנטרול פתוגנים, צבירה או צבירה של פתוגנים וציטוטוקסיות בתיווך תאים תלויי נוגדנים.
האזור הקבוע של מולקולת הנוגדנים כולל את תא המטען של ה-Y והחלק התחתון של כל זרוע של ה-Y. תא המטען של ה-Y נקרא גם אזור Fc, עבור "שבר התגבשות", והוא האתר של קישור גורם משלים וקשירה לתאים פגוציטים במהלך אופסוניזציה בתיווך נוגדנים.
תרגיל \(\PageIndex{4}\)
תאר את הפונקציות השונות של אזור Fab ואזור Fc.
שיעורי נוגדנים
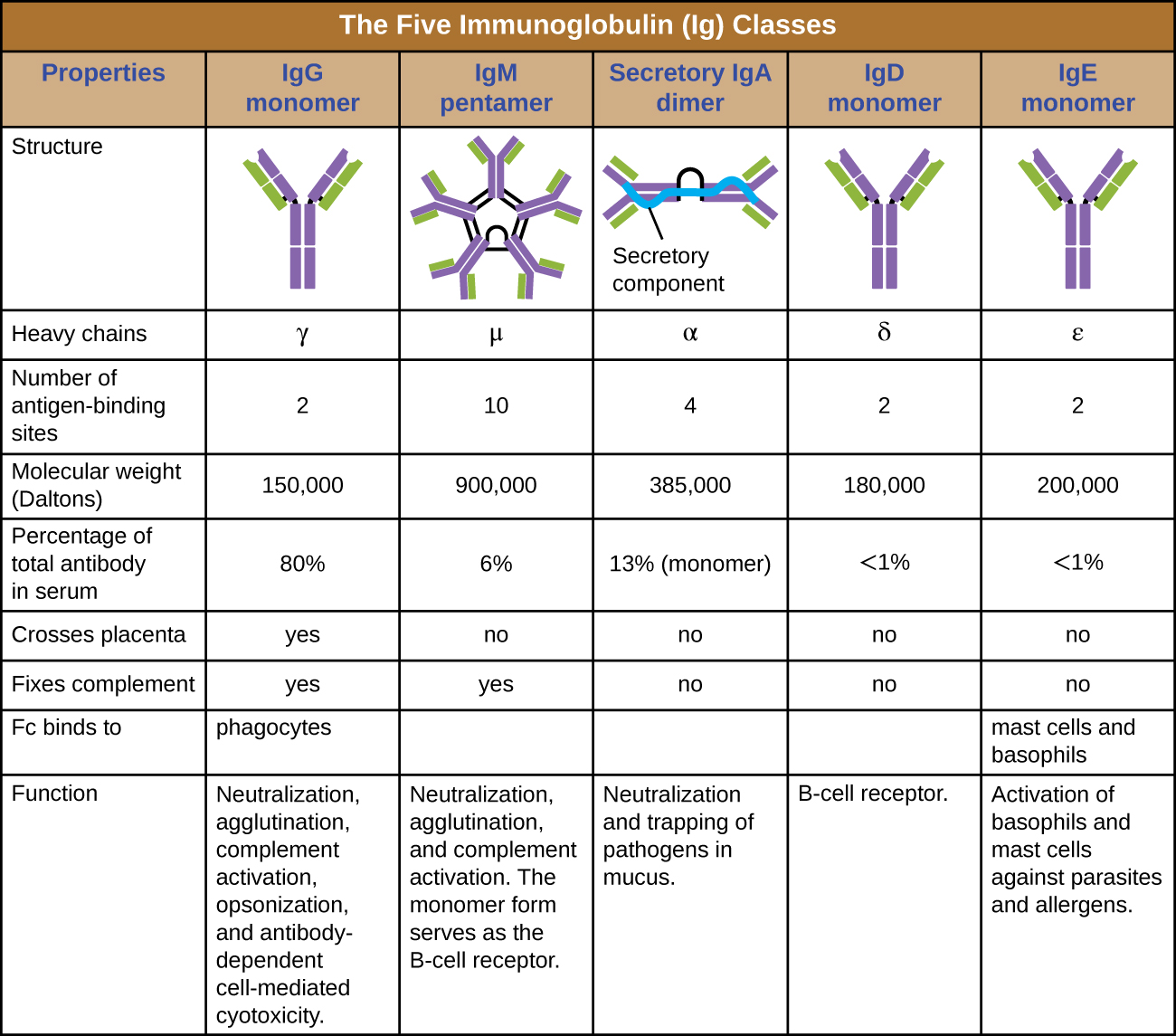
האזור הקבוע של מולקולת נוגדנים קובע את המעמד, או האיזוטיפ שלה. חמשת סוגי הנוגדנים הם IgG, IgM, IgA, IgD ו- IgE. לכל כיתה שרשראות כבדות ייחודיות המיועדות באותיות יווניות γ, μ, α, δ ו- ε, בהתאמה. שיעורי נוגדנים מציגים גם הבדלים חשובים בשפע בסרום, בסידור, באתרי הפעולה בגוף, בתפקידים תפקודיים ובגודל (איור\(\PageIndex{5}\)).
IgG הוא מונומר שהוא ללא ספק הנוגדן הנפוץ ביותר בדם האדם, המהווה כ -80% מכלל הנוגדנים בסרום. IgG חודר ביעילות לחללי רקמות, והוא סוג הנוגדנים היחיד עם היכולת לחצות את מחסום השליה, ומספק חסינות פסיבית לעובר המתפתח במהלך ההריון. IgG הוא גם סוג הנוגדנים הרב-תכליתי ביותר מבחינת תפקידו בהגנה על הגוף מפני פתוגנים.
IgM מיוצר בתחילה בצורה קשורה לממברנה מונומרית המשמשת כקולטן קושר אנטיגן על תאי B. הצורה המופרשת של IgM מתאספת לפנטאמר עם חמישה מונומרים של IgM הקשורים יחד על ידי מבנה חלבון הנקרא שרשרת J. למרות שמיקומה של שרשרת J ביחס לאזורי Fc של חמשת המונומרים מונע מ- IgM לבצע חלק מהפונקציות של IgG, עשרת אתרי ה- Fab הזמינים הקשורים ל- IgM פנטאמרי הופכים אותו לנוגדן חשוב בארסנל ההגנות של הגוף. IgM הוא הנוגדן הראשון המיוצר ומופרש על ידי תאי B במהלך התגובות החיסוניות הראשוניות והמשניות, מה שהופך את IgM ספציפי לפתוגן לסמן אבחוני בעל ערך במהלך זיהומים פעילים או אחרונים.
IgA מהווה כ -13% מכלל הנוגדנים בסרום, ו- IgA המפריש הוא סוג הנוגדנים הנפוץ והשופע ביותר שנמצא בהפרשות הריר המגנות על הריריות הריריות. ניתן למצוא IgA גם בהפרשות אחרות כמו חלב אם, קרעים ורוק. IgA הפרשה מורכבת לצורה דימרית עם שני מונומרים המחוברים למבנה חלבון הנקרא רכיב ההפרשה. אחד התפקידים החשובים של IgA המפריש הוא ללכוד פתוגנים בריר כך שניתן יהיה לחסל אותם מאוחר יותר מהגוף.
בדומה ל- IgM, IgD הוא מונומר הקשור לממברנה המצוי על פני תאי B, שם הוא משמש כקולטן המחייב אנטיגן. עם זאת, IgD אינו מופרש על ידי תאי B, ורק כמויות עקבות מזוהות בסרום. כמויות עקבות אלה נובעות ככל הנראה מהשפלה של תאי B ישנים ושחרור מולקולות IgD מהממברנות הציטופלזמיות שלהם.
IgE הוא סוג הנוגדנים הפחות שופע בסרום. בדומה ל- IgG, הוא מופרש כמונומר, אך תפקידו בחסינות הסתגלותית מוגבל להגנות אנטי-טפיליות. אזור ה- Fc של IgE נקשר לבזופילים ותאי פיטום. אזור ה-Fab של ה-IgE הקשור מקיים אינטראקציה עם אפיטופים ספציפיים של אנטיגן, וגורם לתאים לשחרר מתווכים פרו-דלקתיים חזקים. התגובה הדלקתית הנובעת מהפעלת תאי פיטום ובזופילים מסייעת בהגנה מפני טפילים, אך תגובה זו היא גם מרכזית לתגובות אלרגיות (ראה מחלות של מערכת החיסון.)
תרגיל \(\PageIndex{5}\)
- איזה חלק במולקולת נוגדנים קובע את המעמד שלה?
- איזה סוג של נוגדנים מעורב בהגנה מפני טפילים?
- תאר את ההבדל במבנה בין IgM ל- IgG.
אינטראקציות אנטיגן-נוגדנים
סוגים שונים של נוגדנים ממלאים תפקידים חשובים בהגנה על הגוף מפני פתוגנים. פונקציות אלה כוללות נטרול פתוגנים, אופסוניזציה לפגוציטוזיס, צבירה, הפעלת משלים וציטוטוקסיות בתיווך תאים תלויי נוגדנים. עבור רוב הפונקציות הללו, נוגדנים מספקים גם קשר חשוב בין חסינות ספציפית אדפטיבית לבין חסינות לא ספציפית מולדת.
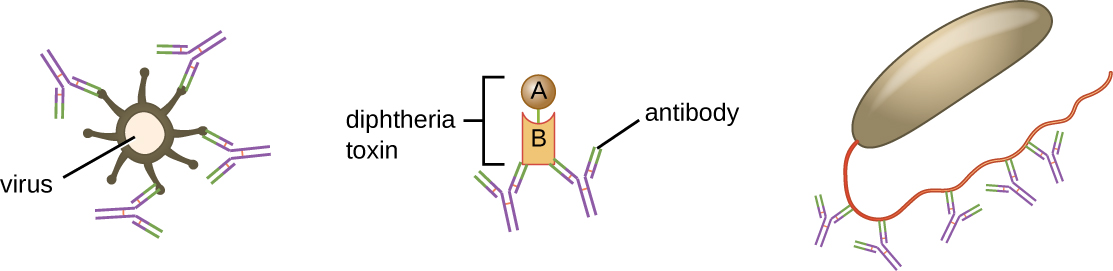
ניטרול כרוך בקשירה של נוגדנים מסוימים (IgG, IgM או IgA) לאפיטופים על פני השטח של פתוגנים או רעלים, ומונע את התקשרותם לתאים. לדוגמה, IgA הפרשה יכולה להיקשר לפתוגנים ספציפיים ולחסום התקשרות ראשונית לתאי רירית המעי. באופן דומה, נוגדנים ספציפיים יכולים להיקשר לרעלים מסוימים, לחסום אותם מלהיצמד לתאי המטרה ובכך לנטרל את השפעותיהם הרעילות. ניתן לנטרל וירוסים ולמנוע מהם להדביק תא על ידי אותו מנגנון (איור\(\PageIndex{6}\)).
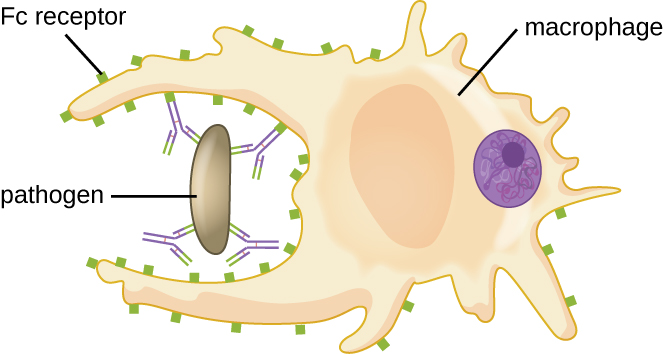
כפי שמתואר בהגנות כימיות, אופסוניזציה היא ציפוי של פתוגן במולקולות, כגון גורמי השלמה, חלבון C-reactive ועמילואיד A בסרום, כדי לסייע בקשירת פגוציטים כדי להקל על פגוציטוזיס. נוגדני IgG משמשים גם כאופסונינים מצוינים, המחייבים את אתרי ה- Fab שלהם לאפיטופים ספציפיים על פני הפתוגנים. לתאים פגוציטים כגון מקרופאגים, תאים דנדריטים ונויטרופילים יש קולטנים על פני השטח שלהם המזהים ונקשרים לחלק ה-Fc של מולקולות ה-IgG; לפיכך, IgG עוזר לפגוציטים כאלה להיצמד ולבלוע את הפתוגנים שהם קשרו (איור). \(\PageIndex{7}\)
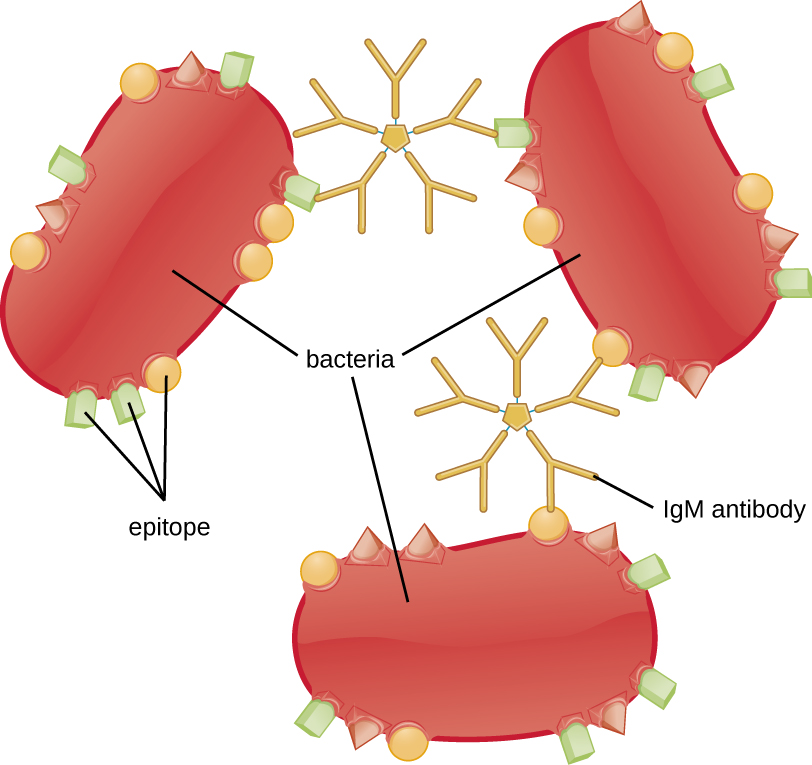
צבירה או צבירה כרוכה בקישור צולב של פתוגנים על ידי נוגדנים ליצירת אגרגטים גדולים (איור). \(\PageIndex{8}\) ל-IgG יש שני אתרים המחייבים אנטיגן Fab, שיכולים להיקשר לשני תאי פתוגן נפרדים, ולגבש אותם יחד. כאשר מעורבים מספר נוגדני IgG, אגרגטים גדולים יכולים להתפתח; אגרגטים אלה קלים יותר עבור הכליות והטחול לסנן מהדם וקל יותר לפגוציטים לבלוע להשמדה. המבנה הפנטמרי של IgM מספק עשרה אתרי קישור Fab לכל מולקולה, מה שהופך אותו לנוגדן היעיל ביותר לאגלוטינציה.
פונקציה חשובה נוספת של נוגדנים היא הפעלת מפל המשלים. כפי שנדון בפרק הקודם, מערכת המשלים היא מרכיב חשוב בהגנות המולדות, מקדמת את התגובה הדלקתית, מגייסת פגוציטים לאתר ההדבקה, משפרת את הפגוציטוזיס על ידי אופסוניזציה והרג פתוגנים חיידקיים גרם שליליים עם קומפלקס התקפת הממברנה (MAC). הפעלת משלים יכולה להתרחש באמצעות שלושה מסלולים שונים (ראה איור 17.2.2), אך היעיל ביותר הוא המסלול הקלאסי, הדורש קישור ראשוני של נוגדני IgG או IgM לפני השטח של תא פתוגן, המאפשר גיוס והפעלה של קומפלקס C1.
תפקיד חשוב נוסף של נוגדנים הוא ציטוטוקסיות בתיווך תאים תלויי נוגדנים (ADCC), המשפרת את ההרג של פתוגנים גדולים מכדי לעבור פגוציטוזה. תהליך זה מאופיין בצורה הטובה ביותר עבור תאים הורגים טבעיים (תאי NK), כפי שמוצג באיור\(\PageIndex{9}\), אך הוא יכול לכלול גם מקרופאגים ואוזינופילים. ADCC מתרחש כאשר אזור Fab של נוגדן IgG נקשר לפתוגן גדול; קולטני Fc על תאי אפקטור (למשל, תאי NK) נקשרים לאחר מכן לאזור Fc של הנוגדן, ומביאים אותם לקרבה עם פתוגן המטרה. תא האפקטור מפריש אז ציטוטוקסינים רבי עוצמה (למשל, פרפורין וגרנזימים) ההורגים את הפתוגן.
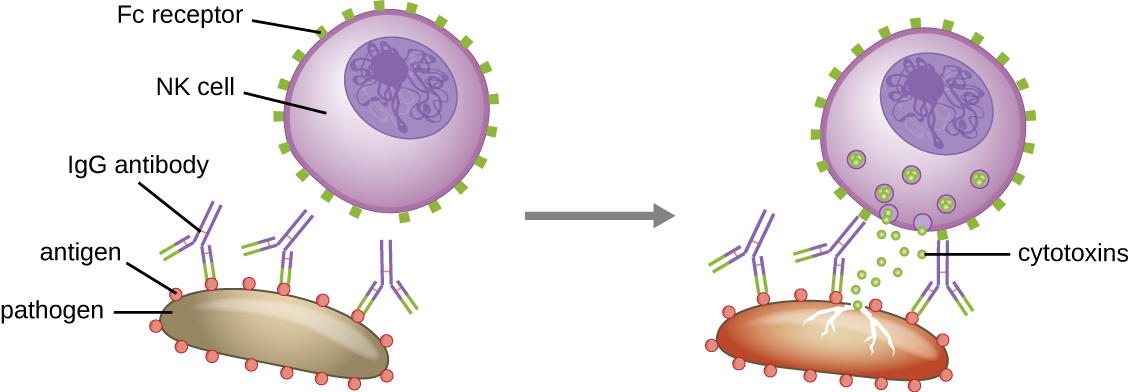
תרגיל \(\PageIndex{6}\)
- היכן נמצא IgA בדרך כלל?
- איזה סוג של נוגדנים חוצה את השליה, ומספק הגנה לעובר?
- השווה את המנגנונים של אופסוניזציה וציטוטוקסיות בתיווך תאים תלויי נוגדנים.
מושגי מפתח וסיכום
- חסינות מסתגלת היא הגנה נרכשת מפני פתוגנים זרים המאופיינת בספציפיות ובזיכרון. החשיפה הראשונה לאנטיגן מעוררת תגובה ראשונית, וחשיפות שלאחר מכן מעוררות תגובה משנית מהירה וחזקה יותר.
- חסינות מסתגלת היא מערכת כפולה הכוללת חסינות הומורלית (נוגדנים המיוצרים על ידי תאי B) וחסינות תאית (תאי T המכוונים נגד פתוגנים תאיים).
- אנטיגנים, הנקראים גם אימונוגנים, הם מולקולות המפעילות חסינות אדפטיבית. לאנטיגן בודד יש אפיטופים קטנים יותר, שכל אחד מהם מסוגל לעורר תגובה חיסונית אדפטיבית ספציפית.
- יכולתו של אנטיגן לעורר תגובה חיסונית תלויה במספר גורמים, כולל המעמד המולקולרי שלו, המורכבות המולקולרית וגודלו.
- נוגדנים (אימונוגלובולינים) הם גליקופרוטאינים בצורת Y עם שני אתרי Fab לקשירת אנטיגנים וחלק Fc המעורב בהפעלת משלים ובאופסוניזציה.
- חמשת סוגי הנוגדנים הם IgM, IgG, IgA, IgE ו - IgD, כל אחד שונה בגודל, בסידור, במיקום בגוף ובתפקוד. חמשת התפקידים העיקריים של נוגדנים הם נטרול, אופסוניזציה, צבירה, הפעלת משלים וציטוטוקסיות בתיווך תאים תלויי נוגדנים (ADCC).


