13.4: Mahesabu ya usawa
- Page ID
- 176838
- Andika milinganyo inayowakilisha mabadiliko katika mkusanyiko na shinikizo kwa aina za kemikali katika mifumo ya usawa
- Tumia algebra kufanya aina mbalimbali za mahesabu ya usawa
Tunajua kwamba katika usawa, thamani ya quotient ya majibu ya mmenyuko wowote ni sawa na mara kwa mara yake ya usawa. Hivyo, tunaweza kutumia usemi wa hisabati kwa Q kuamua idadi ya kiasi kinachohusishwa na mmenyuko kwenye usawa au msawazo unaokaribia. Wakati tumejifunza kutambua katika mwelekeo gani mmenyuko utabadilika kufikia usawa, tunataka kupanua uelewa huo kwa mahesabu ya kiasi. Tunafanya hivyo kwa kutathmini njia ambazo viwango vya bidhaa na reactants hubadilika kama mmenyuko unakaribia usawa, kukumbuka uwiano wa stoichiometric wa mmenyuko. Njia hii ya algebraic ya mahesabu ya usawa itachunguzwa katika sehemu hii.
Mabadiliko katika viwango au shinikizo la reactants na bidhaa hutokea kama mfumo wa mmenyuko unakaribia usawa. Katika sehemu hii tutaona kwamba tunaweza kuhusisha mabadiliko haya kwa kila mmoja kwa kutumia coefficients katika usawa kemikali equation kuelezea mfumo. Tunatumia utengano wa amonia kama mfano.
Juu ya joto, amonia hutengana na nitrojeni na hidrojeni kulingana na equation hii:
\[\ce{2NH3}(g)⇌\ce{N2}(g)+\ce{3H2}(g) \nonumber \]
Ikiwa sampuli ya amonia hutengana katika mfumo uliofungwa na mkusanyiko wa N 2 huongezeka kwa 0.11 M, mabadiliko katika mkusanyiko wa N 2, Δ [N 2], mkusanyiko wa mwisho chini ya mkusanyiko wa awali, ni 0.11 M. Mabadiliko ni chanya kwa sababu mkusanyiko wa N 2 huongezeka.
Mabadiliko katika mkusanyiko wa H 2, Δ [H 2], pia ni chanya- ukolezi wa H 2 huongezeka kama amonia hutengana. Equation ya kemikali inatuambia kwamba mabadiliko katika mkusanyiko wa H 2 ni mara tatu mabadiliko katika mkusanyiko wa N 2 kwa sababu kwa kila mole ya N 2 zinazozalishwa, 3 moles ya H 2 huzalishwa.
\[ \begin{align*} \ce{Δ[H2]} &=3×\ce{Δ[N2]} \\[4pt] &=3×(0.11\:M) \\[4pt] &=0.33\:M \end{align*} \nonumber \]
Mabadiliko katika mkusanyiko wa NH 3, Δ [NH 3], ni mara mbili ya Δ [N 2]; equation inaonyesha kwamba 2 moles ya NH 3 lazima kuoza kwa kila mole ya N 2 sumu. Hata hivyo, mabadiliko katika mkusanyiko wa NH 3 ni hasi kwa sababu mkusanyiko wa amonia hupungua kadiri inapoharibika.
\[ \begin{align*} Δ[\ce{NH3}] &=−2×Δ[\ce{N2}] \\[4pt] &=−2×(0.11\:M) \\[4pt] &=−0.22\:M \end{align*} \nonumber \]
Tunaweza kuhusisha mahusiano haya moja kwa moja na coefficients katika equation
\ [kuanza {align}
&\ njozi {Δ [N3}\ ce {2NH3} (g)
&&&&\ njozi {Δ [N2}\ ce {N2} (g)
&&+
&&\ njozi {Δ [H2]}\ ce {3H2} (g)\\
&Δ [\ ce {N3}] =ї2×Δ [\ ce {\ ce {N3}] =ї2×Δ [\ ce N2}] & & Δ [\ ce {N2}] = 0.11\ :M & amp; &Δ [\ ce {H2}] =3×Δ [\ ce {N2}]
\ mwisho {align}\ nambari\]
Kumbuka kuwa mabadiliko yote upande mmoja wa mishale ni ya ishara sawa na kwamba mabadiliko yote upande wa pili wa mishale ni ya ishara tofauti.
Ikiwa hatujui ukubwa wa mabadiliko katika mkusanyiko wa N 2, tunaweza kuiwakilisha kwa ishara x.
Mabadiliko katika viwango vingine ingekuwa kisha kuwakilishwa kama:
\(Δ[\ce{H2}]=3×Δ[\ce{N2}]=3x\)
Coefficients katika maneno Δ ni sawa na wale walio katika usawa wa usawa kwa majibu.
\ (\ kuanza {alignat} {3}
&\ ce {2NH3} (g)\ :&\ ce {N2} (g) +\ :&&\ ce {3H2} (g)\\
&&2x & x & 3x
\ mwisho {alignat}\)
Njia rahisi zaidi kwa sisi kupata coefficients kwa mabadiliko ya mkusanyiko katika mmenyuko wowote ni kutumia coefficients katika usawa wa kemikali. Ishara ya mgawo ni chanya wakati ukolezi unaongezeka; ni hasi wakati ukolezi unapungua.
Jaza mabadiliko katika viwango kwa kila moja ya athari zifuatazo.
(a)\ (kuanza {alignat} {3}
&\ ce {C2H2} (g) +\ :&&\ ce {2Br2} (g)\
:&&\ ce {C2H2Br4} (g)\\ &x &\ kusisitiza {\ hnafasi {40px}
}\)
(b)\ (kuanza {alignat} {3}
&\ ce {I2} (aq) +\ :&&\ ce {I-} (aq)\ :&&\ ce {I3-} (aq)\\
&\ kusisitiza {\ hnafasi {40px}} &\ kusisitiza {\ hspace {40px}}} & x
\ mwisho {alignat}\)
(c)\ (kuanza {alignat} {3}
&\ ce {C3H8} (g) +\ :&&\ ce {5O2} (g)\ :&&\ ce {3CO2} (g) +\ :&&\ ce {4H2O} (g)\\
&x &\ kusisitiza {\ hspace {40px}} &\ kusisitiza {\ hspace {40px}}
\ mwisho {alignat}\)
Suluhisho la S
(a)\ (\ kuanza {alignat} {3}
&\ ce {C2H2} (g) +\ :&&\ ce {2Br2} (g)\ :&&\ ce {C2H2Br4} (g)\\
&x &2x &-x
\ mwisho {alignat}\)
(b)\ (\ kuanza {alignat} {3}
&\ ce {I2} (aq) +\ :&&\ ce {I-} (aq)\ :&&\ ce {I3-} (aq)\\
&-x &-x &&x
\ mwisho {alignat}\)
(c)\ (\ kuanza {alignat} {3}
&\ ce {C3H8} (g) +\ :&&\ ce {5O2} (g)\ :&\ ce {3CO2} (g) +\ :&\ ce {4H2O} (g)\\
&x &&x &-3x & -4x
\ mwisho {alignat}\)
Jaza mabadiliko katika viwango kwa kila moja ya athari zifuatazo:
(a)\ (kuanza {alignat} {3}
&\ ce {2SO2} (g) +\ :&&\ ce {O2} (g)\ :&&\ ce {2SO3} (g)\\
&\ kusisitiza {\ hnafasi {40px}} & x &\ kusisitiza {\ hspace {40px}}
\ mwisho {alignat}\)
(b)\ (\ kuanza {alignat} {3}
&\ ce {C4H8} (g)\ :&&\ ce {2C2H4} (g)\\
&\ kusisitiza {\ hspace {40px}}} &&-2x
\ mwisho {alignat}\)
(c)\ (kuanza {alignat} {3}
&\ ce {4NH3} (g) +\ :&&\ ce {7H2O} (g)\ :&&\ ce {4NO2} (g) +\ :&&\ ce {6H2O} (g)\\
&\ kusisitiza {\ hspace {40px}} &\ kusisitiza {\ nafasi {40px}} &\ kusisitiza {\ nafasi {40px}}
\ mwisho { alignat}\)
- Jibu
-
2 x, x, -2 x
- Jibu b
-
x, -2 x
- Jibu c
-
4 x, 7 x, -4 x, -6 x au -4 x, -7 x, 4 x, 6 x
Mahesabu Kuhusisha Msawazo Viwango
Kwa sababu thamani ya quotient ya mmenyuko wa mmenyuko wowote katika usawa ni sawa na mara kwa mara yake ya usawa, tunaweza kutumia usemi wa hisabati kwa Q c (yaani, sheria ya hatua ya molekuli) kuamua idadi ya kiasi kinachohusiana na mmenyuko kwenye usawa. Inaweza kusaidia ikiwa tunakumbuka kwamba Q c = K c (katika usawa) katika hali hizi zote na kwamba kuna aina tatu tu za msingi za mahesabu:
- Kuhesabu mara kwa mara ya usawa. Ikiwa viwango vya reactants na bidhaa katika usawa hujulikana, thamani ya mara kwa mara ya usawa kwa mmenyuko inaweza kuhesabiwa.
- Uhesabuji wa viwango vya usawa wa kukosa. Ikiwa thamani ya mara kwa mara ya usawa na viwango vyote vya usawa, isipokuwa moja, hujulikana, mkusanyiko uliobaki unaweza kuhesabiwa.
- Uhesabuji wa viwango vya usawa kutoka kwa viwango vya awali. Ikiwa thamani ya mara kwa mara ya usawa na seti ya viwango vya reactants na bidhaa ambazo hazipo katika usawa zinajulikana, viwango vya usawa vinaweza kuhesabiwa.
Orodha sawa inaweza kuzalishwa kwa kutumia Q P, K P, na shinikizo la sehemu. Tutaangalia kutatua kila kesi hizi kwa mlolongo.
Uhesabuji wa Mara kwa mara ya usawa
Kwa kuwa sheria ya hatua ya molekuli ni equation pekee tuna kuelezea uhusiano kati ya K c na viwango vya reactants na bidhaa, tatizo lolote ambalo linahitaji sisi kutatua kwa K c lazima kutoa taarifa za kutosha kuamua reactant na viwango vya bidhaa katika usawa. Silaha na viwango, tunaweza kutatua equation kwa K c, kama itakuwa haijulikani tu.
Mfano\(\PageIndex{1}\) ulituonyesha jinsi ya kuamua mara kwa mara ya usawa wa mmenyuko ikiwa tunajua viwango vya reactants na bidhaa katika usawa. Mfano unaofuata unaonyesha jinsi ya kutumia stoichiometri ya mmenyuko na mchanganyiko wa viwango vya awali na viwango vya usawa ili kuamua mara kwa mara ya usawa. Mbinu hii, inayoitwa meza ya ICE-kwa maana mimi ya awali, C mabadiliko, na E usawa - itakuwa na manufaa katika kutatua matatizo mengi ya usawa. Chati huzalishwa kuanzia na mmenyuko wa usawa katika swali. Chini ya mmenyuko viwango vya awali vya reactants na bidhaa zimeorodheshwa-hali hizi hutolewa kwa kawaida katika tatizo na tunaona hakuna mabadiliko kuelekea usawa kuwa kilichotokea. Mstari uliofuata wa data ni mabadiliko ambayo hutokea kama mabadiliko ya mfumo kuelekea usawa-usisahau kuzingatia stoichiometry mmenyuko kama ilivyoelezwa katika sehemu ya awali ya sura hii. Mstari wa mwisho una viwango mara moja usawa umefikiwa.
Molekuli za iodini huguswa reversibly na ioni iodidi kuzalisha ioni triodidi.
\[\ce{I2}(aq)+\ce{I-}(aq)⇌\ce{I3-}(aq) \nonumber \]
Ikiwa suluhisho na viwango vya I 2 na I - wote sawa na 1.000 × 10 1-3 M kabla ya mmenyuko hutoa msawazo mkusanyiko wa I 2 ya 6.61 × 10 -4 M, ni mara kwa mara ya usawa gani kwa mmenyuko?
Suluhisho
Tutaanza tatizo hili kwa kuhesabu mabadiliko katika ukolezi kama mfumo unaendelea kwa usawa. Kisha tunaamua viwango vya usawa na, hatimaye, mara kwa mara ya usawa. Kwanza, tunaanzisha meza na viwango vya awali, mabadiliko katika viwango, na viwango vya usawa kwa kutumia - x kama mabadiliko katika mkusanyiko wa I 2.
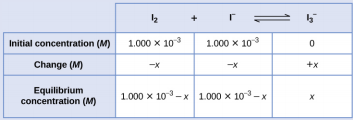
Kwa kuwa mkusanyiko wa usawa wa I 2 unapewa, tunaweza kutatua kwa x. Katika usawa mkusanyiko wa I 2 ni 6.61 × 10 -4 M ili
\(1.000×10^{−3}−x=6.61×10^{−4}\)
\(x=1.000×10^{−3}−6.61×10^{−4}\)
\(=3.39×10^{−4}\:M\)
Sasa tunaweza kujaza meza na viwango vya usawa.

Sasa tunahesabu thamani ya mara kwa mara ya usawa.
\(K_c=Q_c=\ce{\dfrac{[I3- ]}{[I2][I- ]}}\)
\(=\dfrac{3.39×10^{−4}\:M}{(6.61×10^{−4}\:M)(6.61×10^{−4}\:M)}=776\)
Ethanol na asidi ya asidi huguswa na kuunda maji na acetate ya ethyl, kutengenezea kuwajibika kwa harufu ya kuondosha baadhi ya msumari wa msumari.
\(\ce{C2H5OH + CH3CO2H ⇌ CH3CO2C2H5 + H2O}\)
Wakati 1 mol kila moja ya C 2 H 5 OH na CH 3 CO 2 H wanaruhusiwa kuguswa katika 1 L ya dioxane kutengenezea, usawa ni imara wakati\(\dfrac{1}{3}\) mol ya kila moja ya reactants bado. Tumia mara kwa mara ya usawa kwa majibu. (Kumbuka: Maji sio kutengenezea katika mmenyuko huu.)
- Jibu
-
K c = 4
Uhesabuji wa Mkazo wa Msawazo
Ikiwa tunajua mara kwa mara ya usawa kwa mmenyuko na kujua viwango katika usawa wa reactants wote na bidhaa isipokuwa moja, tunaweza kuhesabu mkusanyiko kukosa.
Oksidi za nitrojeni ni uchafuzi wa hewa unaozalishwa na mmenyuko wa nitrojeni na oksijeni kwenye joto la juu. Katika 2000 °C, thamani ya mara kwa mara ya usawa kwa mmenyuko\(\ce{N2}(g)+\ce{O2}(g)⇌\ce{2NO}(g)\), ni 4.1 × 10 -4. Pata mkusanyiko wa NO (g) katika mchanganyiko wa usawa na hewa kwenye shinikizo la atm 1 kwenye joto hili. Katika hewa, [N 2] = 0.036 mol/L na [O 2] 0.0089 mol/L.
Suluhisho
Tunapewa viwango vyote vya usawa isipokuwa ile ya NO. Hivyo, tunaweza kutatua kwa kukosa msawazo mkusanyiko kwa upya equation kwa mara kwa mara usawa.
\(K_c=Q_c=\ce{\dfrac{[NO]^2}{[N2][O2]}}\)
\(\ce{[NO]^2}=K_c\ce{[N2][O2]}\)
\(\ce{[NO]}=\sqrt{K_c\ce{[N2][O2]}}\)
\(=\sqrt{(4.1×10^{−4})(0.036)(0.0089)}\)
\(=\sqrt{1.31×10^{−7}}\)
\(=3.6×10^{−4}\)
Hivyo [NO] ni 3.6 × 10 -4 Mol/L katika usawa chini ya masharti haya.
Tunaweza kuangalia jibu letu kwa kubadili viwango vyote vya usawa katika usemi kwa quotient ya majibu ili kuona kama ni sawa na mara kwa mara ya usawa.
\[ \begin{align*} Q_c=\ce{\dfrac{[NO]^2}{[N2][O2]}} \\[4pt] &=\dfrac{(3.6×10^{−4})^2}{(0.036)(0.0089)} \\[4pt] &=4.0×10^{−4}=K_c \end{align*} \nonumber \]
Hundi ya jibu; thamani yetu ya mahesabu inatoa mara kwa mara ya usawa ndani ya kosa lililohusishwa na takwimu muhimu katika tatizo.
Mara kwa mara ya usawa kwa mmenyuko wa nitrojeni na hidrojeni kuzalisha amonia kwa joto fulani ni 6.00 × 10 -1 -2. Tumia mkusanyiko wa usawa wa amonia ikiwa viwango vya usawa wa nitrojeni na hidrojeni ni 4.26 M na 2.09 M, kwa mtiririko huo.
- Jibu
-
1.53 mol/L
Mahesabu ya Mabadiliko katika Mkazo
Ikiwa tunajua mara kwa mara ya usawa kwa mmenyuko na seti ya viwango vya reactants na bidhaa ambazo hazipo katika usawa, tunaweza kuhesabu mabadiliko katika viwango kama mfumo unakuja kwa usawa, pamoja na viwango vipya katika usawa. Utaratibu wa kawaida unaweza kufupishwa kwa hatua nne.
- Kuamua mwelekeo majibu yanaendelea kuja usawa.
- Andika usawa wa kemikali kwa mmenyuko.
- Ikiwa mwelekeo ambao majibu yanapaswa kuendelea kufikia usawa si dhahiri, hesabu Q c kutoka viwango vya awali na kulinganisha na K c kuamua mwelekeo wa mabadiliko.
- Kuamua mabadiliko ya jamaa yanahitajika kufikia usawa, kisha uandike viwango vya usawa kulingana na mabadiliko haya.
- Eleza mabadiliko katika viwango vya awali vinavyohitajika kwa mmenyuko kufikia usawa. Kwa ujumla, tunawakilisha mabadiliko madogo na alama x na kuelezea mabadiliko mengine kwa suala la mabadiliko madogo.
- Kufafanua kukosa viwango vya usawa katika suala la viwango vya awali na mabadiliko katika mkusanyiko kuamua katika (a).
- Tatua mabadiliko na viwango vya usawa.
- Badilisha viwango vya usawa katika usemi kwa mara kwa mara ya usawa, kutatua kwa x, na uangalie mawazo yoyote yaliyotumiwa kupata x.
- Tumia viwango vya usawa.
- Angalia hesabu.
- Angalia viwango vya usawa wa mahesabu kwa kuzibadilisha katika kujieleza kwa usawa na kuamua kama hutoa mara kwa mara ya usawa.
Wakati mwingine hatua fulani inaweza kutofautiana kutoka tatizo hadi tatizo-inaweza kuwa ngumu zaidi katika matatizo fulani na chini ya ngumu kwa wengine. Hata hivyo, kila hesabu ya viwango vya usawa kutoka kwa seti ya viwango vya awali itahusisha hatua hizi.
Katika kutatua matatizo ya usawa ambayo yanahusisha mabadiliko katika mkusanyiko, wakati mwingine ni rahisi kuanzisha meza ya ICE, kama ilivyoelezwa katika sehemu iliyopita.
Chini ya hali fulani, mara kwa mara ya usawa kwa kuharibika kwa PCL 5 (g) katika PCL 3 (g) na Cl 2 (g) ni 0.0211. Je, ni viwango vya usawa wa PCL 5, PCL 3, na Cl 2 ikiwa mkusanyiko wa awali wa PCL 5 ulikuwa 1.00 M?
Suluhisho
Tumia mchakato wa hatua kwa hatua ulioelezwa hapo awali.
- Equation ya usawa kwa kuharibika kwa PCL 5 ni
\(\ce{PCl5}(g)⇌\ce{PCl3}(g)+\ce{Cl2}(g)\)
Kwa sababu hatuna bidhaa awali, Q c = 0 na majibu itaendelea kwa haki.
- Hebu tuwakilisha ongezeko la mkusanyiko wa PCL 3 kwa ishara x. Mabadiliko mengine yanaweza kuandikwa kwa suala la x kwa kuzingatia coefficients katika equation ya kemikali.
\ (\ kuanza {alignat} {3}
&\ ce {pCl5} (g)\ :&\ ce {PCL3} (g) +\ :&\ ce {Cl2} (g)\\
&-x &x & x
\ mwisho {alignat}\) -
Mabadiliko katika mkusanyiko na maneno ya viwango vya usawa ni:

Jedwali hili lina nguzo mbili kuu na safu nne. Mstari wa kwanza wa safu ya kwanza haina kichwa na kisha ina zifuatazo katika safu ya kwanza: Mkusanyiko wa awali (M), Mabadiliko (M), mkusanyiko wa usawa (M). Safu ya pili ina kichwa, “P C l subscript 5 mshale wa usawa P C l subscript 3 pamoja C l subscript 2.” Chini ya safu ya pili ni kikundi cha safu tatu na nguzo tatu. Safu ya kwanza ina yafuatayo: 1.00, x hasi, 1.00 bala x. safu ya pili ina yafuatayo: 0, x chanya, 0 pamoja x sawa x. safu ya tatu ina yafuatayo: 0, x chanya, 0 pamoja x sawa x. - Kubadilisha viwango vya usawa katika usawa wa mara kwa mara equation inatoa
\(K_c=\ce{\dfrac{[PCl3][Cl2]}{[PCl5]}}=0.0211\)\(=\dfrac{(x)(x)}{(1.00−x)}\)
Equation hii ina variable moja tu, x, mabadiliko katika mkusanyiko. Tunaweza kuandika equation kama equation quadratic na kutatua kwa x kutumia formula quadratic.
\(0.0211=\dfrac{(x)(x)}{(1.00−x)}\)\(0.0211(1.00−x)=x^2\)\(x^2+0.0211x−0.0211=0\)Equation ya shaba ya fomu 2 + bx + c = 0 inaweza kupangwa upya ili kutatua kwa x:
\(x=\dfrac{−b±\sqrt{b^2−4ac}}{2a}\)Katika kesi hii, a = 1, b = 0.0211, na c = -0.0211. Kubadilisha maadili sahihi kwa mavuno, b, na c:
\(x=\dfrac{−0.0211±\sqrt{(0.0211)^2−4(1)(−0.0211)}}{2(1)}\)\(=\dfrac{−0.0211±\sqrt{(4.45×10^{−4})+(8.44×10^{−2})}}{2}\)\(=\dfrac{−0.0211±0.291}{2}\)Hivyo
\(x=\dfrac{−0.0211+0.291}{2}=0.135\)au
\(x=\dfrac{−0.0211−0.291}{2}=−0.156\)Ulinganifu wa Quadratic mara nyingi una ufumbuzi mbili tofauti, moja ambayo inawezekana kimwili na moja ambayo haiwezekani kimwili (mizizi ya nje). Katika kesi hiyo, suluhisho la pili (-0.156) haliwezekani kimwili kwa sababu tunajua mabadiliko lazima iwe namba nzuri (vinginevyo tutaishia na maadili hasi kwa viwango vya bidhaa). Hivyo, x = 0.135 M.
Viwango vya usawa ni
\(\ce{[PCl5]}=1.00−0.135=0.87\:M\)
\(\ce{[PCl3]}=x=0.135\:M\)
\(\ce{[Cl2]}=x=0.135\:M\) - Kubadilisha katika maneno ya K c (kuangalia hesabu) inatoa
\(K_c=\ce{\dfrac{[PCl3][Cl2]}{[PCl5]}}=\dfrac{(0.135)(0.135)}{0.87}=0.021\)
Mara kwa mara ya usawa mahesabu kutoka viwango vya usawa ni sawa na thamani ya K c iliyotolewa katika tatizo (wakati mviringo kwa idadi sahihi ya takwimu muhimu). Hivyo, viwango vya usawa wa mahesabu hundi.
Asetiki, CH 3 CO 2 H, humenyuka na ethanol, C 2 H 5 OH, kuunda maji na ethyl acetate, CH 3 CO 2 C 2 H 5.
\[\ce{CH3CO2H + C2H5OH ⇌ CH3CO2C2H5 + H2O} \nonumber \]
Mara kwa mara ya usawa kwa mmenyuko huu na dioxane kama kutengenezea ni 4.0. Je, ni viwango vya usawa wakati mchanganyiko ambao ni 0.15 M katika CH 3 CO 2 H, 0.15 M katika C 2 H 5 OH, 0.40 M katika CH 3 CO 2 C 2 H 5, na 0.40 M katika H 2 O ni mchanganyiko katika dioxane ya kutosha kufanya 1.0 L ya suluhisho?
- Jibu
-
[CH 3 CO 2 H] = 0.36 M, [C 2 H 5 OH] = 0.36 M, [CH 3 CO 2 C 2 H 5] = 0.17 M, [H 2 O] = 0.17 M, [H 2 O] = 0.17 M
Flask 1.00-L imejaa 1.00 moles ya H 2 na 2.00 moles ya I 2. Thamani ya mara kwa mara ya usawa kwa mmenyuko wa hidrojeni na iodini inayoitikia kuunda iodidi ya hidrojeni ni 50.5 chini ya hali iliyotolewa. Je, ni viwango vya usawa wa H 2, I 2, na HI katika moles/L?
\[\ce{H2}(g)+\ce{I2}(g)\rightleftharpoons\ce{2HI}(g) \nonumber \]
- Jibu
-
[H 2] = 0.06 M, [I 2] = 1.06 M, [HI] = 1.88 M
Wakati mwingine inawezekana kutumia ufahamu wa kemikali ili kupata ufumbuzi wa matatizo ya usawa bila kweli kutatua equation quadratic (au ngumu zaidi). Kwanza, hata hivyo, ni muhimu kuthibitisha kwamba usawa unaweza kupatikana kuanzia extremes mbili: wote (au zaidi) reactants na wote (au zaidi) bidhaa.
Fikiria ionization ya 0.150 M HA, asidi dhaifu.
Njia ya wazi zaidi ya kuamua viwango vya usawa itakuwa kuanza na reactants tu. Hii inaweza kuitwa “wote reactant” kuanzia hatua. Kutumia x kwa kiasi cha asidi ionized katika usawa, hii ni meza ya ICE na suluhisho.

Kuweka na kutatua equation quadratic inatoa
Kutumia mizizi nzuri (kimwili), viwango vya usawa ni
Njia isiyo wazi ya kutatua tatizo itakuwa kudhani HA yote ionizes kwanza, basi mfumo unakuja usawa. Hii inaweza kuitwa “bidhaa zote” kuanzia. Kutokana yote ya HA ionizes anatoa
Kutumia hizi kama viwango vya awali na “y” kuwakilisha mkusanyiko wa HA katika usawa, hii ni meza ya ICE kwa hatua hii ya kuanzia.
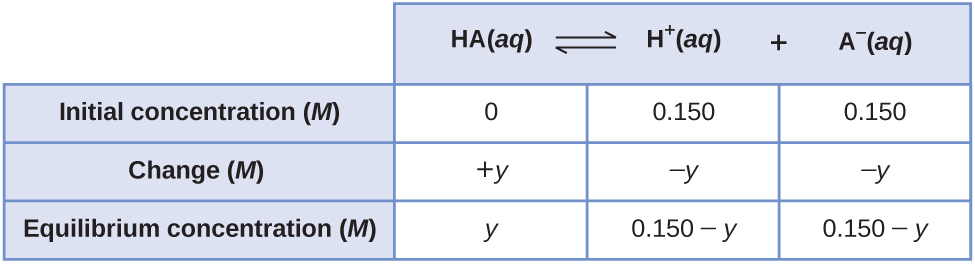
Kuweka na kutatua equation quadratic inatoa
Kuhifadhi chache takwimu za ziada muhimu ili kupunguza matatizo rounding.
Rounding kila ufumbuzi wa takwimu tatu muhimu inatoa
Kutumia mizizi muhimu ya kimwili (0.140 M) hutoa viwango vya usawa kama
Hivyo, mbinu mbili hutoa matokeo sawa (kwa maeneo matatu ya decimal), na kuonyesha kwamba pointi zote mbili za kuanzia husababisha hali sawa ya usawa. “All reactant” kuanzia ilisababisha mabadiliko madogo kiasi (x) kwa sababu mfumo ulikuwa karibu na usawa, wakati “bidhaa zote” kuanzia ilikuwa na mabadiliko makubwa kiasi (y) iliyokuwa karibu ukubwa wa viwango vya awali. Inaweza kusema kuwa mfumo unaoanza “karibu” na usawa utahitaji tu “ndogo” mabadiliko katika hali (x) kufikia usawa.
Kumbuka kwamba ndogo K c ina maana kwamba kidogo sana ya reactants huunda bidhaa na K c kubwa ina maana kwamba wengi wa reactants huunda bidhaa. Ikiwa mfumo unaweza kupangwa hivyo huanza “karibu” na usawa, basi ikiwa mabadiliko (x) ni madogo ikilinganishwa na viwango vyovyote vya awali, inaweza kupuuzwa. Ndogo hufafanuliwa kama kusababisha kosa la chini ya 5%. Mifano miwili ifuatayo inaonyesha hili.
Je, ni viwango gani katika usawa wa ufumbuzi wa 0.15 M wa HCN?
\[\ce{HCN}(aq)⇌\ce{H+}(aq)+\ce{CN-}(aq) \hspace{20px} K_c=4.9×10^{−10} \nonumber \]
Suluhisho katika
Kutumia “x” kuwakilisha mkusanyiko wa kila bidhaa katika usawa hutoa meza hii ya ICE.
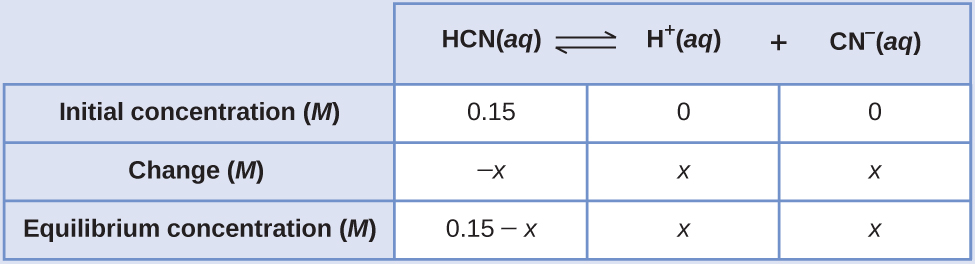
Suluhisho halisi linaweza kupatikana kwa kutumia formula ya quadratic na
\[K_c=\dfrac{(x)(x)}{0.15−x} \nonumber \]
kusuluhisha
\[x^2+4.9×10^{−10}−7.35×10^{−11}=0 \nonumber \]
\[x=8.56×10^{−6}\:M\textrm{ (3 sig. figs.)}=8.6×10^{−6}\:M\textrm{ (2 sig. figs.)} \nonumber \]
Hivyo [H +] = [CN -] = x = 8.6 × 10 —6 M na [HCN] = 0.15 — x = 0.15 M.
Katika kesi hiyo, intuition ya kemikali inaweza kutoa suluhisho rahisi. Kutoka mara kwa mara ya usawa na hali ya awali, x lazima iwe ndogo ikilinganishwa na 0.15 M. Zaidi rasmi, kama\(x≪0.15\), basi 0.15 — x ≈ 0.15. Ikiwa dhana hii ni ya kweli, basi inafungua kupata x
\[K_c=\dfrac{(x)(x)}{0.15−x}≈\dfrac{x^2}{0.15} \nonumber \]
\[4.9×10^{−10}=\dfrac{x^2}{0.15} \nonumber \]
\[x^2=(0.15)(4.9×10^{−10})=7.4×10^{−11} \nonumber \]
\[x=\sqrt{7.4×10^{−11}}=8.6×10^{−6}\:M \nonumber \]
Katika mfano huu, kutatua halisi (quadratic) equation na kutumia makadirio alitoa matokeo sawa na takwimu mbili muhimu. Wakati zaidi ya muda makadirio ni tofauti kidogo na ufumbuzi halisi, kwa muda mrefu kama makosa ni chini ya 5%, ufumbuzi takriban ni kuchukuliwa halali. Katika tatizo hili, 5% inatumika kwa IF (0.15 — x) ≈ 0.15 M, hivyo kama
\[\dfrac{x}{0.15}×100\%=\dfrac{8.6×10^{−6}}{0.15}×100\%=0.006\% \nonumber \]
ni chini ya 5%, kama ilivyo katika kesi hii, dhana ni halali. Suluhisho la takriban ni suluhisho halali.
Je, ni viwango vya usawa katika ufumbuzi wa 0.25 M NH 3?
Fikiria kwamba x ni chini ya 0.25 M na uhesabu kosa katika dhana yako.
- Jibu
-
\(\ce{[OH- ]}=\ce{[NH4+]}=0.0021\:M\); [NH 3] = 0.25 M, kosa = 0.84%
Mfano wa pili inahitaji kwamba taarifa ya awali kusindika kidogo, lakini bado inaweza kutatuliwa kwa kutumia ndogo x makadirio.
Copper (II) ions huunda ion tata mbele ya amonia
\[\ce{Cu^2+}(aq)+\ce{4NH3}(aq)⇌\ce{Cu(NH3)4^2+}(aq) \hspace{20px} K_c=5.0×10^{13}=\ce{\dfrac{[Cu(NH3)4^2+]}{[Cu^2+(aq)][NH3]^4}} \nonumber \]
Ikiwa 0.010 mol Cu 2 + imeongezwa kwa 1.00 L ya suluhisho yaani 1.00 M NH 3 ni viwango gani wakati mfumo unakuja usawa?
Suluhisho Mkusanyiko wa awali wa shaba (II) ni 0.010 M. Mara kwa mara ya usawa ni kubwa sana hivyo itakuwa bora kuanza na bidhaa nyingi iwezekanavyo kwa sababu “bidhaa zote” ni karibu sana na usawa kuliko “majibu yote.” Kumbuka kuwa Cu 2 + ni reactant kikwazo; kama wote 0.010 M ya humenyuka kuunda bidhaa viwango itakuwa
\[\ce{[Cu^2+]}=0.010−0.010=0\:M \nonumber \]
\[\ce{[Cu(NH3)4^2+]}=0.010\:M \nonumber \]
\[\ce{[NH3]}=1.00−4×0.010=0.96\:M \nonumber \]
Kutumia maadili haya “yaliyobadilishwa” kama viwango vya awali na x kama mkusanyiko wa ion wa shaba (II) wa bure katika usawa hutoa meza hii ya ICE.

Tangu sisi ni mapya karibu na usawa, x lazima ndogo ili
Chagua mkusanyiko mdogo kwa utawala wa 5%.
Hii ni chini ya 5%, hivyo mawazo ni halali. Viwango katika usawa ni
Kwa kuanzia na kiwango cha juu cha bidhaa, mfumo huu ulikuwa karibu na usawa na mabadiliko (x) yalikuwa ndogo sana. Kwa mabadiliko madogo tu yanayotakiwa kupata usawa, equation kwa x ilikuwa rahisi sana na kutoa matokeo halali vizuri ndani ya kiwango cha juu cha kosa la 5%.
Je, ni viwango vya usawa wakati 0.25 mol Ni 2 + imeongezwa kwa 1.00 L ya ufumbuzi wa 2.00 M NH 3?
\[\ce{Ni^2+}(aq)+\ce{6NH3}(aq)⇌\ce{Ni(NH3)6^2+}(aq) \nonumber \]
na\(K_c=5.5×10^8\).Kwa mara kwa mara kubwa ya usawa, fomu ya kwanza kama bidhaa nyingi iwezekanavyo, kisha kudhani kuwa kiasi kidogo tu (x) cha mabadiliko ya bidhaa kushoto. Tumia hitilafu katika dhana yako.
- Jibu
-
\(\ce{[Ni(NH3)6^2+]}=0.25\:M\), [NH 3] = 0.50 M, [Ni 2 +] = 2.9 × 10 —8 M, hitilafu = 1.2 × 10 —5%
Muhtasari
Uwiano wa kiwango cha mabadiliko katika viwango vya mmenyuko ni sawa na uwiano wa coefficients katika usawa wa kemikali. Ishara ya mgawo wa X ni chanya wakati ukolezi unaongezeka na hasi wakati unapungua. Tulijifunza kukabiliana na aina tatu za msingi za matatizo ya usawa. Tunapopewa viwango vya reactants na bidhaa katika usawa, tunaweza kutatua kwa mara kwa mara ya usawa; tunapopewa mara kwa mara ya usawa na baadhi ya viwango vinavyohusika, tunaweza kutatua kwa viwango vya kukosa; na tunapopewa mara kwa mara ya usawa na viwango vya awali, tunaweza kutatua kwa viwango katika usawa.


