10.E: Liquids na Yabisi (Mazoezi)
- Page ID
- 176122
10.1: Vikosi vya Intermolecular
Q10.1.1
Kwa upande wa mali zao nyingi, vinywaji na vinywaji vinatofautiana? Je, ni sawa na jinsi gani?
S10.1.1
Liquids na yabisi ni sawa kwa kuwa ni suala linajumuisha atomi, ioni, au molekuli. Wao ni incompressible na kuwa na densities sawa ambayo ni kubwa zaidi kuliko ile ya gesi. Wao ni tofauti kwa kuwa majimaji hawana sura fasta, na yabisi ni rigid.
Q10.1.2
Kwa upande wa nadharia ya molekuli ya kinetic, kwa njia gani ni vinywaji vinavyofanana na vilivyo sawa na vikali? Kwa njia gani ni vinywaji tofauti na yabisi?
Q10.1.3
Kwa upande wa nadharia ya molekuli ya kinetic, kwa njia gani ni vinywaji sawa na gesi? Kwa njia gani ni vinywaji tofauti na gesi?
S10.1.3
Wanafanana kwa kuwa atomi au molekuli ni huru kuhamia kutoka nafasi moja hadi nyingine. Wanatofautiana kwa kuwa chembe za kioevu zimefungwa kwa sura ya chombo ambacho huwekwa. Kwa upande mwingine, gesi itapanua bila kikomo ili kujaza nafasi ambayo imewekwa.
Q10.1.4
Eleza kwa nini vinywaji huchukua sura ya chombo chochote ambacho hutiwa, wakati solids ni rigid na kuhifadhi sura yao.
Q10.1.5
Ni ushahidi gani kwamba atomi zote za neutral na molekuli hufanya nguvu za kuvutia kwa kila mmoja?
S10.1.5
Atomi zote na molekuli zitapungua ndani ya kioevu au imara ambayo nguvu za kuvutia zinazidi nishati ya kinetic ya molekuli, kwa joto la kutosha.
Q10.1.6
Fungua Phet States of Matter Simulation kujibu maswali yafuatayo:
- Chagua kichupo cha Mango, Kioevu, Gesi. Kuchunguza kwa kuchagua vitu tofauti, inapokanzwa na baridi mifumo, na kubadilisha hali. Ni sawa gani unaona kati ya vitu vinne kwa kila awamu (imara, kioevu, gesi)? Unaona tofauti gani?
- Kwa kila dutu, chagua kila moja ya majimbo na rekodi joto lililopewa. Je! Joto lililopewa kwa kila hali linahusiana na nguvu za vivutio vyao vya intermolecular? Eleza.
- Chagua kichupo cha Uwezo wa Mwingiliano, na utumie atomi za neon za Hoja atomi Ne juu ya haki na kuchunguza jinsi mabadiliko ya nishati uwezo. Chagua Jumla ya Nguvu kifungo, na hoja Ne atomi kama hapo awali. Je! Nguvu ya jumla ya kila atomi inavutia na kubwa ya kutosha? Kisha chagua kifungo cha Vikosi vya Kipengele, na uhamishe atomi ya Ne. Je, kuvutia (van der Waals) na repulsive (elektroni kuingiliana) vikosi usawa? Je, hii inahusianaje na nishati inayoweza dhidi ya umbali kati ya grafu ya atomi? Eleza.
Q10.1.7
Eleza zifuatazo na kutoa mfano wa kila mmoja:
- nguvu ya utawanyiko
- kivutio cha dipole-dipole
- hidrojeni dhamana
S10.1.7
- Vikosi vya kueneza hutokea kama atomi inakua muda wa dipole wakati elektroni zake zinasambazwa asymmetrically kuhusu kiini. Muundo huu umeenea zaidi katika atomi kubwa kama vile argoni au radoni. Atomu ya pili inaweza kisha kupotoshwa na kuonekana kwa dipole katika atomu ya kwanza. Elektroni za atomu ya pili huvutiwa kuelekea mwisho chanya wa atomu ya kwanza, ambayo huweka dipole katika atomu ya pili. Matokeo halisi yanabadilika kwa kasi, dipoles za muda ambazo huvutia kila mmoja (mfano: Ar).
- Kivutio cha dipole-dipole ni nguvu inayotokana na mvuto wa umeme wa mwisho mzuri wa molekuli moja ya polar kwa mwisho mbaya wa molekuli nyingine ya polar (mfano: molekuli za ICI huvutia kila mmoja kwa mwingiliano wa dipole-dipole).
- Vifungo vya hidrojeni huunda wakati wowote atomi ya hidrojeni inaunganishwa na atomi moja ya electronegative zaidi, kama vile florini, oksijeni, nitrojeni, au atomi ya klorini. Mvuto wa umeme kati ya atomi ya hidrojeni yenye sehemu chanya katika molekuli moja na atomi ya sehemu hasi katika molekuli nyingine hutoa mwingiliano mkali wa dipole-dipole unaoitwa dhamana ya hidrojeni (mfano:\(\mathrm{HF⋯HF}\)).
Q10.1.8
Aina za vikosi vya intermolecular katika dutu ni sawa kama ni imara, kioevu, au gesi. Kwa nini basi dutu hubadilisha awamu kutoka gesi hadi kioevu au imara?
Q10.1.9
Kwa nini pointi za kuchemsha za gesi zenye heshima zinaongezeka kwa utaratibu Yeye <Ne <Ar <Kr <Xe?
S10.1.9
Vikosi vya London kawaida huongezeka kadiri idadi ya elektroni inavyoongezeka.
Q10.1.10
Neon na HF zina takriban raia wa Masi sawa.
- Eleza kwa nini pointi za kuchemsha za Neon na HF zinatofautiana.
- Linganisha mabadiliko katika pointi za kuchemsha za Ne, Ar, Kr, na Xe na mabadiliko ya pointi za kuchemsha za HF, HCl, HbR, na HI, na kuelezea tofauti kati ya mabadiliko na kuongezeka kwa molekuli ya atomiki au Masi.
Q10.1.11
Panga kila seti zifuatazo za misombo ili kuongeza joto la kiwango cha kuchemsha:
- HCl, H 2 O, Hh 4
- F 2, Cl 2, Br 2
- CH 4, C 2 H 6, C 3 H 8
- YA 2, HAPANA, KATIKA 2
S10.1.11
(a) SiH 4 <HCl <H 2 O; (b) F 2 <Cl 2 <Br 2; (c) CH 4 <C 2 H 6 <C 3 H 8; (d) N 2 <O 2 <HAPANA
Q10.1.12
Masi ya masi ya butanoli, C 4 H 9 OH, ni 74.14; ile ya ethylene glikoli, CH 2 (OH) CH 2 OH, ni 62.08, lakini pointi zao za kuchemsha ni 117.2 °C na 174 °C, mtawalia. Eleza sababu ya tofauti.
Q10.1.13
Kwa misingi ya vivutio vya intermolecular, eleza tofauti katika pointi za kuchemsha za n —butane (-1 °C) na kloroethane (12 °C), ambazo zina raia za molar zinazofanana.
S10.1.13
Tu badala ndogo dipole-dipole mwingiliano kutoka C-H vifungo zinapatikana kwa kushikilia n -butane katika hali ya kioevu. Chloroethane, hata hivyo, ina mwingiliano mkubwa wa dipole kwa sababu ya dhamana ya Cl-C; mwingiliano huo una nguvu, na kusababisha kiwango cha juu cha kuchemsha.
Q10.1.14
Kwa misingi ya wakati wa dipole na/au kuunganisha hidrojeni, kueleza kwa njia ya ubora tofauti katika pointi za kuchemsha za asetoni (56.2 °C) na 1-propanol (97.4 °C), ambazo zina raia wa molar sawa.
Q10.1.15
Kiwango cha kuyeyuka cha H 2 O (s) ni 0 °C Je, unatarajia kiwango cha kuyeyuka cha H 2 S (s) kuwa -85 °C, 0 °C, au 185 °C? Eleza jibu lako.
S10.1.15
-85 °C Maji yana vifungo vya hidrojeni vikali hivyo huyeyuka kwenye halijoto ya juu.
Q10.1.16
Silane (SiH 4), fosfini (PH 3), na sulfidi hidrojeni (H 2 S) huyeyuka saa -185 °C, -133 °C, na -85 °C, mtawalia. Hii inaonyesha nini kuhusu tabia ya polar na vivutio vya intermolecular ya misombo mitatu?
Q10.1.17
Eleza kwa nini dhamana ya hidrojeni kati ya molekuli mbili za maji ni dhaifu kuliko dhamana ya hidrojeni kati ya molekuli mbili za flu
S10.1.17
dhamana hidrojeni kati ya molekuli mbili fluoride hidrojeni ni nguvu zaidi kuliko ile kati ya molekuli mbili maji kwa sababu electronegativity ya F ni kubwa kuliko ile ya O. Kwa hiyo, sehemu hasi malipo juu ya F ni kubwa kuliko ile ya O. dhamana hidrojeni kati ya H sehemu chanya na kubwa sehemu hasi F itakuwa na nguvu zaidi kuliko ile iliyoundwa kati ya H na O.
Q10.1.18
Katika hali fulani, molekuli ya asidi asetiki, CH 3 COOH, fomu “dimers,” jozi ya molekuli asidi asetiki uliofanyika pamoja na vivutio nguvu intermolecular:

Chora dimer ya asidi asetiki, kuonyesha jinsi mbili CH 3 COOH molekuli ni uliofanyika pamoja, na kusema aina ya IMF kwamba ni wajibu.
Q10.1.19
Protini ni minyororo ya asidi amino ambayo inaweza kuunda katika mipango mbalimbali, moja ambayo ni helix. Ni aina gani ya IMF inayohusika na kushikilia kamba ya protini katika sura hii? Kwenye picha ya protini, onyesha maeneo ya IMF ambazo zinashikilia protini pamoja:

S10.1.19
H-bonding ni kanuni IMF kufanya DNA strands pamoja. H-bonding ni kati ya\(\mathrm{N−H}\) and \(\mathrm{C=O}\).
Q10.1.20
The density of liquid NH3 is 0.64 g/mL; the density of gaseous NH3 at STP is 0.0007 g/mL. Explain the difference between the densities of these two phases.
Q10.1.21
Identify the intermolecular forces present in the following solids:
- CH3CH2OH
- CH3CH2CH3
- CH3CH2Cl
S10.1.21
(a) hydrogen bonding and dispersion forces; (b) dispersion forces; (c) dipole-dipole attraction and dispersion forces
10.2: Properties of Liquids
Q10.2.1
The test tubes shown here contain equal amounts of the specified motor oils. Identical metal spheres were dropped at the same time into each of the tubes, and a brief moment later, the spheres had fallen to the heights indicated in the illustration. Rank the motor oils in order of increasing viscosity, and explain your reasoning:
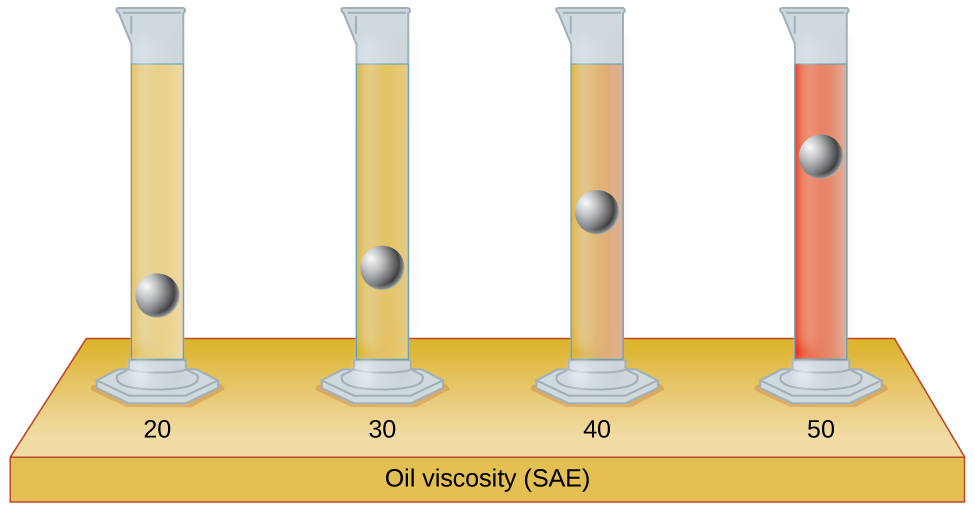
Q10.2.2
Ingawa chuma ni denser kuliko maji, sindano ya chuma au kipande cha karatasi kuwekwa kwa makini urefu juu ya uso wa maji bado inaweza kufanywa kuelea. Eleza kwa kiwango cha Masi jinsi hii inawezekana:

(mikopo: Cory Zanker)
S10.2.2
Molekuli ya maji ina nguvu za nguvu za intermolecular za kuunganisha hidrojeni. Molekuli ya maji huvutiwa sana na kuonyesha mvutano mkubwa wa uso, na kutengeneza aina ya “ngozi” kwenye uso wake. Ngozi hii inaweza kusaidia mdudu au kipande cha karatasi kama upole kuwekwa kwenye maji.
Q10.2.3
Mvutano wa uso na maadili ya viscosity kwa ether ya diethyl, acetone, ethanol, na ethylene glycol huonyeshwa hapa.
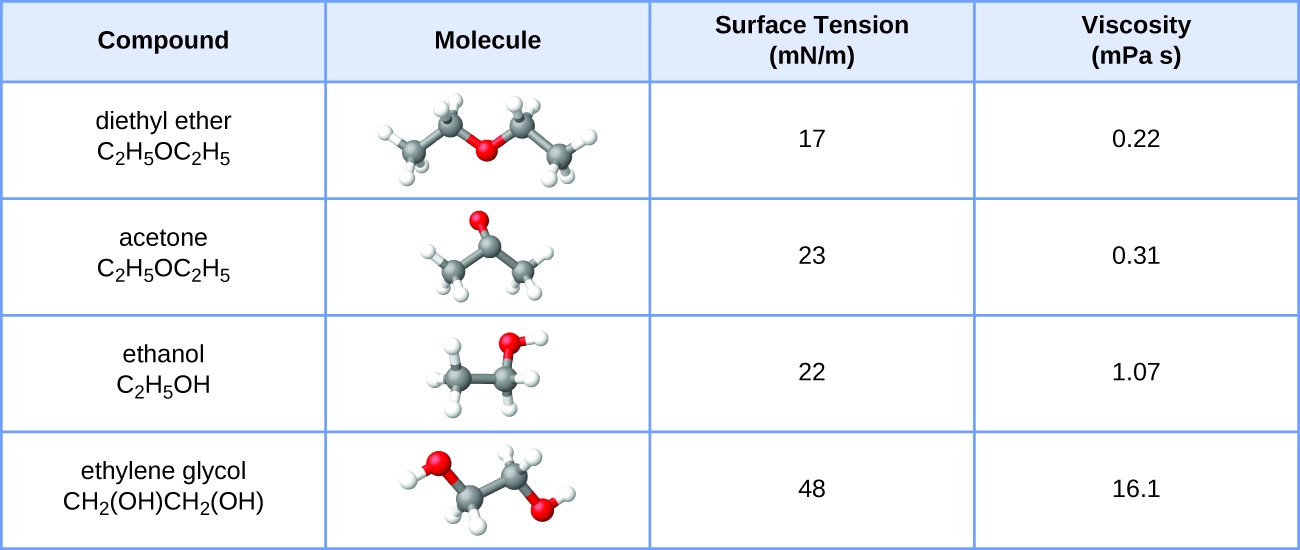
- Eleza tofauti zao katika viscosity kwa suala la ukubwa na sura ya molekuli zao na IMF zao.
- Eleza tofauti zao katika mvutano wa uso kwa suala la ukubwa na sura ya molekuli zao na IMF zao:
Q10.2.4
Huenda umesikia mtu anatumia takwimu ya hotuba “polepole kuliko molasses wakati wa baridi” kuelezea mchakato unaotokea polepole. Eleza kwa nini hii ni idiom inayofaa, kwa kutumia dhana za ukubwa wa Masi na sura, mwingiliano wa molekuli, na athari za kubadilisha joto.
S10.2.4
Joto ina athari juu ya vikosi vya intermolecular: joto la juu, nguvu kubwa ya kinetic ya molekuli na kiwango kikubwa ambacho vikosi vyao vya intermolecular vinashindwa, na hivyo maji zaidi (chini ya viscous) kioevu; chini ya joto, chini ya intermolecular vikosi ni kushinda, na hivyo chini KINATACHO kioevu.
Q10.2.5
Mara nyingi hupendekezwa kwamba unaruhusu inji yako ya gari ikimbie bila kujali ili joto kabla ya kuendesha gari, hasa siku za baridi za baridi. Wakati faida ya idling ya muda mrefu ni ya kushangaza, ni hakika kwamba inji ya joto ni ufanisi zaidi ya mafuta kuliko baridi. Eleza sababu ya hili.
Q10.2.6
Mvutano wa uso na viscosity ya maji katika joto tofauti hutolewa katika meza hii.
| Maji | Mvutano wa uso (Mn/m) | Viscosity (MPa s) |
|---|---|---|
| 0 °C | 75.6 | 1.79 |
| 20 °C | 72.8 | 1.00 |
| 60 °C | 66.2 | 0.47 |
| 100 °C | 58.9 | 0.28 |
- Kama joto linavyoongezeka, kinachotokea kwa mvutano wa uso wa maji? Eleza kwa nini hii hutokea, kwa suala la mwingiliano wa Masi na athari za kubadilisha joto.
- Kama joto linavyoongezeka, kinachotokea kwa viscosity ya maji? Eleza kwa nini hii hutokea, kwa suala la mwingiliano wa Masi na athari za kubadilisha joto.
S10.2.6
(a) Kama maji yanafikia joto la juu, nguvu za kinetic zilizoongezeka za molekuli zake zinafaa zaidi katika kushinda ushirikiano wa hidrojeni, na hivyo mvutano wake wa uso hupungua. Mvutano wa uso na majeshi ya intermolecular ni moja kwa moja (b) Mwelekeo huo katika viscosity unaonekana kama katika mvutano wa uso, na kwa sababu hiyo hiyo.
Q10.2.7
Katika 25 °C, maji yataongezeka kwa kiasi gani katika tube ya kapilari ya kioo yenye kipenyo cha ndani cha 0.63 mm? Rejea Mfano kwa taarifa zinazohitajika.
Q10.2.8
Maji huongezeka katika tube ya capillary ya kioo hadi urefu wa cm 17. Je, ni kipenyo cha tube ya capillary?
S10.2.8
9.5 × 10 -5 m
10.3: Mabadiliko ya Awamu
Q10.3.1
Joto huongezwa kwa maji ya moto. Eleza kwa nini joto la maji ya moto halibadilika. Je, mabadiliko gani?
Q10.3.2
Joto linaongezwa kwa barafu kwenye 0 °C Eleza kwa nini halijoto la barafu halibadilika. Je, mabadiliko gani?
S10.3.2
Joto linafyonzwa na barafu, kutoa nishati inayohitajika kuondokana na vikosi vya kuvutia vya intermolecular katika imara na kusababisha mabadiliko ya awamu kwa maji ya kioevu. Suluhisho linabaki saa 0 °C hadi barafu yote ikayeyuka. Ni kiasi tu cha maji kilichopo kama barafu kinabadilika hadi barafu kutoweka. Kisha joto la maji linaweza kuongezeka.
Q10.3.3
Ni kipengele gani kinachofafanua usawa wa nguvu kati ya kioevu na mvuke wake katika chombo kilichofungwa?
Q10.3.4
Tambua uchunguzi wawili wa kawaida unaoonyesha baadhi ya vinywaji vina shinikizo la kutosha la mvuke ili kuenea kwa kiasi kikubwa?
S10.3.4
Tunaweza kuona kiasi cha kioevu katika chombo kilicho wazi kinapungua na tunaweza kunuka harufu ya vinywaji vingine.
Q10.3.5
Kutambua mbili uchunguzi wa kawaida kuonyesha baadhi yabisi, kama vile barafu kavu na mothballs, na mvuke shinikizo kutosha tukufu?
Q10.3.6
Ni uhusiano gani kati ya vikosi vya intermolecular katika kioevu na shinikizo lake la mvuke?
S10.3.7
Shinikizo la mvuke la kioevu hupungua kama nguvu za vikosi vyake vya intermolecular huongezeka.
Q10.3.7
Ni uhusiano gani kati ya vikosi vya intermolecular katika joto kali na kiwango chake?
Q10.3.8
Kwa nini petroli iliyomwagika hupuka kwa kasi zaidi siku ya moto kuliko siku ya baridi?
S10.3.8
Kama joto linavyoongezeka, wastani wa nishati ya kinetic ya molekuli ya petroli huongezeka na hivyo sehemu kubwa ya molekuli zina nishati ya kutosha kutoroka kutoka kiowevu kuliko joto la chini.
Q10.3.9
Tetrakloridi ya kaboni, cCl 4, mara moja ilitumiwa kama kutengenezea kavu ya kusafisha, lakini haitumiwi tena kwa sababu ni kansa. Katika 57.8 °C, shinikizo la mvuke la cCl 4 ni 54.0 kPa, na enthalpy yake ya uvukizi ni 33.05 kJ/mol. Tumia habari hii ili kukadiria kiwango cha kawaida cha kuchemsha kwa cCl 4.
Q10.3.10
Je! Ni wakati gani wa kuchemsha wa kioevu sawa na kiwango chake cha kawaida cha kuchemsha?
S10.3.10
Wakati shinikizo la gesi juu ya kioevu ni hasa 1 atm
Q10.3.11
Je, kuchemsha kwa kioevu hutofautiana na uvukizi wake?
Q10.3.12
Tumia habari katika Kielelezo ili kukadiria kiwango cha kuchemsha cha maji huko Denver wakati shinikizo la anga ni 83.3 kPa.
S10.3.12
takriban 95 °C
Q10.3.13
Sindano kwenye halijoto ya 20 °C imejaa ether kiowevu kwa namna ambayo hakuna nafasi kwa mvuke wowote. Ikiwa hali ya joto huhifadhiwa mara kwa mara na plunger huondolewa ili kuunda kiasi ambacho kinaweza kuingizwa na mvuke, ni nini shinikizo la karibu la mvuke zinazozalishwa?
Q10.3.14
Eleza uchunguzi wafuatayo:
- Inachukua muda mrefu kupika yai katika Ft. Davis, Texas (urefu, 5000 miguu juu ya usawa wa bahari) kuliko ilivyo katika Boston (katika usawa wa bahari).
- Kujitokeza ni utaratibu wa kuimarisha mwili.
S10.3.14
(a) Kwa miguu 5000, shinikizo la anga ni la chini kuliko usawa wa bahari, na maji yatapika kwa joto la chini. Joto hili la chini litasababisha mabadiliko ya kimwili na kemikali yanayohusika katika kupikia yai ili kuendelea polepole zaidi, na muda mrefu unahitajika kupika kikamilifu yai. (b) Kwa muda mrefu kama hewa inayozunguka mwili ina mvuke mdogo wa maji kuliko kiwango cha juu ambacho hewa inaweza kushikilia kwenye joto hilo, jasho litaenea, na hivyo kuimarisha mwili kwa kuondoa joto la uvukizi linalohitajika kuvukiza maji.
Q10.3.15
Enthalpy ya mvuke ya maji ni kubwa kuliko enthalpy yake ya fusion. Eleza kwa nini.
Q10.3.16
Eleza kwa nini enthalpies ya molar ya uvukizi wa dutu zifuatazo huongezeka kwa utaratibu CH 4 <C 2 H 6 <C 3 H 8, ingawa vitu vyote vitatu hupata majeshi sawa ya utawanyiko wakati wa hali ya kioevu.
S10.3.16
Majeshi ya utawanyiko huongezeka kwa molekuli au ukubwa wa Masi. Kama idadi ya atomi inayojumuisha molekuli katika mfululizo huu wa homologous huongezeka, ndivyo kiwango cha kivutio cha intermolecular kupitia vikosi vya utawanyiko na, kwa hiyo, nishati inayotakiwa kuondokana na majeshi haya na kuvukiza majimaji.
Q10.3.17
Eleza kwa nini enthalpies ya uvukizi wa dutu zifuatazo huongezeka kwa utaratibu CH 4 <NH 3 <H 2 O, ingawa vitu vyote vitatu vina takriban molekuli sawa ya molar.
Q10.3.18
Enthalpy ya uvukizi wa CO 2 (l) ni 9.8 kJ/mol. Je, unatarajia enthalpy ya uvukizi wa CS 2 (l) kuwa 28 kJ/mol, 9.8 kJ/mol, au -8.4 kJ/mol? Jadili uwezekano wa kila moja ya majibu haya.
S10.3.18
Kiwango cha kuchemsha cha CS 2 ni cha juu kuliko ile ya CO 2 kwa sababu ya uzito wa juu wa Masi ya CS 2; kwa hiyo, nguvu za kuvutia zina nguvu katika CS 2. Kwa hiyo, itatarajiwa kwamba joto la uvukizi litakuwa kubwa zaidi kuliko ile ya 9.8 kJ/mol kwa CO 2. thamani ya 28 KJ/mol inaweza kuonekana busara. Thamani ya -8.4 kJ/mol ingeonyesha kutolewa kwa nishati juu ya uvukizi, ambayo ni wazi implausible.
Q10.3.19
Molekuli ya fluoride ya hidrojeni, HF, ni polar zaidi kuliko molekuli ya maji, H 2 O (kwa mfano, ina muda mkubwa wa dipole), lakini enthalpy ya molar ya mvuke kwa fluoride ya hidrojeni kioevu ni mdogo kuliko ile ya maji. Eleza.
Q10.3.20
Kloridi ya ethyl (kiwango cha kuchemsha, 13 °C) hutumiwa kama anesthetic ya ndani. Wakati kioevu kinachopunjwa kwenye ngozi, kinapunguza ngozi ya kutosha kufungia na kuifuta. Eleza athari ya baridi ya kloridi ya ethyl kioevu.
S10.3.20
Nishati ya joto (joto) inahitajika kuenea kioevu huondolewa kwenye ngozi.
Q10.3.21
Ambayo ina misombo iliyoorodheshwa kwa usahihi ili kuongeza pointi za kuchemsha?
- N 2 <CS 2 <H 2 O <KCl
- H 2 O <N 2 <C 2 <KCl
- N 2 <KCl <CS 2 <H 2 O
- CS 2 <N 2 <KCl <H 2 O
- KCl <H 2 O <CS 2 <N 2
Q10.3.22
Kiasi gani cha joto kinahitajika kubadili 422 g ya kiowevu H 2 O saa 23.5 °C kuwa mvuke kwenye 150 °C?
S10.3.22
1130 kJ
Q10.3.22
Uvukizi wa jasho unahitaji nishati na hivyo kuchukua joto kali mbali na mwili. Baadhi ya maji kwamba kunywa inaweza hatimaye kuwa waongofu katika jasho na kuyeyuka. Ikiwa unywa chupa ya maji ya aunsi 20 iliyokuwa kwenye jokofu saa 3.8 °C, ni kiasi gani cha joto kinahitajika ili kubadilisha maji hayo yote kuwa jasho halafu kuwa mvuke?? (Kumbuka: Joto lako la mwili ni 36.6 °C Kwa kusudi la kutatua tatizo hili, kudhani kuwa mali ya joto ya jasho ni sawa na kwa maji.)
Q10.3.24
Titanium tetrakloridi, TiCl 4, ina kiwango cha kuyeyuka cha -23.2 °C na ina fusion Δ H = 9.37 kJ/mol.
- Ni kiasi gani cha nishati kinachohitajika kuyeyuka 263.1 g TiCl 4?
- Kwa TiCl 4, ambayo inawezekana kuwa na ukubwa mkubwa: Δ H fusion au Δ H vaporization? Eleza hoja zako.
S10.3.24
(a) 13.0 kJ; (b) Inawezekana kwamba joto la uvukizi litakuwa na ukubwa mkubwa kwani katika kesi ya uvukizi mwingiliano wa intermolecular unapaswa kushinda kabisa, huku kuyeyuka kunapunguza au kuharibu baadhi yao tu.
10.4: Mipango ya Awamu
Q10.4.1
Kutoka kwenye mchoro wa awamu ya maji, tambua hali ya maji katika:
- 35 °C na 85 kPa
- -15 °C na 40 kPa
- -15 °C na 0.1 kPa
- 75 °C na 3 kPa
- 40 °C na 0.1 kPa
- 60 °C na 50 kPa
Q10.4.2
Ni mabadiliko gani ya awamu yatakayofanyika wakati maji yanakabiliwa na shinikizo tofauti kwenye joto la mara kwa mara la 0.005 °C? Katika 40 °C? Saa -40 °C?
S10.4.2
Kwa shinikizo la chini na 0.005 °C, maji ni gesi. Kama shinikizo linavyoongezeka hadi 4.6 torr, maji huwa imara; kama shinikizo linavyoongezeka zaidi, inakuwa kioevu. Katika 40 °C, maji kwenye shinikizo la chini ni mvuke; kwa shinikizo la juu kuliko takriban 75 torr, inabadilika kuwa kiowevu. Kwenye -40 °C, maji huenda kutoka gesi hadi imara kadiri shinikizo linavyoongezeka juu ya maadili ya chini sana.
Q10.4.3
Wapishi wa shinikizo huruhusu chakula kupika kwa kasi kwa sababu shinikizo la juu ndani ya jiko la shinikizo huongeza joto la kuchemsha la maji. Mpikaji fulani wa shinikizo ana valve ya usalama ambayo imewekwa kwa vent mvuke ikiwa shinikizo linazidi 3.4 atm. Je, ni kiwango cha juu cha joto ambacho kinaweza kufikiwa ndani ya jiko hili la shinikizo? Eleza hoja zako.
Q10.4.4
Kutoka kwenye mchoro wa awamu ya dioksidi kaboni, tambua hali ya CO 2 katika:
- 20 °C na 1000 kPa
- 10 °C na 2000 kPa
- 10 °C na 100 kPa
- -40 °C na 500 kPa
- -80 °C na 1500 kPa
- -80 °C na 10 kPa

Shinikizo na joto la shaba kwenye mchoro huu wa awamu ya dioksidi kaboni haipatikani kwa kiwango cha mara kwa mara ili kuonyesha mali kadhaa muhimu.
S10.4.4
(a) kioevu; (b) imara; (c) gesi; (d) gesi; (e) gesi; (f) gesi
Q10.4.5
Kuamua mabadiliko ya awamu ambayo dioksidi kaboni hupitia kama shinikizo linabadilika ikiwa halijoto inafanyika saa -50 °C? Ikiwa hali ya joto inafanyika saa -40 °C? Katika 20 °C?

Shinikizo na joto la shaba kwenye mchoro huu wa awamu ya dioksidi kaboni haipatikani kwa kiwango cha mara kwa mara ili kuonyesha mali kadhaa muhimu.
Q10.4.6
Fikiria silinda iliyo na mchanganyiko wa dioksidi kaboni kioevu katika usawa na dioksidi kaboni ya gesi kwenye shinikizo la awali la atm 65 na joto la 20 °C Mchoro njama inayoonyesha mabadiliko katika shinikizo la silinda na wakati kama dioksidi kaboni ya gesi inatolewa kwa joto la mara kwa mara.
S10.4.6

Q10.4.7
Barafu kavu, CO 2 (s), haina kuyeyuka kwenye shinikizo la anga. Ni sublimes katika halijoto ya -78 °C Je, ni shinikizo la chini kabisa ambalo CO 2 (s) itayeyuka ili kutoa CO 2 (l) nini? Kwa takriban joto gani hili litatokea? (Angalia Mchoro kwa mchoro wa awamu.)
S10.4.7
Barafu kavu, CO 2 (s), itayeyuka ili kutoa CO 2 (l) saa 5.11 atm saa -56.6 °C, hatua tatu ya dioksidi kaboni.
Q10.4.8
Ikiwa dhoruba kali husababisha kupoteza umeme, inaweza kuwa muhimu kutumia nguo ya nguo ili kukausha kufulia. Katika sehemu nyingi za nchi katika wafu wa majira ya baridi, nguo zitafungia haraka wakati zimefungwa kwenye mstari. Ikiwa haina theluji, je, watauka hata hivyo? Eleza jibu lako.
S10.4.8
Ndiyo, barafu itakuwa nzuri, ingawa inaweza kuchukua siku kadhaa. Ice ina shinikizo dogo la mvuke, na baadhi ya molekuli za barafu huunda gesi na kutoroka kutoka fuwele za barafu. Wakati unapopita, zaidi na zaidi imara hubadilisha gesi hadi hatimaye nguo zime kavu.
Q10.4.9
Inawezekana kunyunyiza nitrojeni kwenye joto la kawaida (karibu 25 °C)? Inawezekana kuondokana na dioksidi ya sulfuri kwenye joto la kawaida? Eleza majibu yako.
Q10.4.10
Kaboni ya msingi ina awamu moja ya gesi, awamu moja ya kioevu, na awamu tatu tofauti imara, kama inavyoonekana katika mchoro wa awamu:
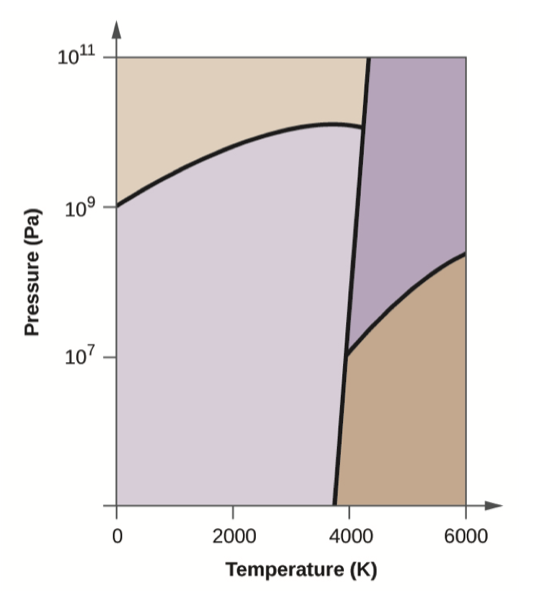
- Katika mchoro wa awamu, lebo ya mikoa ya gesi na kioevu.
- Graphite ni awamu imara zaidi ya kaboni katika hali ya kawaida. Katika mchoro wa awamu, lebo ya awamu ya grafiti.
- Kama grafiti katika hali ya kawaida ni joto kwa 2500 K wakati shinikizo ni kuongezeka kwa 10 10 Pa, ni waongofu kuwa almasi. Weka awamu ya almasi.
- Mzunguko kila hatua tatu kwenye mchoro wa awamu.
- Katika awamu gani kaboni iko katika 5000 K na 10 8 Pa?
- Ikiwa joto la sampuli ya kaboni huongezeka kutoka 3000 K hadi 5000 K kwa shinikizo la mara kwa mara la 10 6 Pa, ni mabadiliko gani ya awamu hutokea, ikiwa kuna?
10.5: Hali imara ya Suala
Q10.5.1
Ni aina gani za vinywaji kawaida huunda solidi za amofasi?
S10.5.1
Vipu vya amorphous hawana muundo wa ndani ulioamuru. Vifaa vya kiowevu ambavyo vina molekuli kubwa, mbaya ambazo haziwezi kuhamia kwa urahisi katika nafasi zilizoamriwa kwa ujumla huunda yabisi vile.
Q10.5.2
Katika joto la chini sana oksijeni, O 2, hufungua na hufanya imara ya fuwele. Ambayo bora inaelezea fuwele hizi?
- ioniki
- mtandao wa covalent
- metali
- kidude
- fuwele za molekuli
S10.5.3
(e) fuwele za molekuli
Q10.5.4
Kama inavyozidi, mafuta ya mzeituni huimarisha polepole na hufanya imara juu ya joto mbalimbali. Ambayo bora inaelezea imara?
- ioniki
- mtandao wa covalent
- metali
- kidude
- fuwele za molekuli
S10.5.4
(d) amofasi
Q10.5.5
Eleza kwa nini barafu, ambayo ni imara ya fuwele, ina joto la kuyeyuka la 0 °C, ilhali siagi, ambayo ni imara ya amofasi, hupunguza juu ya joto mbalimbali.
S10.5.6
Ice ina muundo fuwele imetulia na bonding hidrojeni. Majeshi haya ya intermolecular yana nguvu sawa na hivyo yanahitaji kiasi sawa cha nishati kushinda. Matokeo yake, barafu hutengana kwa joto moja na sio juu ya joto la aina mbalimbali. Mbalimbali, kubwa sana molekuli kwamba kutunga siagi uzoefu mbalimbali van der Waals vivutio ya nguvu mbalimbali kwamba ni kushinda katika joto mbalimbali, na hivyo mchakato wa kuyeyuka hutokea juu ya mbalimbali joto mbalimbali.
Q10.5.7
Tambua aina ya fuwele imara (metali, mtandao covalent, ionic, au Masi) iliyoundwa na kila moja ya vitu vifuatavyo:
- ISO 2
- KCl
- Cu
- CO 2
- C (almasi)
- Baso 4
- NH 3
- NH 4 F
- C 2 H 5 OH
S10.5.7
(a) SiO 2, mtandao wa covalent; (b) kCl, ionic; (c) Cu, metali; (d) CO, Masi; (e) C (almasi), mtandao wa covalent; (f) BaSO 4, ionic; (g) NH 3, Masi; (h) NH 4 F, ionic; (i) C 2 H 5 OH, Masi
Q10.5.8
Tambua aina ya fuwele imara (metali, mtandao covalent, ionic, au Masi) iliyoundwa na kila moja ya vitu vifuatavyo:
- CaCl 2
- sic
- N 2
- Fe
- C (grafiti)
- CH 3 CH 2 CH 2 CH 3
- HCl
- NH 4 NO 3
- K 3 PO 4
S10.5.8
(a) CaCl 2, ionic; (b) sic, mtandao wa covalent; (c) N 2, Masi; (d) Fe, chuma; (e) C (grafiti), mtandao wa covalent; (f) CH 3 CH 2 CH 2 CH 3, Masi; (g) HCl, Masi; (h) NH 4 NO 3, ionic; (i) K 3 PO 4, ionic
Q10.5.9
Kuainisha kila dutu katika meza kama ama metali, ionic, Masi, au covalent mtandao imara:
| Dutu | Uonekano | kiwango cha kuyeyuka | Uendeshaji wa Umeme | Umumunyifu katika Maji |
|---|---|---|---|---|
| X | yenye kung'aa, isiyoweza kuharibika | 1500 °C | juu | isiyoweza kutatuliwa |
| Y | laini, njano | 113 °C | hakuna | isiyoweza kutatuliwa |
| Z | ngumu, nyeupe | 800 °C | tu ikiwa imeyeyuka/kufutwa | mumunyifu |
S10.5.9
X = metali; Y = mtandao wa covalent; Z = ionic
Q10.5.10
Kuainisha kila dutu katika meza kama ama metali, ionic, Masi, au covalent mtandao imara:
| Dutu | Uonekano | kiwango cha kuyeyuka | Uendeshaji wa Umeme | Umumunyifu katika Maji |
|---|---|---|---|---|
| X | brittle, nyeupe | 800 °C | tu ikiwa imeyeyuka/kufutwa | mumunyifu |
| Y | shiny, isiyoweza kuharibika | 1100 °C | juu | isiyoweza kutatuliwa |
| Z | ngumu, isiyo rangi | 3550 °C | hakuna | isiyoweza kutatuliwa |
S10.5.10
X = ionic; Y = metali; Z = mtandao wa covalent
Q10.5.11
Tambua vitu vifuatavyo kama ionic, metali, mtandao wa covalent, au yabisi ya Masi:
Dutu A ni ya kuyeyuka, ductile, inafanya umeme vizuri, na ina kiwango cha kuyeyuka ya 1135 °C Dutu B ni brittle, haifanyi umeme kama imara lakini hufanya wakati wa kuyeyuka, na ina kiwango cha kuyeyuka cha 2072 °C Dutu C ni ngumu sana, haifanyi umeme, na ina kiwango cha kuyeyuka cha 3440 °C. Dutu D ni laini, haifanyi umeme, na ina kiwango cha kuyeyuka cha 185 °C.
S10.5.11
A = metali; B = ionic; C = mtandao wa covalent; D = Masi
Q10.5.12
Dutu A ni shiny, hufanya umeme vizuri, na huyeyuka kwenye 975 °C Dutu A inawezekana a (n):
- ionic imara
- metali imara
- Masi imara
- covalent mtandao imara
S10.5.12
(b) chuma imara
Q10.5.13
Dutu B ni ngumu, haifanyi umeme, na huyeyuka kwenye 1200 °C Dutu B ni uwezekano a (n):
- ionic imara
- metali imara
- Masi imara
- covalent mtandao imara
S10.5.13
(d) mtandao wa covalent imara
10.6: Miundo ya bandia
Q10.6.1
Eleza muundo wa kioo wa chuma, ambayo huangaza na atomi mbili za chuma sawa katika kiini cha kitengo cha ujazo.
S10.6.1
Muundo wa aina hii ya chini-joto ya chuma (chini ya 910 °C) ni ujazo unaozingatia mwili. Kuna atomi moja ya nane kwenye kila pembe nane za mchemraba na atomi moja katikati ya mchemraba.
Q10.6.2
Eleza muundo wa kioo wa Pt, ambayo huangaza na atomi nne za chuma sawa katika kiini cha kitengo cha ujazo.
Q10.6.3
Nambari ya uratibu wa atomi ya chromium ni nini katika muundo wa ujazo wa chromium unaozingatia mwili?
S10.6.3
nane
Q10.6.4
Ni nambari gani ya uratibu wa atomi ya alumini katika muundo wa ujazo wa uso wa alumini?
Q10.6.5
Cobalt chuma crystallizes katika hexagonal karibu packed muundo. Nambari ya uratibu wa atomi ya cobalt ni nini?
S10.6.5
12
Q10.6.6
Nickel chuma crystallizes katika ujazo karibu packed muundo. Nambari ya uratibu wa atomi ya nickel ni nini?
Q10.6.7
Tungsten crystallizes katika mwili unaozingatia cubic kitengo kiini na makali urefu wa 3.165 Å.
- Je, ni radius ya atomiki ya tungsten katika muundo huu?
- Tumia wiani wa tungsten.
S10.6.7
(a) 1.370 Å; (b) 19.26 g/sentimita
Q10.6.8
Platinum (atomiki radius = 1.38 Å) crystallizes katika ujazo karibu packed muundo. Tumia urefu wa makali ya kiini cha kitengo cha ujazo cha uso na wiani wa platinamu.
Q10.6.9
Bariamu huganda katika kiini cha kitengo cha ujazo cha mwili na urefu wa makali ya 5.025
- Je, ni radius ya atomiki ya bariamu katika muundo huu?
- Tumia wiani wa bariamu.
S10.6.9
(a) 2.176 Å; (b) 3.595 g/cm 3
Q10.6.10
Aluminium (atomiki radius = 1.43 Å) crystallizes katika ujazo karibu packed muundo. Tumia urefu wa makali ya kiini cha kitengo cha ujazo cha uso na wiani wa alumini.
Q10.6.11
Uzito wa alumini ni 2.7 g/cm 3; ile ya silicon ni 2.3 g/cm 3. Eleza kwa nini Si ina wiani wa chini ingawa ina atomi nzito.
S10.6.11
Muundo wa kioo wa Si unaonyesha kuwa ni chini tightly packed (uratibu namba 4) katika imara kuliko Al (uratibu namba 12).
Q10.6.12
Sehemu ya bure katika chuma inaweza kupatikana kwa kuondoa kiasi cha atomi katika kiini cha kitengo kutoka kwa kiasi cha seli. Tumia asilimia ya nafasi ya bure katika kila moja ya lattices tatu za ujazo ikiwa atomi zote katika kila moja zina ukubwa sawa na kugusa majirani zao wa karibu. Ni ipi kati ya miundo hii inawakilisha kufunga kwa ufanisi zaidi? Hiyo ni, ni pakiti gani zilizo na kiasi kidogo cha nafasi isiyoyotumiwa?
Q10.6.13
Cadmium sulfidi, wakati mwingine kutumika kama rangi ya njano na wasanii, crystallizes na cadmium, wanaomiliki nusu ya mashimo tetrahedral katika safu karibu packed ya ions sulfidi. Nini formula ya sulfidi ya cadmium? Eleza jibu lako.
S10.6.13
Katika safu iliyojaa karibu, mashimo mawili ya tetrahedral yanapo kwa kila anion. Ikiwa nusu tu ya mashimo ya tetrahedral huchukua, idadi ya anions na cations ni sawa. Fomu ya sulfidi ya cadmium ni CD.
Q10.6.14
Kiwanja cha cadmium, bati, na fosforasi hutumiwa katika utengenezaji wa baadhi ya semiconductors. Ni crystallizes na cadmium wanaomiliki moja ya nne ya mashimo tetrahedral na bati kuchukua moja ya nne ya mashimo tetrahedral katika karibu packed safu ya ions phosphide. Nini formula ya kiwanja? Eleza jibu lako.
Q10.6.15
Je, ni formula ya oksidi magnetic ya cobalt, kutumika katika kurekodi kanda, ambayo crystallizes na atomi cobalt wanaomiliki moja ya nane ya mashimo tetrahedral na nusu ya mashimo octahedral katika safu karibu packed ya ioni oksidi?
S10.6.15
Co 3 Ya 4
Q10.6.16
Kiwanja kilicho na zinki, alumini, na sulfuri huangaza na safu ya karibu ya ions za sulfidi. Ions zinki hupatikana katika moja ya nane ya mashimo ya tetrahedral na ions alumini katika nusu moja ya mashimo ya octahedral. Je, ni formula ya maandishi ya kiwanja?
Q10.6.17
Kiwanja cha thalliamu na iodini huangaza katika safu rahisi za ujazo wa ioni za iodidi na ioni za thalliamu katika mashimo yote ya ujazo. Nini formula ya iodidi hii? Eleza jibu lako.
S10.6.17
Katika safu rahisi za ujazo, shimo moja tu la ujazo linaweza kuchukuliwa kuwa cation kwa kila anion katika safu. Uwiano wa thalliamu kwa iodidi lazima iwe 1:1; kwa hiyo, formula ya thalliamu ni tLi.
Q10.6.18
Ni ipi kati ya mambo yafuatayo humenyuka na sulfuri kuunda imara ambayo atomi za sulfuri huunda safu iliyojaa karibu na mashimo yote ya octahedral ulichukua: Li, Na, Be, Ca, au Al?
Q10.6.19
Je, ni asilimia kwa wingi wa titani katika rutile, madini ambayo ina titanium na oksijeni, kama muundo inaweza kuelezwa kama karibu packed safu ya ions oksidi na ions titanium katika nusu ya mashimo octahedral? Nambari ya oxidation ya titani ni nini?
S10.6.19
59.95%; Idadi ya oxidation ya titani ni +4.
Q10.6.20
Eleza kwa nini kloridi za chuma za alkali zinazofanana na kemikali NaCl na CsCl zina miundo tofauti, wakati NaCl na MNs tofauti za kemikali zina muundo sawa.
Q10.6.21
Kama madini yalitengenezwa kutoka magma iliyoyeyuka, ions tofauti zilichukua cites sawa katika fuwele. Lithiamu mara nyingi hutokea pamoja na magnesiamu katika madini licha ya tofauti katika malipo kwenye ions zao. Pendekeza maelezo.
S10.6.21
Ions zote mbili ni karibu na ukubwa: Mg, 0.65; Li, 0.60. Ufanana huu unaruhusu mbili kubadilishana badala ya urahisi. Tofauti katika malipo kwa ujumla hulipwa kwa kubadili Si 4+ kwa Al 3+.
Q10.6.22
Iodidi ya Rubidium huangaza na kiini cha kitengo cha ujazo ambacho kina ioni za iodidi kwenye pembe na ion ya rubidium katikati. Nini formula ya kiwanja?
Q10.6.23
Moja ya oksidi mbalimbali za manganese huangaza na kiini cha kitengo cha ujazo ambacho kina ions za manganese kwenye pembe na katikati. Ions ya oksidi iko katikati ya kila makali ya kiini cha kitengo. Nini formula ya kiwanja?
S10.6.23
Mtu - 2 ya 3
Q10.6.24
NaH crystallizes na muundo huo kioo kama NaCl. Urefu wa makali ya kiini cha kitengo cha ujazo cha NaH ni 4.880 Å.
- Tumia radius ionic ya H -. (Radius ionic ya Li + ni 0.0.95 Å.)
- Tumia wiani wa NaH.
Q10.6.25
Thallium (I) iodidi huangaza na muundo sawa na CsCl. Urefu wa makali ya kiini cha kitengo cha TLi ni 4.20 Å. Tumia radius ionic ya TI +. (Radius ionic ya I - ni 2.16 Å.)
S10.6.25
1.48 SAA
Q10.6.26
Kiini cha kitengo cha ujazo kina ioni za manganese kwenye pembe na ioni za fluoride katikati ya kila makali.
- Nini formula ya kimapenzi ya kiwanja hiki? Eleza jibu lako.
- Nambari ya uratibu wa ion ya Mn 3+ ni nini?
- Tumia urefu wa makali ya kiini cha kitengo ikiwa radius ya ion Mn 3+ ni 0.65 A.
- Tumia wiani wa kiwanja.
Q10.6.27
Je, ni nafasi gani kati ya ndege za kioo ambazo hutenganisha X-rays na wavelength ya 1.541 nm kwa angle ρ ya 15.55° (tafakari ya kwanza ya utaratibu)?
S10.6.27
2.874 SAA
Q10.6.28
Diffractometer kwa kutumia eksirei na wavelength ya 0.2287 nm zinazozalishwa kilele cha kwanza cha diffraction kwa angle ya kioo ρ = 16.21°. Kuamua nafasi kati ya ndege diffracting katika kioo hii.
Q10.6.29
Chuma na nafasi kati ya ndege sawa na 0.4164 nm inatofautiana na X-rays na wavelength ya 0.2879 nm. Je, ni angle ya diffraction kwa kilele cha kwanza cha diffraction?
S10.6.29
20.2°
Q10.6.30
Dhahabu huangaza katika kiini cha kitengo cha ujazo cha uso. Kutafakari kwa pili (n = 2) ya X-rays kwa ndege zinazounda vichwa na vifungo vya seli za kitengo ni saa ρ = 22.20°. Urefu wa X-rays ni 1.54 Å. Uzito wa dhahabu ya metali ni nini?
Q10.6.31
Wakati elektroni katika atomi ya molybdenum yenye msisimko huanguka kutoka L hadi kwenye shell ya K, X-ray inatolewa. Radi hizi za eksirei zinatenganishwa kwa pembe ya 7.75° kwa ndege zenye kutengana kwa 2.64 Å. Ni tofauti gani kati ya nishati kati ya shell K na shell L katika molybdenum kuchukua diffraction ya kwanza ya utaratibu?
S10.6.31
1.74 × 10 4 eV


