37.3: Regulação dos processos corporais
- Page ID
- 182009
Habilidades para desenvolver
- Explique como os hormônios regulam o sistema excretor
- Discuta o papel dos hormônios no sistema reprodutivo
- Descreva como os hormônios regulam o metabolismo
- Explicar o papel dos hormônios em diferentes doenças
Os hormônios têm uma ampla gama de efeitos e modulam muitos processos corporais diferentes. Os principais processos regulatórios que serão examinados aqui são aqueles que afetam o sistema excretor, o sistema reprodutivo, o metabolismo, as concentrações de cálcio no sangue, o crescimento e a resposta ao estresse.
Regulação hormonal do sistema excretor
Manter um equilíbrio hídrico adequado no corpo é importante para evitar a desidratação ou a superexidratação (hiponatremia). A concentração de água no corpo é monitorada por osmorreceptores no hipotálamo, que detectam a concentração de eletrólitos no fluido extracelular. A concentração de eletrólitos no sangue aumenta quando há perda de água causada por transpiração excessiva, ingestão inadequada de água ou baixo volume sanguíneo devido à perda de sangue. Um aumento nos níveis de eletrólitos no sangue resulta no envio de um sinal neuronal pelos osmorreceptores nos núcleos hipotalâmicos. A glândula pituitária tem dois componentes: anterior e posterior. A hipófise anterior é composta por células glandulares que secretam hormônios proteicos. A hipófise posterior é uma extensão do hipotálamo. É composto em grande parte por neurônios que são contínuos com o hipotálamo.
O hipotálamo produz um hormônio polipeptídico conhecido como hormônio antidiurético (ADH), que é transportado e liberado da glândula pituitária posterior. A principal ação do ADH é regular a quantidade de água excretada pelos rins. Como o ADH (também conhecido como vasopressina) causa reabsorção direta de água dos túbulos renais, os sais e resíduos se concentram no que eventualmente será excretado como urina. O hipotálamo controla os mecanismos de secreção de ADH, seja regulando o volume sanguíneo ou a concentração de água no sangue. A desidratação ou o estresse fisiológico podem causar um aumento da osmolaridade acima de 300 mOsm/L, o que, por sua vez, aumenta a secreção de ADH e a água será retida, causando um aumento na pressão arterial. O ADH viaja na corrente sanguínea até os rins. Uma vez nos rins, o ADH transforma os rins para se tornarem mais permeáveis à água, inserindo temporariamente canais de água, aquaporinas, nos túbulos renais. A água sai dos túbulos renais através das aquaporinas, reduzindo o volume de urina. A água é reabsorvida pelos capilares, reduzindo a osmolaridade do sangue ao normal. À medida que a osmolaridade sanguínea diminui, um mecanismo de feedback negativo reduz a atividade dos osmorreceptores no hipotálamo e a secreção de ADH é reduzida. A liberação de ADH pode ser reduzida por certas substâncias, incluindo álcool, que podem causar aumento da produção de urina e desidratação.
A subprodução crônica de ADH ou uma mutação no receptor de ADH resulta em diabetes insípido. Se a hipófise posterior não liberar ADH suficiente, a água não pode ser retida pelos rins e é perdida como urina. Isso causa aumento da sede, mas a água absorvida é perdida novamente e deve ser consumida continuamente. Se a condição não for grave, a desidratação pode não ocorrer, mas casos graves podem levar a desequilíbrios eletrolíticos devido à desidratação.
Outro hormônio responsável por manter as concentrações de eletrólitos nos fluidos extracelulares é a aldosterona, um hormônio esteróide produzido pelo córtex adrenal. Em contraste com o ADH, que promove a reabsorção de água para manter o equilíbrio hídrico adequado, a aldosterona mantém o equilíbrio hídrico adequado, aumentando a reabsorção de Na+ e a secreção de K + do fluido extracelular das células nos túbulos renais. Por ser produzida no córtex da glândula adrenal e afetar as concentrações dos minerais Na + e K +, a aldosterona é conhecida como mineralocorticóide, um corticosteróide que afeta o equilíbrio de íons e água. A liberação de aldosterona é estimulada por uma diminuição nos níveis de sódio no sangue, volume ou pressão arterial, ou um aumento nos níveis de potássio no sangue. Também evita a perda de Na + do suor, saliva e suco gástrico. A reabsorção de Na + também resulta na reabsorção osmótica da água, o que altera o volume sanguíneo e a pressão arterial.
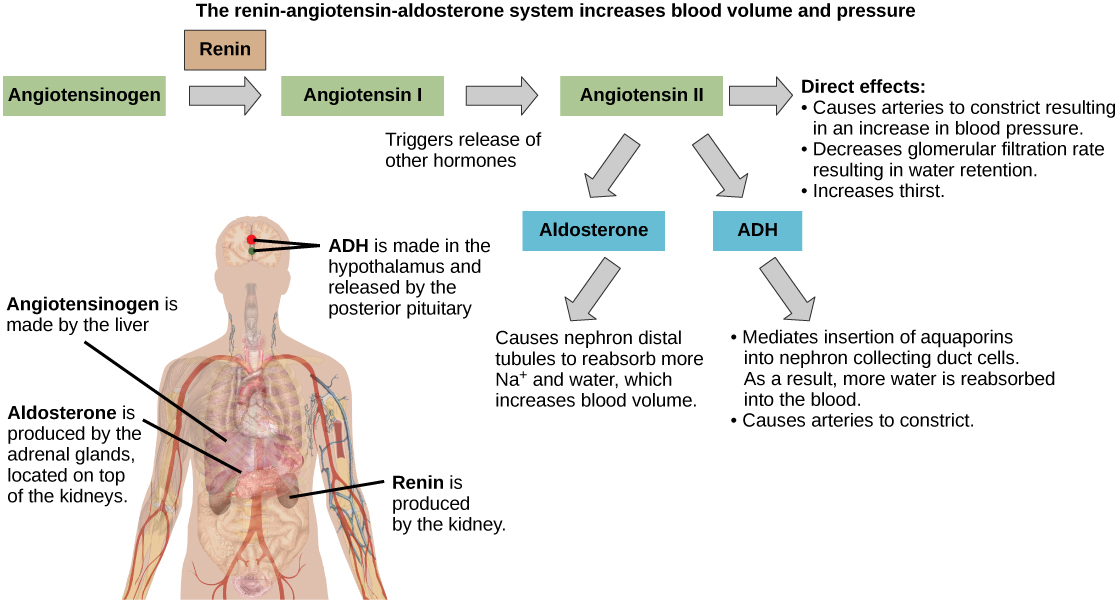
A produção de aldosterona pode ser estimulada pela pressão arterial baixa, que desencadeia uma sequência de liberação química, conforme ilustrado na Figura\(\PageIndex{1}\). Quando a pressão arterial cai, o sistema renina-angiotensina-aldosterona (RAAS) é ativado. As células do aparelho justaglomerular, que regula as funções dos néfrons do rim, detectam isso e liberam renina. A renina, uma enzima, circula no sangue e reage com uma proteína plasmática produzida pelo fígado chamada angiotensinogênio. Quando o angiotensinogênio é clivado pela renina, ele produz angiotensina I, que é então convertida em angiotensina II nos pulmões. A angiotensina II funciona como um hormônio e, em seguida, causa a liberação do hormônio aldosterona pelo córtex adrenal, resultando em aumento da reabsorção de Na +, retenção de água e aumento da pressão arterial. A angiotensina II, além de ser um potente vasoconstritor, também causa aumento do ADH e aumento da sede, os quais ajudam a elevar a pressão arterial.
Regulação hormonal do sistema reprodutivo
A regulação do sistema reprodutivo é um processo que requer a ação de hormônios da glândula pituitária, do córtex adrenal e das gônadas. Durante a puberdade em homens e mulheres, o hipotálamo produz o hormônio liberador de gonadotrofina (GnRH), que estimula a produção e liberação do hormônio folículo-estimulante (FSH) e do hormônio luteinizante (LH) da glândula pituitária anterior. Esses hormônios regulam as gônadas (testículos em homens e ovários em mulheres) e, portanto, são chamados de gonadotrofinas. Tanto em homens quanto em mulheres, o FSH estimula a produção de gametas e o LH estimula a produção de hormônios pelas gônadas. Um aumento nos níveis do hormônio gonadal inibe a produção de GnRH por meio de um ciclo de feedback negativo.
Regulação do Sistema Reprodutor Masculino
Nos homens, o FSH estimula a maturação dos espermatozóides. A produção de FSH é inibida pelo hormônio inibina, que é liberado pelos testículos. O LH estimula a produção de hormônios sexuais (andrógenos) pelas células intersticiais dos testículos e, portanto, também é chamado de hormônio estimulador de células intersticiais. O andrógeno mais conhecido nos homens é a testosterona. A testosterona promove a produção de espermatozóides e características masculinas. O córtex adrenal também produz pequenas quantidades de precursor de testosterona, embora o papel dessa produção adicional de hormônio não seja totalmente compreendido.
Conexão diária: os perigos dos hormônios sintéticos
Alguns atletas tentam melhorar seu desempenho usando hormônios artificiais que melhoram o desempenho muscular. Os esteróides anabolizantes, uma forma do hormônio sexual masculino testosterona, são uma das drogas mais conhecidas para melhorar o desempenho. Os esteróides são usados para ajudar a construir massa muscular. Outros hormônios usados para melhorar o desempenho atlético incluem a eritropoetina, que desencadeia a produção de glóbulos vermelhos, e o hormônio do crescimento humano, que pode ajudar na construção da massa muscular. A maioria dos medicamentos que melhoram o desempenho são ilegais para fins não médicos. Eles também são proibidos por órgãos governamentais nacionais e internacionais, incluindo o Comitê Olímpico Internacional, o Comitê Olímpico dos EUA, a National Collegiate Athletic Association, a Major League Baseball e a National Football League.

Os efeitos colaterais dos hormônios sintéticos costumam ser significativos e irreversíveis e, em alguns casos, fatais. Os andrógenos produzem várias complicações, como disfunções hepáticas e tumores hepáticos, aumento da próstata, dificuldade em urinar, fechamento prematuro das cartilagens epifisárias, atrofia testicular, infertilidade e depressão do sistema imunológico. A tensão fisiológica causada por essas substâncias costuma ser maior do que o corpo pode suportar, levando a efeitos imprevisíveis e perigosos e vinculando seu uso a ataques cardíacos, derrames e comprometimento da função cardíaca.
Regulação do sistema reprodutor feminino
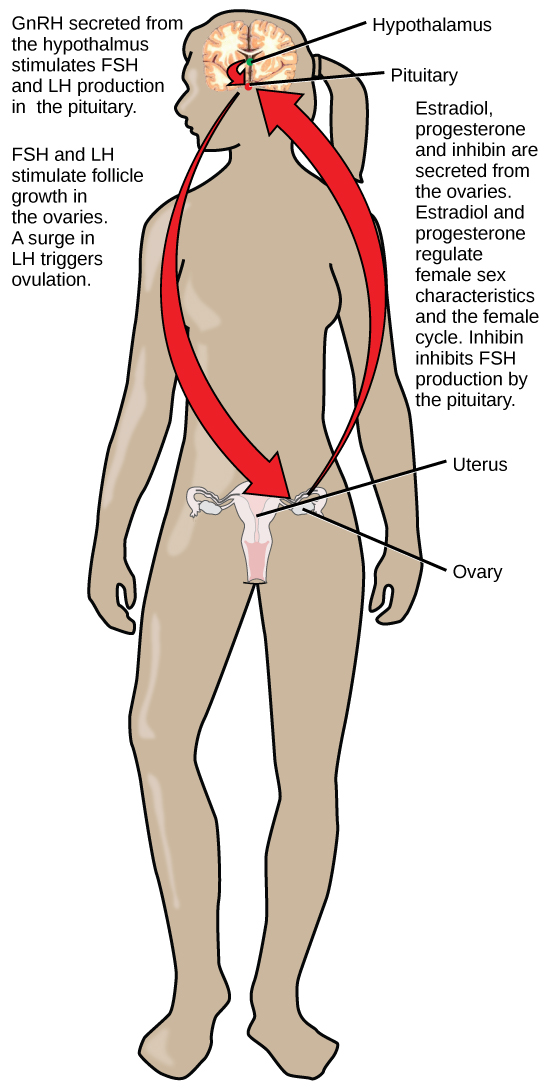
Nas mulheres, a FSH estimula o desenvolvimento de óvulos, chamados óvulos, que se desenvolvem em estruturas chamadas folículos. As células foliculares produzem o hormônio inibina, que inibe a produção de FSH. O LH também desempenha um papel no desenvolvimento dos óvulos, na indução da ovulação e na estimulação da produção de estradiol e progesterona pelos ovários, conforme ilustrado na Figura\(\PageIndex{3}\). Estradiol e progesterona são hormônios esteróides que preparam o corpo para a gravidez. O estradiol produz características sexuais secundárias nas mulheres, enquanto o estradiol e a progesterona regulam o ciclo menstrual.
Além de produzir FSH e LH, a porção anterior da glândula pituitária também produz o hormônio prolactina (PRL) em mulheres. A prolactina estimula a produção de leite pelas glândulas mamárias após o parto. Os níveis de prolactina são regulados pelos hormônios hipotalâmicos hormônio liberador de prolactina (PRH) e hormônio inibidor de prolactina (PIH), que agora é conhecido como dopamina. O PRH estimula a liberação de prolactina e o PIH a inibe.
A hipófise posterior libera o hormônio oxitocina, que estimula as contrações uterinas durante o parto. Os músculos lisos uterinos não são muito sensíveis à ocitocina até o final da gravidez, quando o número de receptores de ocitocina no útero atinge o pico. O alongamento dos tecidos do útero e do colo do útero estimula a liberação de ocitocina durante o parto. As contrações aumentam de intensidade à medida que os níveis sanguíneos de ocitocina aumentam por meio de um mecanismo de feedback positivo até a conclusão do parto. A ocitocina também estimula a contração das células mioepiteliais ao redor das glândulas mamárias produtoras de leite. À medida que essas células se contraem, o leite é forçado dos alvéolos secretores para os dutos de leite e é ejetado dos seios no reflexo de ejeção (“decepção”) do leite. A liberação de ocitocina é estimulada pela amamentação de um bebê, que desencadeia a síntese de ocitocina no hipotálamo e sua liberação em circulação na hipófise posterior.
Regulação hormonal do metabolismo
Os níveis de glicose no sangue variam muito ao longo de um dia, pois os períodos de consumo de alimentos se alternam com os períodos de jejum. A insulina e o glucagon são os dois hormônios principais responsáveis pela manutenção da homeostase dos níveis de glicose no sangue. A regulação adicional é mediada pelos hormônios tireoidianos.
Regulação dos níveis de glicose no sangue por insulina e glucagon
As células do corpo precisam de nutrientes para funcionar, e esses nutrientes são obtidos por meio da alimentação. Para controlar a ingestão de nutrientes, armazenar o excesso de ingestão e utilizar as reservas quando necessário, o corpo usa hormônios para moderar os estoques de energia. A insulina é produzida pelas células beta do pâncreas, que são estimuladas a liberar insulina à medida que os níveis de glicose no sangue aumentam (por exemplo, após o consumo de uma refeição). A insulina reduz os níveis de glicose no sangue, aumentando a taxa de captação e utilização de glicose pelas células-alvo, que usam glicose para a produção de ATP. Também estimula o fígado a converter glicose em glicogênio, que é então armazenado pelas células para uso posterior. A insulina também aumenta o transporte de glicose para certas células, como as células musculares e o fígado. Isso resulta de um aumento mediado pela insulina no número de proteínas transportadoras de glicose nas membranas celulares, que removem a glicose da circulação por difusão facilitada. À medida que a insulina se liga à sua célula-alvo por meio de receptores de insulina e transdução de sinal, ela aciona a célula a incorporar proteínas transportadoras de glicose em sua membrana. Isso permite que a glicose entre na célula, onde ela pode ser usada como fonte de energia. No entanto, isso não ocorre em todas as células: algumas células, incluindo as dos rins e do cérebro, podem acessar a glicose sem o uso de insulina. A insulina também estimula a conversão de glicose em gordura nos adipócitos e a síntese de proteínas. Essas ações mediadas pela insulina fazem com que as concentrações de glicose no sangue caiam, chamado de efeito hipoglicêmico de “baixo teor de açúcar”, que inibe a liberação adicional de insulina das células beta por meio de um ciclo de feedback negativo.
Link para o aprendizado
Esta animação descreve o papel da insulina e do pâncreas no diabetes.
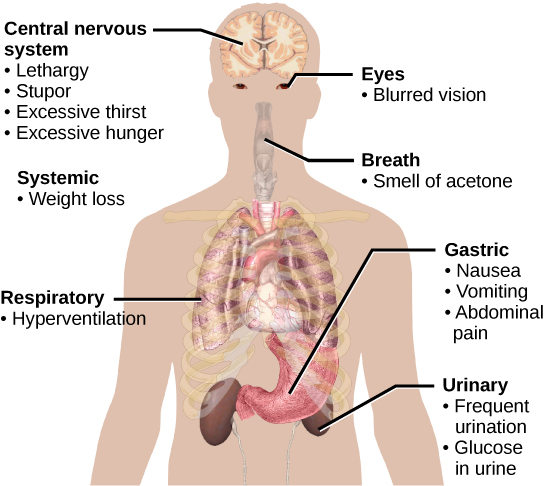
O comprometimento da função da insulina pode levar a uma condição chamada diabetes mellitus, cujos principais sintomas são ilustrados na Figura\(\PageIndex{4}\). Isso pode ser causado por baixos níveis de produção de insulina pelas células beta do pâncreas ou pela redução da sensibilidade das células do tecido à insulina. Isso evita que a glicose seja absorvida pelas células, causando altos níveis de glicose no sangue ou hiperglicemia (alto teor de açúcar). Níveis elevados de glicose no sangue dificultam que os rins recuperem toda a glicose da urina nascente, resultando na perda de glicose na urina. Altos níveis de glicose também resultam em menos água sendo reabsorvida pelos rins, fazendo com que grandes quantidades de urina sejam produzidas; isso pode resultar em desidratação. Com o tempo, altos níveis de glicose no sangue podem causar danos nos nervos nos olhos e nos tecidos periféricos do corpo, bem como danos aos rins e ao sistema cardiovascular. A secreção excessiva de insulina pode causar hipoglicemia, baixos níveis de glicose no sangue. Isso causa disponibilidade insuficiente de glicose para as células, muitas vezes levando à fraqueza muscular, e às vezes pode causar inconsciência ou morte se não for tratada.
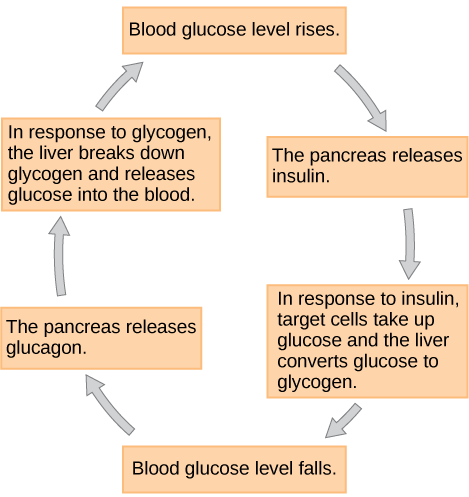
Quando os níveis de glicose no sangue diminuem abaixo dos níveis normais, por exemplo, entre as refeições ou quando a glicose é utilizada rapidamente durante o exercício, o hormônio glucagon é liberado das células alfa do pâncreas. O glucagon aumenta os níveis de glicose no sangue, provocando o que é chamado de efeito hiperglicêmico, estimulando a degradação do glicogênio em glicose nas células musculares esqueléticas e hepáticas em um processo chamado glicogenólise. A glicose pode então ser utilizada como energia pelas células musculares e liberada na circulação pelas células do fígado. O glucagon também estimula a absorção de aminoácidos do sangue pelo fígado, que os converte em glicose. Esse processo de síntese de glicose é chamado de gliconeogênese. O glucagon também estimula as células adiposas a liberar ácidos graxos no sangue. Essas ações mediadas pelo glucagon resultam em um aumento nos níveis de glicose no sangue para níveis homeostáticos normais. O aumento dos níveis de glicose no sangue inibe a liberação adicional de glucagon pelo pâncreas por meio de um mecanismo de feedback negativo. Dessa forma, a insulina e o glucagon trabalham juntos para manter os níveis homeostáticos de glicose, conforme mostrado na Figura\(\PageIndex{5}\).
Exercício
Os tumores pancreáticos podem causar excesso de secreção de glucagon. O diabetes tipo I resulta da falha do pâncreas em produzir insulina. Qual das seguintes afirmações sobre essas duas condições é verdadeira?
- Um tumor pancreático e diabetes tipo I terão efeitos opostos nos níveis de açúcar no sangue.
- Um tumor pancreático e o diabetes tipo I causam hiperglicemia.
- Um tumor pancreático e o diabetes tipo I causam hipoglicemia.
- Tanto os tumores pancreáticos quanto o diabetes tipo I resultam na incapacidade das células de absorver glicose.
- Responda
-
B
Regulação dos níveis de glicose no sangue pelos hormônios tireoidi
A taxa metabólica basal, que é a quantidade de calorias exigida pelo corpo em repouso, é determinada por dois hormônios produzidos pela glândula tireoide: tiroxina, também conhecida como tetraiodotironina ou T 4, e triiodotironina, também conhecida como T 3. Esses hormônios afetam quase todas as células do corpo, exceto o cérebro adulto, o útero, os testículos, as células sanguíneas e o baço. Eles são transportados pela membrana plasmática das células-alvo e se ligam aos receptores nas mitocôndrias, resultando no aumento da produção de ATP. No núcleo, T 3 e T 4 ativam genes envolvidos na produção de energia e na oxidação da glicose. Isso resulta em aumento das taxas de metabolismo e produção de calor corporal, o que é conhecido como efeito calorigênico do hormônio.
A liberação de T 3 e T 4 da glândula tireoide é estimulada pelo hormônio estimulador da tireoide (TSH), que é produzido pela hipófise anterior. A ligação do TSH nos receptores do folículo da tireoide desencadeia a produção de T 3 e T 4 a partir de uma glicoproteína chamada tireoglobulina. A tireoglobulina está presente nos folículos da tireoide e é convertida em hormônios tireoidianos com a adição de iodo. O iodo é formado a partir de íons de iodeto que são transportados ativamente da corrente sanguínea para o folículo tireoidiano. Uma enzima peroxidase então liga o iodo ao aminoácido tirosina encontrado na tiroglobulina. T 3 tem três íons de iodo conectados, enquanto T 4 tem quatro íons de iodo conectados. T 3 e T 4 são então liberados na corrente sanguínea, com T 4 sendo liberado em quantidades muito maiores do que T 3. Como o T 3 é mais ativo que o T 4 e é responsável pela maioria dos efeitos dos hormônios tireoidianos, os tecidos do corpo convertem T 4 em T 3 pela remoção de um íon iodo. A maioria dos T 3 e T 4 liberados se liga às proteínas transportadoras na corrente sanguínea e é incapaz de atravessar a membrana plasmática das células. Essas moléculas ligadas às proteínas só são liberadas quando os níveis sanguíneos do hormônio não ligado começam a diminuir. Dessa forma, uma semana de hormônio de reserva é mantida no sangue. Níveis aumentados de T 3 e T 4 no sangue inibem a liberação de TSH, o que resulta em menor liberação de T 3 e T 4 da tireoide.
As células foliculares da tireoide necessitam de iodetos (ânions de iodo) para sintetizar T 3 e T 4. Os iodetos obtidos da dieta são transportados ativamente para as células do folículo, resultando em uma concentração aproximadamente 30 vezes maior do que no sangue. A dieta típica na América do Norte fornece mais iodo do que o necessário devido à adição de iodeto ao sal de cozinha. A ingestão inadequada de iodo, que ocorre em muitos países em desenvolvimento, resulta na incapacidade de sintetizar os hormônios T 3 e T 4. A glândula tireoide aumenta em uma condição chamada bócio, causada pela superprodução de TSH sem a formação do hormônio tireoidiano. A tireoglobulina está contida em um fluido chamado colóide, e a estimulação do TSH resulta em níveis mais altos de acúmulo de coloide na tireoide. Na ausência de iodo, ele não é convertido em hormônio tireoidiano, e o colóide começa a se acumular cada vez mais na glândula tireoidea, levando ao bócio.
Os distúrbios podem surgir tanto da subprodução quanto da superprodução dos hormônios tireoidianos. O hipotireoidismo, subprodução dos hormônios tireoidianos, pode causar uma baixa taxa metabólica, levando ao ganho de peso, sensibilidade ao frio e redução da atividade mental, entre outros sintomas. Em crianças, o hipotireoidismo pode causar cretinismo, o que pode levar a retardo mental e defeitos de crescimento. O hipertireoidismo, a superprodução dos hormônios tireoidianos, pode levar ao aumento da taxa metabólica e seus efeitos: perda de peso, produção excessiva de calor, sudorese e aumento da frequência cardíaca. A doença de Graves é um exemplo de doença hipertireoidiana.
Controle hormonal dos níveis de cálcio no sangue
A regulação das concentrações de cálcio no sangue é importante para a geração de contrações musculares e impulsos nervosos, que são estimulados eletricamente. Se os níveis de cálcio ficarem muito altos, a permeabilidade da membrana ao sódio diminui e as membranas se tornam menos responsivas. Se os níveis de cálcio ficarem muito baixos, a permeabilidade da membrana ao sódio aumenta e podem ocorrer convulsões ou espasmos musculares.
Os níveis de cálcio no sangue são regulados pelo hormônio da paratireóide (PTH), que é produzido pelas glândulas paratireóides, conforme ilustrado na Figura\(\PageIndex{6}\). O PTH é liberado em resposta aos baixos níveis de Ca 2+ no sangue. O PTH aumenta os níveis de Ca 2+ ao atingir o esqueleto, os rins e o intestino. No esqueleto, o PTH estimula os osteoclastos, o que faz com que o osso seja reabsorvido, liberando Ca 2+ do osso para o sangue. O PTH também inibe os osteoblastos, reduzindo a deposição de Ca 2+ no osso. Nos intestinos, o PTH aumenta a absorção de Ca 2+ na dieta e, nos rins, o PTH estimula a reabsorção do CA 2+. Enquanto o PTH atua diretamente nos rins para aumentar a reabsorção de Ca 2+, seus efeitos no intestino são indiretos. O PTH desencadeia a formação do calcitriol, uma forma ativa da vitamina D, que atua no intestino aumentando a absorção do cálcio na dieta. A liberação de PTH é inibida pelo aumento dos níveis de cálcio no sangue.
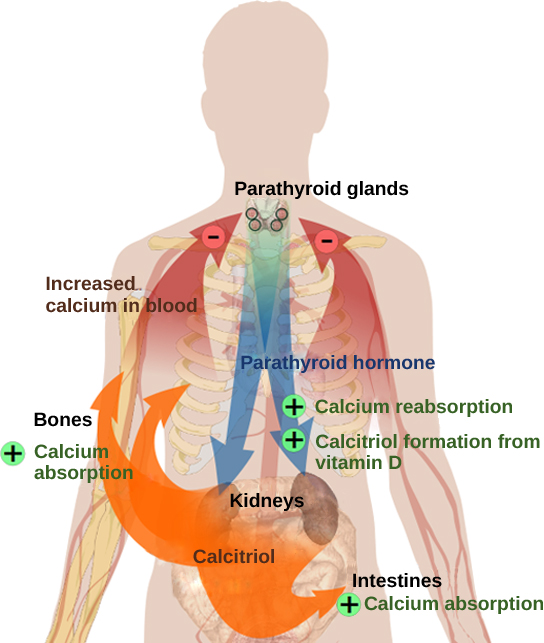
O hiperparatireoidismo resulta de uma superprodução do hormônio da paratireóide. Isso resulta na remoção excessiva de cálcio dos ossos e na introdução na circulação sanguínea, produzindo fraqueza estrutural dos ossos, o que pode levar à deformação e fraturas, além de comprometimento do sistema nervoso devido aos altos níveis de cálcio no sangue. O hipoparatireoidismo, a subprodução de PTH, resulta em níveis extremamente baixos de cálcio no sangue, o que causa comprometimento da função muscular e pode resultar em tetania (contração muscular sustentada severa).
O hormônio calcitonina, produzido pelas células parafoliculares ou C da tireoide, tem o efeito oposto nos níveis de cálcio no sangue, assim como o PTH. A calcitonina diminui os níveis de cálcio no sangue ao inibir os osteoclastos, estimular os osteoblastos e estimular a excreção de cálcio pelos rins. Isso resulta na adição de cálcio aos ossos para promover a integridade estrutural. A calcitonina é mais importante em crianças (quando estimula o crescimento ósseo), durante a gravidez (quando reduz a perda óssea materna) e durante a inanição prolongada (porque reduz a perda de massa óssea). Em adultos saudáveis, não gestantes e sem fome, o papel da calcitonina não está claro.
Regulação hormonal do crescimento
A regulação hormonal é necessária para o crescimento e a replicação da maioria das células do corpo. O hormônio do crescimento (GH), produzido pela porção anterior da glândula pituitária, acelera a taxa de síntese protéica, particularmente no músculo esquelético e nos ossos. O hormônio do crescimento tem mecanismos de ação diretos e indiretos. A primeira ação direta do GH é estimular a degradação dos triglicérides (lipólise) e a liberação no sangue pelos adipócitos. Isso resulta em uma mudança, por parte da maioria dos tecidos, da utilização de glicose como fonte de energia para a utilização de ácidos graxos. Esse processo é chamado de efeito poupador de glicose. Em outro mecanismo direto, o GH estimula a degradação do glicogênio no fígado; o glicogênio é então liberado no sangue como glicose. Os níveis de glicose no sangue aumentam, pois a maioria dos tecidos está utilizando ácidos graxos em vez de glicose para suas necessidades energéticas. O aumento mediado pelo GH nos níveis de glicose no sangue é chamado de efeito diabetogênico porque é semelhante aos altos níveis de glicose no sangue observados no diabetes mellitus.
O mecanismo indireto da ação do GH é mediado por fatores de crescimento semelhantes à insulina (IGFs) ou somatomedinas, que são uma família de proteínas promotoras de crescimento produzidas pelo fígado, que estimulam o crescimento dos tecidos. Os IGFs estimulam a absorção de aminoácidos do sangue, permitindo a formação de novas proteínas, particularmente nas células musculares esqueléticas, cartilaginosas e outras células-alvo, conforme mostrado na Figura\(\PageIndex{7}\). Isso é especialmente importante após uma refeição, quando os níveis de concentração de glicose e aminoácidos estão altos no sangue. Os níveis de GH são regulados por dois hormônios produzidos pelo hipotálamo. A liberação de GH é estimulada pelo hormônio liberador de hormônio do crescimento (GHRH) e é inibida pelo hormônio inibidor do hormônio do crescimento (GHIH), também chamado de somatostatina.
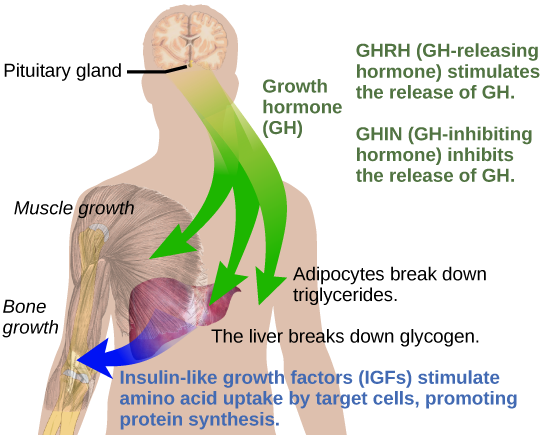
Uma produção equilibrada do hormônio do crescimento é fundamental para o desenvolvimento adequado. A subprodução de GH em adultos não parece causar anormalidades, mas em crianças pode resultar em nanismo hipofisário, no qual o crescimento é reduzido. O nanismo hipofisário é caracterizado pela formação corporal simétrica. Em alguns casos, os indivíduos têm menos de 30 polegadas de altura. A secreção excessiva do hormônio do crescimento pode levar ao gigantismo em crianças, causando crescimento excessivo. Em alguns casos documentados, os indivíduos podem atingir alturas de mais de oito pés. Em adultos, o excesso de GH pode levar à acromegalia, uma condição na qual há aumento dos ossos da face, mãos e pés que ainda são capazes de crescer.
Regulação hormonal do estresse
Quando uma ameaça ou perigo é percebido, o corpo responde liberando hormônios que o preparam para a resposta de “lutar ou fugir”. Os efeitos dessa resposta são familiares para qualquer pessoa que tenha passado por uma situação estressante: aumento da frequência cardíaca, boca seca e cabelos em pé.
Evolution Connection: resposta de luta ou fuga
As interações dos hormônios endócrinos evoluíram para garantir que o ambiente interno do corpo permaneça estável. Os estressores são estímulos que interrompem a homeostase. A divisão simpática do sistema nervoso autônomo dos vertebrados desenvolveu a resposta de luta ou fuga para combater as interrupções da homeostase induzidas pelo estresse. Na fase inicial de alarme, o sistema nervoso simpático estimula o aumento dos níveis de energia por meio do aumento dos níveis de glicose no sangue. Isso prepara o corpo para atividades físicas que podem ser necessárias para responder ao estresse: lutar pela sobrevivência ou fugir do perigo.
No entanto, alguns estresses, como doenças ou lesões, podem durar muito tempo. As reservas de glicogênio, que fornecem energia na resposta de curto prazo ao estresse, se esgotam após várias horas e não podem atender às necessidades energéticas de longo prazo. Se as reservas de glicogênio fossem a única fonte de energia disponível, o funcionamento neural não poderia ser mantido depois que as reservas se esgotassem devido à alta necessidade de glicose do sistema nervoso. Nessa situação, o corpo desenvolveu uma resposta para combater o estresse de longo prazo por meio das ações dos glicocorticóides, que garantem que as necessidades de energia de longo prazo possam ser atendidas. Os glicocorticóides mobilizam reservas de lipídios e proteínas, estimulam a gliconeogênese, conservam a glicose para uso pelo tecido neural e estimulam a conservação de sais e água. Os mecanismos para manter a homeostase descritos aqui são aqueles observados no corpo humano. No entanto, a resposta de luta ou fuga existe de alguma forma em todos os vertebrados.
O sistema nervoso simpático regula a resposta ao estresse por meio do hipotálamo. Estímulos estressantes fazem com que o hipotálamo sinalize a medula adrenal (que medeia respostas de estresse de curto prazo) por meio de impulsos nervosos e o córtex adrenal, que medeia as respostas de estresse de longo prazo, por meio do hormônio adrenocorticotrófico (ACTH), que é produzido pela hipófise anterior.
Resposta ao estresse de curto prazo
Quando confrontado com uma situação estressante, o corpo responde pedindo a liberação de hormônios que fornecem uma explosão de energia. Os hormônios epinefrina (também conhecida como adrenalina) e noradrenalina (também conhecida como noradrenalina) são liberados pela medula adrenal. Como esses hormônios fornecem uma explosão de energia? A epinefrina e a norepinefrina aumentam os níveis de glicose no sangue estimulando o fígado e os músculos esqueléticos a decompor o glicogênio e estimulando a liberação de glicose pelas células do fígado. Além disso, esses hormônios aumentam a disponibilidade de oxigênio para as células, aumentando a frequência cardíaca e dilatando os bronquíolos. Os hormônios também priorizam a função corporal, aumentando o suprimento de sangue para órgãos essenciais, como coração, cérebro e músculos esqueléticos, ao mesmo tempo em que restringem o fluxo sanguíneo para órgãos que não precisam imediatamente, como pele, sistema digestivo e rins. A epinefrina e a norepinefrina são chamadas coletivamente de catecolaminas.
Link para o aprendizado
Assista a esta animação do Discovery Channel que descreve a resposta de voo ou voo.
Resposta ao estresse de longo prazo
A resposta ao estresse de longo prazo difere da resposta ao estresse de curto prazo O corpo não consegue sustentar as explosões de energia mediadas pela epinefrina e norepinefrina por muito tempo. Em vez disso, outros hormônios entram em ação. Em uma resposta ao estresse de longo prazo, o hipotálamo desencadeia a liberação de ACTH da glândula pituitária anterior. O córtex adrenal é estimulado pelo ACTH a liberar hormônios esteróides chamados corticosteróides. Os corticosteróides ativam a transcrição de certos genes nos núcleos das células-alvo. Eles alteram as concentrações de enzimas no citoplasma e afetam o metabolismo celular. Existem dois corticosteroides principais: glicocorticóides, como o cortisol, e mineralocorticóides, como a aldosterona. Esses hormônios visam a decomposição da gordura em ácidos graxos no tecido adiposo. Os ácidos graxos são liberados na corrente sanguínea para que outros tecidos sejam usados na produção de ATP. Os glicocorticóides afetam principalmente o metabolismo da glicose, estimulando a síntese de glicose. Os glicocorticóides também têm propriedades anti-inflamatórias por meio da inibição do sistema imunológico. Por exemplo, a cortisona é usada como medicamento anti-inflamatório; no entanto, não pode ser usada a longo prazo, pois aumenta a suscetibilidade a doenças devido aos seus efeitos imunossupressores.
Os mineralocorticóides funcionam para regular o equilíbrio de íons e água do corpo. O hormônio aldosterona estimula a reabsorção de água e íons de sódio no rim, o que resulta em aumento da pressão arterial e do volume.
A hipersecreção de glicocorticóides pode causar uma condição conhecida como doença de Cushing, caracterizada por uma mudança nas áreas de armazenamento de gordura do corpo. Isso pode causar o acúmulo de tecido adiposo no rosto e pescoço e excesso de glicose no sangue. A hiposecreção dos corticosteroides pode causar a doença de Addison, que pode resultar em bronzeamento da pele, hipoglicemia e baixos níveis de eletrólitos no sangue.
Resumo
Os níveis de água no corpo são controlados pelo hormônio antidiurético (ADH), que é produzido no hipotálamo e desencadeia a reabsorção de água pelos rins. A subprodução de ADH pode causar diabetes insípido. A aldosterona, um hormônio produzido pelo córtex adrenal dos rins, aumenta a reabsorção de Na+ dos fluidos extracelulares e a subsequente reabsorção de água por difusão. O sistema renina-angiotensina-aldosterona é uma forma de controlar a liberação de aldosterona.
O sistema reprodutivo é controlado pelas gonadotrofinas, hormônio folículo-estimulante (FSH) e hormônio luteinizante (LH), que são produzidas pela glândula pituitária. A liberação de gonadotrofina é controlada pelo hormônio hipotalâmico, hormônio liberador de gonadotrofina (GnRH). O FSH estimula a maturação dos espermatozóides nos homens e é inibido pelo hormônio inibina, enquanto o LH estimula a produção do andrógeno testosterona. O FSH estimula a maturação do ovo nas fêmeas, enquanto o LH estimula a produção de estrogênios e progesterona. Os estrogênios são um grupo de hormônios esteróides produzidos pelos ovários que desencadeiam o desenvolvimento de características sexuais secundárias nas mulheres, bem como controlam a maturação dos óvulos. Nas mulheres, a hipófise também produz prolactina, que estimula a produção de leite após o parto, e ocitocina, que estimula a contração uterina durante o parto e a liberação do leite durante a amamentação.
A insulina é produzida pelo pâncreas em resposta ao aumento dos níveis de glicose no sangue e permite que as células utilizem a glicose no sangue e armazenem o excesso de glicose para uso posterior. O diabetes mellitus é causado pela redução da atividade da insulina e causa altos níveis de glicose no sangue ou hiperglicemia. O glucagon é liberado pelo pâncreas em resposta aos baixos níveis de glicose no sangue e estimula a decomposição do glicogênio em glicose, que pode ser usada pelo organismo. A taxa metabólica basal do corpo é controlada pelos hormônios tireoidianos tiroxina (T 4) e triiodotironina (T 3). A hipófise anterior produz o hormônio estimulador da tireoide (TSH), que controla a liberação de T 3 e T 4 da glândula tireoide. O iodo é necessário na produção do hormônio tireoidiano, e a falta de iodo pode levar a uma condição chamada bócio.
O hormônio da paratireóide (PTH) é produzido pelas glândulas paratireóides em resposta aos baixos níveis de Ca 2+ no sangue. As células parafoliculares da tireoide produzem calcitonina, que reduz os níveis de Ca 2+ no sangue. O hormônio do crescimento (GH) é produzido pela hipófise anterior e controla a taxa de crescimento do músculo e osso. A ação do GH é mediada indiretamente por fatores de crescimento semelhantes à insulina (IGFs). O estresse de curto prazo faz com que o hipotálamo acione a medula adrenal para liberar epinefrina e norepinefrina, que desencadeiam a resposta de luta ou fuga. O estresse de longo prazo faz com que o hipotálamo acione a hipófise anterior para liberar o hormônio adrenocorticotrófico (ACTH), que causa a liberação de corticosteroides, glicocorticóides e mineralocorticóides do córtex adrenal.
Glossário
- acromegalia
- condição causada pela superprodução de GH em adultos
- Doença de Addison
- distúrbio causado pela hiposecreção de corticosteróides
- hormônio adrenocorticotrófico (ACTH)
- hormônio liberado pela hipófise anterior, que estimula o córtex adrenal a liberar corticosteroides durante a resposta ao estresse a longo prazo
- aldosterona
- hormônio esteróide produzido pelo córtex adrenal que estimula a reabsorção de Na + dos fluidos extracelulares e a secreção de K +.
- andrógeno
- hormônio sexual masculino, como testosterona
- hormônio antidiurético (ADH)
- hormônio produzido pelo hipotálamo e liberado pela hipófise posterior que aumenta a reabsorção de água pelos rins
- calcitonina
- hormônio produzido pelas células parafoliculares da glândula tireoide que funciona para reduzir os níveis de Ca 2+ no sangue e promover o crescimento ósseo
- corticosteróide
- hormônio liberado pelo córtex adrenal em resposta ao estresse de longo prazo
- cortisol
- glicocorticóide produzido em resposta ao estresse
- Doença de Cushing
- distúrbio causado pela hipersecreção de glicocorticóides
- diabetes insípido
- transtorno causado pela subprodução de ADH
- diabetes mellitus
- distúrbio causado por baixos níveis de atividade de insulina
- efeito diabetogênico
- efeito do GH que faz com que os níveis de glicose no sangue aumentem, semelhante ao diabetes mellitus
- epinefrina
- hormônio liberado pela medula adrenal em resposta a um estresse de curto prazo
- estrogênios
- - um grupo de hormônios esteróides, incluindo estradiol e vários outros, que são produzidos pelos ovários e provocam características sexuais secundárias nas fêmeas, bem como controlam a maturação dos óvulos
- hormônio folículo-estimulante (FSH)
- hormônio produzido pela hipófise anterior que estimula a produção de gametas
- gigantismo
- condição causada pela superprodução de GH em crianças
- glucagon
- hormônio produzido pelas células alfa do pâncreas em resposta ao baixo nível de açúcar no sangue; funciona para elevar os níveis de açúcar no sangue
- glicocorticóide
- corticosteroide que afeta o metabolismo da glicose
- gliconeogênese
- síntese de glicose a partir de aminoácidos
- efeito poupador de glicose
- efeito do GH que faz com que os tecidos usem ácidos graxos em vez de glicose como fonte de energia
- glicogenólise
- decomposição do glicogênio em glicose
- bócio
- aumento da glândula tireoide causado por níveis insuficientes de iodo na dieta
- gonadotrofina
- hormônio que regula as gônadas, incluindo FSH e LH
- hormônio do crescimento (GH)
- hormônio produzido pela hipófise anterior que promove a síntese protéica e o crescimento corporal
- hormônio inibidor do hormônio do crescimento (GHIH)
- hormônio produzido pelo hipotálamo que inibe a produção do hormônio do crescimento, também chamado somatostatina
- hormônio liberador de hormônio do crescimento (GHRH)
- hormônio liberado pelo hipotálamo que desencadeia a liberação de GH
- hiperglicemia
- alto nível de açúcar no sangue
- hipertireoidismo
- hiperatividade da glândula tireoidea
- hipoglicemia
- baixo nível de açúcar no sangue
- hipotireoidismo
- subatividade da glândula tireoidea
- insulina
- hormônio produzido pelas células beta do pâncreas em resposta a altos níveis de glicose no sangue; funciona para reduzir os níveis de glicose no sangue
- fator de crescimento semelhante à insulina (IGF)
- proteína promotora de crescimento produzida pelo fígado
- mineralocorticóide
- corticosteroide que afeta o equilíbrio de íons e água
- norepinefrina
- hormônio liberado pela medula adrenal em resposta a uma produção de hormônio do estresse de curto prazo pelas gônadas
- osmorreceptor
- receptor no hipotálamo que monitora a concentração de eletrólitos no sangue
- ocitocina
- hormônio liberado pela hipófise posterior para estimular as contrações uterinas durante o parto e a liberação de leite nas glândulas mamárias
- hormônio da paratireóide (PTH)
- hormônio produzido pelas glândulas paratireóides em resposta a níveis baixos de Ca 2+ no sangue; funções para elevar os níveis de Ca 2+ no sangue
- nanismo hipofisário
- condição causada pela subprodução de GH em crianças
- prolactina (PRL)
- hormônio produzido pela hipófise anterior que estimula a produção de leite
- hormônio inibidor da prolactina
- hormônio produzido pelo hipotálamo que inibe a liberação de prolactina
- hormônio liberador de prolactina
- hormônio produzido pelo hipotálamo que estimula a liberação de prolactina
- renina
- enzima produzida pelo aparelho justaglomerular dos rins que reage com o angiotensinogênio para causar a liberação de aldosterona
- tireoglobulina
- glicoproteína encontrada na tireoide que é convertida em hormônio tireoidiano
- hormônio estimulador da tireoide (TSH)
- hormônio produzido pela hipófise anterior que controla a liberação de T 3 e T 4 da glândula tireoidea
- tiroxina (tetraiodotironina, T 4)
- hormônio tireoidiano que controla a taxa metabólica basal
- triiodotironina (T 3)
- hormônio tireoidiano que controla a taxa metabólica basal


