7.4: Fosforilação oxidativa
- Page ID
- 182057
Habilidades para desenvolver
- Descreva como os elétrons se movem pela cadeia de transporte de elétrons e o que acontece com seus níveis de energia
- Explicar como um gradiente de prótons (H +) é estabelecido e mantido pela cadeia de transporte de elétrons
Você acabou de ler sobre duas vias no catabolismo da glicose - a glicólise e o ciclo do ácido cítrico - que geram ATP. A maior parte do ATP gerado durante o catabolismo aeróbico da glicose, no entanto, não é gerada diretamente a partir dessas vias. Em vez disso, é derivado de um processo que começa com a movimentação de elétrons por meio de uma série de transportadores de elétrons que sofrem reações redox. Isso faz com que os íons de hidrogênio se acumulem no espaço da matriz. Portanto, um gradiente de concentração se forma no qual os íons de hidrogênio se difundem para fora do espaço da matriz passando pela ATP sintase. A corrente de íons de hidrogênio alimenta a ação catalítica da ATP sintase, que fosforila o ADP, produzindo ATP.
Cadeia de transporte de eletrônicos
A cadeia de transporte de elétrons (Figura\(\PageIndex{1}\)) é o último componente da respiração aeróbica e é a única parte do metabolismo da glicose que usa oxigênio atmosférico. O oxigênio se difunde continuamente nas plantas; nos animais, ele entra no corpo pelo sistema respiratório. O transporte de elétrons é uma série de reações redox que se assemelham a uma corrida de relés ou brigada de caçamba, na qual os elétrons são passados rapidamente de um componente para o outro, até o ponto final da cadeia, onde os elétrons reduzem o oxigênio molecular, produzindo água. Existem quatro complexos compostos de proteínas, marcados de I a IV na Figura\(\PageIndex{1}\), e a agregação desses quatro complexos, junto com os portadores de elétrons móveis e acessórios associados, é chamada de cadeia de transporte de elétrons. A cadeia de transporte de elétrons está presente em várias cópias na membrana mitocondrial interna dos eucariotos e na membrana plasmática dos procariontes.
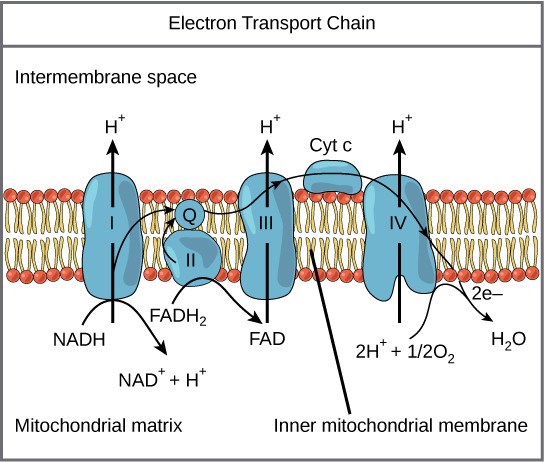
Complexo I
Para começar, dois elétrons são transportados para o primeiro complexo a bordo do NADH. Esse complexo, denominado I, é composto por mononucleotídeo de flavina (FMN) e uma proteína contendo ferro-enxofre (Fe-S). O FMN, que é derivado da vitamina B 2, também chamada de riboflavina, é um dos vários grupos protéticos ou cofatores na cadeia de transporte de elétrons. Um grupo protético é uma molécula não proteica necessária para a atividade de uma proteína. Os grupos protéticos são moléculas orgânicas ou inorgânicas, não peptídicas, ligadas a uma proteína que facilita sua função; os grupos protéticos incluem coenzimas, que são os grupos protéticos de enzimas. A enzima do complexo I é a NADH desidrogenase e é uma proteína muito grande, contendo 45 cadeias de aminoácidos. O complexo I pode bombear quatro íons de hidrogênio através da membrana da matriz para o espaço intermembranar, e é dessa forma que o gradiente de íons de hidrogênio é estabelecido e mantido entre os dois compartimentos separados pela membrana mitocondrial interna.
Q e Complexo II
O complexo II recebe diretamente o FADH 2, que não passa pelo complexo I. O composto que liga o primeiro e o segundo complexos ao terceiro é a ubiquinona (Q). A molécula Q é lipossolúvel e se move livremente através do núcleo hidrofóbico da membrana. Uma vez reduzida (QH 2), a ubiquinona entrega seus elétrons para o próximo complexo na cadeia de transporte de elétrons. Q recebe os elétrons derivados do NADH do complexo I e os elétrons derivados do FADH 2 do complexo II, incluindo a succinato desidrogenase. Essa enzima e o FADH 2 formam um pequeno complexo que fornece elétrons diretamente para a cadeia de transporte de elétrons, contornando o primeiro complexo. Como esses elétrons contornam e, portanto, não energizam a bomba de prótons no primeiro complexo, menos moléculas de ATP são produzidas a partir dos elétrons FADH 2. O número de moléculas de ATP finalmente obtidas é diretamente proporcional ao número de prótons bombeados pela membrana mitocondrial interna.
Complexo III
O terceiro complexo é composto por citocromo b, outra proteína Fe-S, centro de Rieske (centro 2Fe-2S) e proteínas do citocromo c; esse complexo também é chamado de citocromo oxidorredutase. As proteínas do citocromo têm um grupo protético de heme. A molécula heme é semelhante ao heme da hemoglobina, mas carrega elétrons, não oxigênio. Como resultado, o íon ferro em seu núcleo é reduzido e oxidado à medida que passa pelos elétrons, flutuando entre os diferentes estados de oxidação: Fe ++ (reduzido) e Fe +++ (oxidado). As moléculas de heme nos citocromos têm características ligeiramente diferentes devido aos efeitos das diferentes proteínas que as ligam, dando características ligeiramente diferentes a cada complexo. O complexo III bombeia prótons através da membrana e passa seus elétrons para o citocromo c para transporte para o quarto complexo de proteínas e enzimas (o citocromo c é o aceitador de elétrons de Q; no entanto, enquanto Q carrega pares de elétrons, o citocromo c pode aceitar apenas um de cada vez).
Complexo IV
O quarto complexo é composto pelas proteínas do citocromo c, a e a 3. Este complexo contém dois grupos heme (um em cada um dos dois citocromos, a e a 3) e três íons de cobre (um par de Cu A e um Cu B no citocromo a 3). Os citocromos mantêm uma molécula de oxigênio muito forte entre os íons ferro e cobre até que o oxigênio seja completamente reduzido. O oxigênio reduzido então pega dois íons de hidrogênio do meio circundante para produzir água (H 2 O). A remoção dos íons hidrogênio do sistema contribui para o gradiente iônico usado no processo de quimiosmose.
Quimiosmose
Na quimiosmose, a energia livre da série de reações redox que acabamos de descrever é usada para bombear íons de hidrogênio (prótons) através da membrana. A distribuição desigual de íons H+ pela membrana estabelece tanto a concentração quanto os gradientes elétricos (portanto, um gradiente eletroquímico), devido à carga positiva dos íons de hidrogênio e sua agregação em um lado da membrana.
Se a membrana estivesse aberta à difusão pelos íons de hidrogênio, os íons tenderiam a se difundir de volta para a matriz, impulsionados por seu gradiente eletroquímico. Lembre-se de que muitos íons não podem se difundir pelas regiões não polares das membranas fosfolipídicas sem o auxílio de canais iônicos. Da mesma forma, os íons de hidrogênio no espaço da matriz só podem passar pela membrana mitocondrial interna através de uma proteína de membrana integral chamada ATP sintase (Figura\(\PageIndex{2}\)). Essa proteína complexa atua como um pequeno gerador, girado pela força dos íons de hidrogênio que se difundem por ela, descendo seu gradiente eletroquímico. O torneamento de partes dessa máquina molecular facilita a adição de um fosfato ao ADP, formando ATP, usando a energia potencial do gradiente de íons hidrogênio.
Conexão artística
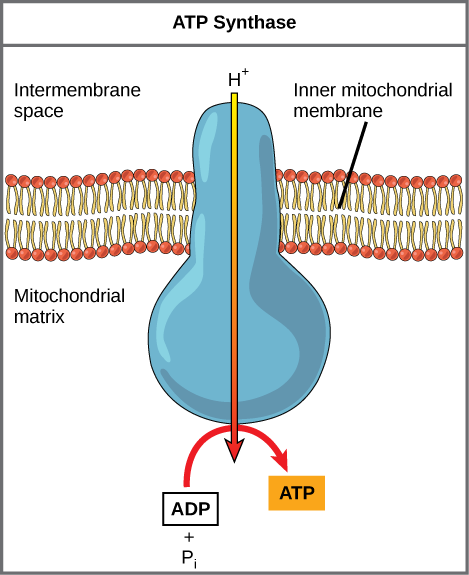
O dinitrofenol (DNP) é um desacoplador que faz com que a membrana mitocondrial interna vaze para prótons. Foi usado até 1938 como medicamento para perda de peso. Que efeito você esperaria que o DNP tivesse na mudança de pH na membrana mitocondrial interna? Por que você acha que isso pode ser um medicamento eficaz para perder peso?
A quimiosmose (Figura\(\PageIndex{3}\)) é usada para gerar 90 por cento do ATP produzido durante o catabolismo aeróbico da glicose; é também o método usado nas reações de luz da fotossíntese para aproveitar a energia da luz solar no processo de fotofosforilação. Lembre-se de que a produção de ATP usando o processo de quimiosmose na mitocôndria é chamada de fosforilação oxidativa. O resultado geral dessas reações é a produção de ATP a partir da energia dos elétrons removidos dos átomos de hidrogênio. Esses átomos eram originalmente parte de uma molécula de glicose. No final do caminho, os elétrons são usados para reduzir uma molécula de oxigênio a íons de oxigênio. Os elétrons extras no oxigênio atraem íons de hidrogênio (prótons) do meio circundante e a água é formada.
Conexão artística
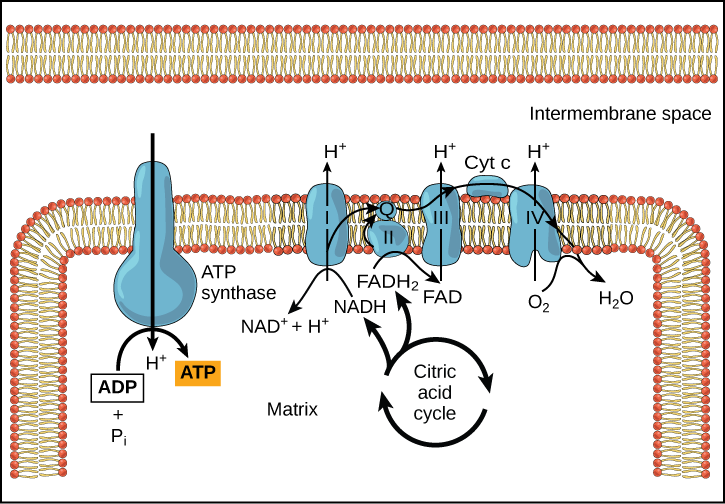
O cianeto inibe a citocromo c oxidase, um componente da cadeia de transporte de elétrons. Se ocorrer intoxicação por cianeto, você esperaria que o pH do espaço intermembranar aumentasse ou diminuísse? Que efeito o cianeto teria na síntese de ATP?
Rendimento do ATP
O número de moléculas de ATP geradas pelo catabolismo da glicose varia. Por exemplo, o número de íons de hidrogênio que os complexos da cadeia de transporte de elétrons podem bombear através da membrana varia entre as espécies. Outra fonte de variação decorre do transporte de elétrons pelas membranas das mitocôndrias. (O NADH gerado pela glicólise não pode entrar facilmente nas mitocôndrias.) Assim, os elétrons são captados no interior das mitocôndrias por NAD + ou FAD +. Como você aprendeu anteriormente, essas moléculas FAD + podem transportar menos íons; consequentemente, menos moléculas de ATP são geradas quando o FAD + atua como transportador. O NAD + é usado como transportador de elétrons no fígado e o FAD + atua no cérebro.
Outro fator que afeta o rendimento das moléculas de ATP geradas a partir da glicose é o fato de que compostos intermediários nessas vias são usados para outros fins. O catabolismo da glicose se conecta às vias que constroem ou decompõem todos os outros compostos bioquímicos nas células, e o resultado é um pouco mais confuso do que as situações ideais descritas até agora. Por exemplo, outros açúcares além da glicose são introduzidos na via glicolítica para extração de energia. Além disso, os açúcares de cinco carbonos que formam os ácidos nucléicos são feitos de intermediários na glicólise. Certos aminoácidos não essenciais podem ser produzidos a partir de intermediários da glicólise e do ciclo do ácido cítrico. Lipídios, como colesterol e triglicérides, também são produzidos a partir de intermediários nessas vias, e tanto os aminoácidos quanto os triglicérides são decompostos por energia por meio dessas vias. No geral, em sistemas vivos, essas vias de catabolismo da glicose extraem cerca de 34 por cento da energia contida na glicose.
Resumo
A cadeia de transporte de elétrons é a porção da respiração aeróbica que usa oxigênio livre como o aceitador final de elétrons removidos dos compostos intermediários no catabolismo da glicose. A cadeia de transporte de elétrons é composta por quatro grandes complexos multiproteicos embutidos na membrana mitocondrial interna e dois pequenos portadores de elétrons difusíveis transportando elétrons entre eles. Os elétrons passam por uma série de reações redox, com uma pequena quantidade de energia livre usada em três pontos para transportar íons de hidrogênio através de uma membrana. Esse processo contribui para o gradiente usado na quimiosmose. Os elétrons que passam pela cadeia de transporte de elétrons gradualmente perdem energia. Os elétrons de alta energia doados à cadeia pelo NADH ou pelo FADH 2 completam a cadeia, pois elétrons de baixa energia reduzem as moléculas de oxigênio e formam água. O nível de energia livre dos elétrons cai de cerca de 60 kcal/mol em NADH ou 45 kcal/mol em FADH 2 para cerca de 0 kcal/mol em água. Os produtos finais da cadeia de transporte de elétrons são água e ATP. Vários compostos intermediários do ciclo do ácido cítrico podem ser desviados para o anabolismo de outras moléculas bioquímicas, como aminoácidos não essenciais, açúcares e lipídios. Essas mesmas moléculas podem servir como fontes de energia para as vias da glicose.
Conexões artísticas
Figura\(\PageIndex{2}\): O dinitrofenol (DNP) é um desacoplador que faz com que a membrana mitocondrial interna vaze para prótons. Foi usado até 1938 como medicamento para perda de peso. Que efeito você esperaria que o DNP tivesse na mudança de pH na membrana mitocondrial interna? Por que você acha que isso pode ser um medicamento eficaz para perder peso?
- Responda
-
Após o envenenamento por DNP, a cadeia de transporte de elétrons não pode mais formar um gradiente de prótons e a ATP sintase não pode mais produzir ATP. O DNP é um medicamento dietético eficaz porque desacopla a síntese de ATP; em outras palavras, depois de tomá-lo, a pessoa obtém menos energia dos alimentos que ingere. Curiosamente, um dos piores efeitos colaterais dessa droga é a hipertermia ou o superaquecimento do corpo. Como o ATP não pode ser formado, a energia do transporte de elétrons é perdida como calor.
Figura\(\PageIndex{3}\): O cianeto inibe a citocromo c oxidase, um componente da cadeia de transporte de elétrons. Se ocorrer intoxicação por cianeto, você esperaria que o pH do espaço intermembranar aumentasse ou diminuísse? Que efeito o cianeto teria na síntese de ATP?
- Responda
-
Após o envenenamento por cianeto, a cadeia de transporte de elétrons não pode mais bombear elétrons para o espaço intermembranar. O pH do espaço intermembranar aumentaria, o gradiente de pH diminuiria e a síntese de ATP pararia.
Glossário
- ATP sintase
- (também, F1F0 ATP sintase) complexo proteico incorporado em membrana que adiciona um fosfato ao ADP com energia dos prótons se difundindo através dele
- grupo protético
- (também, cofator protético) molécula ligada a uma proteína que facilita a função da proteína
- ubiquinona
- transportador de elétrons solúvel na cadeia de transporte de elétrons que conecta o primeiro ou o segundo complexo ao terceiro


