1.2: Temperatura e equilíbrio térmico
- Page ID
- 184535
Ao final desta seção, você poderá:
- Defina a temperatura e descreva-a qualitativamente
- Explicar o equilíbrio térmico
- Explicar a lei zero da termodinâmica
O calor é familiar para todos nós. Podemos sentir o calor entrando em nossos corpos pelo sol do verão ou pelo café ou chá quente após um passeio de inverno. Também podemos sentir o calor saindo do nosso corpo enquanto sentimos o frio da noite ou o efeito refrescante do suor após o exercício.
O que é calor? Como o definimos e como está relacionado à temperatura? Quais são os efeitos do calor e como ele flui de um lugar para outro? Descobriremos que, apesar da riqueza dos fenômenos, um pequeno conjunto de princípios físicos subjacentes une esses assuntos e os vincula a outros campos. Começamos examinando a temperatura e como defini-la e medi-la.
Temperatura
O conceito de temperatura evoluiu dos conceitos comuns de quente e frio. A definição científica de temperatura explica mais do que nossos sentidos de calor e frio. Como você já deve ter aprendido, muitas grandezas físicas são definidas apenas em termos de como são observadas ou medidas, ou seja, são definidas operacionalmente. A temperatura é definida operacionalmente como a quantidade do que medimos com um termômetro. Como veremos em detalhes em um capítulo posterior sobre a teoria cinética dos gases, a temperatura é proporcional à energia cinética média de tradução, fato que fornece uma definição mais física. As diferenças de temperatura mantêm a transferência de calor, ou transferência de calor, por todo o universo. A transferência de calor é o movimento de energia de um local ou material para outro como resultado de uma diferença de temperatura. (Você aprenderá mais sobre transferência de calor mais adiante neste capítulo.)
Equilíbrio térmico
Um conceito importante relacionado à temperatura é o equilíbrio térmico. Dois objetos estão em equilíbrio térmico se estiverem em contato próximo, o que permite que um deles ganhe energia do outro, mas, no entanto, nenhuma energia líquida é transferida entre eles. Mesmo quando não estão em contato, eles estão em equilíbrio térmico se, ao serem colocados em contato, nenhuma energia líquida for transferida entre eles. Se dois objetos permanecerem em contato por muito tempo, eles normalmente se equilibram. Em outras palavras, dois objetos em equilíbrio térmico não trocam energia.
Experimentalmente, se o objeto A está em equilíbrio com o objeto B e o objeto B está em equilíbrio com o objeto C, então (como você já deve ter adivinhado) o objeto A está em equilíbrio com o objeto C. Essa declaração de transitividade é chamada de lei zero da termodinâmica. (O número “zero” foi sugerido pelo físico britânico Ralph Fowler na década de 1930. A primeira, a segunda e a terceira leis da termodinâmica já foram nomeadas e numeradas na época. A lei zero raramente havia sido declarada, mas precisa ser discutida antes das outras, então Fowler deu a ela um número menor.) Considere o caso em que A é um termômetro. A lei zero nos diz que se A ler uma determinada temperatura quando em equilíbrio com B e for então colocada em contato com C, ela não trocará energia com C; portanto, sua leitura de temperatura permanecerá a mesma (Figura\(\PageIndex{1}\)). Em outras palavras, se dois objetos estão em equilíbrio térmico, eles têm a mesma temperatura.
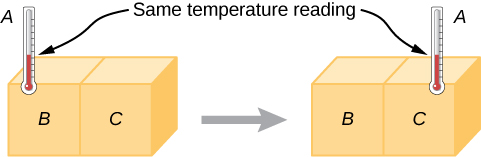
A thermometer measures its own temperature. It is through the concepts of thermal equilibrium and the zeroth law of thermodynamics that we can say that a thermometer measures the temperature of something else, and to make sense of the statement that two objects are at the same temperature.
In the rest of this chapter, we will often refer to “systems” instead of “objects.” As in the chapter on linear momentum and collisions, a system consists of one or more objects—but in thermodynamics, we require a system to be macroscopic, that is, to consist of a huge number (such as \(10^{23}\)) of molecules. Then we can say that a system is in thermal equilibrium with itself if all parts of it are at the same temperature. (We will return to the definition of a thermodynamic system in the chapter on the first law of thermodynamics.)


