10.5: Reações nucleares
- Page ID
- 183126
Ao final desta seção, você poderá:
- Descreva e compare três tipos de radiação nuclear
- Use símbolos nucleares para descrever as mudanças que ocorrem durante as reações nucleares
- Descreva os processos envolvidos na série de decaimento de elementos pesados
Os primeiros experimentos revelaram três tipos de “raios” nucleares ou radiação: alfa\((\alpha)\) rays\((\beta)\) rays, beta e gama\((\gamma)\) rays. Esses três tipos de radiação são diferenciados por sua capacidade de penetrar na matéria. A radiação alfa mal consegue passar por uma fina folha de papel. A radiação beta pode penetrar no alumínio até uma profundidade de cerca de 3 mm, e a radiação gama pode penetrar até uma profundidade de 2 ou mais centímetros (Figura\(\PageIndex{1}\)).
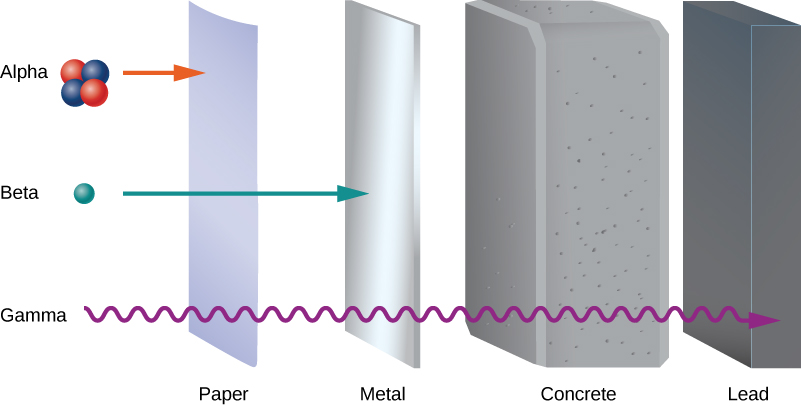
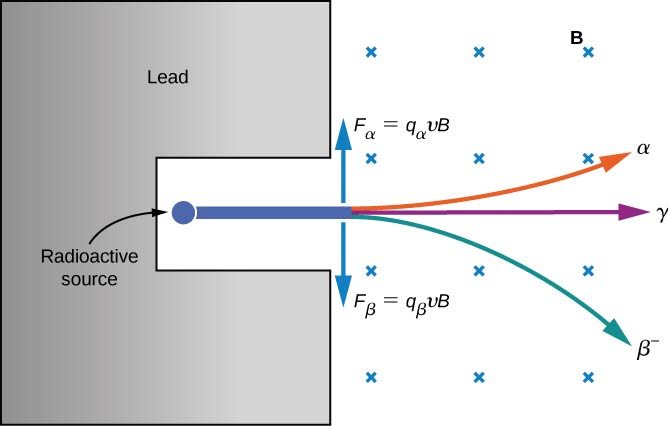
As propriedades elétricas desses três tipos de radiação são investigadas passando-as por um campo magnético uniforme, conforme mostrado na Figura\(\PageIndex{2}\). De acordo com a equação da força magnética para uma carga em movimento em um campo magnético
\[\vec{F} = q\vec{v} \times \vec{B} \nonumber \]
onde partículas carregadas positivamente são desviadas para cima, partículas carregadas negativamente são desviadas para baixo e partículas sem carga passam pelo campo magnético sem desvio. Eventualmente,\(\alpha\) os raios foram identificados com núcleos de hélio\((^4He)\),\(\beta\) raios com elétrons e pósitrons (elétrons carregados positivamente ou antielétrons) e\(\gamma\) raios com fótons de alta energia. Discutimos a radiação alfa, beta e gama em detalhes no restante desta seção.
Decaimento alfa
Núcleos pesados e instáveis emitem\(\alpha\) radiação. No decaimento de\(\alpha\) partículas -( ou decaimento alfa), o núcleo perde dois prótons e dois nêutrons, então o número atômico diminui em dois, enquanto seu número de massa diminui em quatro. Antes da decadência, o núcleo é chamado de núcleo parental. O núcleo ou núcleos produzidos na decadência são chamados de núcleo filho ou núcleo filho. Representamos uma\(\alpha\) decadência simbolicamente por
\[\ce{_Z^AX \rightarrow _{Z-2}^{A-4}X + _2^4He} \label{alpha} \]
onde\(_Z^AX\) está o núcleo pai,\(_{Z-2}^{A-4}X\) é o núcleo filho e\(_2^4He\) é a\(\alpha\) partícula. Em\(\alpha\) decadência, um núcleo do número atômico Z decai em um núcleo de número atômico\(Z - 2\) e massa atômica\(A - 4\). Curiosamente, o sonho dos antigos alquimistas de transformar outros metais em ouro é cientificamente viável por meio do processo de decaimento alfa. Os esforços dos alquimistas falharam porque eles dependiam de interações químicas em vez de interações nucleares.
Veja as partículas alfa escaparem de um núcleo de polônio, causando decaimento alfa radioativo. Veja como tempos de decaimento aleatórios se relacionam com a meia-vida. Para tentar uma simulação de decaimento alfa, visite partículas alfa
Um exemplo de decaimento alfa é o urânio-238:
\[\ce{_{92}^{238}U \rightarrow _{90}^{234}X + _2^4He} \nonumber \]
O número atômico caiu de 92 para 90. O elemento químico com\(Z = 90\) é o tório. Portanto, o urânio-238 decaiu para tório-234 pela emissão de uma\(\alpha\) partícula, escrita
\[\ce{_{92}^{238}U \rightarrow _{90}^{234}Th + _2^4He} \nonumber \]
Posteriormente,\(_{90}^{234}Th\) decai por\(\beta\) emissão com meia-vida de 24 dias. A energia liberada nesse decaimento alfa assume a forma de energias cinéticas dos núcleos de tório e hélio, embora a energia cinética do tório seja menor que o hélio devido à sua massa mais pesada e menor velocidade.
Determinar a energia emitida no\(\alpha\) decaimento de\(^{230}Pu\) pode ser encontrado usando a equação\(E = (\Delta m)c^2\). Devemos primeiro encontrar\(\Delta m\) a diferença de massa entre o núcleo parental e os produtos da decomposição.
Solução
A equação de decaimento é
\[\ce{^{230}Pu \rightarrow ^{235}U + ^4He}. \nonumber \]
Assim, as massas pertinentes são as de\(^{230}Pu\)\(^{235}U\), e a\(\alpha\) partícula ou\(^4He\), todas conhecidas. A missa inicial foi\(m(^{230}Pu) = 230.052157 \, u\). A massa final é a soma
\[\ce{m(^{235}U) + m(^4He) = 235.043924 \, u + 4.002602 \, u} \nonumber \]
Assim,
\[ \ce{\Delta m = m(^{230}Pu) - [m(^{235}U) + m(^4He)]} \nonumber \]
\[= 239.052157 \, u - 239.046526 \, u \nonumber \]
\[= 0.0005631 \, u. \nonumber \]
Agora podemos encontrar E\(\Delta m\) inserindo a equação:
\[E = (\Delta m) c^2 = (0.005631 \, u)c^2. \nonumber \]
Nós sabemos\(1 \, u = 931.5 \, MeV/c^2\), então temos
\[\begin{align} E & = (0.005631)(931.5 \, MeV/c^2)(c^2) \nonumber \\[4pt] &= 5.25 \, MeV. \nonumber \end{align} \nonumber \]
Significância
A energia liberada nesse\(\alpha\) decaimento está na faixa de MeV, muitas vezes maior do que as energias de reação química. A maior parte dessa energia se torna energia cinética da\(\alpha\) partícula (ou\(^4He\) núcleo), que se afasta em alta velocidade. A energia transportada pelo recuo do\(^{235}U\) núcleo é muito menor devido à sua massa relativamente grande. O\(^{235}U\) núcleo pode ser deixado em um estado excitado para posteriormente emitir fótons (\(\gamma\)raios). 239 Pu → 235 U + 4 Ele.
Decadência beta
Na maioria dos decaimentos de\(\beta\) partículas (ou decaimento beta), um elétron (\(\beta^-\)) ou um pósitron (\(\beta^+\)) é emitido por um núcleo. Um pósitron tem a mesma massa do elétron, mas sua carga é\(+e\). Por esse motivo, um pósitron às vezes é chamado de antielétron. Como ocorre a\(\beta\) decadência? Uma possível explicação é que o elétron (pósitron) está confinado ao núcleo antes do decaimento e de alguma forma escapa. Para obter uma estimativa aproximada da energia de escape, considere um modelo simplificado de um elétron preso em uma caixa (ou na terminologia da mecânica quântica, um poço quadrado unidimensional) que tenha a largura de um núcleo típico (\(10^{-14}\)). De acordo com o princípio da incerteza de Heisenberg na Mecânica Quântica, a incerteza do momento do elétron é:
\[\begin{align} \Delta p &\ge \dfrac{h}{\Delta x} \nonumber \\[4pt] &= \dfrac{6.6 \times 10^{-34} m^2 \cdot kg/s}{10^{-14}m} \nonumber \\[4pt] &= 6.6 \times 10^{-20} kg \cdot m/s. \end{align} \nonumber \]
Considerando esse valor de momento (uma subestimativa) como o “valor real”, a energia cinética do elétron na fuga é de aproximadamente
\[\begin{align} \dfrac{(\Delta p)^2}{2m_e} &= \dfrac{6.6 \times 10^{-20} m^2 \cdot kg/s)^2}{2(9.1 \times 10^{-31}kg)} \nonumber \\[4pt] &= 2.0 \times 10^{-9} J \nonumber \\[4pt] &= 12,400 \, MeV. \end{align} \nonumber \]
Experimentalmente, descobriu-se que os elétrons emitidos em\(\beta^-\) decaimento têm energias cinéticas da ordem de apenas alguns MeV. Concluímos, portanto, que o elétron é de alguma forma produzido no decaimento, em vez de escapar do núcleo. A produção de partículas (aniquilação) é descrita por teorias que combinam mecânica quântica e relatividade, um assunto de um curso mais avançado em física.
O decaimento beta nuclear envolve a conversão de um nucleon em outro. Por exemplo, um nêutron pode decair para um próton pela emissão de um elétron (\(\beta^-\)) e uma partícula quase sem massa chamada antineutrino (\(\overline{\nu}\)):
\[\ce{_0^1n \rightarrow _1^1p + _1^0e + \overline{\nu}. } \nonumber \]
A notação\(_{-1}^0e\) é usada para designar o elétron. Seu número de massa é 0 porque não é um nucleon, e seu número atômico significa que ele tem uma carga de\(-e\).\(-1\) O próton é representado\(_1^1p\) porque seu número de massa e número atômico são 1. Quando isso ocorre dentro de um núcleo atômico, temos a seguinte equação para decaimento beta:
\[\ce{_z^AX \rightarrow _{Z+1} ^AX + _1^0e + \overline{\nu}.} \label{beta} \]
Esse processo ocorre devido à fraca força nuclear.
Veja o decaimento beta ocorrer para uma coleção de núcleos ou para um núcleo individual.
Como exemplo, o isótopo\(_{90}^{234}Th\) é instável e decai por\(\beta^-\) emissão com meia-vida de 24 dias. Sua decadência pode ser representada como
\[\ce{_{90}^{234}Th \rightarrow _{91}^{234}X + _1^0e^+ + \overline{\nu}.} \nonumber \]
Como o elemento químico com número atômico 91 é o protactínio (Pa), podemos escrever a\(\beta^-\) decomposição do tório como
\[\ce{_{90}^{234}Th \rightarrow _{91}^{234}Pa + _1^0e^+ + \overline{\nu}.} \nonumber \]
O processo inverso também é possível: um próton pode decair em um nêutron pela emissão de um pósitron (\(e^+\)e uma partícula quase sem massa chamada nêutrin o (\(v\)). Essa reação é escrita como
\[\ce{_1^1p \rightarrow _0^1n + _{+1}^0e + \nu.} \nonumber \]
O pósitron\(_1^0e\) é emitido com o neutrino\(\nu\) e o nêutron permanece no núcleo. (Assim como o\(\beta^-\) decaimento, o pósitron não precede o decaimento, mas é produzido no decaimento.) Para um próton isolado, esse processo é impossível porque o nêutron é mais pesado que o próton. No entanto, esse processo é possível dentro do núcleo porque o próton pode receber energia de outros nucleons para a transição. Como um exemplo, o isótopo de alumínio\(_{13}^{26}Al\) decai por\(\beta^+\) emissão com meia-vida de\(7.40 \times 10^5 y\). A decadência é escrita como
\[\ce{_{13}^{26}Al \rightarrow _{12}^{26}X + _1^0e + \nu.} \nonumber \]
O número atômico 12 corresponde ao magnésio. Conseqüentemente,
\[\ce{_{13}^{26}Al \rightarrow _{12}^{26}Mg + _1^0 e + \nu.} \nonumber \]
Como uma reação nuclear, a emissão de pósitrons pode ser escrita como
\[\ce{_Z^AX \rightarrow _{Z-1} ^AX + _1^{0} e + \nu.} \nonumber \]
O neutrino não foi detectado nos primeiros experimentos de\(β\) decaimento. No entanto, as leis da energia e do momento pareciam exigir tal partícula. Posteriormente, os neutrinos foram detectados por meio de suas interações com os núcleos.
O\(_{83}^{211}Bi\) núcleo sofre as duas coisas\(\alpha\) e se\(\beta^-\) decompõe. Para cada caso, o que é o núcleo filho?
Estratégia
Podemos usar os processos descritos pela Equação\ ref {alpha} e pela Equação\ ref {beta}, bem como pela Tabela Periódica, para identificar os elementos resultantes.
Solução
O número atômico e o número de massa da\(\alpha\) partícula são 2 e 4, respectivamente. Assim, quando um núcleo de bismuto-211 emite uma\(\alpha\) partícula, o núcleo filho tem um número atômico 81 e um número de massa de 207. O elemento com um número atômico de 81 é tálio, então o decaimento é dado por
\[\ce{_{83}^{211}Bi \rightarrow _{81}^{207} Ti + _2^4He.} \nonumber \]
Em\(\beta^-\) decadência, o número atômico aumenta em 1, enquanto o número de massa permanece o mesmo. O elemento com um número atômico de 84 é polônio, então o decaimento é dado por
\[\ce{_{83}^{211}Bi \rightarrow _{84}^{211}Po + _{-1}^0e + \overline{\nu}.} \nonumber \]
No decaimento beta radioativo, o número de massa atômica, A, aumenta ou diminui?
Solução
Nenhum deles; permanece o mesmo.
Decaimento gama
Um núcleo em estado excitado pode decair para um estado de nível inferior pela emissão de um fóton de “raio gama”, e isso é conhecido como decaimento gama. Isso é análogo à desexcitação de um elétron atômico. O decaimento gama é representado simbolicamente por
\[\ce{_{Z}^{A}X}^{*} \ce{\rightarrow _{Z}^{A}X + \gamma} \label{gamma} \]
onde o asterisco (*) no núcleo indica um estado excitado. Em\(\gamma\) decadência, nem o número atômico nem o número de massa mudam, então o tipo de núcleo não muda.
Série Radioactive Decay
Os núcleos com\(Z > 82\) são instáveis e decaem naturalmente. Muitos desses núcleos têm vida útil muito curta, então eles não são encontrados na natureza. Exceções notáveis incluem\(_{90}^{232}Th\) (ou Th-232) com meia-vida de\(1.39 \times 10^{10}\) anos e\(_{92}^{238}U\) (ou U-238) com meia-vida de\(7.04 \times 10^8\) anos. Quando um núcleo pesado decai para um mais leve, o núcleo filho mais leve pode se tornar o núcleo pai para a próxima decadência, e assim por diante. Esse processo pode produzir uma longa série de decaimentos nucleares chamada de série de decaimento. A série termina com um núcleo estável.
Para ilustrar o conceito de uma série de decaimento, considere o decaimento da série Th-232 (Figura\(\PageIndex{3}\)). O número de nêutrons, N, é plotado no eixo vertical y, e o número atômico, Z, é plotado no eixo horizontal x, então Th-232 é encontrado nas coordenadas\((N, Z) = (142.90)\). O Th-232 decai por\(\alpha\) emissão com meia-vida de\(1.39 \times 10^{10}\) anos. O decaimento alfa diminui o número atômico em 2 e o número de massa em 4, então temos
\[\ce{_{90}^{232}Th \rightarrow _{88}^{228}Ra + _2^4He.} \nonumber \]
O número de nêutrons para o Rádio-228 é 140, portanto, é encontrado no diagrama nas coordenadas\((N,Z) = (140, \, 90)\). O rádio-228 também é instável e decai por\(\alpha\) emissão com uma meia-vida de 5,76 anos para Actinum-228. O número atômico aumenta em 1, o número de massa permanece o mesmo e o número de nêutrons diminui em 1. Observe que no gráfico, a\(α\) emissão aparece como uma linha inclinada para baixo para a esquerda, com N e Z diminuindo em 2. A emissão beta, por outro lado, aparece como uma linha inclinada para baixo para a direita, com N diminuindo em 1 e Z aumentando em 1. Após vários decaimentos alfa e beta adicionais, a série termina com o núcleo estável Pb-208.
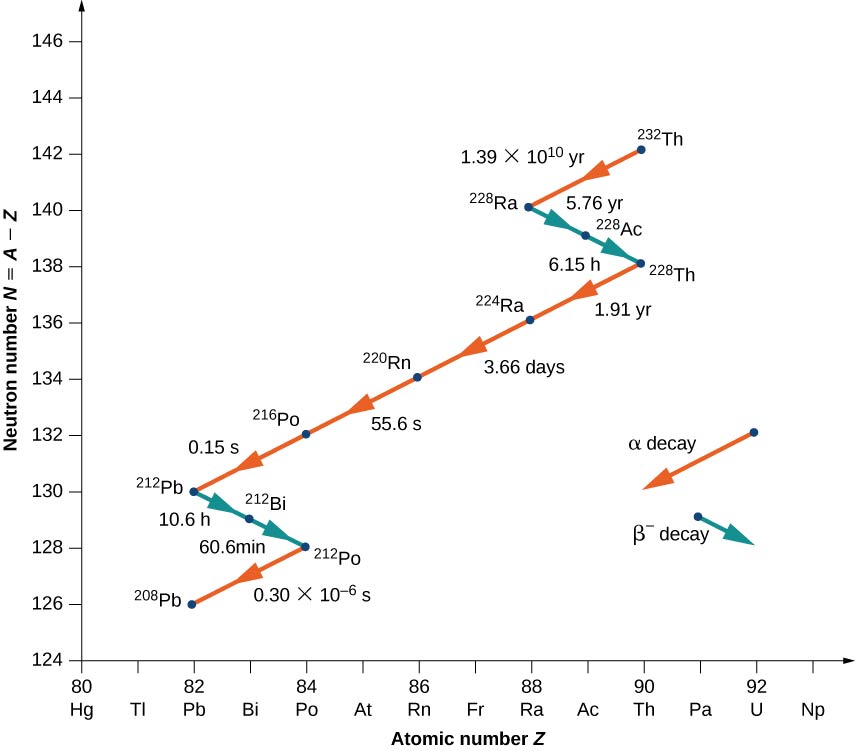
A frequência relativa de diferentes tipos de decaimentos radioativos (alfa, beta e gama) depende de muitos fatores, incluindo a força das forças envolvidas e o número de maneiras pelas quais uma determinada reação pode ocorrer sem violar a conservação de energia e momento. A frequência com que ocorre um decaimento radioativo geralmente depende de um equilíbrio sensível das forças fortes e eletromagnéticas.
Como outro exemplo, considere a série de decaimento U-238 mostrada na Figura\(\PageIndex{4}\). Após vários decaimentos alfa e beta, a série termina com o núcleo estável Pb-206.
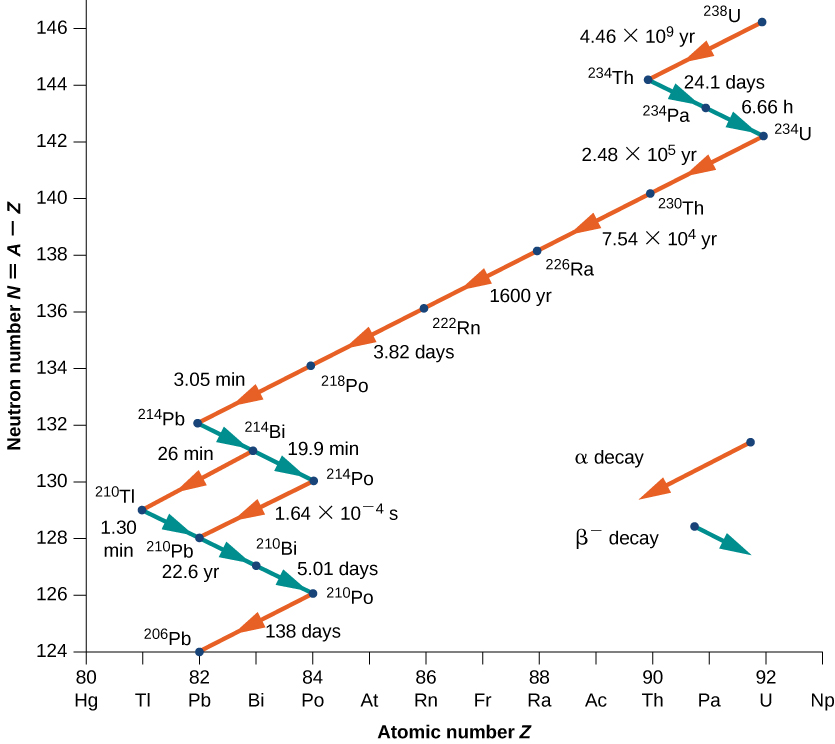
Um exemplo de decaimento cujo núcleo parental não existe mais naturalmente é mostrado na Figura\(\PageIndex{5}\). Começa com Neptúnio-237 e termina no núcleo estável Bismuth-209. O neptúnio é chamado de elemento transurânico porque está além do urânio na tabela periódica. O urânio tem o maior número atômico\((Z + 92)\) de qualquer elemento encontrado na natureza. Elementos com\(Z > 92\) podem ser produzidos somente em laboratório. Eles provavelmente também existiam na natureza na época da formação da Terra, mas por causa de sua vida útil relativamente curta, eles se deterioraram completamente. Não há nada fundamentalmente diferente entre elementos naturais e artificiais.
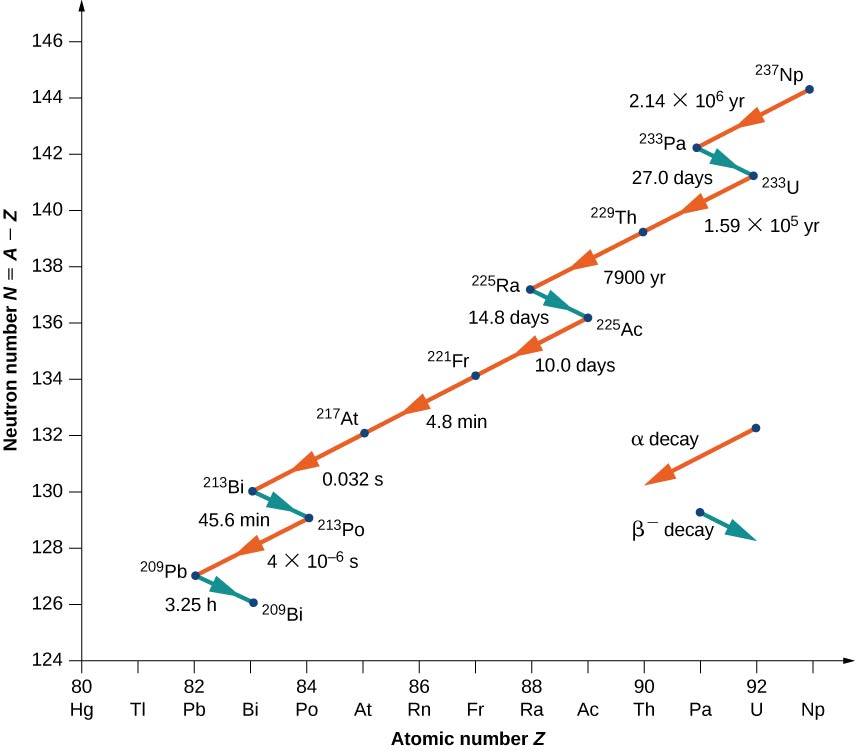
Observe que, para Bi (21), o decaimento pode prosseguir por decaimento alfa ou beta.
Radioatividade na Terra
De acordo com geólogos, se não houvesse fonte de calor, a Terra deveria ter esfriado até sua temperatura atual em no máximo 1 bilhão de anos. No entanto, a Terra tem mais de 4 bilhões de anos. Por que a Terra está esfriando tão lentamente? A resposta é a radioatividade nuclear, ou seja, partículas de alta energia produzidas em decaimentos radioativos aquecem a Terra por dentro (Figura\(\PageIndex{6}\)).
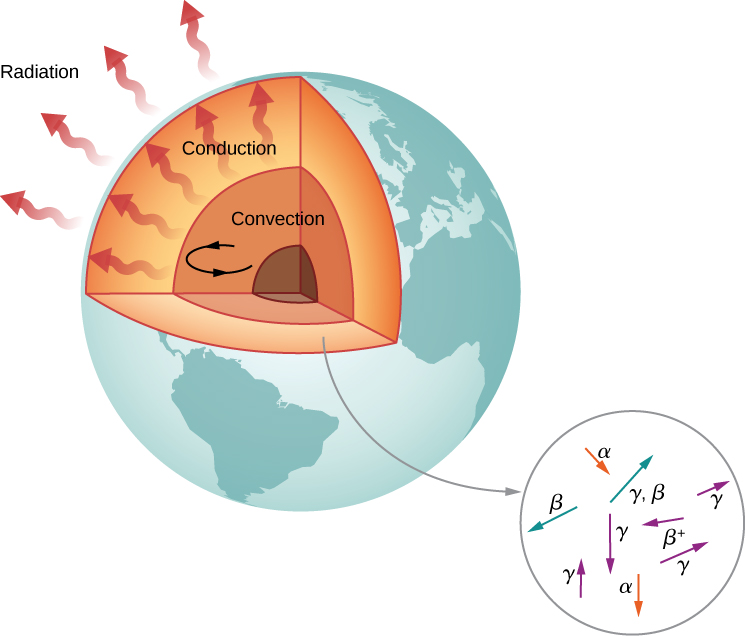
Os núcleos candidatos a esse modelo de aquecimento são\(^{238}U\) e\(^{40}K\), que possuem meias-vidas semelhantes ou maiores que a idade da Terra. A energia produzida por esses decaimentos (por segundo por metro cúbico) é pequena, mas a energia não pode escapar facilmente, então o núcleo da Terra é muito quente. A energia térmica no núcleo da Terra é transferida para a superfície da Terra e para longe dela por meio dos processos de convecção, condução e radiação.


