8.4 : Fermentation
- Page ID
- 187713
Objectifs d'apprentissage
- Définissez la fermentation et expliquez pourquoi elle ne nécessite pas d'oxygène
- Décrivez les voies de fermentation et leurs produits finaux et donnez des exemples de microorganismes qui utilisent ces voies
- Comparez et opposez la fermentation et la respiration anaérobie
De nombreuses cellules sont incapables de respirer en raison d'une ou de plusieurs des circonstances suivantes :
- La cellule ne dispose pas d'une quantité suffisante de tout accepteur d'électrons final inorganique approprié pour effectuer la respiration cellulaire.
- La cellule ne possède pas les gènes nécessaires pour fabriquer des complexes et des porteurs d'électrons appropriés dans le système de transport d'électrons.
- La cellule ne possède pas les gènes nécessaires à la production d'une ou de plusieurs enzymes dans le cycle de Krebs.
Alors que l'absence d'un accepteur final d'électrons inorganique approprié dépend de l'environnement, les deux autres conditions sont déterminées génétiquement. Ainsi, de nombreux procaryotes, y compris des membres du genre Streptococcus, important sur le plan clinique, sont définitivement incapables de respirer, même en présence d'oxygène. À l'inverse, de nombreux procaryotes sont facultatifs, ce qui signifie que, si les conditions environnementales changent pour fournir un accepteur final d'électrons inorganique approprié pour la respiration, les organismes contenant tous les gènes nécessaires à cette fin passeront à la respiration cellulaire pour le métabolisme du glucose parce que la respiration permet une production d'ATP beaucoup plus importante par molécule de glucose.
Si la respiration ne se produit pas, le NADH doit être réoxydé en NAD+ pour être réutilisé comme porteur d'électrons pour la glycolyse, le seul mécanisme cellulaire de production d'ATP, pour continuer. Certains systèmes vivants utilisent une molécule organique (généralement du pyruvate) comme accepteur final d'électrons par le biais d'un processus appelé fermentation. La fermentation n'implique pas de système de transport d'électrons et ne produit pas directement d'ATP supplémentaire par rapport à celui produit lors de la glycolyse par phosphorylation au niveau du substrat. Les organismes effectuant la fermentation, appelés fermenteurs, produisent au maximum deux molécules d'ATP par glucose pendant la glycolyse. Le tableau\(\PageIndex{1}\) compare les accepteurs d'électrons finaux et les méthodes de synthèse de l'ATP en respiration aérobie, en respiration anaérobie et en fermentation. Notez que le nombre de molécules d'ATP indiqué pour la glycolyse suppose la voie Embden-Meyerhof-Parnas. Le nombre de molécules d'ATP fabriquées par phosphorylation au niveau du substrat (SLP) par rapport à la phosphorylation oxydative (OP) est indiqué.
| Type de métabolisme | Exemple | Accepteur d'électrons final | Voies impliquées dans la synthèse de l'ATP (type de phosphorylation) | Rendement maximal en molécules d'ATP |
|---|---|---|---|---|
| Respiration aérobie | Pseudomonas aeruginosa | \(\ce{O2}\) |
Glycolyse EMP (SLP) Cycle de Krebs (SLP) Transport d'électrons et chimiosmose (OP) : |
2 2 34 |
| Totale | 38 | |||
| Respiration anaérobie | Paracoccus denitrificans |
\(\ce{NO3-}\),\(\ce{SO4^{-2}}\)\(\ce{Fe^{+3}}\),\(\ce{CO2}\), autres matières inorganiques |
Glycolyse EMP (SLP) Cycle de Krebs (SLP) Transport d'électrons et chimiosmose (OP) : |
2 2 1 à 32 |
| Totale | 5 — 36 | |||
| Fermentation | Candida albicans |
Produits organiques (généralement du pyruvate) |
Glycolyse EMP (SLP) Fermentation |
2 0 |
| Totale | 2 |
Les processus de fermentation microbienne ont été manipulés par l'homme et sont largement utilisés dans la production de divers aliments et d'autres produits commerciaux, y compris des produits pharmaceutiques. La fermentation microbienne peut également être utile pour identifier les microbes à des fins diagnostiques.
La fermentation par certaines bactéries, comme celles présentes dans le yogourt et d'autres produits alimentaires acides, et par les animaux dans les muscles lors de la déplétion en oxygène, est une fermentation à l'acide lactique. La réaction chimique de la fermentation de l'acide lactique est la suivante :
\[\ce{Pyruvate + NADH \leftrightarrow lactic\: acid + NAD+}\]
Les bactéries de plusieurs genres Gram positif, dont Lactobacillus, Leuconostoc et Streptococcus, sont collectivement appelées bactéries de l'acide lactique (LAB), et diverses souches jouent un rôle important dans la production alimentaire. Lors de la production de yaourts et de fromages, l'environnement très acide généré par la fermentation de l'acide lactique dénature les protéines contenues dans le lait, ce qui provoque sa solidification. Lorsque l'acide lactique est le seul produit de fermentation, on parle de fermentation homolactique ; c'est le cas pour Lactobacillus delbrueckii et S. thermophiles utilisés dans la production de yaourts. Cependant, de nombreuses bactéries effectuent une fermentation hétérolactique, produisant ainsi un mélange d'acide lactique, d'éthanol et/ou d'acide acétique et de CO 2, en raison de leur utilisation de la voie du pentose phosphate ramifié au lieu de la voie EMP pour la glycolyse. Un fermenteur hétérolactique important est le Leuconostoc mesenteroides, qui est utilisé pour acidifier des légumes tels que les concombres et les choux, pour produire des cornichons et de la choucroute, respectivement.
Les bactéries lactiques sont également importantes sur le plan médical. La production d'environnements à faible pH dans l'organisme inhibe l'établissement et la croissance d'agents pathogènes dans ces zones. Par exemple, le microbiote vaginal est principalement composé de bactéries lactiques, mais lorsque ces bactéries sont réduites, les levures peuvent proliférer, provoquant une infection à levures. De plus, les bactéries lactiques jouent un rôle important dans le maintien de la santé du tractus gastro-intestinal et constituent donc le principal composant des probiotiques.
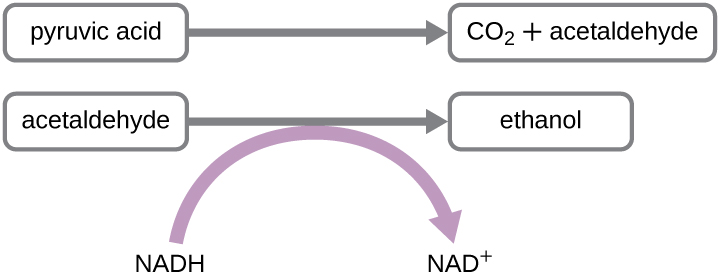
Un autre procédé de fermentation connu est la fermentation alcoolique, qui produit de l'éthanol. La réaction de fermentation de l'éthanol est illustrée sur la figure\(\PageIndex{1}\). Dans la première réaction, l'enzyme pyruvate décarboxylase élimine un groupe carboxyle du pyruvate, libérant du CO 2 gazeux tout en produisant l'acétaldéhyde à deux atomes de carbone. La seconde réaction, catalysée par l'enzyme alcool déshydrogénase, transfère un électron du NADH à l'acétaldéhyde, produisant de l'éthanol et du NAD+. La fermentation à l'éthanol du pyruvate par la levure Saccharomyces cerevisiae est utilisée dans la production de boissons alcoolisées et augmente également la production de produits de boulangerie en raison de la production de CO 2. En dehors de l'industrie alimentaire, la fermentation à l'éthanol des produits végétaux joue un rôle important dans la production de biocarburants.
Au-delà de la fermentation de l'acide lactique et de la fermentation alcoolique, de nombreuses autres méthodes de fermentation sont utilisées chez les procaryotes, toutes dans le but de garantir un apport adéquat en NAD+ pour la glycolyse (Tableau\(\PageIndex{2}\)). Sans ces voies, la glycolyse ne se produirait pas et aucun ATP ne serait prélevé lors de la dégradation du glucose. Il convient de noter que la plupart des formes de fermentation, outre la fermentation homolactique, produisent du gaz, généralement du CO 2 et/ou de l'hydrogène gazeux. Bon nombre de ces différents types de voies de fermentation sont également utilisés dans la production alimentaire et chacune entraîne la production de différents acides organiques, contribuant ainsi à la saveur unique d'un produit alimentaire fermenté particulier. L'acide propionique produit lors de la fermentation de l'acide propionique contribue au goût distinctif du fromage suisse, par exemple.
Plusieurs produits de fermentation sont importants sur le plan commercial en dehors de l'industrie alimentaire. Par exemple, des solvants chimiques tels que l'acétone et le butanol sont produits lors de la fermentation acétone-butanol-éthanol. Les composés pharmaceutiques organiques complexes utilisés dans les antibiotiques (par exemple, la pénicilline), les vaccins et les vitamines sont produits par fermentation acide mixte. Les produits de fermentation sont utilisés en laboratoire pour différencier diverses bactéries à des fins diagnostiques. Par exemple, les bactéries entériques sont connues pour leur capacité à effectuer une fermentation acide mixte, réduisant ainsi le pH, qui peut être détecté à l'aide d'un indicateur de pH. De même, la production bactérienne d'acétoïne lors de la fermentation du butanediol peut également être détectée. La production de gaz par fermentation peut également être observée dans un tube de Durham inversé qui piège le gaz produit dans un bouillon de culture.
Les microbes peuvent également être différenciés en fonction des substrats qu'ils peuvent fermenter. Par exemple, E. coli peut fermenter le lactose et former du gaz, alors que certains de ses proches parents gram-négatifs ne le peuvent pas. La capacité de fermenter le sorbitol, un alcool de sucre, est utilisée pour identifier la souche entérohémorragique pathogène O157:H7 d'E. coli car, contrairement aux autres souches d'E. coli, elle est incapable de fermenter le sorbitol. Enfin, la fermentation du mannitol permet de différencier le Staphylococcus aureus fermentant du mannitol des autres staphylocoques qui ne fermentent pas le mannitol.
| Sentier | Produits finaux | Exemple de microbes | Produits commerciaux |
|---|---|---|---|
| Acétone-butanol-éthanol | Acétone, butanol, éthanol, CO 2 | Clostridium acetobutylicum | Solvants commerciaux, solution de rechange |
| Alcool | Éthanol, CO 2 | Candida, Saccharomyces | Bière, pain |
| Butanediol | Acide formique et lactique ; éthanol ; acétoïne ; 2,3-butanediol ; CO 2 ; hydrogène gazeux | Klebsiella, Enterobacter | Vin Chardonnay |
| Acide butyrique | Acide butyrique, CO 2, hydrogène | Clostridium butyricum | beurre |
| Acide lactique | Acide lactique | Streptocoque, Lactobacillus | Choucroute, yaourt, fromage |
| Acide mixte | Acides acétique, formique, lactique et succinique ; éthanol, CO 2, hydrogène gazeux | Escherichia, Shigella | Vinaigre, cosmétiques, produits pharmaceutiques |
| Acide propionique | Acide acétique, acide propionique, CO 2 | Propionibacterium, Bifidobacterium | Fromage suisse |
Exercice\(\PageIndex{1}\)
Quand un microbe métaboliquement polyvalent effectuerait-il la fermentation plutôt que la respiration cellulaire ?
Identification des bactéries à l'aide de panels de test API
L'identification d'un isolat microbien est essentielle au bon diagnostic et au traitement approprié des patients. Les scientifiques ont développé des techniques qui identifient les bactéries en fonction de leurs caractéristiques biochimiques. En général, ils examinent l'utilisation de sources de carbone spécifiques comme substrats pour la fermentation ou d'autres réactions métaboliques, ou ils identifient les produits de fermentation ou les enzymes spécifiques présents dans les réactions. Dans le passé, les microbiologistes utilisaient des tubes à essai et des plaques individuels pour effectuer des tests biochimiques. Cependant, les scientifiques, en particulier ceux des laboratoires cliniques, utilisent désormais de plus en plus fréquemment des panneaux multitests jetables en plastique qui contiennent un certain nombre de tubes de réaction miniatures, chacun comprenant généralement un substrat et un indicateur de pH spécifiques. Après inoculation du panel d'essai avec un petit échantillon du microbe en question et incubation, les scientifiques peuvent comparer les résultats à une base de données qui inclut les résultats attendus pour des réactions biochimiques spécifiques pour des microbes connus, permettant ainsi l'identification rapide d'un échantillon de microbe. Ces panels de test ont permis aux scientifiques de réduire les coûts tout en améliorant l'efficacité et la reproductibilité en effectuant un plus grand nombre de tests simultanément.
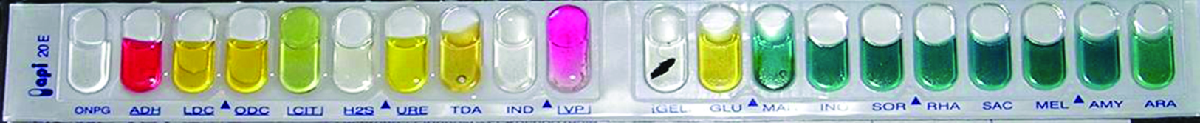
De nombreux panels d'essais biochimiques miniaturisés commerciaux couvrent un certain nombre de groupes de bactéries et de levures cliniquement importants. L'un des panels de test les plus anciens et les plus populaires est le panneau Analytical Profile Index (API) inventé dans les années 1970. Une fois qu'une caractérisation de base en laboratoire d'une souche donnée a été effectuée, telle que la détermination de la morphologie de Gram de la souche, une bandelette de test appropriée contenant 10 à 20 tests biochimiques différents pour différencier les souches au sein de ce groupe microbien peut être utilisée. Actuellement, les différentes bandelettes API peuvent être utilisées pour identifier rapidement et facilement plus de 600 espèces de bactéries, aérobies et anaérobies, et environ 100 types de levures différents. Sur la base des couleurs des réactions lorsque des produits finaux métaboliques sont présents, en raison de la présence d'indicateurs de pH, un profil métabolique est créé à partir des résultats (Figure\(\PageIndex{2}\)). Les microbiologistes peuvent ensuite comparer le profil de l'échantillon à celui de la base de données pour identifier le microbe spécifique.
Orientation clinique : partie 2
De nombreux symptômes de Hannah sont compatibles avec plusieurs infections différentes, dont la grippe et la pneumonie. Cependant, ses réflexes léthargiques, sa sensibilité à la lumière et sa raideur de la nuque suggèrent une atteinte possible du système nerveux central, ce qui indique peut-être une méningite. La méningite est une infection du liquide céphalorachidien (LCR) qui entoure le cerveau et la moelle épinière et qui provoque une inflammation des méninges, les couches protectrices qui recouvrent le cerveau. La méningite peut être causée par des virus, des bactéries ou des champignons. Bien que toutes les formes de méningite soient graves, la méningite bactérienne l'est particulièrement. La méningite bactérienne peut être causée par plusieurs bactéries différentes, mais la bactérie Neisseria meningitidis, un diplocoque en forme de haricot à Gram négatif, est une cause fréquente et entraîne la mort en 1 à 2 jours chez 5 % à 10 % des patients.
Compte tenu de la gravité potentielle de l'état de santé d'Hannah, son médecin a conseillé à ses parents de l'emmener à l'hôpital de Banjul, la capitale gambienne, où elle sera testée et traitée pour une éventuelle méningite. Après 3 heures de route jusqu'à l'hôpital, Hannah a été immédiatement admise. Les médecins ont prélevé un échantillon de sang et pratiqué une ponction lombaire pour tester son LCR. Ils lui ont également immédiatement administré l'antibiotique ceftriaxone, le médicament de choix pour le traitement de la méningite causée par N. meningitidis, sans attendre les résultats des tests de laboratoire.
Exercice\(\PageIndex{2}\)
- Comment utiliser les tests biochimiques pour confirmer l'identité de N. meningitidis ?
- Pourquoi les médecins d'Hannah ont-ils décidé de lui administrer des antibiotiques sans attendre les résultats des tests ?
Concepts clés et résumé
- La fermentation utilise une molécule organique comme accepteur d'électrons final pour régénérer le NAD+ à partir du NADH afin que la glycolyse puisse se poursuivre.
- La fermentation n'implique pas de système de transport d'électrons et aucun ATP n'est produit directement par le processus de fermentation. Les fermenteurs produisent très peu d'ATP, soit seulement deux molécules d'ATP par molécule de glucose pendant la glycolyse.
- Les procédés de fermentation microbienne ont été utilisés pour la production d'aliments et de produits pharmaceutiques et pour l'identification de microbes.
- Au cours de la fermentation de l'acide lactique, le pyruvate accepte les électrons du NADH et est réduit en acide lactique. Les microbes effectuant une fermentation homolactique produisent uniquement de l'acide lactique comme produit de fermentation ; les microbes effectuant une fermentation hétérolactique produisent un mélange d'acide lactique, d'éthanol et/ou d'acide acétique et de CO 2.
- La production d'acide lactique par le microbiote normal empêche la croissance d'agents pathogènes dans certaines régions du corps et est importante pour la santé du tractus gastro-intestinal.
- Pendant la fermentation de l'éthanol, le pyruvate est d'abord décarboxylé (libérant du CO 2) en acétaldéhyde, qui accepte ensuite les électrons du NADH, réduisant l'acétaldéhyde en éthanol. La fermentation à l'éthanol est utilisée pour la production de boissons alcoolisées, pour la production de produits de boulangerie et pour la production de biocarburants.
- Les produits de fermentation des voies (par exemple, la fermentation à l'acide propionique) confèrent des saveurs distinctives aux produits alimentaires. La fermentation est utilisée pour produire des solvants chimiques (fermentation acétone-butanol-éthanol) et des produits pharmaceutiques (fermentation acide mixte).
- Des types spécifiques de microbes peuvent être distingués par leurs voies de fermentation et leurs produits. Les microbes peuvent également être différenciés en fonction des substrats qu'ils sont capables de fermenter.


