8.3 : Respiration cellulaire
- Page ID
- 187714
Objectifs d'apprentissage
- Comparer et contraster la localisation et la fonction du système de transport d'électrons dans une cellule procaryote et une cellule eucaryote
- Comparer et contraster les différences entre la phosphorylation au niveau du substrat et la phosphorylation oxydative
- Expliquer la relation entre la chimiosmose et la force motrice des protons
- Décrire la fonction et la localisation de l'ATP synthase dans une cellule procaryote par rapport à une cellule eucaryote
- Comparez et comparez la respiration aérobie et anaérobie
Nous venons de discuter de deux voies du catabolisme du glucose, la glycolyse et le cycle de Krebs, qui génèrent de l'ATP par phosphorylation au niveau du substrat. Cependant, la majeure partie de l'ATP est générée lors d'un processus distinct appelé phosphorylation oxydative, qui se produit pendant la respiration cellulaire. La respiration cellulaire commence lorsque les électrons sont transférés du NADH et du FADH 2, produits lors de la glycolyse, de la réaction de transition et du cycle de Krebs, par le biais d'une série de réactions chimiques vers un accepteur d'électrons inorganique final (soit de l'oxygène dans la respiration aérobie, soit des molécules inorganiques non oxygénées dans respiration anaérobie). Ces transferts d'électrons ont lieu sur la partie interne de la membrane cellulaire des cellules procaryotes ou dans des complexes protéiques spécialisés de la membrane interne des mitochondries des cellules eucaryotes. L'énergie des électrons est récoltée pour générer un gradient électrochimique à travers la membrane, qui est utilisé pour fabriquer de l'ATP par phosphorylation oxydative.
Système de transport d'électrons
Le système de transport d'électrons (ETS) est le dernier composant impliqué dans le processus de respiration cellulaire ; il comprend une série de complexes protéiques associés à la membrane et de porteurs d'électrons accessoires mobiles associés. Le transport d'électrons est une série de réactions chimiques qui ressemblent à une brigade de seaux en ce sens que les électrons du NADH et du FADH 2 passent rapidement d'un porteur d'électrons ETS à l'autre. Ces porteurs peuvent faire passer des électrons dans l'ETS en raison de leur potentiel redox. Pour qu'une protéine ou un produit chimique accepte les électrons, elle doit avoir un potentiel redox plus positif que le donneur d'électrons. Par conséquent, les électrons passent des porteurs d'électrons ayant un potentiel redox négatif vers ceux qui ont un potentiel redox plus positif. Les quatre principales classes de porteurs d'électrons impliqués dans les systèmes de transport d'électrons eucaryotes et procaryotes sont les cytochromes, les flavoprotéines, les protéines fer-soufre et les quinones.
Lors de la respiration aérobie, l'accepteur d'électrons final (c'est-à-dire celui ayant le potentiel redox le plus positif) à la fin de l'ETS est une molécule d'oxygène (O 2) qui est réduite en eau (H 2 O) par le porteur final de l'ETS. Ce vecteur d'électrons, la cytochrome oxydase, diffère selon les types de bactéries et peut être utilisé pour différencier des bactéries étroitement apparentées à des fins diagnostiques. Par exemple, l'opportuniste à Gram négatif Pseudomonas aeruginosa et le Vibrio cholerae responsable du choléra à Gram négatif utilisent la cytochrome c oxydase, qui peut être détectée par le test à l'oxydase, tandis que d'autres entérobactéries à Gram négatif, comme E. coli, sont négatives pour cela test car ils produisent différents types de cytochrome oxydase.
Il existe de nombreuses circonstances dans lesquelles la respiration aérobie n'est pas possible, notamment dans l'une ou plusieurs des situations suivantes :
- La cellule ne possède pas de gènes codant pour une cytochrome oxydase appropriée pour transférer les électrons vers l'oxygène à la fin du système de transport d'électrons.
- La cellule ne possède pas de gènes codant pour des enzymes permettant de minimiser les effets graves des dangereux radicaux d'oxygène produits lors de la respiration aérobie, tels que le peroxyde d'hydrogène (H 2 O 2) ou le superoxyde\((\ce{O2-})\).
- La cellule ne dispose pas d'une quantité suffisante d'oxygène pour effectuer la respiration aérobie.
Une alternative possible à la respiration aérobie est la respiration anaérobie, qui utilise une molécule inorganique autre que l'oxygène comme accepteur final d'électrons. Il existe de nombreux types de respiration anaérobie chez les bactéries et les archées. Les dénitrifiants sont d'importantes bactéries du sol qui utilisent le nitrate\((\ce{NO3-})\) et le nitrite\((\ce{NO2-})\) comme accepteurs finaux d'électrons, produisant de l'azote gazeux (N 2). De nombreuses bactéries respirant par voie aérobie, y compris E. coli, utilisent le nitrate comme accepteur final d'électrons et produisent du nitrite lorsque les niveaux d'oxygène sont épuisés.
Les microbes utilisant la respiration anaérobie ont généralement un cycle de Krebs intact, de sorte que ces organismes peuvent accéder à l'énergie des molécules de NADH et de FADH 2 formées. Cependant, les respirateurs anaérobies utilisent des porteurs ETS modifiés codés par leur génome, y compris des complexes distincts pour le transfert d'électrons vers leurs accepteurs d'électrons finaux. De plus petits gradients électrochimiques sont générés par ces systèmes de transfert d'électrons, de sorte que moins d'ATP est formé par la respiration anaérobie.
Exercice\(\PageIndex{1}\)
La respiration aérobie et la respiration anaérobie utilisent-elles toutes deux une chaîne de transport d'électrons ?
Chimiosmose, force motrice des protons et phosphorylation oxydative
Lors de chaque transfert d'un électron à travers l'ETS, l'électron perd de l'énergie, mais lors de certains transferts, l'énergie est stockée sous forme d'énergie potentielle en l'utilisant pour pomper des ions hydrogène (H +) à travers une membrane. Dans les cellules procaryotes, le H + est pompé vers l'extérieur de la membrane cytoplasmique (appelé espace périplasmique chez les bactéries gram-négatives et grampositives), et dans les cellules eucaryotes, il est pompé de la matrice mitochondriale à travers la membrane mitochondriale interne vers l'espace intermembranaire. La distribution inégale de H + à travers la membrane crée un gradient électrochimique, car les ions H + sont chargés positivement (électricité) et leur concentration (chimique) est plus élevée sur un côté de la membrane. Ce gradient électrochimique formé par l'accumulation de H + (également appelé proton) d'un côté de la membrane par rapport à l'autre est appelé force motrice du proton (PMF). Comme les ions impliqués sont H +, un gradient de pH est également établi, la face de la membrane présentant la plus forte concentration de H + étant plus acide. Au-delà de l'utilisation du PMF pour fabriquer de l'ATP, comme indiqué dans ce chapitre, le PMF peut également être utilisé pour entraîner d'autres processus défavorables sur le plan énergétique, notamment le transport des nutriments et la rotation des flagelles pour la motilité.
L'énergie potentielle de ce gradient électrochimique généré par l'ETS provoque la diffusion du H + à travers une membrane (la membrane plasmique des cellules procaryotes et la membrane interne des mitochondries des cellules eucaryotes). Ce flux d'ions hydrogène à travers la membrane, appelé chimiosmose, doit se produire par un canal de la membrane via un complexe enzymatique lié à la membrane appelé ATP synthase (Figure\(\PageIndex{1}\)). La tendance à ce mouvement est similaire à celle de l'eau accumulée d'un côté d'un barrage et traverse le barrage lorsqu'elle est ouverte. L'ATP synthase (comme une combinaison de l'absorption et du générateur d'un barrage hydroélectrique) est une protéine complexe qui agit comme un minuscule générateur, tournant sous l'effet de la force du H + diffusant à travers l'enzyme, vers le bas de leur gradient électrochimique, d'où de nombreux H + se repoussent mutuellement vers où il y a moins de H +. Dans les cellules procaryotes, le H + s'écoule de l'extérieur de la membrane cytoplasmique vers le cytoplasme, tandis que dans les mitochondries eucaryotes, le H + s'écoule de l'espace intermembranaire vers la matrice mitochondriale. La rotation des pièces de cette machine moléculaire permet de régénérer l'ATP à partir de l'ADP et du phosphate inorganique (P i) par phosphorylation oxydative, un deuxième mécanisme de fabrication de l'ATP qui exploite l'énergie potentielle stockée dans un gradient électrochimique.
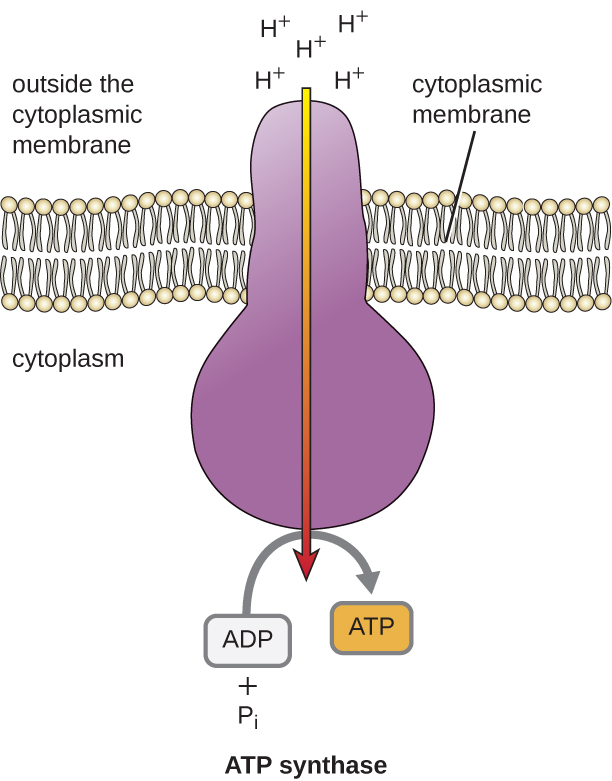
Le nombre de molécules d'ATP générées par le catabolisme du glucose varie. Par exemple, le nombre d'ions hydrogène que les complexes du système de transport d'électrons peuvent pomper à travers la membrane varie selon les espèces d'organismes. Lors de la respiration aérobie des mitochondries, le passage des électrons d'une molécule de NADH génère suffisamment de force motrice pour fabriquer trois molécules d'ATP par phosphorylation oxydative, alors que le passage des électrons d'une molécule de FADH 2 génère une force motrice suffisante pour n'en fabriquer que deux Molécules d'ATP Ainsi, les 10 molécules de NADH fabriquées par glucose pendant la glycolyse, la réaction de transition et le cycle de Krebs transportent suffisamment d'énergie pour fabriquer 30 molécules d'ATP, tandis que les deux molécules de FADH 2 fabriquées par glucose au cours de ces processus fournissent suffisamment d'énergie pour fabriquer quatre molécules d'ATP. Dans l'ensemble, le rendement maximal théorique en ATP produit pendant la respiration aérobie complète du glucose est de 38 molécules, dont quatre sont fabriquées par phosphorylation au niveau du substrat et 34 par phosphorylation oxydative (Figure\(\PageIndex{2}\)). En réalité, le rendement total en ATP est généralement inférieur, allant de une à 34 molécules d'ATP, selon que la cellule utilise la respiration aérobie ou la respiration anaérobie ; dans les cellules eucaryotes, une partie de l'énergie est dépensée pour transporter les intermédiaires du cytoplasme vers les mitochondries, affectant ainsi le rendement en ATP.
La figure\(\PageIndex{2}\) résume les rendements maximaux théoriques d'ATP résultant de divers processus au cours de la respiration aérobie complète d'une molécule de glucose.
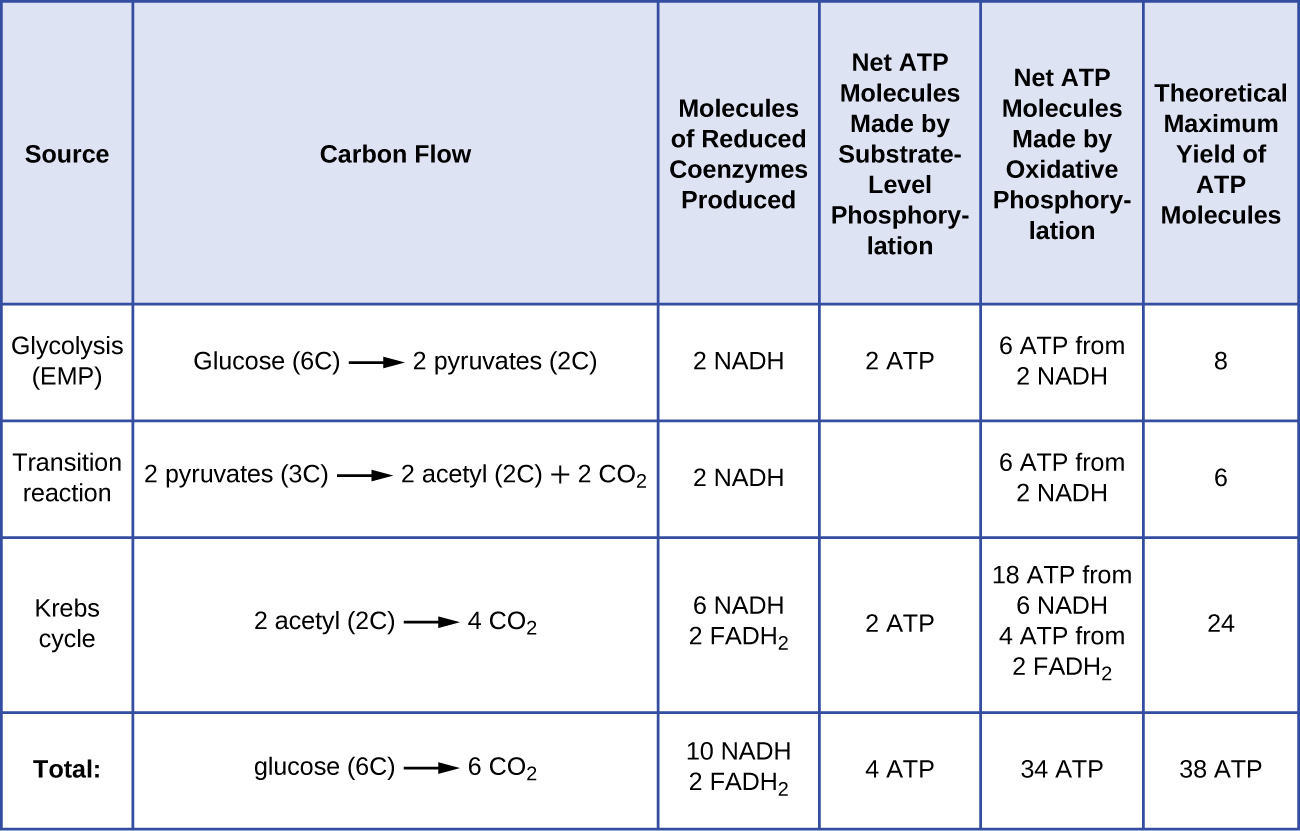
Exercice\(\PageIndex{1}\)
Quelles sont les fonctions de la force motrice du proton ?
Résumé
- La majeure partie de l'ATP générée lors de la respiration cellulaire du glucose est produite par phosphorylation oxydative.
- Un système de transport d'électrons (ETS) est composé d'une série de complexes protéiques associés à la membrane et de porteurs d'électrons accessoires mobiles associés. L'ETS est intégré dans la membrane cytoplasmique des procaryotes et dans la membrane mitochondriale interne des eucaryotes.
- Chaque complexe ETS possède un potentiel redox différent, et les électrons passent des porteurs d'électrons ayant un potentiel redox négatif à ceux ayant un potentiel redox plus positif.
- Pour effectuer la respiration aérobie, une cellule a besoin d'oxygène comme accepteur d'électrons final. Une cellule a également besoin d'un cycle de Krebs complet, d'une cytochrome oxydase appropriée et d'enzymes de détoxification à l'oxygène pour prévenir les effets nocifs des radicaux oxygénés produits lors de la respiration aérobie.
- Les organismes pratiquant la respiration anaérobie utilisent des systèmes de transport d'électrons alternatifs pour le transfert final des électrons vers les accepteurs d'électrons finaux autres que l'oxygène.
- Les microbes présentent de grandes variations dans la composition de leurs systèmes de transport d'électrons, qui peuvent être utilisés à des fins diagnostiques pour aider à identifier certains agents pathogènes.
- Lorsque les électrons passent du NADH et du FADH 2 à travers un ETS, l'électron perd de l'énergie. Cette énergie est stockée par le pompage de H + à travers la membrane, générant ainsi une force motrice du proton.
- L'énergie de cette force motrice du proton peut être exploitée en permettant aux ions hydrogène de rediffuser à travers la membrane par chimiosmose à l'aide de l'ATP synthase. Lorsque les ions hydrogène se diffusent le long de leur gradient électrochimique, les composants de l'ATP synthase tournent et produisent de l'ATP à partir de l'ADP et du P i par phosphorylation oxydative.
- La respiration aérobie produit plus d'ATP (un maximum de 34 molécules d'ATP) lors de la phosphorylation oxydative que la respiration anaérobie (entre une et 32 molécules d'ATP).


