6.1 : Virus
- Page ID
- 187608
Objectifs d'apprentissage
- Décrire les caractéristiques générales des virus en tant qu'agents pathogènes
- Décrire les génomes viraux
- Décrire les caractéristiques générales des cycles de vie des virus
- Différencier les bactériophages, les virus végétaux et les virus animaux
- Décrire les caractéristiques utilisées pour identifier les virus en tant que parasites intracellulaires obligatoires
Orientation clinique : 1ère partie
David, un journaliste de 45 ans, vient de rentrer aux États-Unis après des voyages en Russie, en Chine et en Afrique. Comme il ne se sent pas bien, il se rend chez son médecin généraliste pour se plaindre d'une faiblesse des bras et des jambes, de fièvre, de maux de tête, d'une agitation perceptible et d'un léger malaise. Il pense que cela peut être lié à une morsure de chien qu'il a subie lors d'un entretien avec un fermier chinois. Il ressent des sensations de picotement et de démangeaisons sur le site de la morsure, mais il dit au médecin que le chien semblait en bonne santé et qu'il ne s'inquiétait pas jusqu'à présent. Le médecin a prescrit une culture et un test de sensibilité pour exclure toute infection bactérienne de la plaie, et les résultats se sont révélés négatifs pour toute bactérie pathogène éventuelle.
Exercice\(\PageIndex{1}\)
- Sur la base de ces informations, quels tests supplémentaires doivent être effectués sur le patient ?
- Quel type de traitement le médecin devrait-il recommander ?
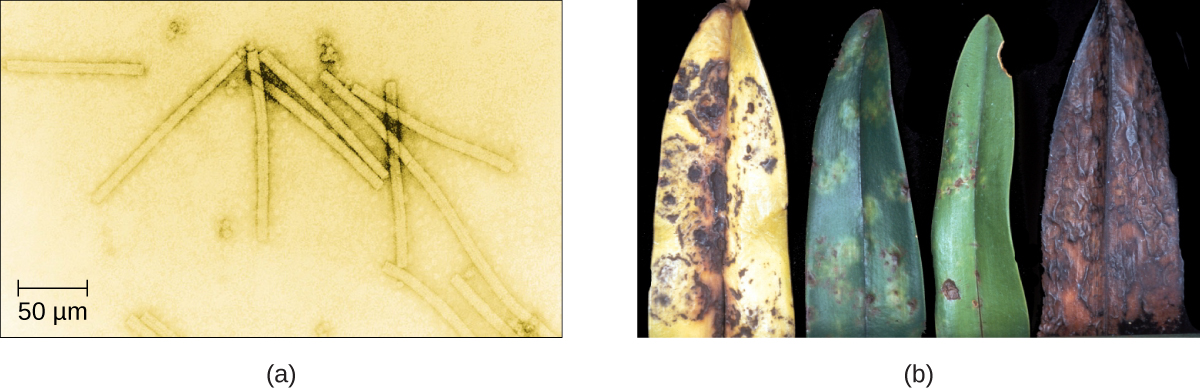
Malgré leur petite taille, qui les empêchait d'être vus au microscope optique, la découverte d'un composant filtrable plus petit qu'une bactérie responsable de la maladie de la mosaïque du tabac (TMD) remonte à 1892. 1 À cette époque, Dimitri Ivanovski, un botaniste russe, a découvert la source de la TMD en utilisant un dispositif de filtration en porcelaine inventé pour la première fois par Charles Chamberland et Louis Pasteur à Paris en 1884. Les filtres Chamberland en porcelaine ont une taille de pores de 0,1 µm, ce qui est suffisamment petit pour éliminer toutes les bactéries ≥ 0,2 µm présentes dans les liquides passant à travers l'appareil. Un extrait obtenu à partir de plants de tabac infectés par le TMD a été produit afin de déterminer la cause de la maladie. Au départ, on pensait que la source de la maladie était bactérienne. Tout le monde a été surpris lorsqu'Ivanovski, à l'aide d'un filtre Chamberland, a découvert que la cause de la TMD n'avait pas été éliminée après avoir fait passer l'extrait à travers le filtre en porcelaine. Donc, si une bactérie n'est pas à l'origine de l'ATM, qu'est-ce qui pourrait être à l'origine de la maladie ? Ivanovski a conclu que la cause de la TMD devait être une bactérie ou une spore bactérienne extrêmement petite. D'autres scientifiques, dont Martinus Beijerinck, ont poursuivi leurs recherches sur la cause du TMD. C'est Beijerinck, en 1899, qui a fini par conclure que l'agent causal n'était pas une bactérie mais plutôt un produit chimique, comme un poison biologique que nous qualifierions aujourd'hui de toxine. En conséquence, le mot virus, qui signifie poison en latin, a été utilisé pour décrire la cause de l'ATM quelques années après la découverte initiale d'Ivanovski. Même s'il n'a pas été en mesure de détecter le virus à l'origine de l'ATM et qu'il ne s'est pas rendu compte que la cause n'était pas une bactérie, Ivanovski est considéré comme le premier découvreur de virus et l'un des fondateurs du domaine de la virologie.
Aujourd'hui, nous pouvons observer des virus à l'aide de microscopes électroniques (Figure\(\PageIndex{1}\)) et nous en savons beaucoup plus à leur sujet. Les virus sont des entités biologiques distinctes ; toutefois, leur origine évolutive reste une question de spéculation. En termes de taxonomie, elles ne sont pas incluses dans l'arbre de vie car elles sont acellulaires (elles ne sont pas constituées de cellules). Pour survivre et se reproduire, les virus doivent infecter un hôte cellulaire, ce qui oblige celui-ci à infecter des parasites intracellulaires. Le génome d'un virus entre dans une cellule hôte et dirige la production des composants viraux, des protéines et des acides nucléiques, nécessaires à la formation de nouvelles particules virales appelées virions. De nouveaux virions sont fabriqués dans la cellule hôte par assemblage de composants viraux. Les nouveaux virions transportent le génome viral vers une autre cellule hôte pour provoquer une nouvelle vague d'infection. \(\PageIndex{1}\)Le tableau résume les propriétés des virus.
| Caractéristiques des virus |
|---|
| Agents pathogènes acellulaires infectieux |
| Parasites intracellulaires obligatoires ayant une spécificité d'hôte et de type cellulaire |
| Génome d'ADN ou d'ARN (jamais les deux) |
| Le génome est entouré d'une capside protéique et, dans certains cas, d'une membrane phospholipidique parsemée de glycoprotéines virales |
| Manque de gènes pour de nombreux produits nécessaires à une reproduction réussie, ce qui nécessite l'exploitation des génomes des cellules hôtes pour se reproduire |
Exercice\(\PageIndex{2}\)
Pourquoi le premier virus étudié a-t-il été confondu avec une toxine ?
Hôtes et transmission virale
Les virus peuvent infecter tous les types de cellules hôtes, y compris celles des plantes, des animaux, des champignons, des protistes, des bactéries et des archées. La plupart des virus ne pourront infecter que les cellules d'une ou de quelques espèces d'organismes. C'est ce qu'on appelle la plage d'hôtes. Cependant, il n'est pas courant de disposer d'une large gamme d'hôtes et les virus n'infectent généralement que des hôtes spécifiques et uniquement des types de cellules spécifiques au sein de ces hôtes. Les virus qui infectent les bactéries sont appelés bactériophages, ou simplement phages. Le mot phage vient du mot grec qui signifie dévorer. D'autres virus sont simplement identifiés par leur groupe d'hôtes, tels que les virus animaux ou végétaux. Une fois qu'une cellule est infectée, les effets du virus peuvent varier en fonction du type de virus. Les virus peuvent provoquer une croissance anormale de la cellule ou la mort cellulaire, modifier le génome de la cellule ou provoquer des effets peu visibles sur la cellule.
Les virus peuvent être transmis par contact direct, par contact indirect avec des vecteurs ou par l'intermédiaire d'un vecteur : un animal qui transmet un agent pathogène d'un hôte à un autre. Les arthropodes tels que les moustiques, les tiques et les mouches sont des vecteurs typiques de maladies virales et peuvent agir comme des vecteurs mécaniques ou biologiques. La transmission mécanique se produit lorsque l'arthropode transporte un agent pathogène viral à l'extérieur de son corps et le transmet à un nouvel hôte par contact physique. La transmission biologique se produit lorsque l'arthropode transporte le pathogène viral à l'intérieur de son corps et le transmet au nouvel hôte par morsure.
Chez l'homme, une grande variété de virus sont capables de provoquer diverses infections et maladies. Certains des agents pathogènes émergents les plus mortels chez l'homme sont les virus, mais nous disposons de peu de traitements ou de médicaments pour traiter les infections virales, ce qui rend leur éradication difficile.
Les virus qui peuvent être transmis d'un hôte animal à un hôte humain peuvent provoquer des zoonoses. Par exemple, le virus de la grippe aviaire prend naissance chez les oiseaux, mais peut provoquer des maladies chez les humains. Les zoonoses inverses sont causées par l'infection d'un animal par un virus d'origine humaine.
Combattre les bactéries avec des virus
L'émergence de superbactéries, ou bactéries multirésistantes, est devenue un défi majeur pour les sociétés pharmaceutiques et un grave problème de santé. Selon un rapport publié en 2013 par les Centers for Disease Control and Prevention (CDC) des États-Unis, plus de 2 millions de personnes sont infectées par des bactéries pharmacorésistantes aux États-Unis chaque année, entraînant au moins 23 000 décès. 2 L'utilisation continue et la surutilisation d'antibiotiques entraîneront probablement l'apparition de souches encore plus résistantes aux médicaments.
L'une des solutions possibles est l'utilisation de la phagothérapie, une procédure qui utilise des virus destructeurs de bactéries (bactériophages) pour traiter les infections bactériennes. La phagothérapie n'est pas une idée nouvelle. La découverte des bactériophages remonte au début du 20e siècle et la phagothérapie a été utilisée pour la première fois en Europe en 1915 par le bactériologiste anglais Frederick Twort. 3 Cependant, la découverte ultérieure de pénicilline et d'autres antibiotiques a entraîné le quasi-abandon de cette forme de traitement, sauf dans l'ex-Union soviétique et dans quelques pays d'Europe de l'Est. L'intérêt pour la phagothérapie en dehors des pays de l'ancienne Union soviétique ne fait que récemment surface en raison de l'augmentation du nombre de bactéries résistantes aux antibiotiques. 4
La phagothérapie présente certains avantages par rapport aux antibiotiques en ce sens que les phages ne tuent qu'une seule bactérie spécifique, alors que les antibiotiques tuent non seulement le pathogène mais également les bactéries bénéfiques du microbiote normal. La mise au point de nouveaux antibiotiques est également coûteuse pour les sociétés pharmaceutiques et pour les patients, en particulier pour ceux qui vivent dans des pays où le taux de pauvreté est élevé.
Des phages ont également été utilisés pour prévenir la détérioration des aliments. En 2006, la Food and Drug Administration des États-Unis a approuvé l'utilisation d'une solution contenant six bactériophages pouvant être pulvérisés sur des viandes telles que la bologne, le jambon et la dinde pour tuer Listeria monocytogenes, une bactérie responsable de la listériose, une forme d'intoxication alimentaire. Certains consommateurs s'inquiètent toutefois de l'utilisation de phages sur les aliments, en particulier compte tenu de la popularité croissante des produits biologiques. Les aliments qui ont été traités avec des phages doivent déclarer « préparation bactériophages » dans la liste des ingrédients ou inclure une étiquette indiquant que la viande a été « traitée avec une solution antimicrobienne pour réduire les microorganismes ». 5
Exercice\(\PageIndex{3}\)
- Pourquoi les humains n'ont-ils pas à se préoccuper de la présence de bactériophages dans leurs aliments ?
- Quels sont les trois moyens de transmission des virus entre hôtes ?
Structures virales
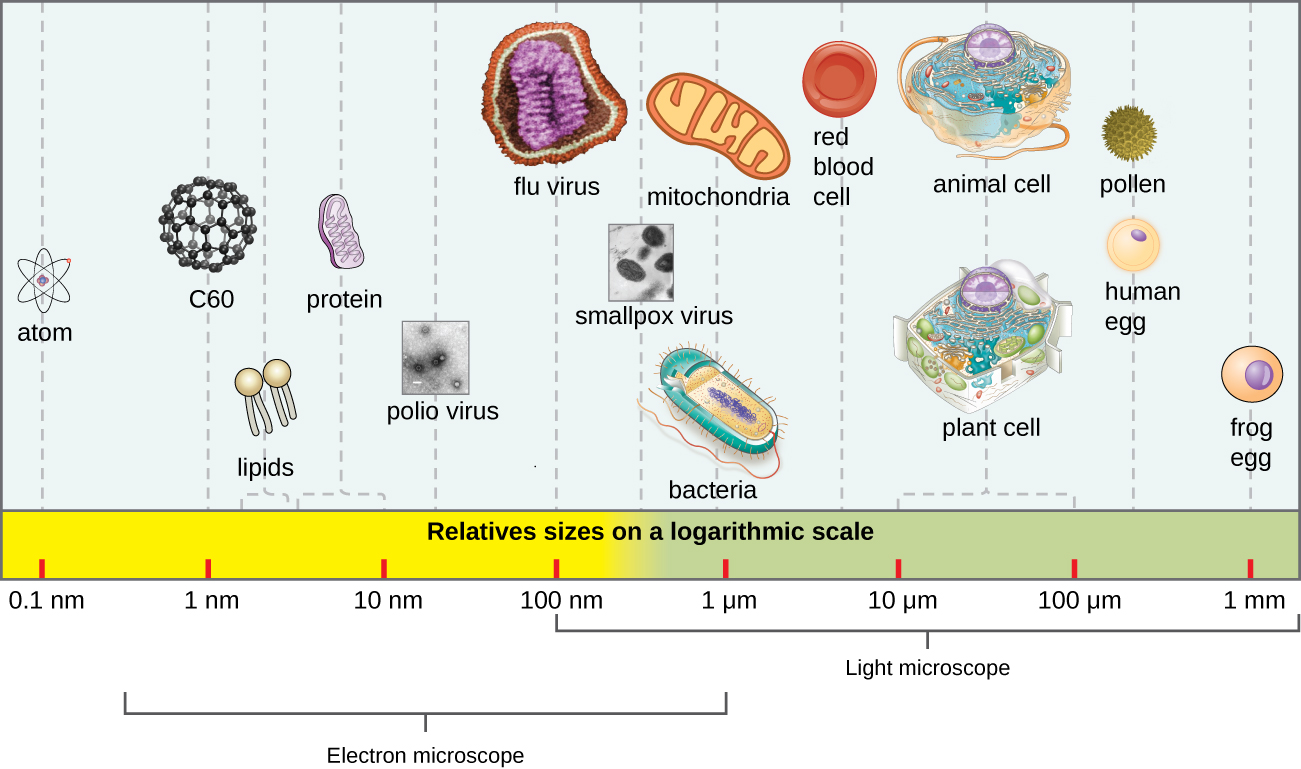
En général, les virions (particules virales) sont petits et ne peuvent pas être observés au microscope optique ordinaire. Elles sont beaucoup plus petites que les cellules procaryotes et eucaryotes ; il s'agit d'une adaptation qui permet aux virus d'infecter ces cellules plus grosses (voir Figure\(\PageIndex{2}\)). La taille d'un virion peut aller de 20 nm pour les petits virus à 900 nm pour les virus classiques de grande taille (voir Figure\(\PageIndex{3}\)). Des découvertes récentes ont toutefois permis d'identifier de nouvelles espèces virales géantes, telles que le Pandoravirus salinus et le Pithovirus sibericum, dont la taille se rapproche de celle d'une cellule bactérienne. 6

En 1935, après la mise au point du microscope électronique, Wendell Stanley a été le premier scientifique à cristalliser la structure du virus de la mosaïque du tabac et a découvert qu'il était composé d'ARN et de protéines. En 1943, il a isolé le virus de la grippe B, ce qui a contribué à la mise au point d'un vaccin antigrippal. Les découvertes de Stanley ont révélé le mystère de la nature des virus qui intriguait les scientifiques depuis plus de 40 ans et ses contributions au domaine de la virologie lui ont valu le prix Nobel en 1946.
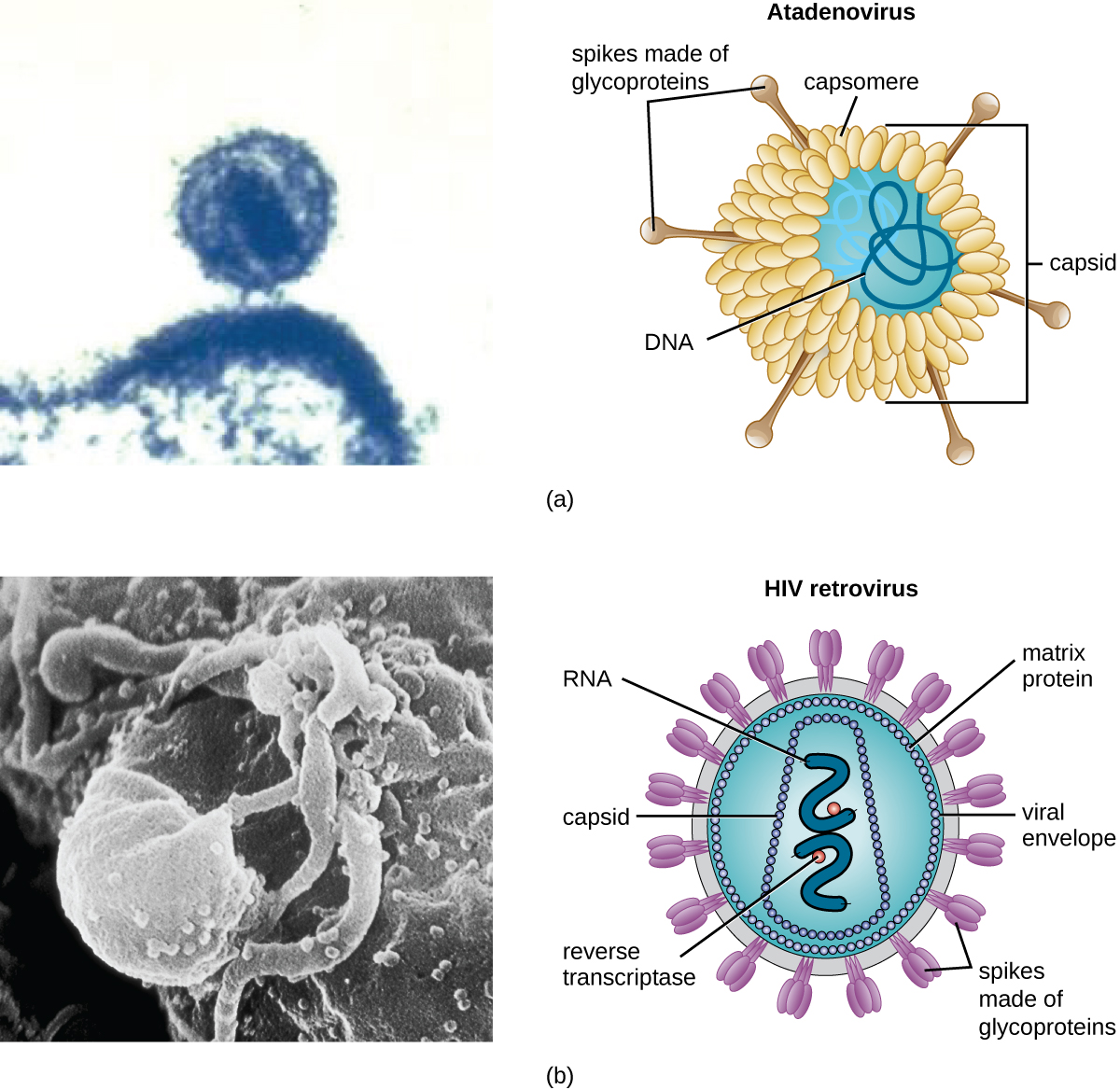
Grâce à des recherches continues sur la nature des virus, nous savons maintenant qu'ils sont constitués d'un acide nucléique (ARN ou ADN, mais jamais les deux) entouré d'une enveloppe protéique appelée capside (voir Figure\(\PageIndex{4}\)). L'intérieur de la capside n'est pas rempli de cytosol, comme dans une cellule, mais contient le strict nécessaire en termes de génome et d'enzymes nécessaires pour diriger la synthèse de nouveaux virions. Chaque capside est composée de sous-unités protéiques appelées capsomères constituées d'un ou de plusieurs types différents de protéines de capsomères qui s'entrelacent pour former une capside serrée.
Il existe deux catégories de virus en fonction de leur composition générale. Les virus formés uniquement à partir d'un acide nucléique et d'une capside sont appelés virus nus ou virus non enveloppés. Les virus formés d'une capside remplie d'acides nucléiques entourée d'une couche lipidique sont appelés virus enveloppés (voir Figure\(\PageIndex{4}\)). L'enveloppe virale est une petite partie de la membrane phospholipidique obtenue sous forme de bourgeons de virion à partir d'une cellule hôte. L'enveloppe virale peut être d'origine intracellulaire ou cytoplasmique.
Des structures protéiques appelées pointes s'étendent vers l'extérieur et s'éloignent de la capside de certains virus nus et de virus enveloppés. À l'extrémité de ces pointes se trouvent des structures qui permettent au virus de se fixer et de pénétrer dans une cellule, comme les pointes d'hémagglutinine (H) du virus de la grippe ou des enzymes telles que les pointes du virus de la grippe à la neuraminidase (N) qui permettent au virus de se détacher de la surface cellulaire lors de la libération de nouveaux virions. Les virus de la grippe sont souvent identifiés par leurs pointes H et N. Par exemple, les virus de la grippe H1N1 étaient responsables des pandémies de 1918 et 2009, 7 H2N2 de la pandémie de 1957 et le virus H3N2 de la pandémie de 1968.
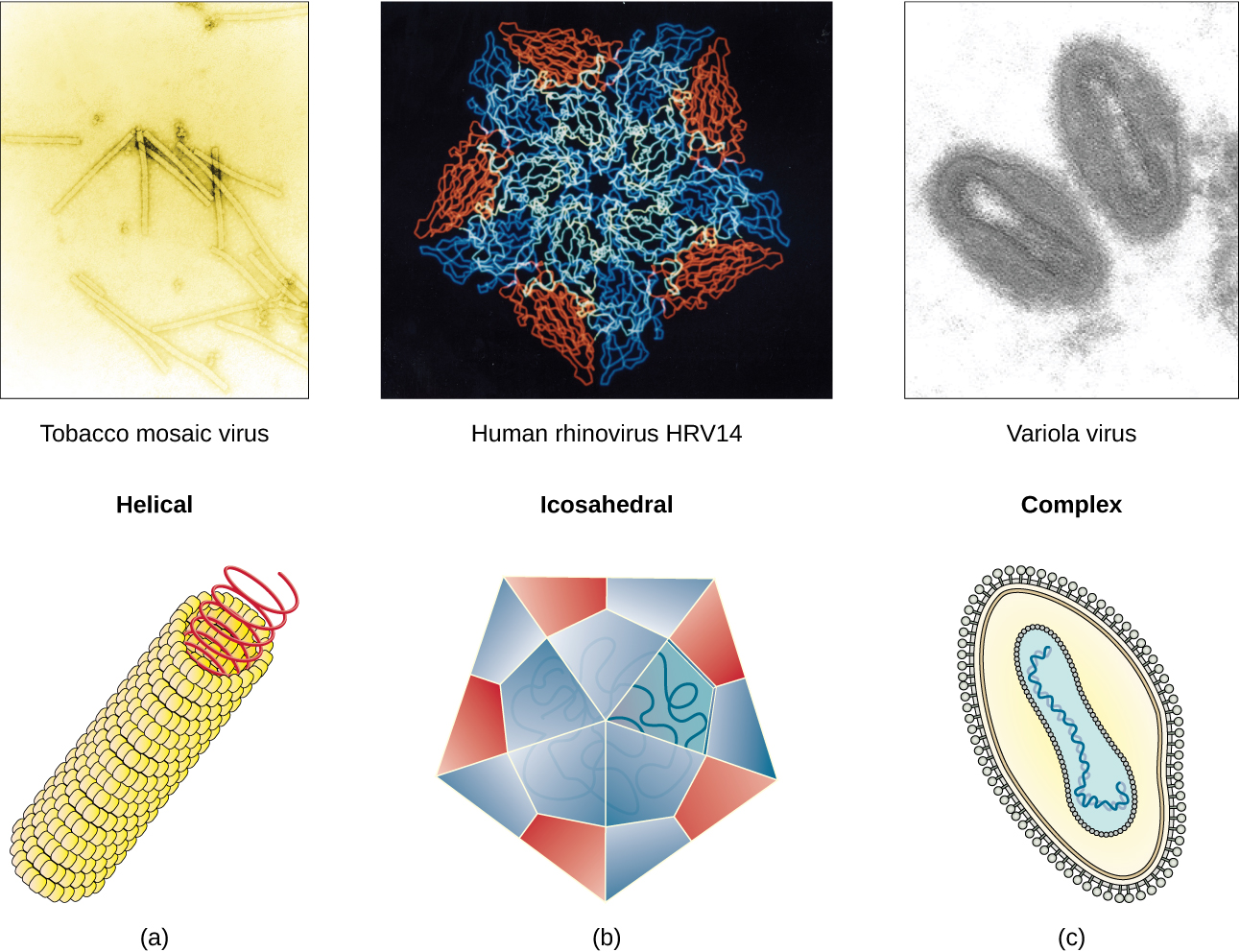
La forme des capsides des virus varie, qui peut être hélicoïdale, polyédrique ou complexe. Une capside hélicoïdale prend la forme du virus de la mosaïque du tabac (TMV), un virus hélicoïdal nu, et du virus Ebola, un virus hélicoïdal enveloppé. La capside est cylindrique ou en forme de bâtonnet, le génome s'insère juste à l'intérieur de la longueur de la capside. Les capsides polyédriques ont la forme d'un poliovirus et d'un rhinovirus et sont constituées d'un acide nucléique entouré d'une capside polyédrique (à plusieurs côtés) en forme d'icosaèdre. Une capside icosaédrique est une structure tridimensionnelle à 20 côtés comportant 12 sommets. Ces capsides ressemblent un peu à un ballon de football. Les virus hélicoïdaux et polyédriques peuvent avoir des enveloppes. Les formes virales observées dans certains types de bactériophages, tels que le phage T4, et les poxvirus, comme le virus de la vaccine, peuvent présenter des caractéristiques à la fois de virus polyédriques et hélicoïdaux, de sorte qu'elles sont décrites comme une forme virale complexe (voir Figure\(\PageIndex{5}\)). Dans la forme complexe des bactériophages, le génome est situé à l'intérieur de la tête polyédrique et la gaine relie la tête aux fibres caudales et aux épingles caudales qui aident le virus à se fixer aux récepteurs situés à la surface de la cellule hôte. Les poxvirus aux formes complexes sont souvent en forme de brique et présentent des caractéristiques de surface complexes que l'on ne retrouve pas dans les autres catégories de capsides.
Exercice\(\PageIndex{4}\)
Quels types de virus présentent des pics ?
Classification et taxonomie des virus
Bien que les virus ne soient pas classés dans les trois domaines de la vie, leur nombre est suffisamment élevé pour nécessiter une classification. Depuis 1971, la Division de virologie de l'Union internationale des sociétés de microbiologie a confié la tâche de développer, d'affiner et de maintenir une taxonomie virale universelle au Comité international de taxonomie des virus (ICTV). Comme les virus peuvent muter si rapidement, il peut être difficile de les classer en genre et en épithète d'espèce à l'aide du système de nomenclature binomiale. Ainsi, le système de nomenclature virale de l'ICTV classe les virus en familles et en genres en fonction de la génétique virale, de la chimie, de la morphologie et du mécanisme de multiplication. À ce jour, l'ICTV a classé les virus connus en sept ordres, 96 familles et 350 genres. Les noms de famille viraux se terminent par - viridae (par exemple, Parvoviridae) et les noms de genre se terminent par −virus (par exemple, Parvovirus). Les noms des ordres viraux, des familles et des genres sont tous en italique. Lorsque nous faisons référence à une espèce virale, nous utilisons souvent un genre et une épithète d'espèce tels que Pandoravirus dulcis ou Pandoravirus salinus.
Le système de classification de Baltimore est une alternative à la nomenclature ICTV. Le système de Baltimore classe les virus en fonction de leur génome (ADN ou ARN, monocaténaire ou double brin, et mode de réplication). Ce système crée ainsi sept groupes de virus qui ont une génétique et une biologie communes.
Découvrez la dernière taxonomie des virus sur le site Web de l'ICTV.
Outre les systèmes formels de nomenclature, les virus sont souvent regroupés de manière informelle en catégories en fonction de leur chimie, de leur morphologie ou d'autres caractéristiques communes. Les catégories peuvent inclure des structures nues ou enveloppées, des génomes d'ADN simple brin (ss) ou double brin (ds) ou d'ARN ss ou ds, des génomes segmentés ou non segmentés et de l'ARN brin positif (+) ou négatif (−). Par exemple, les virus de l'herpès peuvent être classés en tant que virus enveloppés d'ADNd ; le virus de l'immunodéficience humaine (VIH) est un virus enveloppé d'ARN+sRNA et le virus de la mosaïque du tabac est un virus +SSRNA. D'autres caractéristiques telles que la spécificité de l'hôte, la spécificité tissulaire, la forme de la capside et des gènes ou enzymes spéciaux peuvent également être utilisées pour décrire des groupes de virus similaires. Le tableau\(\PageIndex{2}\) répertorie certains des virus les plus courants qui sont des agents pathogènes humains par type de génome.
| Génome | Famille | Exemple de virus | Caractéristiques cliniques |
|---|---|---|---|
| DSDNA, enveloppé | Poxviridae | Orthopoxvirus | Papules, pustules, lésions cutanées |
| Poxviridae | Parapoxvirus | Lésions cutanées | |
| Herpesviridae | Virus Simplex | boutons de fièvre, herpès génital, maladies sexuellement transmissibles | |
| DSDNA, nue | Adénoviridae | Atadénovirus | Infection respiratoire (rhume) |
| Papillomaviridae | Papillomavirus | Verrues génitales, cancer du col de l'utérus, de la vulve ou du vagin | |
| Réoviridae | Réovirus | Gastro-entérite, diarrhée sévère (grippe intestinale) | |
| SSDNA, nue | Parvoviridae | Dépendoparvovirus A adéno-associé | Infection des voies respiratoires |
| Parvoviridae | Dépendoparvovirus B adéno-associé | Infection des voies respiratoires | |
| DSRNA, nue | Réoviridae | Rotavirus | Gastro-entérite |
| + SSRna, nue | Picornaviridés | Entérovirus C | Poliomyélite |
| Picornaviridés | Rhinovirus | Infection des voies respiratoires supérieures (rhume) | |
| Picornaviridés | Hépatovirus | L'hépatite | |
| +SSRNA, enveloppé | Togaviridae | Alphavirus | Encéphalite, fièvre hémorragique |
| Togaviridae | Rubivirus | Rubéole | |
| Rétroviridae | Lentivirus | Syndrome d'immunodéficience acquise (SIDA) | |
| −SSRNA, enveloppé | Filoviridae | Ébolavirus du Zaïre | Fièvre hémorragique |
| Orthomyxoviridae | Influenzavirus A, B, C | Grippe | |
| Rhabdoviridae | Lyssavirus | La rage |
Exercice\(\PageIndex{5}\)
Quels sont les types de génomes des virus ?
Classification des maladies virales
Bien que l'ICTV ait été chargée de la classification biologique des virus, elle a également joué un rôle important dans la classification des maladies causées par des virus. Pour faciliter le suivi des maladies humaines liées aux virus, l'ICTV a créé des classifications liées à la Classification internationale des maladies (CIM), la taxonomie standard des maladies maintenue et mise à jour par l'Organisation mondiale de la santé (OMS). L'ICD attribue un code alphanumérique de six caractères maximum à chaque type d'infection virale, ainsi qu'à tous les autres types de maladies, d'affections médicales et de causes de décès. Ce code ICD est utilisé conjointement avec deux autres systèmes de codage (la terminologie procédurale actuelle et le Healthcare Common Procedure Coding System) pour classer les affections des patients aux fins du traitement et du remboursement de l'assurance.
Par exemple, lorsqu'un patient cherche à se faire soigner pour une infection virale, les codes ICD sont couramment utilisés par les cliniciens pour commander des tests de laboratoire et prescrire des traitements spécifiques au virus soupçonné d'être à l'origine de la maladie. Ce code ICD est ensuite utilisé par les laboratoires médicaux pour identifier les tests qui doivent être effectués pour confirmer le diagnostic. Le code ICD est utilisé par le système de gestion des soins de santé pour vérifier que tous les traitements et tous les travaux de laboratoire effectués sont adaptés au virus donné. Les codeurs médicaux utilisent les codes ICD pour attribuer le code approprié aux interventions effectuées, et les fournisseurs de services médicaux utilisent à leur tour ces informations pour traiter les demandes de remboursement par les compagnies d'assurance. Les responsables de l'état civil utilisent les codes CIM pour enregistrer la cause du décès sur les certificats de décès, et les épidémiologistes ont utilisé les codes CIM pour calculer les statistiques de morbidité et de mortalité.
Exercice\(\PageIndex{6}\)
Identifiez deux endroits où vous trouverez probablement un code ICD.
Orientation clinique : partie 2
Le médecin de David craignait que ses symptômes incluent des picotements et des démangeaisons au site de la morsure du chien ; ces sensations pourraient être des symptômes précoces de la rage. Plusieurs tests sont disponibles pour diagnostiquer la rage chez des patients vivants, mais aucun test antémomortem n'est adéquat. Le médecin a décidé de prélever des échantillons de sang, de salive et de peau de David à des fins d'analyse. L'échantillon de peau a été prélevé sur la nuque (face postérieure du cou, près de la racine des cheveux). Il mesurait environ 6 mm de long et contenait au moins 10 follicules pileux, y compris le nerf cutané superficiel. Une technique de coloration par immunofluorescence a été utilisée sur l'échantillon de biopsie cutanée afin de détecter la présence d'anticorps antirabiques dans les nerfs cutanés situés à la base des follicules pileux. Un test a également été effectué sur un échantillon de sérum prélevé dans le sang de David afin de déterminer si des anticorps contre le virus de la rage avaient été produits.
Entre-temps, l'échantillon de salive a été utilisé pour une analyse par réaction en chaîne par transcriptase-polymérase inverse (RT-PCR), un test qui permet de détecter la présence d'acide nucléique (ARN) viral. Les analyses sanguines se sont révélées positives pour la présence d'antigènes du virus de la rage, ce qui a incité le médecin de David à prescrire un traitement prophylactique. David reçoit une série d'injections intramusculaires d'immunoglobulines antirabiques humaines ainsi qu'une série de vaccins antirabiques.
Exercice\(\PageIndex{7}\)
- Pourquoi la technique d'immunofluorescence recherche-t-elle les anticorps antirabiques plutôt que le virus de la rage lui-même ?
- Si David a contracté la rage, quel est son pronostic ?
Résumé
- Les virus sont généralement ultramicroscopiques, généralement d'une longueur comprise entre 20 nm et 900 nm. Certains virus de grande taille ont été découverts.
- Les virions sont acellulaires et consistent en un acide nucléique, un ADN ou un ARN, mais pas les deux, entourés d'une capside protéique. Une membrane phospholipidique peut également entourer la capside.
- Les virus sont des parasites intracellulaires obligatoires.
- Les virus sont connus pour infecter divers types de cellules présentes dans les plantes, les animaux, les champignons, les protistes, les bactéries et les archées. Les virus ont généralement une gamme d'hôtes limitée et infectent des types de cellules spécifiques.
- Les virus peuvent avoir des formes hélicoïdales, polyédriques ou complexes.
- La classification des virus est basée sur la morphologie, le type d'acide nucléique, la gamme d'hôtes, la spécificité cellulaire et les enzymes présentes dans le virion.
- Comme les autres maladies, les maladies virales sont classées à l'aide des codes ICD.
Notes
- 1 H. Lecoq. « [Découverte du premier virus, le virus de la mosaïque du tabac : 1892 ou 1898 ?]. » Comptes rendus de l'Académie des sciences — Série III — Sciences de la Vie 324, n° 10 (2001) : 929—933.
- 2 Département américain de la santé et des services sociaux, Centres pour le contrôle et la prévention des maladies. « Antibiotic Resistance Threats in the United States, 2013 ». www.cdc.gov/drugresistance/pd... s-2013-508.pdf (consulté le 22 septembre 2015).
- 3 M. Clokie et coll. « Des phages dans la nature. » Bactériophage 1, no 1 (2011) : 31—45.
- 4 A. Sulakvelidze et coll. « Thérapie aux bactériophages. » Agents antimicrobiens et chimiothérapie 45, n° 3 (2001) : 649—659.
- 5 Administration américaine des produits alimentaires et pharmaceutiques. « Approbation par la FDA de la préparation de bactériophages spécifiques à la Listeria sur les produits de viande et de volaille prêts à manger (RTE). » www.fda.gov/food/ingredientsp... /ucm083572.htm (consulté le 22 septembre 2015).
- 6 N. Philippe et coll. « Pandoravirus : virus d'amibe dont le génome atteint 2,5 Mo atteignant celui des eucaryotes parasites. » Science 341, n° 6143 (2013) : 281—286.
- 7 J. Cohen. « Ce qui est ancien est nouveau : le virus de 1918 correspond à la souche H1N1 de 2009. Science 327, n° 5973 (2010) : 1563—1564.


