15.4 : Traitement de l'ARN chez les eucaryotes
- Page ID
- 189817
Compétences à développer
- Décrire les différentes étapes du traitement de l'ARN
- Comprendre l'importance des exons, des introns et de l'épissage
- Expliquer comment les ARNt et les ARNr sont traités
Après la transcription, les pré-ARNm eucaryotes doivent subir plusieurs étapes de traitement avant de pouvoir être traduits. Les ARNt et ARNr eucaryotes (et procaryotes) sont également traités avant de pouvoir fonctionner en tant que composants du mécanisme de synthèse des protéines.
Traitement des ARNm
Le pré-ARNm eucaryote subit un traitement approfondi avant d'être prêt à être traduit. Les étapes supplémentaires impliquées dans la maturation de l'ARNm eucaryote créent une molécule dont la demi-vie est beaucoup plus longue que celle d'un ARNm procaryote. Les ARNm des eucaryotes durent plusieurs heures, alors que l'ARNm typique d'E. coli ne dure pas plus de cinq secondes.
Les pré-ARNm sont d'abord enrobés de protéines stabilisant l'ARN ; celles-ci protègent le pré-ARNm de la dégradation pendant qu'il est traité et exporté hors du noyau. Les trois étapes les plus importantes du traitement pré-ARNm sont l'ajout de facteurs de stabilisation et de signalisation aux extrémités 5' et 3' de la molécule, et l'élimination des séquences intermédiaires qui ne spécifient pas les acides aminés appropriés. Dans de rares cas, le transcrit de l'ARNm peut être « édité » après sa transcription.
Evolution Connection : édition de l'ARN dans les trypanosomes
Les trypanosomes sont un groupe de protozoaires qui comprend l'agent pathogène Trypanosoma brucei, responsable de la maladie du sommeil chez l'homme (Figure\(\PageIndex{1}\)). Les trypanosomes, comme pratiquement tous les autres eucaryotes, possèdent des organites appelés mitochondries qui fournissent de l'énergie chimique à la cellule. Les mitochondries sont des organites qui expriment leur propre ADN et sont considérées comme les vestiges d'une relation symbiotique entre un eucaryote et un procaryote englué. L'ADN mitochondrial des trypanosomes présente une exception intéressante au Dogme central : leurs pré-ARNm ne contiennent pas les informations correctes pour spécifier une protéine fonctionnelle. Habituellement, cela est dû au fait qu'il manque plusieurs nucléotides U à l'ARNm. La cellule effectue une étape supplémentaire de traitement de l'ARN appelée édition de l'ARN pour y remédier.
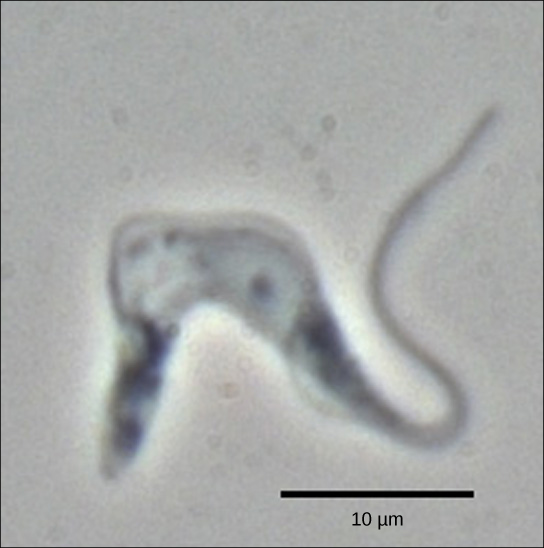
D'autres gènes du génome mitochondrial codent pour des ARNs-guides de 40 à 80 nucléotides. Une ou plusieurs de ces molécules interagissent par appariement de bases complémentaires avec certains des nucléotides du transcrit pré-ARNm. Cependant, l'ARN guide contient plus de nucléotides A que le pré-ARNm ne possède de nucléotides U auxquels se lier. Dans ces régions, l'ARN guide se boucle. Les extrémités 3' des ARN guides ont une longue queue en poly-U, et ces bases U sont insérées dans les régions du transcrit pré-ARNm où les ARN guides sont bouclés. Ce processus est entièrement médié par les molécules d'ARN. C'est-à-dire que les ARN guides, plutôt que les protéines, servent de catalyseurs dans l'édition de l'ARN.
L'édition de l'ARN n'est pas uniquement un phénomène de trypanosomes. Dans les mitochondries de certaines plantes, presque tous les pré-ARNm sont édités. L'édition de l'ARN a également été identifiée chez des mammifères tels que des rats, des lapins et même des humains. Quelle pourrait être la raison évolutive de cette étape supplémentaire du traitement pré-ARNm ? Il est possible que les mitochondries, qui sont des vestiges d'anciens procaryotes, possèdent une méthode tout aussi ancienne basée sur l'ARN pour réguler l'expression des gènes. À l'appui de cette hypothèse, les modifications apportées aux pré-ARNm diffèrent selon les conditions cellulaires. Bien que spéculatif, le processus d'édition de l'ARN peut être un vestige d'une époque primordiale où les molécules d'ARN, au lieu des protéines, étaient responsables des réactions catalysantes.
Plafonnement de 5 minutes
Alors que le pré-ARNm est toujours en cours de synthèse, une capsule de 7-méthylguanosine est ajoutée à l'extrémité 5' du transcrit en croissance par une liaison phosphate. Cette fraction (groupe fonctionnel) protège l'ARNm naissant de la dégradation. De plus, les facteurs impliqués dans la synthèse des protéines reconnaissent le bouchon pour aider à initier la traduction par les ribosomes.
Queue en Poly-A de 3 pieds
Une fois l'élongation terminée, le pré-ARNm est clivé par une endonucléase entre une séquence consensuelle AAUAAA et une séquence riche en Gu, laissant la séquence AAUAAA sur le pré-ARNm. Une enzyme appelée poly-A polymérase ajoute ensuite une chaîne d'environ 200 résidus A, appelée queue de poly-A. Cette modification protège davantage le pré-ARNm de la dégradation et signale l'exportation des facteurs cellulaires dont le transcrit a besoin vers le cytoplasme.
Épissage pré-ARNm
Les gènes eucaryotes sont composés d'exons, qui correspondent à des séquences codant pour les protéines (ex- on signifie qu'ils sont exprimés), et de séquences inertes appelées introns (l'int- ron indique leur rôle int ervenant), qui peuvent être impliqués dans la régulation génique mais sont retirés du pré-ARNm au cours du traitement. Les séquences d'intron présentes dans l'ARNm ne codent pas pour les protéines fonctionnelles.
La découverte d'introns a surpris les chercheurs des années 1970, qui s'attendaient à ce que les pré-ARNm permettent de spécifier des séquences protéiques sans autre traitement, comme ils l'avaient observé chez les procaryotes. Les gènes des eucaryotes supérieurs contiennent très souvent un ou plusieurs introns. Ces régions peuvent correspondre à des séquences régulatrices ; toutefois, la signification biologique de la présence de nombreux introns ou de très longs introns dans un gène n'est pas claire. Il est possible que les introns ralentissent l'expression des gènes parce que la transcription des pré-ARNm avec de nombreux introns prend plus de temps. Les introns peuvent également être des restes de séquences non fonctionnels résultant de la fusion de gènes anciens au cours de l'évolution. Cela est confirmé par le fait que des exons distincts codent souvent des sous-unités ou des domaines protéiques distincts. Dans la plupart des cas, les séquences d'introns peuvent être mutées sans finalement affecter le produit protéique.
Tous les introns d'un pré-ARNm doivent être complètement et précisément éliminés avant la synthèse des protéines. Si le processus se trompe ne serait-ce que par un seul nucléotide, le cadre de lecture des exons réunis changerait et la protéine résultante serait dysfonctionnelle. Le processus d'élimination des introns et de reconnexion des exons est appelé épissage (Figure\(\PageIndex{2}\)). Les introns sont retirés et dégradés alors que le pré-ARNm est encore dans le noyau. L'épissage se fait par un mécanisme spécifique à la séquence qui garantit que les introns seront retirés et que les exons seront rejoints avec la précision d'un seul nucléotide. L'épissage des pré-ARNm est effectué par des complexes de protéines et de molécules d'ARN appelés épissages.
Art Connection
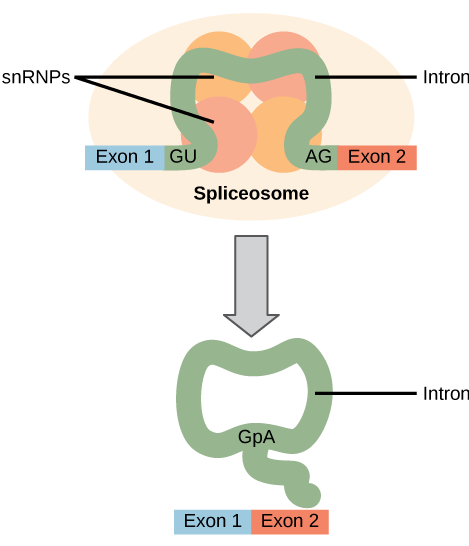
Les erreurs d'épissage sont impliquées dans les cancers et autres maladies humaines. Quels types de mutations peuvent entraîner des erreurs d'épissage ? Pensez aux différents résultats possibles si des erreurs d'épissage se produisent.
Notez que plus de 70 introns individuels peuvent être présents, et que chacun doit subir un processus d'épissage, en plus d'une coiffe de 5' et de l'ajout d'une queue en poly-A, juste pour générer une seule molécule d'ARNm traduisible.
Lien vers l'apprentissage
Découvrez comment les introns sont éliminés lors de l'épissage de l'ARN sur ce site Web.
Traitement des ARNt et des ARNr
Les ARNt et les ARNr sont des molécules structurales qui jouent un rôle dans la synthèse des protéines ; cependant, ces ARN ne sont pas eux-mêmes traduits. Les pré-ARNr sont transcrits, traités et assemblés en ribosomes dans le nucléole. Les pré-ARNt sont transcrits et traités dans le noyau, puis libérés dans le cytoplasme où ils sont liés à des acides aminés libres pour la synthèse des protéines.
La plupart des ARNt et des ARNr des eucaryotes et des procaryotes sont d'abord transcrits sous la forme d'une longue molécule précurseur qui couvre plusieurs ARNr ou ARNt. Les enzymes clivent ensuite les précurseurs en sous-unités correspondant à chaque ARN structurel. Certaines des bases des pré-ARNr sont méthylées, c'est-à-dire qu'une fraction —CH 3 (groupe fonctionnel méthyle) est ajoutée à des fins de stabilité. Les molécules pré-ARNt subissent également une méthylation. Comme pour les pré-ARNm, l'excision des sous-unités se produit dans les pré-ARN eucaryotes destinés à devenir des ARNt ou des ARNr.
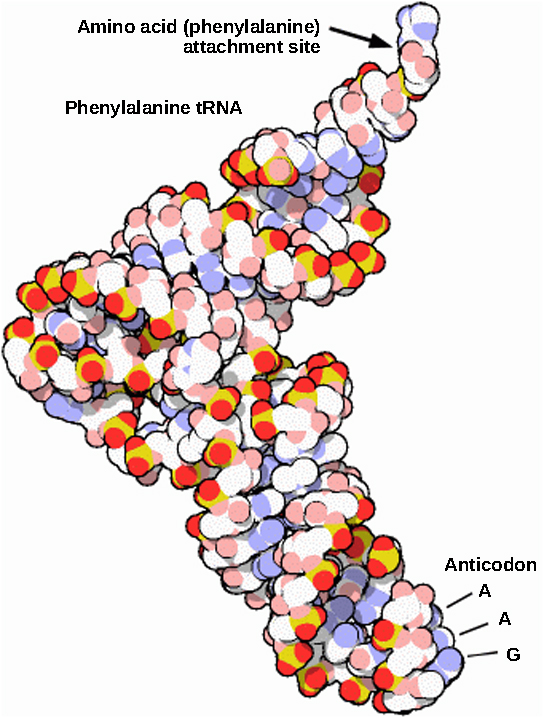
Les ARNr matures constituent environ 50 % de chaque ribosome. Certaines molécules d'ARN d'un ribosome sont purement structurales, tandis que d'autres ont des activités catalytiques ou de liaison. Les ARNt matures adoptent une structure tridimensionnelle par liaison hydrogène intramoléculaire pour positionner le site de liaison des acides aminés à une extrémité et l'anticodon à l'autre extrémité (Figure\(\PageIndex{3}\)). L'anticodon est une séquence de trois nucléotides dans un ARNt qui interagit avec un codon d'ARNm par le biais d'un appariement de bases complémentaires.
Résumé
Les pré-ARNm des eucaryotes sont modifiés par une calotte 5' de méthylguanosine et une queue en poly-A. Ces structures protègent l'ARNm mature de la dégradation et aident à l'exporter du noyau. Les pré-ARNm subissent également un épissage, au cours duquel les introns sont retirés et les exons sont reconnectés avec une précision mononucléotidique. Seuls les ARNm finis qui ont subi un coiffage en 5', une polyadénylation en 3' et un épissage par intron sont exportés du noyau vers le cytoplasme. Les pré-ARNr et les pré-ARNt peuvent être traités par clivage intramoléculaire, épissage, méthylation et conversion chimique des nucléotides. Dans de rares cas, l'édition de l'ARN est également réalisée pour insérer les bases manquantes après la synthèse d'un ARNm.
Connexions artistiques
Figure\(\PageIndex{2}\) : Des erreurs d'épissage sont impliquées dans des cancers et d'autres maladies humaines. Quels types de mutations peuvent entraîner des erreurs d'épissage ? Pensez aux différents résultats possibles si des erreurs d'épissage se produisent.
- Réponse
-
Des mutations dans la séquence de reconnaissance de l'épissage à chaque extrémité de l'intron, ou dans les protéines et les ARN qui composent l'épissage, peuvent altérer l'épissage. Les mutations peuvent également ajouter de nouveaux sites de reconnaissance des épissures. Des erreurs d'épissage peuvent entraîner la rétention d'introns dans l'ARN épissé, l'excision d'exons ou des modifications de l'emplacement du site d'épissage.
Lexique
- Capuchon de 7-méthylguanosine
- modification ajoutée à l'extrémité 5' des pré-ARNm pour protéger l'ARNm de la dégradation et faciliter la traduction
- anticodon
- séquence de trois nucléotides dans une molécule d'ARNt qui correspond à un codon d'ARNm
- exon
- séquence présente dans l'ARNm codant pour les protéines après la fin de l'épissage pré-ARNm
- intron
- séquences intermédiaires ne codant pas pour des protéines qui sont épissées à partir de l'ARNm pendant le traitement
- Queue en poly-A
- modification ajoutée à l'extrémité 3' des pré-ARNm pour protéger l'ARNm de la dégradation et faciliter l'exportation de l'ARNm depuis le noyau
- Édition de l'ARN
- altération directe d'un ou de plusieurs nucléotides dans un ARNm déjà synthétisé
- épissage
- processus d'élimination des introns et de reconnexion des exons dans un pré-ARNm


