7.4 : Phosphorylation oxydative
- Page ID
- 189472
Compétences à développer
- Décrire comment les électrons se déplacent dans la chaîne de transport des électrons et ce qu'il advient de leurs niveaux d'énergie
- Expliquer comment un gradient de protons (H +) est établi et maintenu par la chaîne de transport d'électrons
Vous venez de découvrir deux voies du catabolisme du glucose, la glycolyse et le cycle de l'acide citrique, qui génèrent de l'ATP. La majeure partie de l'ATP généré lors du catabolisme aérobie du glucose ne provient toutefois pas directement de ces voies. Il est plutôt dérivé d'un processus qui commence par le déplacement d'électrons à travers une série de transporteurs d'électrons soumis à des réactions d'oxydoréduction. Cela provoque l'accumulation d'ions hydrogène dans l'espace matriciel. Il se forme donc un gradient de concentration dans lequel les ions hydrogène diffusent hors de l'espace matriciel en passant par l'ATP synthase. Le courant d'ions hydrogène alimente l'action catalytique de l'ATP synthase, qui phosphoryle l'ADP et produit de l'ATP.
Chaîne de transport d'électrons
La chaîne de transport des électrons (Figure\(\PageIndex{1}\)) est le dernier composant de la respiration aérobie et la seule partie du métabolisme du glucose qui utilise l'oxygène atmosphérique. L'oxygène se diffuse continuellement dans les plantes ; chez les animaux, il pénètre dans l'organisme par le système respiratoire. Le transport d'électrons est une série de réactions redox qui ressemblent à une course à relais ou à une brigade à godets en ce sens que les électrons passent rapidement d'un composant à l'autre, jusqu'à l'extrémité de la chaîne où les électrons réduisent l'oxygène moléculaire, produisant ainsi de l'eau. Il existe quatre complexes composés de protéines, marqués de I à IV sur la figure\(\PageIndex{1}\), et l'agrégation de ces quatre complexes, ainsi que des porteurs d'électrons mobiles et accessoires associés, est appelée chaîne de transport d'électrons. La chaîne de transport d'électrons est présente en plusieurs copies dans la membrane mitochondriale interne des eucaryotes et dans la membrane plasmique des procaryotes.
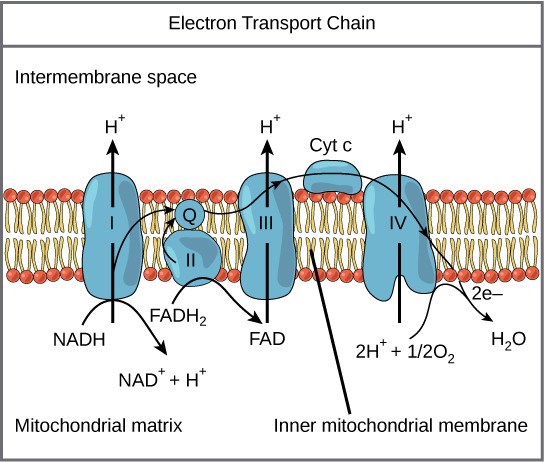
Complexe I
Pour commencer, deux électrons sont transportés vers le premier complexe à bord du NADH. Ce complexe, marqué I, est composé de mononucléotide de flavine (FMN) et d'une protéine contenant du fer-soufre (Fe-S). La FMN, qui est dérivée de la vitamine B 2, également appelée riboflavine, est l'un des nombreux groupes prothétiques ou cofacteurs de la chaîne de transport des électrons. Un groupe prothétique est une molécule non protéique nécessaire à l'activité d'une protéine. Les groupes prothétiques sont des molécules organiques ou inorganiques, non peptidiques liées à une protéine qui facilitent sa fonction ; les groupes prothétiques comprennent les coenzymes, qui sont les groupes prothétiques d'enzymes. L'enzyme du complexe I est la NADH déshydrogénase. Il s'agit d'une très grosse protéine contenant 45 chaînes d'acides aminés. Le complexe I peut pomper quatre ions hydrogène à travers la membrane depuis la matrice jusqu'à l'espace intermembranaire, et c'est ainsi que le gradient d'ions hydrogène est établi et maintenu entre les deux compartiments séparés par la membrane mitochondriale interne.
Q et Complex II
Le complexe II reçoit directement le FADH 2, qui ne traverse pas le complexe I. Le composé reliant les premier et deuxième complexes au troisième est l'ubiquinone (Q). La molécule Q est liposoluble et se déplace librement à travers le noyau hydrophobe de la membrane. Une fois réduite (QH 2), l'ubiquinone livre ses électrons au complexe suivant de la chaîne de transport d'électrons. Q reçoit les électrons dérivés du NADH du complexe I et les électrons dérivés du FADH 2 du complexe II, y compris la succinate déshydrogénase. Cette enzyme et le FADH 2 forment un petit complexe qui fournit des électrons directement à la chaîne de transport d'électrons, en contournant le premier complexe. Comme ces électrons contournent et n'activent donc pas la pompe à protons dans le premier complexe, moins de molécules d'ATP sont fabriquées à partir des électrons du FADH 2. Le nombre de molécules d'ATP finalement obtenues est directement proportionnel au nombre de protons pompés à travers la membrane mitochondriale interne.
Complexe III
Le troisième complexe est composé du cytochrome b, d'une autre protéine Fe-S, du centre Rieske (centre 2Fe-2S) et de protéines du cytochrome c ; ce complexe est également appelé cytochrome oxydoréductase. Les protéines du cytochrome ont un groupe prothétique d'hème. La molécule d'hème est similaire à l'hème de l'hémoglobine, mais elle transporte des électrons et non de l'oxygène. En conséquence, l'ion fer à son cœur est réduit et oxydé lorsqu'il passe les électrons, fluctuant entre différents états d'oxydation : Fe ++ (réduit) et Fe +++ (oxydé). Les molécules d'hème présentes dans les cytochromes présentent des caractéristiques légèrement différentes en raison des effets des différentes protéines qui les lient, conférant des caractéristiques légèrement différentes à chaque complexe. Le complexe III pompe les protons à travers la membrane et fait passer ses électrons vers le cytochrome c pour les transporter vers le quatrième complexe de protéines et d'enzymes (le cytochrome c est l'accepteur des électrons de Q ; cependant, alors que Q transporte des paires d'électrons, le cytochrome c ne peut en accepter qu'un à la fois).
Complexe IV
Le quatrième complexe est composé des protéines cytochromes c, a et a 3. Ce complexe contient deux groupes d'hèmes (un dans chacun des deux cytochromes, a et a 3) et trois ions cuivre (une paire de Cu A et un Cu B dans le cytochrome a 3). Les cytochromes maintiennent une molécule d'oxygène très étroitement entre les ions fer et cuivre jusqu'à ce que l'oxygène soit complètement réduit. L'oxygène réduit capte ensuite deux ions hydrogène du milieu environnant pour produire de l'eau (H 2 O). L'élimination des ions hydrogène du système contribue au gradient d'ions utilisé dans le processus de chimiosmose.
Chimiosmose
Lors de la chimiosmose, l'énergie libre issue de la série de réactions d'oxydoréduction que nous venons de décrire est utilisée pour pomper des ions hydrogène (protons) à travers la membrane. La distribution inégale des ions H + à travers la membrane crée à la fois des gradients de concentration et des gradients électriques (donc un gradient électrochimique), en raison de la charge positive des ions hydrogène et de leur agrégation sur un côté de la membrane.
Si la membrane était ouverte à la diffusion par les ions hydrogène, les ions auraient tendance à rediffuser dans la matrice, sous l'effet de leur gradient électrochimique. Rappelons que de nombreux ions ne peuvent pas diffuser à travers les régions non polaires des membranes phospholipidiques sans l'aide de canaux ioniques. De même, les ions hydrogène présents dans l'espace matriciel ne peuvent traverser la membrane mitochondriale interne qu'à travers une protéine membranaire intégrée appelée ATP synthase (Figure\(\PageIndex{2}\)). Cette protéine complexe agit comme un minuscule générateur, entraîné par la force des ions hydrogène qui la traversent vers le bas de leur gradient électrochimique. La rotation des pièces de cette machine moléculaire facilite l'ajout d'un phosphate à l'ADP, formant de l'ATP, en utilisant l'énergie potentielle du gradient d'ions hydrogène.
Art Connection
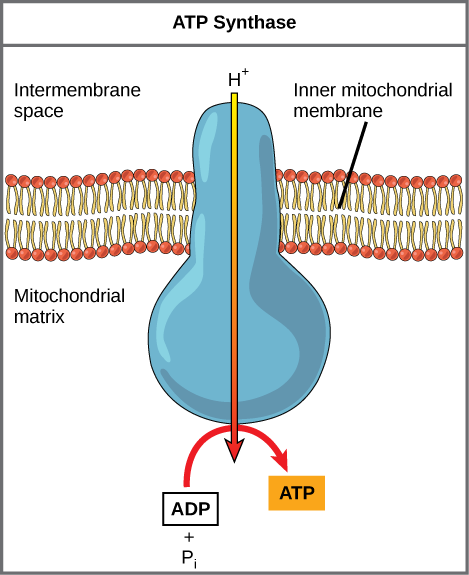
Le dinitrophénol (DNP) est un découpleur qui rend la membrane mitochondriale interne perméable aux protons. Il a été utilisé jusqu'en 1938 comme médicament amaigrissant. Quel effet pensez-vous que le DNP aura sur la modification du pH à travers la membrane mitochondriale interne ? Pourquoi pensez-vous que ce médicament pourrait être efficace pour perdre du poids ?
La chimiosmose (Figure\(\PageIndex{3}\)) est utilisée pour générer 90 pour cent de l'ATP produit lors du catabolisme aérobie du glucose ; c'est également la méthode utilisée dans les réactions lumineuses de la photosynthèse pour exploiter l'énergie de la lumière solaire lors du processus de photophosphorylation. Rappelons que la production d'ATP par le processus de chimiosmose dans les mitochondries est appelée phosphorylation oxydative. Le résultat global de ces réactions est la production d'ATP à partir de l'énergie des électrons extraits des atomes d'hydrogène. Ces atomes faisaient à l'origine partie d'une molécule de glucose. À la fin du trajet, les électrons sont utilisés pour réduire une molécule d'oxygène en ions oxygène. Les électrons supplémentaires présents sur l'oxygène attirent les ions hydrogène (protons) du milieu environnant et de l'eau se forme.
Art Connection
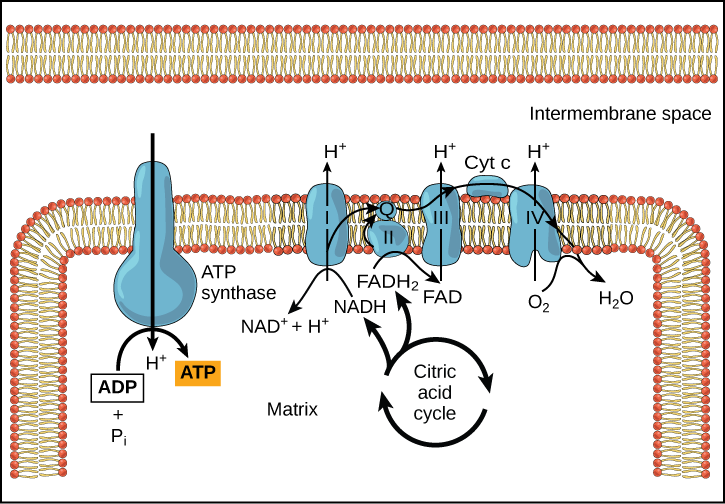
Le cyanure inhibe la cytochrome c oxydase, un composant de la chaîne de transport des électrons. En cas d'empoisonnement au cyanure, vous attendriez-vous à ce que le pH de l'espace intermembranaire augmente ou diminue ? Quel effet le cyanure aurait-il sur la synthèse de l'ATP ?
Rendement ATP
Le nombre de molécules d'ATP générées par le catabolisme du glucose varie. Par exemple, le nombre d'ions hydrogène que les complexes de la chaîne de transport d'électrons peuvent pomper à travers la membrane varie selon les espèces. Une autre source de variance provient de la navette d'électrons à travers les membranes des mitochondries. (Le NADH généré par la glycolyse ne peut pas facilement pénétrer dans les mitochondries.) Ainsi, les électrons sont captés à l'intérieur des mitochondries par le NAD+ ou le FAD+. Comme vous l'avez appris précédemment, ces molécules de FAD+ peuvent transporter moins d'ions ; par conséquent, moins de molécules d'ATP sont générées lorsque le FAD+ agit en tant que support. Le NAD+ est utilisé comme transporteur d'électrons dans le foie et le FAD+ agit dans le cerveau.
Un autre facteur qui influe sur le rendement des molécules d'ATP générées à partir du glucose est le fait que les composés intermédiaires de ces voies sont utilisés à d'autres fins. Le catabolisme du glucose est lié aux voies qui construisent ou décomposent tous les autres composés biochimiques dans les cellules, et le résultat est un peu plus désordonné que les situations idéales décrites jusqu'à présent. Par exemple, des sucres autres que le glucose sont introduits dans la voie glycolytique pour l'extraction d'énergie. De plus, les sucres à cinq carbones qui forment les acides nucléiques sont fabriqués à partir d'intermédiaires de la glycolyse. Certains acides aminés non essentiels peuvent être fabriqués à partir d'intermédiaires de la glycolyse et du cycle de l'acide citrique. Les lipides, tels que le cholestérol et les triglycérides, sont également fabriqués à partir d'intermédiaires dans ces voies, et les acides aminés et les triglycérides sont décomposés en énergie par ces voies. Dans l'ensemble, dans les systèmes vivants, ces voies du catabolisme du glucose extraient environ 34 pour cent de l'énergie contenue dans le glucose.
Résumé
La chaîne de transport d'électrons est la partie de la respiration aérobie qui utilise l'oxygène libre comme dernier accepteur d'électrons des électrons retirés des composés intermédiaires lors du catabolisme du glucose. La chaîne de transport d'électrons est composée de quatre grands complexes multiprotéiques intégrés dans la membrane mitochondriale interne et de deux petits porteurs d'électrons diffusibles qui font la navette entre les électrons. Les électrons sont soumis à une série de réactions d'oxydoréduction, une petite quantité d'énergie libre étant utilisée en trois points pour transporter des ions hydrogène à travers une membrane. Ce processus contribue au gradient utilisé dans la chimiosmose. Les électrons qui traversent la chaîne de transport des électrons perdent progressivement de l'énergie. Les électrons de haute énergie donnés à la chaîne par le NADH ou le FADH 2 complètent la chaîne, car les électrons de faible énergie réduisent les molécules d'oxygène et forment de l'eau. Le niveau d'énergie libre des électrons chute d'environ 60 kcal/mol dans le NADH ou 45 kcal/mol dans le FADH 2 à environ 0 kcal/mol dans l'eau. Les produits finaux de la chaîne de transport des électrons sont l'eau et l'ATP. Un certain nombre de composés intermédiaires du cycle de l'acide citrique peuvent être détournés vers l'anabolisme d'autres molécules biochimiques, telles que les acides aminés non essentiels, les sucres et les lipides. Ces mêmes molécules peuvent servir de sources d'énergie pour les voies du glucose.
Connexions artistiques
Figure\(\PageIndex{2}\) : Le dinitrophénol (DNP) est un découpleur qui rend la membrane mitochondriale interne perméable aux protons. Il a été utilisé jusqu'en 1938 comme médicament amaigrissant. Quel effet pensez-vous que le DNP aura sur la modification du pH à travers la membrane mitochondriale interne ? Pourquoi pensez-vous que ce médicament pourrait être efficace pour perdre du poids ?
- Réponse
-
Après un empoisonnement au DNP, la chaîne de transport d'électrons ne peut plus former de gradient de protons et l'ATP synthase ne peut plus produire d'ATP. Le DNP est un médicament diététique efficace parce qu'il dissocie la synthèse de l'ATP ; en d'autres termes, après l'avoir pris, une personne obtient moins d'énergie des aliments qu'elle mange. Fait intéressant, l'un des pires effets secondaires de ce médicament est l'hyperthermie ou la surchauffe du corps. Comme l'ATP ne peut pas se former, l'énergie provenant du transport des électrons est perdue sous forme de chaleur.
Figure\(\PageIndex{3}\) : Le cyanure inhibe la cytochrome c oxydase, un composant de la chaîne de transport des électrons. En cas d'empoisonnement au cyanure, vous attendriez-vous à ce que le pH de l'espace intermembranaire augmente ou diminue ? Quel effet le cyanure aurait-il sur la synthèse de l'ATP ?
- Réponse
-
Après un empoisonnement au cyanure, la chaîne de transport d'électrons ne peut plus pomper les électrons dans l'espace intermembranaire. Le pH de l'espace intermembranaire augmenterait, le gradient de pH diminuerait et la synthèse d'ATP s'arrêterait.
Lexique
- ATP synthase
- (également, ATP synthase F1F0) complexe protéique intégré à la membrane qui ajoute un phosphate à l'ADP grâce à l'énergie des protons qui y diffusent
- groupe prothétique
- (également, cofacteur prothétique) molécule liée à une protéine qui facilite le fonctionnement de la protéine
- ubiquinone
- transporteur d'électrons soluble dans la chaîne de transport d'électrons qui relie le premier ou le deuxième complexe au troisième


