6.5 : Enzymes
- Page ID
- 189547
Compétences à développer
- Décrire le rôle des enzymes dans les voies métaboliques
- Expliquer comment les enzymes fonctionnent en tant que catalyseurs moléculaires
- Discutez de la régulation enzymatique par divers
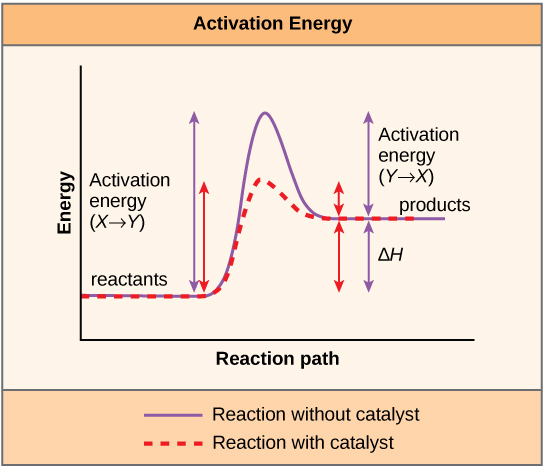
Une substance qui contribue à la survenue d'une réaction chimique est un catalyseur, et les molécules spéciales qui catalysent les réactions biochimiques sont appelées enzymes. Presque toutes les enzymes sont des protéines, constituées de chaînes d'acides aminés, et elles ont pour tâche essentielle de réduire les énergies d'activation des réactions chimiques à l'intérieur de la cellule. Les enzymes y parviennent en se liant aux molécules du réactif et en les maintenant de manière à faciliter les processus chimiques de rupture et de formation de liaisons. Il est important de se rappeler que les enzymes ne modifient pas le ∆G d'une réaction. En d'autres termes, ils ne changent pas si une réaction est exergonique (spontanée) ou endergonique. Cela est dû au fait qu'ils ne modifient pas l'énergie libre des réactifs ou des produits. Ils ne font que réduire l'énergie d'activation requise pour atteindre l'état de transition (Figure\(\PageIndex{1}\)).
Spécificité du site actif et du substrat des enzymes
Les réactifs chimiques auxquels une enzyme se lie sont les substrats de l'enzyme. Il peut y avoir un ou plusieurs substrats, en fonction de la réaction chimique particulière. Dans certaines réactions, un substrat à un seul réactif est décomposé en plusieurs produits. Dans d'autres cas, deux substrats peuvent se réunir pour créer une molécule plus grosse. Deux réactifs peuvent également entrer dans une réaction, se modifier et quitter la réaction sous forme de deux produits. L'emplacement au sein de l'enzyme où le substrat se lie est appelé site actif de l'enzyme. Le site actif est l'endroit où « l'action » se produit, pour ainsi dire. Les enzymes étant des protéines, il existe une combinaison unique de résidus d'acides aminés (également appelés chaînes latérales ou groupes R) au sein du site actif. Chaque résidu se caractérise par des propriétés différentes. Les résidus peuvent être grands ou petits, faiblement acides ou basiques, hydrophiles ou hydrophobes, chargés positivement ou négativement, ou neutres. La combinaison unique de résidus d'acides aminés, de leurs positions, de leurs séquences, de leurs structures et de leurs propriétés crée un environnement chimique très spécifique au sein du site actif. Cet environnement spécifique est adapté pour se lier, quoique brièvement, à un ou plusieurs substrats chimiques spécifiques. En raison de cette correspondance semblable à un puzzle entre une enzyme et ses substrats (qui s'adapte pour trouver la meilleure adéquation entre l'état de transition et le site actif), les enzymes sont connues pour leur spécificité. Le « meilleur ajustement » résulte de la forme et de l'attrait du groupe fonctionnel des acides aminés pour le substrat. Il existe une enzyme spécifiquement adaptée à chaque substrat et donc à chaque réaction chimique ; cependant, il y a également de la flexibilité.
Le fait que les sites actifs soient parfaitement adaptés à des conditions environnementales spécifiques signifie également qu'ils sont soumis aux influences de l'environnement local. Il est vrai que l'augmentation de la température ambiante augmente généralement les vitesses de réaction, catalysées par des enzymes ou non. Cependant, l'augmentation ou la diminution de la température en dehors d'une plage optimale peut affecter les liaisons chimiques au sein du site actif de telle sorte qu'elles sont moins bien adaptées pour lier les substrats. Les températures élevées finiront par provoquer la dénaturation des enzymes, comme les autres molécules biologiques, un processus qui modifie les propriétés naturelles d'une substance. De même, le pH de l'environnement local peut également affecter la fonction enzymatique. Les résidus d'acides aminés du site actif possèdent leurs propres propriétés acides ou basiques qui sont optimales pour la catalyse. Ces résidus sont sensibles aux variations du pH qui peuvent altérer la façon dont les molécules du substrat se lient. Les enzymes sont adaptées pour fonctionner au mieux dans une certaine plage de pH et, comme pour la température, les valeurs extrêmes du pH (acide ou basique) de l'environnement peuvent provoquer la dénaturation des enzymes.
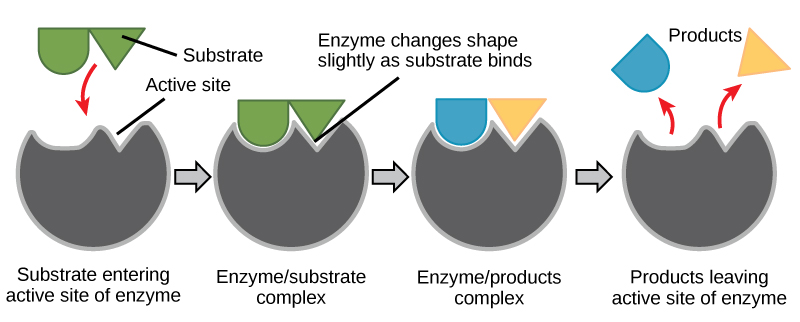
Ajustement induit et fonction enzymatique
Pendant de nombreuses années, les scientifiques ont pensé que la liaison enzyme-substrat se faisait d'une manière simple « verrouillée ». Ce modèle a affirmé que l'enzyme et le substrat s'assemblent parfaitement en une seule étape instantanée. Cependant, les recherches actuelles soutiennent une vision plus affinée appelée ajustement induit (Figure\(\PageIndex{2}\)). Le modèle d'ajustement induit développe le modèle verrouillable en décrivant une interaction plus dynamique entre l'enzyme et le substrat. Lorsque l'enzyme et le substrat se rejoignent, leur interaction provoque une légère modification de la structure de l'enzyme qui confirme un arrangement de liaison idéal entre l'enzyme et l'état de transition du substrat. Cette liaison idéale maximise la capacité de l'enzyme à catalyser sa réaction.
Lorsqu'une enzyme lie son substrat, un complexe enzyme-substrat se forme. Ce complexe réduit l'énergie d'activation de la réaction et favorise sa progression rapide de nombreuses manières. À un niveau élémentaire, les enzymes favorisent des réactions chimiques impliquant plus d'un substrat en rapprochant les substrats dans une orientation optimale. La région appropriée (atomes et liaisons) d'une molécule est juxtaposée à la région appropriée de l'autre molécule avec laquelle elle doit réagir. Les enzymes peuvent également favoriser la réaction de leurs substrats en créant un environnement optimal au sein du site actif pour que la réaction se produise. Certaines réactions chimiques peuvent mieux se produire dans un environnement légèrement acide ou non polaire. Les propriétés chimiques qui se dégagent de la disposition particulière des résidus d'acides aminés au sein d'un site actif créent l'environnement idéal pour la réaction des substrats spécifiques d'une enzyme.
Vous avez appris que l'énergie d'activation requise pour de nombreuses réactions inclut l'énergie nécessaire à la manipulation ou à la légère déformation des liaisons chimiques afin qu'elles puissent facilement se rompre et permettre à d'autres de se reformer. L'action enzymatique peut faciliter ce processus. Le complexe enzyme-substrat peut réduire l'énergie d'activation en contorsionnant les molécules du substrat de manière à faciliter la rupture des liaisons, aidant ainsi à atteindre l'état de transition. Enfin, les enzymes peuvent également réduire les énergies d'activation en participant à la réaction chimique elle-même. Les résidus d'acides aminés peuvent fournir certains ions ou groupes chimiques qui forment en fait des liaisons covalentes avec les molécules du substrat en tant qu'étape nécessaire du processus de réaction. Dans ces cas, il est important de se rappeler que l'enzyme retrouvera toujours son état d'origine à la fin de la réaction. L'une des propriétés caractéristiques des enzymes est qu'elles restent finalement inchangées par les réactions qu'elles catalysent. Une fois qu'une enzyme a fini de catalyser une réaction, elle libère son ou ses produits.
Contrôle du métabolisme grâce à la régulation enzymatique
Il semblerait idéal d'avoir un scénario dans lequel toutes les enzymes codées dans le génome d'un organisme existent en abondance et fonctionnent de manière optimale dans toutes les conditions cellulaires, dans toutes les cellules et à tout moment. En réalité, c'est loin d'être le cas. Divers mécanismes garantissent que cela ne se produise pas. Les besoins et les conditions cellulaires varient d'une cellule à l'autre et changent au sein de chaque cellule au fil du temps. Les enzymes nécessaires et les besoins énergétiques des cellules de l'estomac sont différents de ceux des cellules de stockage des graisses, des cellules de la peau, des cellules sanguines et des cellules nerveuses. De plus, une cellule digestive travaille beaucoup plus dur pour traiter et décomposer les nutriments pendant la période qui suit de près un repas, par rapport à plusieurs heures après un repas. À mesure que ces exigences et conditions cellulaires varient, les quantités et la fonctionnalité des différentes enzymes varient également.
Comme les vitesses des réactions biochimiques sont contrôlées par l'énergie d'activation et que les enzymes diminuent et déterminent les énergies d'activation des réactions chimiques, les quantités relatives et le fonctionnement des diverses enzymes au sein d'une cellule déterminent en fin de compte quelles réactions se produiront et à quelle vitesse. Cette détermination est étroitement contrôlée. Dans certains environnements cellulaires, l'activité enzymatique est partiellement contrôlée par des facteurs environnementaux tels que le pH et la température. Il existe d'autres mécanismes par lesquels les cellules contrôlent l'activité des enzymes et déterminent la vitesse à laquelle diverses réactions biochimiques se produiront.
Régulation des enzymes par des molécules
Les enzymes peuvent être régulées de manière à favoriser ou à réduire leur activité. Il existe de nombreux types de molécules qui inhibent ou favorisent la fonction enzymatique, et divers mécanismes existent pour le faire. Dans certains cas d'inhibition enzymatique, par exemple, une molécule inhibitrice est suffisamment similaire à un substrat pour se lier au site actif et simplement empêcher le substrat de se lier. Lorsque cela se produit, l'enzyme est inhibée par inhibition compétitive, car une molécule inhibitrice entre en compétition avec le substrat pour la liaison au site actif (Figure\(\PageIndex{3}\)). D'autre part, lors d'une inhibition non compétitive, une molécule inhibitrice se lie à l'enzyme à un endroit autre qu'un site allostérique tout en parvenant à bloquer la liaison du substrat au site actif.
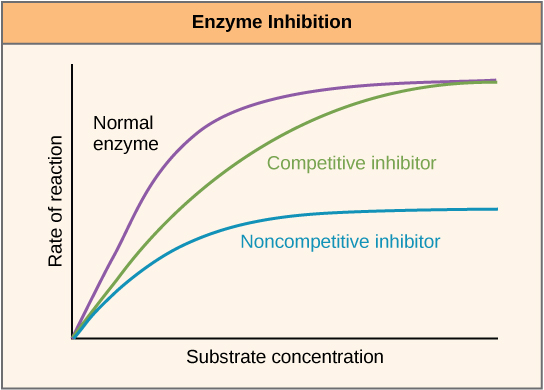
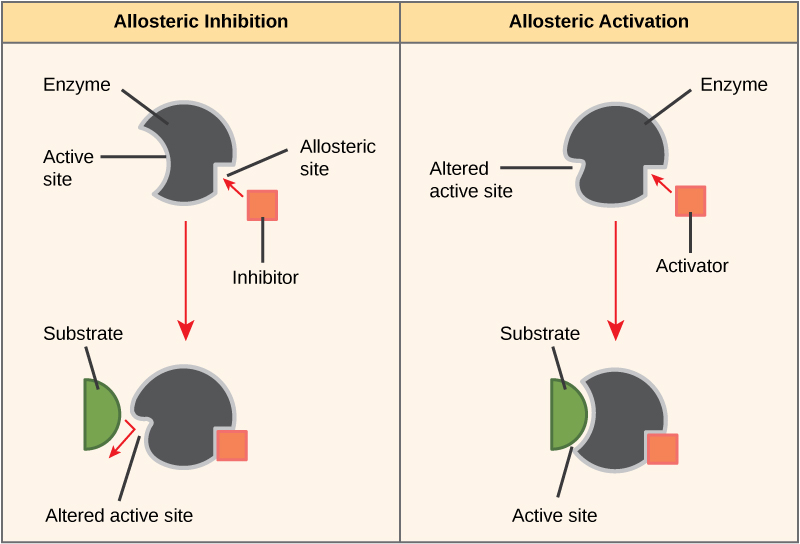
Certaines molécules inhibitrices se lient aux enzymes à un endroit où leur liaison induit un changement de conformation qui réduit l'affinité de l'enzyme pour son substrat. Ce type d'inhibition est appelé inhibition allostérique (Figure\(\PageIndex{4}\)). La plupart des enzymes régulées allostériquement sont constituées de plus d'un polypeptide, ce qui signifie qu'elles possèdent plus d'une sous-unité protéique. Lorsqu'un inhibiteur allostérique se lie à une enzyme, tous les sites actifs des sous-unités protéiques sont légèrement modifiés de telle sorte qu'ils se lient à leurs substrats avec moins d'efficacité. Il existe des activateurs allostériques ainsi que des inhibiteurs. Les activateurs allostériques se lient à des emplacements d'une enzyme éloignés du site actif, induisant un changement de conformation qui augmente l'affinité du ou des sites actifs de l'enzyme pour son ou ses substrats.
Everyday Connection : découverte de médicaments en recherchant des inhibiteurs d'enzymes clés dans des voies spécifiques

Les enzymes sont des composants clés des voies métaboliques. Comprendre le fonctionnement des enzymes et la manière dont elles peuvent être régulées est un principe clé qui sous-tend le développement de nombreux médicaments (Figure\(\PageIndex{5}\)) actuellement sur le marché. Les biologistes travaillant dans ce domaine collaborent avec d'autres scientifiques, généralement des chimistes, pour concevoir des médicaments.
Prenons l'exemple des statines, qui sont le nom donné à la classe de médicaments qui réduisent le taux de cholestérol. Ces composés sont essentiellement des inhibiteurs de l'enzyme HMG-CoA réductase. L'HMG-CoA réductase est l'enzyme qui synthétise le cholestérol à partir des lipides du corps. En inhibant cette enzyme, les taux de cholestérol synthétisés dans l'organisme peuvent être réduits. De même, l'acétaminophène, couramment commercialisé sous le nom de marque Tylenol, est un inhibiteur de l'enzyme cyclooxygénase. Bien qu'il soit efficace pour soulager la fièvre et l'inflammation (douleur), son mécanisme d'action n'est toujours pas complètement compris.
Comment sont développés les médicaments ? L'un des premiers défis du développement de médicaments consiste à identifier la molécule spécifique que le médicament est censé cibler. Dans le cas des statines, l'HMG-CoA réductase est la cible du médicament. Les cibles des médicaments sont identifiées grâce à des recherches minutieuses en laboratoire. Il ne suffit pas d'identifier la cible à elle seule ; les scientifiques doivent également savoir comment la cible agit à l'intérieur de la cellule et quelles réactions se produisent mal en cas de maladie. Une fois que la cible et la voie sont identifiées, le processus proprement dit de conception du médicament commence. Au cours de cette étape, les chimistes et les biologistes travaillent ensemble pour concevoir et synthétiser des molécules capables de bloquer ou d'activer une réaction particulière. Cependant, ce n'est qu'un début : si et quand un prototype de médicament réussit à remplir sa fonction, il doit subir de nombreux tests, des expériences in vitro aux essais cliniques, avant de pouvoir obtenir l'approbation de la FDA pour être mis sur le marché.
De nombreuses enzymes ne fonctionnent pas de manière optimale, voire pas du tout, à moins d'être liées à d'autres molécules auxiliaires spécifiques non protéiques, soit temporairement par des liaisons ioniques ou hydrogène, soit de manière permanente par des liaisons covalentes plus fortes. Deux types de molécules auxiliaires sont les cofacteurs et les coenzymes. La liaison à ces molécules favorise une conformation et une fonction optimales de leurs enzymes respectives. Les cofacteurs sont des ions inorganiques tels que le fer (Fe++) et le magnésium (Mg++). Un exemple d'enzyme qui a besoin d'un ion métallique comme cofacteur est l'enzyme qui construit les molécules d'ADN, l'ADN polymérase, qui a besoin d'un ion zinc lié (Zn++) pour fonctionner. Les coenzymes sont des molécules auxiliaires organiques, dont la structure atomique de base est composée de carbone et d'hydrogène, nécessaires à l'action enzymatique. Les sources les plus courantes de coenzymes sont les vitamines alimentaires (Figure\(\PageIndex{6}\)). Certaines vitamines sont des précurseurs de coenzymes tandis que d'autres agissent directement comme des coenzymes. La vitamine C est une coenzyme de plusieurs enzymes qui participent à la construction du composant important du tissu conjonctif, le collagène. Une étape importante de la dégradation du glucose pour produire de l'énergie est la catalyse par un complexe multi-enzymatique appelé pyruvate déshydrogénase. La pyruvate déshydrogénase est un complexe de plusieurs enzymes qui nécessite en fait un cofacteur (un ion magnésium) et cinq coenzymes organiques différentes pour catalyser sa réaction chimique spécifique. La fonction enzymatique est donc en partie régulée par une abondance de divers cofacteurs et coenzymes, qui sont principalement fournis par le régime alimentaire de la plupart des organismes.
Compartimentalisation enzymatique
Dans les cellules eucaryotes, les molécules telles que les enzymes sont généralement compartimentées en différents organites. Cela permet un niveau supplémentaire de régulation de l'activité enzymatique. Les enzymes nécessaires uniquement à certains processus cellulaires peuvent être hébergées séparément avec leurs substrats, ce qui permet des réactions chimiques plus efficaces. Parmi les exemples de ce type de régulation enzymatique basée sur la localisation et la proximité, citons les enzymes impliquées dans les derniers stades de la respiration cellulaire, qui ont lieu exclusivement dans les mitochondries, et les enzymes impliquées dans la digestion des débris cellulaires et des matières étrangères, situées dans les lysosomes.
Inhibition du feedback dans les voies métaboliques
Les molécules peuvent réguler la fonction enzymatique de nombreuses manières. Une question majeure demeure cependant : quelles sont ces molécules et d'où viennent-elles ? Certains sont des cofacteurs et des coenzymes, des ions et des molécules organiques, comme vous l'avez appris. Quelles autres molécules de la cellule assurent la régulation enzymatique, telle que la modulation allostérique et l'inhibition compétitive et non compétitive ? La réponse est qu'une grande variété de molécules peuvent jouer ces rôles. Certaines de ces molécules comprennent des médicaments pharmaceutiques et non pharmaceutiques, des toxines et des poisons provenant de l'environnement. Les sources les plus pertinentes de molécules régulatrices enzymatiques, en ce qui concerne le métabolisme cellulaire, sont peut-être les produits des réactions métaboliques cellulaires elles-mêmes. De la manière la plus efficace et la plus élégante, les cellules ont évolué pour utiliser les produits de leurs propres réactions pour inhiber par rétroaction l'activité enzymatique. La rétroinhibition implique l'utilisation d'un produit de réaction pour réguler sa propre production ultérieure (Figure\(\PageIndex{7}\)). La cellule répond à l'abondance de produits spécifiques en ralentissant la production lors de réactions anaboliques ou cataboliques. Ces produits de réaction peuvent inhiber les enzymes qui ont catalysé leur production par les mécanismes décrits ci-dessus.
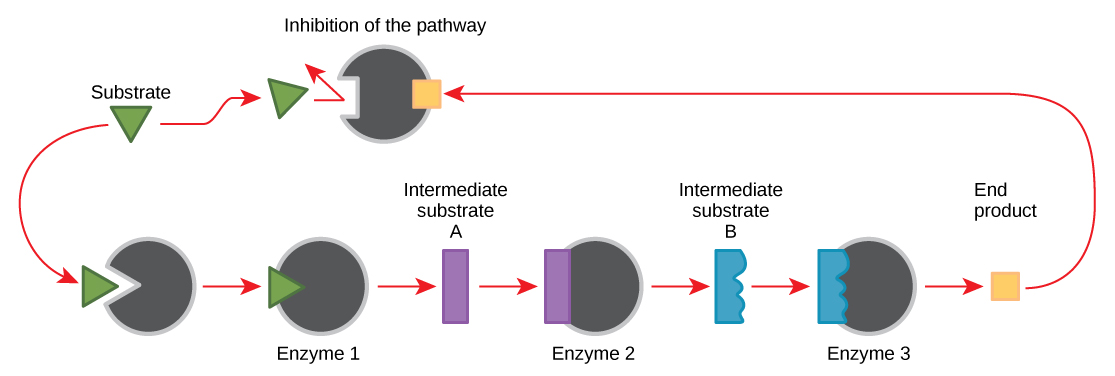
La production d'acides aminés et de nucléotides est contrôlée par une rétroinhibition. De plus, l'ATP est un régulateur allostérique de certaines enzymes impliquées dans la dégradation catabolique du sucre, le processus qui produit l'ATP. Ainsi, lorsque l'ATP est abondant, la cellule peut empêcher sa production ultérieure. N'oubliez pas que l'ATP est une molécule instable qui peut se dissocier spontanément en ADP. Si une trop grande quantité d'ATP était présente dans une cellule, une grande partie serait gaspillée. D'autre part, l'ADP sert de régulateur allostérique positif (activateur allostérique) pour certaines des enzymes inhibées par l'ATP. Ainsi, lorsque les niveaux relatifs d'ADP sont élevés par rapport à l'ATP, la cellule est déclenchée pour produire plus d'ATP par le catabolisme du sucre.
Résumé
Les enzymes sont des catalyseurs chimiques qui accélèrent les réactions chimiques à des températures physiologiques en diminuant leur énergie d'activation. Les enzymes sont généralement des protéines constituées d'une ou de plusieurs chaînes polypeptidiques. Les enzymes possèdent un site actif qui fournit un environnement chimique unique, composé de certains groupes d'acides aminés R (résidus). Cet environnement unique est parfaitement adapté pour convertir des réactifs chimiques spécifiques à cette enzyme, appelés substrats, en intermédiaires instables appelés états de transition. On pense que les enzymes et les substrats se lient par un ajustement induit, ce qui signifie que les enzymes subissent de légers ajustements conformationnels au contact du substrat, conduisant à une liaison complète et optimale. Les enzymes se lient aux substrats et catalysent les réactions de quatre manières différentes : en rapprochant les substrats dans une orientation optimale, en compromettant les structures de liaison des substrats afin que les liaisons puissent être brisées plus facilement, en fournissant des conditions environnementales optimales pour qu'une réaction se produise ou en participant directement à leur réaction chimique en formant des liaisons covalentes transitoires avec les substrats.
L'action enzymatique doit être régulée de telle sorte que, dans une cellule donnée à un moment donné, les réactions souhaitées soient catalysées et que les réactions indésirables ne le soient pas. Les enzymes sont régulées par les conditions cellulaires, telles que la température et le pH. Ils sont également régulés par leur localisation au sein d'une cellule, parfois compartimentés de sorte qu'ils ne peuvent catalyser les réactions que dans certaines circonstances. L'inhibition et l'activation des enzymes via d'autres molécules sont d'autres moyens importants de régulation des enzymes. Les inhibiteurs peuvent agir de manière compétitive, non compétitive ou allostérique ; les inhibiteurs non compétitifs sont généralement allostériques. Les activateurs peuvent également améliorer la fonction des enzymes de manière allostérique. La méthode la plus courante par laquelle les cellules régulent les enzymes des voies métaboliques est la rétroinhibition. Lors de la rétroinhibition, les produits d'une voie métabolique agissent comme inhibiteurs (généralement allostériques) d'une ou de plusieurs enzymes (généralement la première enzyme engagée de la voie) impliquées dans la voie qui les produit.
Lexique
- site actif
- région spécifique de l'enzyme à laquelle le substrat se lie
- inhibition allostérique
- inhibition par un événement de liaison sur un site différent du site actif, ce qui induit un changement de conformation et réduit l'affinité de l'enzyme pour son substrat
- coenzyme
- petite molécule organique, telle qu'une vitamine ou son dérivé, qui est nécessaire pour améliorer l'activité d'une enzyme
- cofacteur
- ion inorganique, tel que les ions fer et magnésium, nécessaires à une régulation optimale de l'activité enzymatique
- inhibition compétitive
- type d'inhibition dans lequel l'inhibiteur entre en compétition avec la molécule substrat en se liant au site actif de l'enzyme
- dénature
- processus qui modifie les propriétés naturelles d'une substance
- inhibition de la rétroaction
- effet d'un produit d'une séquence de réaction visant à diminuer sa production ultérieure en inhibant l'activité de la première enzyme dans la voie qui la produit
- ajustement induit
- ajustement dynamique entre l'enzyme et son substrat, dans lequel les deux composants modifient leurs structures pour permettre une liaison idéale
- substrat
- molécule sur laquelle agit l'enzyme


