3.2: خلايا الجهاز العصبي
- Page ID
- 199249
قد يدرس علماء النفس الذين يسعون جاهدين لفهم العقل البشري الجهاز العصبي. يمكن أن يساعدنا تعلم كيفية عمل خلايا الجسم وأعضائه على فهم الأساس البيولوجي لعلم النفس البشري. يتكون الجهاز العصبي من نوعين أساسيين من الخلايا: الخلايا الدبقية (المعروفة أيضًا باسم الدبقية) والخلايا العصبية. يُعتقد تقليديًا أن الخلايا الدبقية تلعب دورًا داعمًا للخلايا العصبية، جسديًا واستقلابيًا. توفر الخلايا الدبقية السقالات التي يُبنى عليها الجهاز العصبي، وتساعد الخلايا العصبية على الاصطفاف عن كثب مع بعضها البعض للسماح بالاتصال العصبي، وتوفير العزل للخلايا العصبية، ونقل العناصر الغذائية والنفايات، والتوسط في الاستجابات المناعية. لسنوات، اعتقد الباحثون أن هناك العديد من الخلايا الدبقية أكثر من الخلايا العصبية؛ ومع ذلك، فإن العمل الأحدث من مختبر سوزانا هيركولانو-هوزيل قد شكك في هذا الافتراض طويل الأمد وقدم دليلًا مهمًا على أنه قد تكون هناك نسبة 1:1 تقريبًا من خلايا الدبقية إلى الخلايا العصبية. هذا مهم لأنه يشير إلى أن أدمغة الإنسان تشبه أدمغة الرئيسيات الأخرى أكثر مما كان يعتقد سابقًا (أزيفيدو وآخرون، 2009؛ هيركاولانو-هوزل، 2012؛ هيركولانو-هوزل، 2009). من ناحية أخرى، تعمل الخلايا العصبية كمعالجات معلومات مترابطة ضرورية لجميع مهام الجهاز العصبي. يصف هذا القسم بإيجاز بنية ووظيفة الخلايا العصبية.
هيكل الخلايا العصبية
الخلايا العصبية هي اللبنات الأساسية للجهاز العصبي، بقوة 100 مليار عند الولادة. مثل جميع الخلايا، تتكون الخلايا العصبية من عدة أجزاء مختلفة، كل منها يؤدي وظيفة متخصصة (الشكل 3.8). يتكون السطح الخارجي للخلايا العصبية من غشاء نصف نافذ. يسمح هذا الغشاء للجزيئات الصغيرة والجزيئات بدون شحنة كهربائية بالمرور عبره، مع إيقاف الجزيئات الأكبر أو عالية الشحنة.
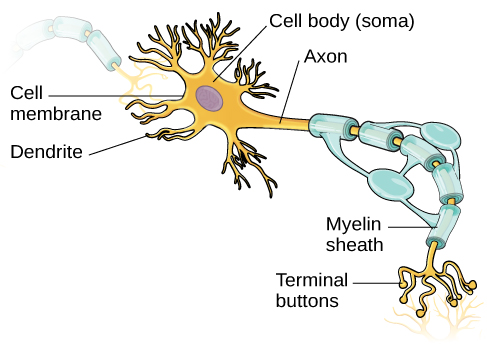
تقع نواة العصبون في سوما أو جسم الخلية. تحتوي السوما على امتدادات متفرعة تعرف باسم التشعبات. العصبون هو معالج معلومات صغير، وتعمل التشعبات كمواقع إدخال حيث يتم استقبال الإشارات من الخلايا العصبية الأخرى. يتم إرسال هذه الإشارات كهربائيًا عبر سوما وأسفل امتداد رئيسي من سوما المعروف باسم المحور، والذي ينتهي عند أزرار طرفية متعددة. تحتوي الأزرار الطرفية على حويصلات متشابكة تحتوي على الناقلات العصبية، وهي الناقلات الكيميائية للجهاز العصبي.
تتراوح المحاور في الطول من جزء من البوصة إلى عدة أقدام. في بعض المحاور العصبية، تشكل الخلايا الدبقية مادة دهنية تعرف باسم غلاف الميالين، والتي تغطي المحور العصبي وتعمل كعازل، مما يزيد من سرعة انتقال الإشارة. غلاف المايلين ليس مستمرًا وهناك فجوات صغيرة تحدث على طول المحور. تُعرف هذه الفجوات في غلاف المايلين باسم عقدة رانفير. يُعد غلاف الميالين أمرًا بالغ الأهمية للتشغيل الطبيعي للخلايا العصبية داخل الجهاز العصبي: فقد يكون فقدان العزل الذي يوفره ضارًا بالوظيفة الطبيعية. لفهم كيفية عمل ذلك، دعنا نفكر في مثال. يتسبب اضطراب PKU، وهو اضطراب وراثي تمت مناقشته سابقًا، في انخفاض الميالين وتشوهات في الهياكل القشرية وتحت القشرية للمادة البيضاء. يرتبط الاضطراب بمجموعة متنوعة من المشكلات بما في ذلك العجز المعرفي الشديد وردود الفعل المبالغ فيها والنوبات (Anderson & Leuzzi، 2010؛ Huttenlocher، 2000). هناك اضطراب آخر، وهو التصلب المتعدد (MS)، وهو اضطراب المناعة الذاتية، وينطوي على فقدان واسع النطاق لغمد الميالين على المحاور العصبية في جميع أنحاء الجهاز العصبي. يمنع التداخل الناتج في الإشارة الكهربائية الإرسال السريع للمعلومات عن طريق الخلايا العصبية ويمكن أن يؤدي إلى عدد من الأعراض، مثل الدوخة والتعب وفقدان التحكم الحركي والضعف الجنسي. في حين أن بعض العلاجات قد تساعد في تعديل مسار المرض وإدارة أعراض معينة، لا يوجد حاليًا علاج معروف للتصلب المتعدد.
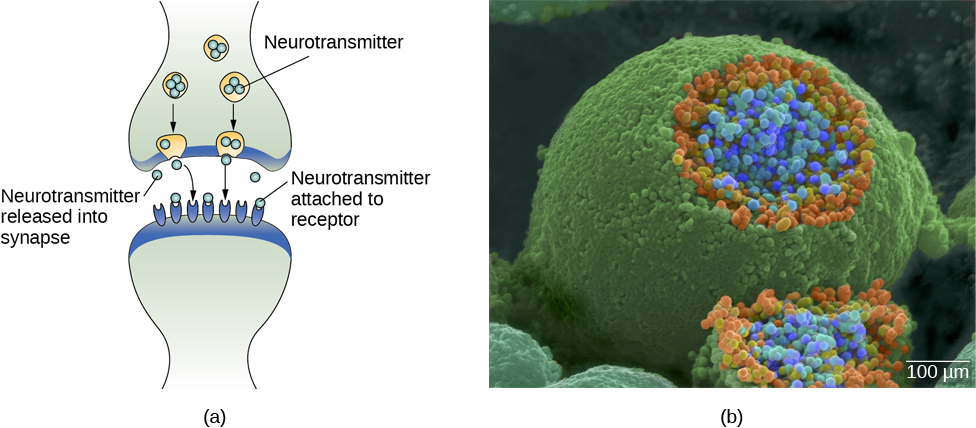
في الأفراد الأصحاء، تتحرك الإشارة العصبية بسرعة أسفل المحور إلى الأزرار الطرفية، حيث تطلق الحويصلات المشبكية الناقلات العصبية في الشق المشبكي (الشكل 3.9). الشق المشبكي هو مساحة صغيرة جدًا بين خليتين عصبيتين وهو موقع مهم يحدث فيه التواصل بين الخلايا العصبية. بمجرد إطلاق الناقلات العصبية في الشق المشبكي، تنتقل عبره وترتبط بالمستقبلات المقابلة على التغصينات العصبية المجاورة. تختلف المستقبلات والبروتينات الموجودة على سطح الخلية حيث تلتصق الناقلات العصبية، في الشكل، بأشكال مختلفة «تطابق» الناقلات العصبية المختلفة.
كيف «يعرف» الناقل العصبي أي مستقبل يرتبط به؟ يحتوي الناقل العصبي والمستقبل على ما يشار إليه بعلاقة القفل والمفتاح - الناقلات العصبية الخاصة تناسب مستقبلات معينة مشابهة لكيفية ملاءمة المفتاح للقفل. يرتبط الناقل العصبي بأي مستقبل يناسبه.
التواصل العصبي
الآن بعد أن تعلمنا عن الهياكل الأساسية للخلايا العصبية والدور الذي تلعبه هذه الهياكل في الاتصال العصبي، دعونا نلقي نظرة فاحصة على الإشارة نفسها - كيف تتحرك عبر الخلايا العصبية ثم تنتقل إلى الخلية العصبية التالية، حيث تتكرر العملية.
نبدأ في الغشاء العصبي. توجد الخلايا العصبية في بيئة سائلة - فهي محاطة بسائل خارج الخلية وتحتوي على سائل داخل الخلايا (أي السيتوبلازم). يحافظ الغشاء العصبي على هذين السائلين منفصلين - وهو دور حاسم لأن الإشارة الكهربائية التي تمر عبر الخلايا العصبية تعتمد على اختلاف السوائل داخل وخارج الخلية كهربائيًا. يوفر هذا الاختلاف في الشحن عبر الغشاء، والذي يسمى إمكانات الغشاء، الطاقة للإشارة.
تحدث الشحنة الكهربائية للسوائل بسبب الجزيئات المشحونة (الأيونات) الذائبة في السائل. تقيد الطبيعة شبه النفاذة للغشاء العصبي إلى حد ما حركة هذه الجزيئات المشحونة، ونتيجة لذلك، تميل بعض الجسيمات المشحونة إلى أن تصبح أكثر تركيزًا إما داخل الخلية أو خارجها.
بين الإشارات، يتم الاحتفاظ بإمكانيات الغشاء العصبي في حالة استعداد، تسمى إمكانات الراحة. مثل الشريط المطاطي الممتد إلى الخارج وينتظر أن يبدأ مفعوله، تصطف الأيونات على جانبي غشاء الخلية، جاهزة للاندفاع عبر الغشاء عندما تنشط الخلية العصبية ويفتح الغشاء بواباتها (أي مضخة الصوديوم والبوتاسيوم التي تسمح بحركة الأيونات عبر الغشاء). تكون الأيونات في المناطق ذات التركيز العالي جاهزة للانتقال إلى مناطق التركيز المنخفض، والأيونات الموجبة جاهزة للانتقال إلى المناطق ذات الشحنة السالبة.
في حالة الراحة، يكون الصوديوم (Na +) بتركيزات أعلى خارج الخلية، لذلك يميل إلى الانتقال إلى الخلية. البوتاسيوم (K +)، من ناحية أخرى، يتركز بشكل أكبر داخل الخلية، ويميل إلى الخروج من الخلية (الشكل 3.10). بالإضافة إلى ذلك، يتم شحن الجزء الداخلي من الخلية بشكل سلبي قليلاً مقارنة بالخارج. يوفر هذا قوة إضافية على الصوديوم، مما يؤدي إلى انتقاله إلى الخلية.
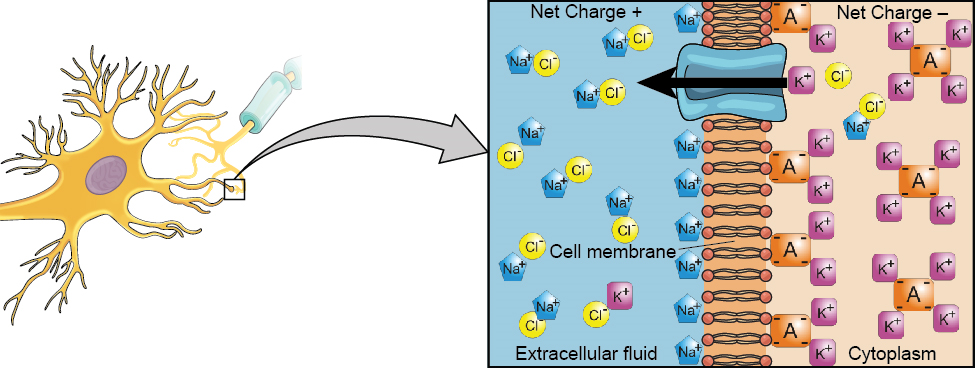
من هذه الحالة المحتملة للراحة، تستقبل الخلية العصبية إشارة وتتغير حالتها فجأة (الشكل 3.11). عندما تستقبل خلية عصبية إشارات عند التشعبات - بسبب الناقلات العصبية من خلية عصبية مجاورة مرتبطة بمستقبلاتها - تنفتح المسام الصغيرة أو البوابات على الغشاء العصبي، مما يسمح لأيونات Na +، المدفوعة باختلافات الشحنة والتركيز، بالانتقال إلى الخلية. مع تدفق الأيونات الموجبة، تصبح الشحنة الداخلية للخلية أكثر إيجابية. إذا وصلت هذه الشحنة إلى مستوى معين، يسمى عتبة الإثارة، تصبح الخلية العصبية نشطة وتبدأ إمكانات الفعل.
يتم فتح العديد من المسام الإضافية، مما يتسبب في تدفق هائل لأيونات Na + وارتفاع إيجابي كبير في إمكانات الغشاء، وهو ذروة الحركة المحتملة. في ذروة السنبلة، تُغلق بوابات الصوديوم وتُفتح بوابات البوتاسيوم. عندما تغادر أيونات البوتاسيوم المشحونة إيجابًا، تبدأ الخلية بسرعة في إعادة الاستقطاب. في البداية، يزداد الاستقطاب، ويصبح أكثر سلبية قليلاً من إمكانات الراحة، ثم يستقر ويعود إلى إمكانات الراحة.
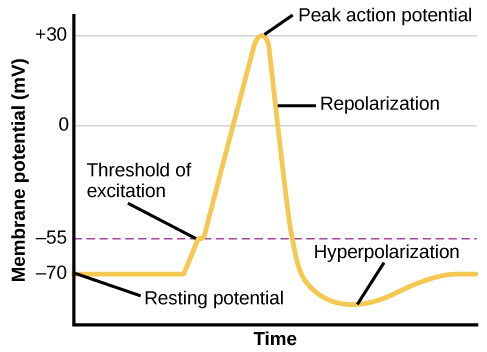
يشكل هذا الارتفاع الإيجابي إمكانات الحركة: الإشارة الكهربائية التي تنتقل عادةً من جسم الخلية إلى أسفل المحور إلى أطراف المحور. تتحرك الإشارة الكهربائية إلى أسفل المحور حيث تقفز النبضات بطريقة قفزة بين عقدة رانفير. عُقد رانفير هي فجوات طبيعية في غلاف المايلين. عند كل نقطة، تنتشر بعض أيونات الصوديوم التي تدخل الخلية إلى القسم التالي من المحور، مما يرفع الشحنة إلى ما بعد عتبة الإثارة ويؤدي إلى تدفق جديد لأيونات الصوديوم. تتحرك إمكانات الحركة على طول المحور بهذه الطريقة حتى تصل إلى الأزرار الطرفية.
إمكانات العمل هي ظاهرة الكل أو لا شيء. بعبارات بسيطة، هذا يعني أن الإشارة الواردة من خلية عصبية أخرى إما كافية أو غير كافية للوصول إلى عتبة الإثارة. لا يوجد وسيط، ولا يوجد إيقاف لإمكانات الإجراء بمجرد أن تبدأ. فكر في الأمر مثل إرسال بريد إلكتروني أو رسالة نصية. يمكنك التفكير في إرسالها كما تريد، ولكن لا يتم إرسال الرسالة حتى تضغط على زر الإرسال. علاوة على ذلك، بمجرد إرسال الرسالة، لا يمكن إيقافها.
نظرًا لوجود كل شيء أو لا شيء، يتم إعادة إنشاء إمكانات الحركة أو نشرها بكامل قوتها في كل نقطة على طول المحور. فهي تشبه إلى حد كبير الصمامات المضاءة للمفرقعات النارية، فهي لا تتلاشى أثناء انتقالها عبر المحور العصبي. إن خاصية الكل أو لا شيء هذه هي التي تفسر حقيقة أن دماغك يرى أن إصابة جزء بعيد من الجسم مثل إصبع قدمك مؤلمة بنفس القدر مثل إصابة أنفك.
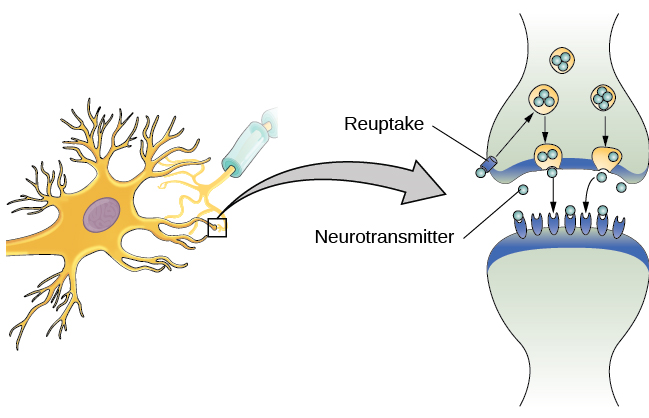
كما ذكرنا سابقًا، عندما تصل إمكانات الحركة إلى الزر الطرفي، تطلق الحويصلات المشبكية ناقلاتها العصبية في الشق المشبكي. تنتقل الناقلات العصبية عبر المشبك وترتبط بالمستقبلات الموجودة على تشعبات الخلايا العصبية المجاورة، وتتكرر العملية في الخلية العصبية الجديدة (بافتراض أن الإشارة قوية بما يكفي لتحفيز إمكانات الفعل). بمجرد تسليم الإشارة، تنجرف الناقلات العصبية الزائدة في الشق المشبكي بعيدًا، ويتم تقسيمها إلى أجزاء غير نشطة، أو يتم إعادة امتصاصها في عملية تعرف باسم إعادة الامتصاص. تتضمن إعادة الامتصاص الناقل العصبي الذي يتم ضخه مرة أخرى إلى العصبون الذي أطلقه، من أجل إزالة المشبك (الشكل 3.12). يعمل مسح المشبك على توفير حالة «تشغيل» و «إيقاف» واضحة بين الإشارات وتنظيم إنتاج الناقل العصبي (توفر الحويصلات المشبكية الكاملة إشارات لا تحتاج إلى إنتاج ناقلات عصبية إضافية).
الناقلات العصبية والأدوية
هناك عدة أنواع مختلفة من الناقلات العصبية التي تطلقها الخلايا العصبية المختلفة، ويمكننا التحدث بعبارات عامة عن أنواع الوظائف المرتبطة بالنواقل العصبية المختلفة (الجدول 3.1). يأتي الكثير مما يعرفه علماء النفس عن وظائف الناقلات العصبية من الأبحاث حول آثار الأدوية في الاضطرابات النفسية. يؤكد علماء النفس الذين يتخذون منظورًا بيولوجيًا ويركزون على الأسباب الفسيولوجية للسلوك أن الاضطرابات النفسية مثل الاكتئاب والفصام ترتبط بالاختلالات في واحد أو أكثر من أنظمة الناقلات العصبية. من هذا المنظور، يمكن للأدوية العقلية أن تساعد في تحسين الأعراض المرتبطة بهذه الاضطرابات. الأدوية العقلية هي أدوية تعالج الأعراض النفسية عن طريق استعادة توازن الناقلات العصبية.
| ناقل عصبي | تشارك في | التأثير المحتمل على السلوك |
|---|---|---|
| أستيل كولين | عمل العضلات والذاكرة | زيادة الإثارة، الإدراك المعزز |
| بيتا إندورفين | الألم والسرور | انخفاض القلق وانخفاض التوتر |
| الدوبامين | المزاج والنوم والتعلم | زيادة المتعة، الشهية المكبوتة |
| حمض غاما-أمينوبوتيريك (GABA) | وظيفة الدماغ والنوم | انخفاض القلق وانخفاض التوتر |
| الغلوتامات | الذاكرة والتعلم | زيادة التعلم والذاكرة المحسنة |
| النوربينفرين | القلب والأمعاء واليقظة | زيادة الإثارة، الشهية المكبوتة |
| سيروتونين | المزاج والنوم | مزاج معدّل، شهية مكبوتة |
يمكن أن تعمل الأدوية ذات التأثير النفساني كمنبهات أو مضادات لنظام ناقل عصبي معين. الناهضات هي مواد كيميائية تحاكي الناقل العصبي في موقع المستقبل. من ناحية أخرى، يقوم المضاد بحظر أو إعاقة النشاط الطبيعي للناقل العصبي في المستقبل. تمثل المنبهات والمضادات الأدوية التي يتم وصفها لتصحيح اختلالات الناقلات العصبية المحددة الكامنة وراء حالة الشخص. على سبيل المثال، يرتبط مرض باركنسون، وهو اضطراب تدريجي في الجهاز العصبي، بمستويات منخفضة من الدوبامين. لذلك، تتضمن استراتيجية العلاج الشائعة لمرض باركنسون استخدام ناهضات الدوبامين، التي تحاكي تأثيرات الدوبامين من خلال الارتباط بمستقبلات الدوبامين.
ترتبط بعض أعراض الفصام بالنقل العصبي المفرط للدوبامين. مضادات الذهان المستخدمة لعلاج هذه الأعراض هي مضادات للدوبامين - فهي تمنع تأثيرات الدوبامين عن طريق ربط مستقبلاته دون تنشيطها. وبالتالي، فإنها تمنع الدوبامين الذي تطلقه خلية عصبية واحدة من إرسال المعلومات إلى الخلايا العصبية المجاورة.
على عكس المنبهات والمضادات، التي تعمل على حد سواء عن طريق الارتباط بمواقع المستقبل، تمنع مثبطات إعادة الامتصاص الناقلات العصبية غير المستخدمة من الانتقال مرة أخرى إلى الخلايا العصبية. هذا يسمح للناقلات العصبية بالبقاء نشطة في الشق المشبكي لفترات أطول، مما يزيد من فعاليتها. عادة ما يتم علاج الاكتئاب، الذي يرتبط باستمرار بانخفاض مستويات السيروتونين، بمثبطات امتصاص السيروتونين الانتقائية (SSRIs). من خلال منع إعادة الامتصاص، تعمل مثبطات استرداد السيروتونين الانتقائية على تقوية تأثير السيروتونين، مما يمنحه مزيدًا من الوقت للتفاعل مع مستقبلات السيروتونين على التشعبات. تشمل مثبطات استرداد السيروتونين الانتقائية الشائعة في السوق اليوم بروزاك وباكسيل وزولوفت. عقار LSD مشابه جدًا من الناحية الهيكلية للسيروتونين، ويؤثر على نفس الخلايا العصبية والمستقبلات مثل السيروتونين. الأدوية العقلية ليست حلولًا فورية للأشخاص الذين يعانون من اضطرابات نفسية. في كثير من الأحيان، يجب على الفرد تناول الدواء لعدة أسابيع قبل رؤية التحسن، والعديد من الأدوية ذات التأثير النفساني لها آثار جانبية سلبية كبيرة. علاوة على ذلك، يختلف الأفراد بشكل كبير في كيفية استجابتهم للأدوية. لتحسين فرص النجاح، ليس من غير المألوف أن يخضع الأشخاص الذين يتلقون العلاج الدوائي لعلاجات نفسية و/أو سلوكية أيضًا. تشير بعض الأبحاث إلى أن الجمع بين العلاج الدوائي وأشكال العلاج الأخرى يميل إلى أن يكون أكثر فعالية من أي علاج بمفرده (على سبيل المثال، انظر March et al.، 2007).


