6.2: دورة الحياة الفيروسية
- Page ID
- 194545
أهداف التعلم
- وصف دورات الحياة الليتية والليسوجينية
- وصف عملية النسخ المتماثل للفيروسات الحيوانية
- وصف الخصائص الفريدة للفيروسات القهقرية والفيروسات الكامنة
- ناقش الفيروسات البشرية وتفاعلات الخلايا المضيفة للفيروسات
- شرح عملية النقل
- وصف عملية النسخ المتماثل لفيروسات النباتات
تعتمد جميع الفيروسات على الخلايا للتكاثر وعمليات التمثيل الغذائي. في حد ذاتها، لا تقوم الفيروسات بتشفير جميع الإنزيمات اللازمة لتكاثر الفيروس. ولكن داخل الخلية المضيفة، يمكن للفيروس أن يستولي على الآلات الخلوية لإنتاج المزيد من الجسيمات الفيروسية. تتكاثر البكتيريا فقط في السيتوبلازم، لأن الخلايا بدائية النواة لا تحتوي على نواة أو عضيات. في الخلايا حقيقية النواة، يمكن لمعظم فيروسات الحمض النووي التكاثر داخل النواة، باستثناء لوحظ في فيروسات الحمض النووي الكبيرة، مثل فيروسات الجدري، التي يمكن أن تتكاثر في السيتوبلازم. غالبًا ما تتكاثر فيروسات RNA التي تصيب الخلايا الحيوانية في السيتوبلازم.
دورة حياة الفيروسات مع مضيفي Prokaryote
كانت دورة حياة البكتيريا نموذجًا جيدًا لفهم كيفية تأثير الفيروسات على الخلايا التي تصيبها، حيث تمت ملاحظة عمليات مماثلة للفيروسات حقيقية النواة، والتي يمكن أن تسبب الموت الفوري للخلية أو إنشاء عدوى كامنة أو مزمنة. عادةً ما تؤدي العاثيات الخبيثة إلى موت الخلية من خلال تحلل الخلية. من ناحية أخرى، يمكن أن تصبح العاهرات المعتدلة جزءًا من الكروموسوم المضيف ويتم تكرارها مع جينوم الخلية حتى يحين الوقت الذي يتم فيه استحداثها لصنع فيروسات مجمعة حديثًا، أو فيروسات ذرية.
دورة ليتيك
خلال الدورة الليتيكية للعاثية الخبيثة، تستولي البكتيريا على الخلية وتعيد إنتاج عاهرات جديدة وتدمر الخلية. تعد عاثية T-even مثالًا جيدًا لفئة مميزة من العاثيات الخبيثة. هناك خمس مراحل في دورة التحلل البكتيري (انظر الشكل\(\PageIndex{1}\)). التعلق هو المرحلة الأولى في عملية العدوى التي تتفاعل فيها العاثية مع مستقبلات سطحية بكتيرية محددة (مثل السكريات الدهنية وبروتين OMPC على الأسطح المضيفة). تحتوي معظم العاهرات على نطاق مضيف ضيق وقد تصيب نوعًا واحدًا من البكتيريا أو سلالة واحدة داخل الأنواع. يمكن استغلال هذا الاعتراف الفريد للعلاج المستهدف للعدوى البكتيرية عن طريق العلاج بالعاهات أو لكتابة العاهرات لتحديد الأنواع الفرعية أو السلالات البكتيرية الفريدة. المرحلة الثانية من العدوى هي الدخول أو الاختراق. يحدث هذا من خلال تقلص غلاف الذيل، الذي يعمل كإبرة تحت الجلد لحقن الجينوم الفيروسي من خلال جدار الخلية والغشاء. يبقى رأس العاهة والمكونات المتبقية خارج البكتيريا.
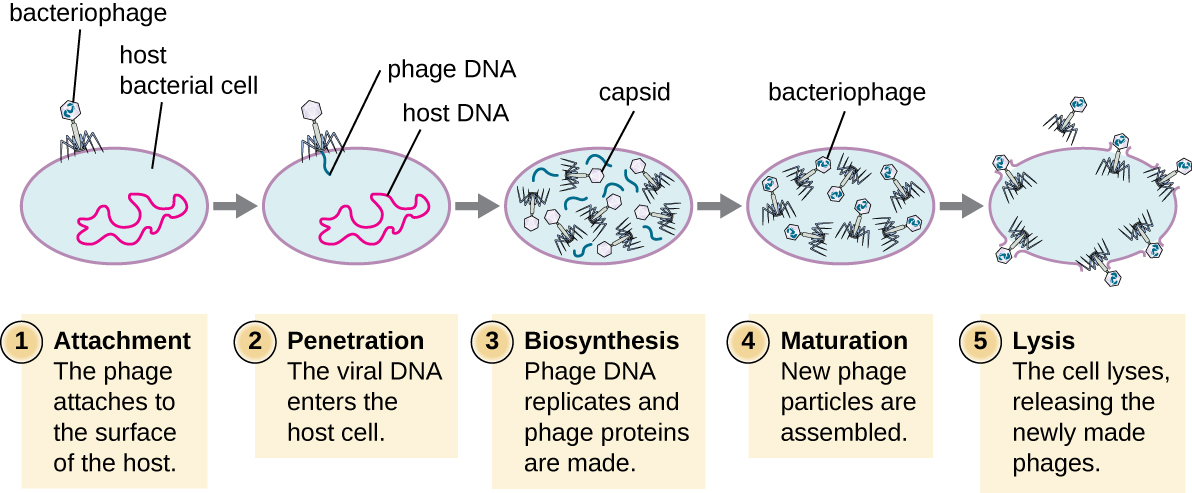
المرحلة الثالثة من العدوى هي التركيب الحيوي للمكونات الفيروسية الجديدة. بعد دخول الخلية المضيفة، يقوم الفيروس بتصنيع كريات الدم البيضاء المشفرة بالفيروسات لتحطيم الكروموسوم البكتيري. ثم تقوم باختطاف الخلية المضيفة لتكرار ونسخ وترجمة المكونات الفيروسية الضرورية (الكابسومير والغمد والألواح الأساسية وألياف الذيل والإنزيمات الفيروسية) لتجميع فيروسات جديدة. عادة ما يتم التعبير عن جينات البوليميراز في وقت مبكر من الدورة، بينما يتم التعبير عن بروتينات الكابسيد والذيل لاحقًا. خلال مرحلة النضج، يتم إنشاء فيروسات جديدة. لتحرير العاهرات الحرة، يتعطل جدار الخلية البكتيرية ببروتينات العاثية مثل الهولين أو الليزوزيم. المرحلة النهائية هي الإصدار. تنفجر الفيروسات الناضجة من الخلية المضيفة في عملية تسمى التحلل ويتم تحرير فيروسات النسل في البيئة لإصابة خلايا جديدة.
الدورة الليسوجينية
في الدورة الليسوجينية، يدخل جينوم العاثية أيضًا إلى الخلية من خلال التعلق والاختراق. والمثال الرئيسي للعاثية مع هذا النوع من دورة الحياة هو lambda phage. خلال الدورة الليسوجينية، بدلاً من قتل المضيف، يتكامل جينوم العاهرات في الكروموسوم البكتيري ويصبح جزءًا من المضيف. يُطلق على جينوم العاثية المتكامل اسم النبوءة. يُطلق على المضيف البكتيري ذو النبوءة اسم الليسوجين. تسمى العملية التي تصاب فيها البكتيريا بعامة معتدلة باسم الليسوجيني. من المعتاد أن تكون العاهرات المعتدلة كامنة أو غير نشطة داخل الخلية. عندما تقوم البكتيريا بتكرار الكروموسوم الخاص بها، فإنها تقوم أيضًا بتكرار الحمض النووي للعاثية وتنقله إلى الخلايا الوليدة الجديدة أثناء التكاثر. قد يؤدي وجود العاهة إلى تغيير النمط الظاهري للبكتيريا، لأنها يمكن أن تجلب جينات إضافية (مثل الجينات السامة التي يمكن أن تزيد من ضراوة البكتيريا). يُطلق على هذا التغيير في النمط الظاهري للمضيف اسم التحويل الليسوجيني أو تحويل العاهرات. بعض البكتيريا، مثل فيبريو كوليراي وكلوستريديوم البوتولينوم، تكون أقل ضراوة في غياب النبوءة. تحمل العاهرات التي تصيب هذه البكتيريا الجينات السامة في جينومها وتعزز ضراوة المضيف عند التعبير عن الجينات السامة. في حالة V. colera، يمكن أن يسبب السم المشفر بالبلغم إسهالًا شديدًا؛ في C. botulinum، يمكن أن يسبب السم الشلل. خلال عملية الليسوجيني، ستستمر النبوءة في الكروموسوم المضيف حتى الحث، مما يؤدي إلى استئصال الجينوم الفيروسي من الكروموسوم المضيف. بعد حدوث التحريض، يمكن أن تستمر العاثة المعتدلة خلال دورة ليتية ثم تخضع لعملية التحلل في خلية مصابة حديثًا (انظر الشكل\(\PageIndex{2}\)).
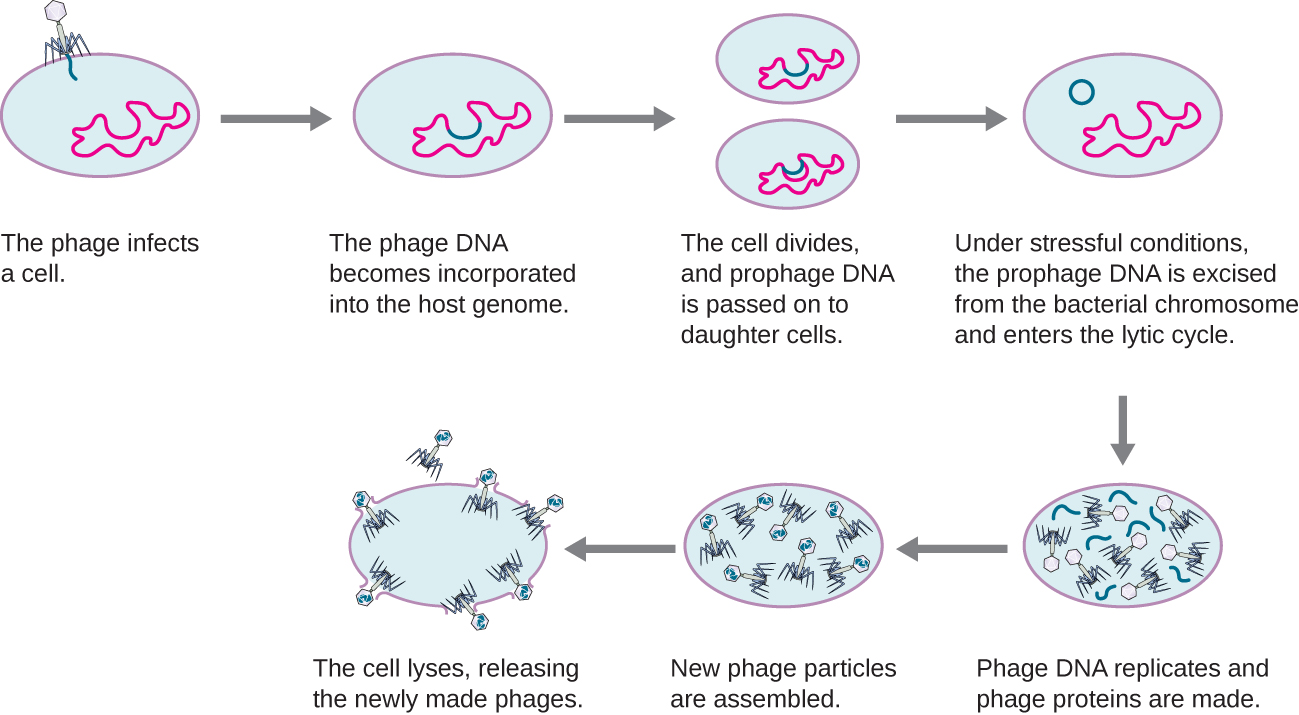
يوضح هذا الفيديو مراحل دورة الحياة الليسوجينية للبكتريا والانتقال إلى المرحلة الليتيكية.
التمارين الرياضية\(\PageIndex{1}\)
هل العاثة الكامنة غير قابلة للكشف في البكتيريا؟
نقل الدم
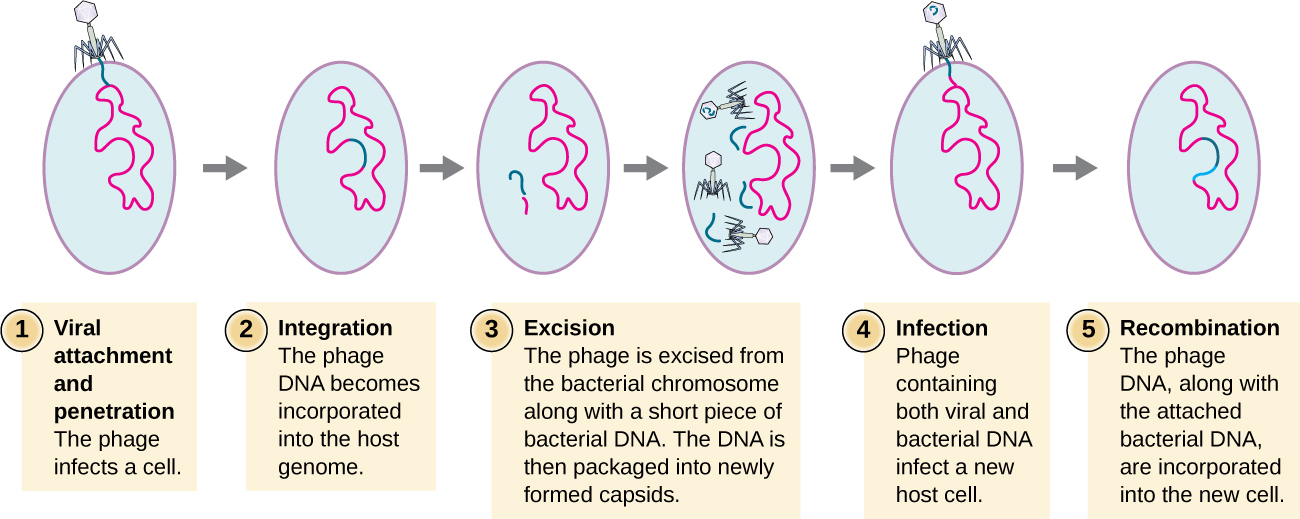
يحدث النقل عندما تنقل البكتيريا الحمض النووي البكتيري من بكتيريا إلى أخرى أثناء العدوى المتسلسلة. هناك نوعان من النقل: النقل العام والمتخصص. خلال الدورة اللايتية للتكاثر الفيروسي، يخطف الفيروس الخلية المضيفة، ويحلل الكروموسوم المضيف، ويصنع المزيد من الجينومات الفيروسية. عندما يقوم التغليف بتجميع الحمض النووي وتعبئته في رأس العاثية، فإن التغليف يحدث أحيانًا خطأ. بدلاً من تعبئة الحمض النووي الفيروسي، فإنه يأخذ قطعة عشوائية من الحمض النووي للمضيف ويدخلها في القفيصة. بمجرد إطلاقه، سيقوم هذا الفيروس بعد ذلك بحقن الحمض النووي للمضيف السابق في مضيف مصاب حديثًا. يمكن أن يسمح النقل اللاجنسي للمعلومات الجينية بحدوث إعادة تركيب الحمض النووي، وبالتالي تزويد المضيف الجديد بجينات جديدة (على سبيل المثال، جين مقاومة المضادات الحيوية، أو جين استقلاب السكر). يحدث النقل العام عندما يتم نقل قطعة عشوائية من الحمض النووي الكروموسومي البكتيري بواسطة العاهة أثناء الدورة اللايتية. يحدث النقل المتخصص في نهاية الدورة الليسوجينية، عندما يتم استئصال النبوءة وتدخل البكتيريا في الدورة اللايتية. نظرًا لأن العاثية مدمجة في جينوم المضيف، يمكن أن تتكاثر النبوءة كجزء من المضيف. ومع ذلك، فإن بعض الحالات (مثل التعرض للأشعة فوق البنفسجية أو التعرض للمواد الكيميائية) تحفز النبوءة على الخضوع للتحريض، مما يؤدي إلى خروج العاثية من الجينوم، ودخول الدورة اللايتية، وإنتاج فاجات جديدة لمغادرة الخلايا المضيفة. أثناء عملية الاستئصال من الكروموسوم المضيف، قد تقوم العاثة أحيانًا بإزالة بعض الحمض النووي البكتيري بالقرب من موقع التكامل الفيروسي. يتم تعبئة العاثية والحمض النووي المضيف من أحد طرفي موقع التكامل أو كلا طرفيه داخل الغطاء ويتم نقلهما إلى المضيف الجديد المصاب. نظرًا لأن الحمض النووي المنقول بواسطة العاثية لا يتم تعبئته عشوائيًا ولكنه بدلاً من ذلك جزء معين من الحمض النووي بالقرب من موقع التكامل، يشار إلى آلية نقل الجينات هذه باسم النقل المتخصص (انظر الشكل\(\PageIndex{3}\)). يمكن بعد ذلك إعادة دمج الحمض النووي مع الكروموسوم المضيف، مما يعطي الخصائص الجديدة الأخيرة. يبدو أن النقل يلعب دورًا مهمًا في العملية التطورية للبكتيريا، مما يمنحها آلية للتبادل اللاجنسي للمعلومات الجينية.
التمارين الرياضية\(\PageIndex{2}\)
ما دورة حياة العاثية المرتبطة بأي شكل من أشكال النقل؟
دورة حياة الفيروسات مع الحيوانات المضيفة
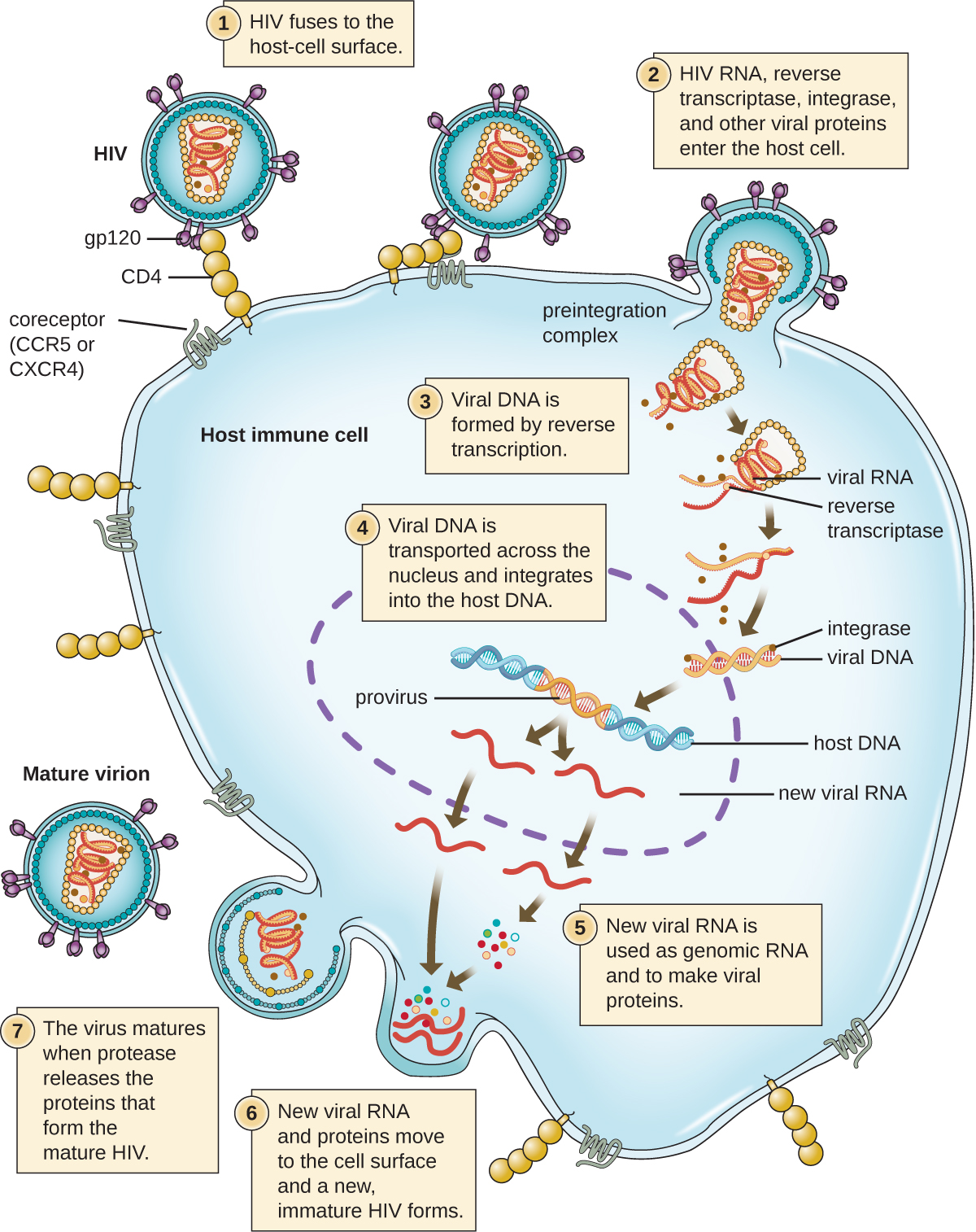
تتبع فيروسات الحيوانات اللايتية مراحل عدوى مماثلة للبكتريا: التعلق والاختراق والتركيب الحيوي والنضج والإطلاق (انظر الشكل\(\PageIndex{4}\)). ومع ذلك، تختلف آليات الاختراق والتركيب الحيوي للحمض النووي والإطلاق بين الفيروسات البكتيرية والحيوانية. بعد الارتباط بمستقبلات المضيف، تدخل الفيروسات الحيوانية من خلال إندوسيتوسيس (اجتياح الخلية المضيفة) أو من خلال الاندماج الغشائي (غلاف فيروسي مع غشاء الخلية المضيفة). العديد من الفيروسات خاصة بالمضيف، مما يعني أنها تصيب نوعًا معينًا من المضيفين فقط؛ وتصيب معظم الفيروسات أنواعًا معينة فقط من الخلايا داخل الأنسجة. هذه الخصوصية تسمى تروبيسم الأنسجة. ومن الأمثلة على ذلك فيروس شلل الأطفال، الذي يُظهر تروبيسًا لأنسجة الدماغ والحبل الشوكي، أو فيروس الإنفلونزا، الذي له تأثير أساسي على الجهاز التنفسي.
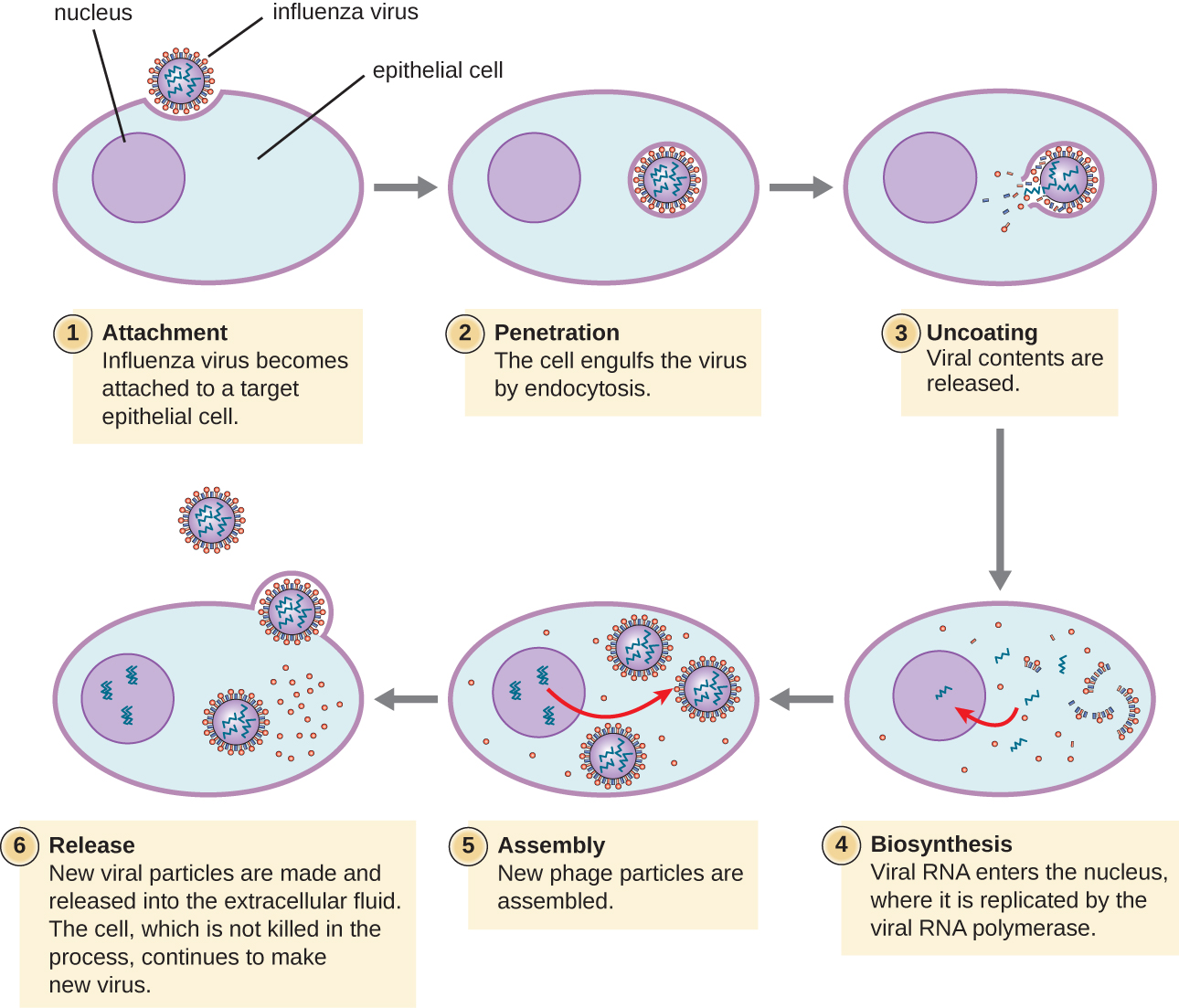
لا تعبر فيروسات الحيوانات دائمًا عن جيناتها باستخدام التدفق الطبيعي للمعلومات الجينية - من الحمض النووي إلى الحمض النووي الريبي إلى البروتين. تحتوي بعض الفيروسات على جينوم dsDNA مثل الكائنات الخلوية ويمكنها متابعة التدفق الطبيعي. ومع ذلك، قد يكون لدى البعض الآخر جينومات ssDNA أو dSrNA أو ssRNA. تحدد طبيعة الجينوم كيفية تكرار الجينوم والتعبير عنه كبروتينات فيروسية. إذا كان الجينوم هو ssDNA، فسيتم استخدام الإنزيمات المضيفة لتجميع خيط ثانٍ مكمل لخيط الجينوم، وبالتالي إنتاج dsDNA. يمكن الآن نسخ dsDNA ونسخه وترجمته على غرار الحمض النووي للمضيف.
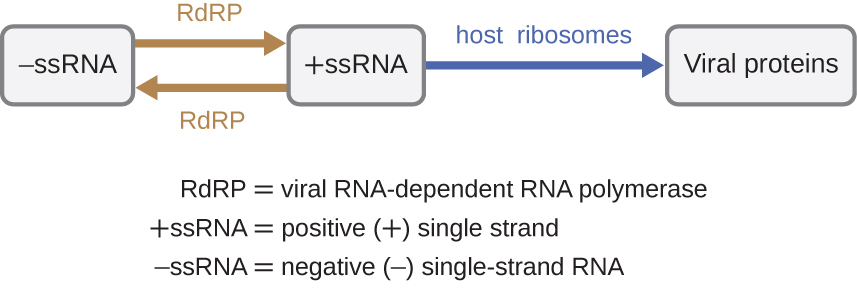
إذا كان الجينوم الفيروسي هو RNA، فيجب استخدام آلية مختلفة. هناك ثلاثة أنواع من جينوم الحمض النووي الريبي: dSrNA، أو الحمض النووي الريبي الموجب (+) أحادي الجديلة (+ SSRNA) أو السالب (−) الحمض النووي الريبي أحادي الجديلة (−SS إذا كان الفيروس يحتوي على جينوم +ssRNA، فيمكن ترجمته مباشرة لإنتاج بروتينات فيروسية. يعمل الجينوم الفيروسي+SSRNA مثل mRNA الخلوي. ومع ذلك، إذا كان الفيروس يحتوي على جينوم −SSRNA، فلا يمكن للريبوسومات المضيفة ترجمته حتى يتم نسخ −ssRNA إلى +ssRNA بواسطة بوليميراز الحمض النووي الريبي الفيروسي المعتمد على الحمض النووي الريبي (RdRP) (انظر الشكل\(\PageIndex{5}\)). يتم جلب RdRp بواسطة الفيروس ويمكن استخدامه لصنع +ssRNA من جينوم −ssRNA الأصلي. يعد RdRp أيضًا إنزيمًا مهمًا لتكرار فيروسات dSrNA، لأنه يستخدم الخيط السالب للجينوم المزدوج كقالب لإنشاء +ssRNA. يمكن بعد ذلك ترجمة نسخ +ssRNA المركبة حديثًا بواسطة الريبوسومات الخلوية.
ولوحظت آلية بديلة لتخليق الحمض النووي الفيروسي في الفيروسات القهقرية، وهي فيروسات +ssRNA (انظر الشكل\(\PageIndex{6}\)). تحمل فيروسات الحمض النووي الريبي أحادية السلسلة مثل فيروس نقص المناعة البشرية إنزيمًا خاصًا يسمى النسخ العكسي داخل القفيصة الذي يقوم بتجميع نسخة SSDNA (cDNA) التكميلية باستخدام جينوم +ssRNA كقالب. يتم بعد ذلك تحويل ssDNA إلى dsDNA، والذي يمكن أن يندمج في الكروموسوم المضيف ويصبح جزءًا دائمًا من المضيف. يُطلق على الجينوم الفيروسي المتكامل اسم provirus. يمكن للفيروس الآن البقاء في المضيف لفترة طويلة لإنشاء عدوى مزمنة. تشبه مرحلة البروفيروس مرحلة النبوءة في العدوى البكتيرية خلال الدورة الليسوجينية. ومع ذلك، على عكس النبوءة، لا يخضع الفيروس للختان بعد ربطه بالجينوم.
التمارين الرياضية\(\PageIndex{3}\)
هل بوليميراز الحمض النووي الريبي المعتمد على الحمض النووي الريبي مصنوع من جين فيروسي أو جين مضيف؟
العدوى المستمرة
تحدث العدوى المستمرة عندما لا يتم إزالة الفيروس تمامًا من نظام المضيف ولكنه يبقى في أنسجة أو أعضاء معينة للشخص المصاب. قد يظل الفيروس صامتًا أو يخضع لعدوى منتجة دون الإضرار بالمضيف أو قتله بشكل خطير. قد تتضمن آليات العدوى المستمرة تنظيم تعبيرات الجينات الفيروسية أو المضيفة أو تغيير الاستجابة المناعية للمضيف. والفئتان الأساسيتان للعدوى المستمرة هما العدوى الكامنة والعدوى المزمنة. تشمل أمثلة الفيروسات التي تسبب العدوى الكامنة فيروس الهربس البسيط (الهربس الفموي والتناسلي) وفيروس الحماق النطاقي (الجدري والهربس) وفيروس Epstein-Barr (كريات الدم البيضاء). يعد فيروس التهاب الكبد C وفيروس نقص المناعة البشرية مثالين على الفيروسات التي تسبب التهابات مزمنة طويلة الأمد.
عدوى كامنة
لا تخضع جميع الفيروسات الحيوانية للتكرار من خلال الدورة الليتية. هناك فيروسات قادرة على البقاء مخفية أو خاملة داخل الخلية في عملية تسمى زمن الوصول. تُعرف هذه الأنواع من الفيروسات باسم الفيروسات الكامنة وقد تسبب التهابات كامنة. قد تتسبب الفيروسات القادرة على الكمون في البداية في حدوث عدوى حادة قبل أن تصبح خاملة.
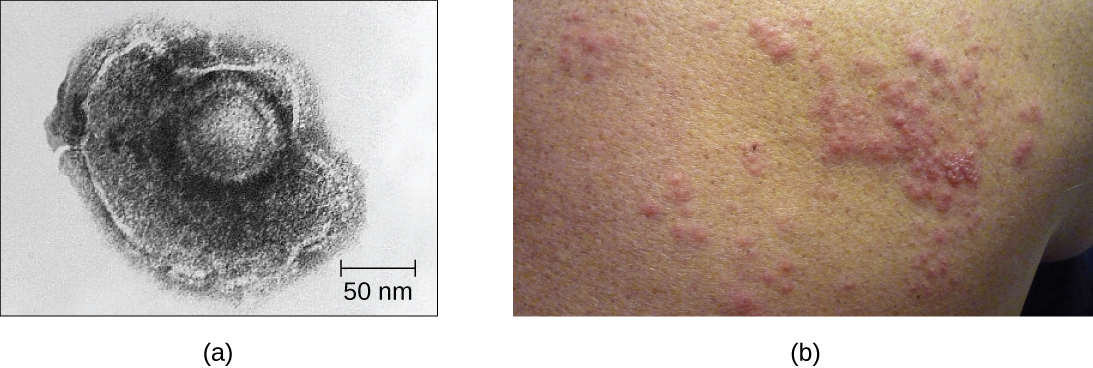
على سبيل المثال، يصيب فيروس varicella-zoster العديد من الخلايا في جميع أنحاء الجسم ويسبب الجدري المائي الذي يتميز بطفح جلدي من البثور التي تغطي الجلد. بعد حوالي 10 إلى 12 يومًا من الإصابة بالعدوى، يزول المرض ويصبح الفيروس خاملًا ويعيش داخل العقد العصبية لسنوات. خلال هذا الوقت، لا يقتل الفيروس الخلايا العصبية أو يستمر في التكاثر. ليس من الواضح لماذا يتوقف الفيروس عن التكاثر داخل الخلايا العصبية ويعبر عن عدد قليل من البروتينات الفيروسية، ولكن في بعض الحالات، عادةً بعد سنوات عديدة من السكون، يتم إعادة تنشيط الفيروس ويسبب مرضًا جديدًا يسمى الهربس النطاقي (الشكل\(\PageIndex{7}\)). في حين أن الجدري المائي يؤثر على العديد من مناطق الجسم، فإن الهربس النطاقي هو مرض خاص بالخلايا العصبية ينشأ من العقد التي كان الفيروس خاملًا فيها.
قد تظل الفيروسات الكامنة خاملة من خلال وجودها كجزيئات جينوم فيروسية دائرية خارج الكروموسوم المضيف. يصبح البعض الآخر موردًا من خلال الاندماج في جينوم المضيف. خلال فترة السكون، لا تسبب الفيروسات أي أعراض للمرض وقد يكون من الصعب اكتشافها. قد لا يدرك المريض أنه يحمل الفيروس ما لم يتم إجراء اختبار تشخيصي فيروسي.
عدوى مزمنة
العدوى المزمنة هي مرض له أعراض متكررة أو مستمرة لفترة طويلة. يمكن أن تكون بعض الالتهابات الفيروسية مزمنة إذا كان الجسم غير قادر على القضاء على الفيروس. فيروس نقص المناعة البشرية هو مثال لفيروس ينتج عدوى مزمنة، غالبًا بعد فترة طويلة من الكمون. بمجرد إصابة الشخص بفيروس نقص المناعة البشرية، يمكن اكتشاف الفيروس في الأنسجة بشكل مستمر بعد ذلك، ولكن المرضى غير المعالجين غالبًا ما لا يعانون من أي أعراض لسنوات. ومع ذلك، يحافظ الفيروس على الثبات المزمن من خلال العديد من الآليات التي تتداخل مع وظيفة المناعة، بما في ذلك منع ظهور المستضدات الفيروسية على سطح الخلايا المصابة، وتغيير الخلايا المناعية نفسها، وتقييد التعبير عن الجينات الفيروسية، وتغيير المستضدات الفيروسية بسرعة من خلال طفرة. في نهاية المطاف، يؤدي تلف الجهاز المناعي إلى تطور المرض مما يؤدي إلى متلازمة نقص المناعة المكتسب (الإيدز). تستخدم أيضًا الآليات المختلفة التي يستخدمها فيروس نقص المناعة البشرية لتجنب التخلص منه من قبل الجهاز المناعي من قبل الفيروسات الأخرى المصابة بشكل مزمن، بما في ذلك فيروس التهاب الكبد C.
التمارين الرياضية\(\PageIndex{4}\)
ما الطريقتان اللتان يمكن للفيروس من خلالهما الحفاظ على العدوى المستمرة؟
دورة حياة الفيروسات مع مضيفي النباتات
تشبه الفيروسات النباتية فيروسات الحيوانات أكثر من الفيروسات الجرثومية. قد تكون الفيروسات النباتية مغلفة أو غير مغلفة. مثل العديد من الفيروسات الحيوانية، يمكن أن تحتوي الفيروسات النباتية إما على جينوم الحمض النووي أو الحمض النووي الريبي وأن تكون مفردة أو مزدوجة. ومع ذلك، لا تحتوي معظم الفيروسات النباتية على جينوم الحمض النووي؛ تحتوي الغالبية على جينوم +ssRNA، الذي يعمل مثل الحمض النووي الريبي المرسل (mRNA). فقط أقلية من الفيروسات النباتية لديها أنواع أخرى من الجينومات.
قد يكون للفيروسات النباتية نطاق مضيف ضيق أو واسع. على سبيل المثال، لا يصيب فيروس تريستيزا الحمضيات سوى عدد قليل من النباتات من جنس الحمضيات، بينما يصيب فيروس فسيفساء الخيار آلاف النباتات من عائلات نباتية مختلفة. تنتقل معظم الفيروسات النباتية عن طريق الاتصال بين النباتات، أو عن طريق الفطريات أو النيماتودا أو الحشرات أو المفصليات الأخرى التي تعمل كناقلات ميكانيكية. ومع ذلك، لا يمكن نقل بعض الفيروسات إلا عن طريق نوع معين من ناقلات الحشرات؛ على سبيل المثال، قد ينتقل فيروس معين عن طريق حشرات المن ولكن ليس الذباب الأبيض. في بعض الحالات، قد تدخل الفيروسات أيضًا النباتات الصحية من خلال الجروح، كما قد يحدث بسبب التقليم أو أضرار الطقس.
تعتبر الفيروسات التي تصيب النباتات طفيليات ذات تغذية حيوية، مما يعني أنها يمكن أن تثبت العدوى دون قتل المضيف، على غرار ما لوحظ في دورات الحياة الليسوجينية للبكتريا. يمكن أن تكون العدوى الفيروسية بدون أعراض (كامنة) أو يمكن أن تؤدي إلى موت الخلايا (عدوى ليتيك). تبدأ دورة الحياة بتغلغل الفيروس في الخلية المضيفة. بعد ذلك، يتم إزالة الفيروس داخل السيتوبلازم في الخلية عند إزالة القفيصة. اعتمادًا على نوع الحمض النووي، تُستخدم المكونات الخلوية لتكرار الجينوم الفيروسي وتوليف البروتينات الفيروسية لتجميع الفيروسات الجديدة. لإثبات وجود عدوى جهازية، يجب أن يدخل الفيروس جزءًا من نظام الأوعية الدموية للنبات، مثل البلغم. قد يختلف الوقت اللازم للعدوى الجهازية من بضعة أيام إلى بضعة أسابيع اعتمادًا على الفيروس وأنواع النباتات والظروف البيئية. تكتمل دورة حياة الفيروس عندما ينتقل من نبات مصاب إلى نبات صحي.
التمارين الرياضية\(\PageIndex{5}\)
ما هي بنية وجينوم فيروس النبات النموذجي؟
منحنى النمو الفيروسي
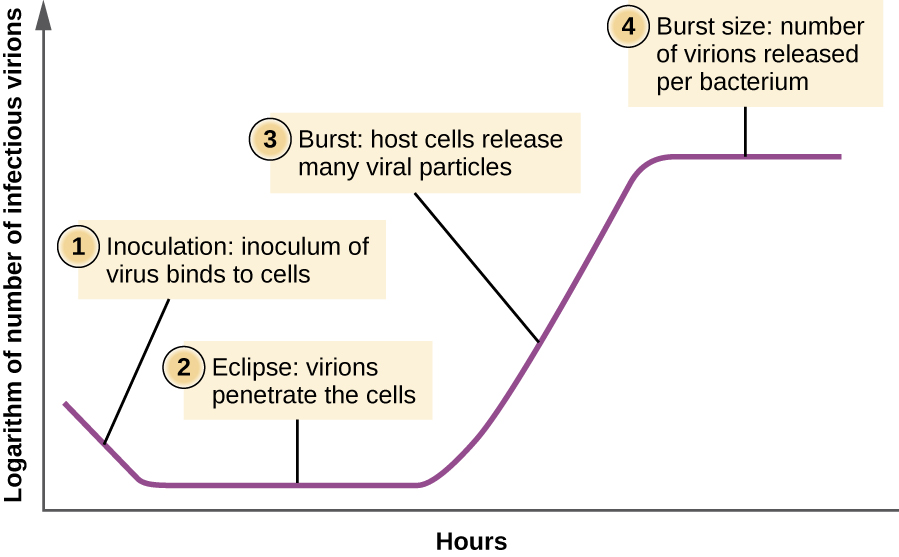
على عكس منحنى النمو لمجموعة البكتيريا، لا يتبع منحنى نمو مجموعة الفيروسات على مدار دورة حياتها منحنى سيني. خلال المرحلة الأولية، يسبب لقاح الفيروس العدوى. في مرحلة الكسوف، تربط الفيروسات الخلايا وتخترقها دون اكتشاف أي فيروسات في الوسط. يحدث الاختلاف الرئيسي الذي يظهر بعد ذلك في منحنى النمو الفيروسي مقارنة بمنحنى نمو البكتيريا عندما يتم إطلاق الفيروسات من الخلية المضيفة المتحللة في نفس الوقت. ويسمى هذا الحدوث بالانفجار، ويوصف عدد الفيروسات لكل بكتيريا يتم إطلاقها بحجم الانفجار. في منحنى التكاثر ذو الخطوة الواحدة للبكتيريا، تتحلل الخلايا المضيفة، وتطلق العديد من الجسيمات الفيروسية إلى الوسط، مما يؤدي إلى ارتفاع حاد جدًا في عيار الفيروس (عدد الفيروسات لكل وحدة حجم). في حالة عدم وجود خلايا مضيفة قابلة للحياة، تبدأ الجسيمات الفيروسية في التحلل أثناء تدهور الثقافة (انظر الشكل\(\PageIndex{8}\)).
التمارين الرياضية\(\PageIndex{6}\)
ما هو جانب دورة حياة الفيروس الذي يؤدي إلى الزيادة المفاجئة في منحنى النمو؟
العلاجات غير المسجلة
الإيبولا غير قابلة للشفاء ومميتة. كان تفشي المرض في غرب إفريقيا في عام 2014 غير مسبوق، مما أدى إلى تضاؤل أوبئة الإيبولا البشرية الأخرى في مستوى الوفيات. من بين 24666 حالة مشتبه بها أو مؤكدة تم الإبلاغ عنها، توفي 10179 شخصًا. 1
لا تتوفر علاجات أو لقاحات معتمدة للإيبولا. في حين أظهرت بعض الأدوية إمكانات في الدراسات المختبرية والنماذج الحيوانية، لم يتم اختبارها على البشر من أجل السلامة والفعالية. لا يقتصر الأمر على عدم اختبار هذه الأدوية أو تسجيلها فحسب، بل هناك نقص أيضًا في المعروض منها.
بالنظر إلى المعاناة الكبيرة ومعدلات الوفيات المرتفعة، من العدل أن نسأل ما إذا كانت الأدوية غير المسجلة وغير المختبرة أفضل من عدم وجودها على الإطلاق. هل ينبغي صرف هذه الأدوية، وإذا كان الأمر كذلك، فمن ينبغي أن يحصل عليها، في ضوء الإمدادات المحدودة للغاية؟ هل من الأخلاقي علاج الأدوية غير المختبرة على مرضى الإيبولا؟ من ناحية أخرى، هل من الأخلاقي حجب الأدوية التي يمكن أن تنقذ الحياة عن المرضى الذين يموتون؟ أو هل ينبغي حجز الأدوية لمقدمي الرعاية الصحية الذين يعملون على احتواء المرض؟
في أغسطس 2014، تم علاج اثنين من عمال الإغاثة الأمريكيين المصابين وكاهن إسباني باستخدام ZmApp، وهو دواء غير مسجل تم اختباره على القرود ولكن ليس على البشر. تعافى عاملتا الإغاثة الأمريكيان، لكن الكاهن مات. في وقت لاحق من ذلك الشهر، أصدرت منظمة الصحة العالمية تقريرًا عن أخلاقيات علاج المرضى بالعقار. نظرًا لأن الإيبولا غالبًا ما يكون مميتًا، فقد خلصت اللجنة إلى أنه من الأخلاقي إعطاء الأدوية غير المسجلة ومن غير الأخلاقي حجبها لأسباب تتعلق بالسلامة. هذا الوضع هو مثال على «الاستخدام الرحيم» خارج النظام الراسخ لتنظيم وإدارة العلاجات.
الإيبولا في الولايات المتحدة
في 24 سبتمبر 2014، وصل توماس إريك دنكان إلى مستشفى تكساس هيلث بريسبيتيريان في دالاس يشكو من الحمى والصداع والقيء والإسهال - وهي أعراض شائعة في مرضى البرد أو الأنفلونزا. بعد الفحص، قام طبيب قسم الطوارئ بتشخيص إصابته بالتهاب الجيوب الأنفية، ووصف بعض المضادات الحيوية، وأرسله إلى المنزل. بعد يومين، عاد دنكان إلى المستشفى بواسطة سيارة إسعاف. تدهورت حالته وأكدت اختبارات الدم الإضافية أنه مصاب بفيروس إيبولا.
كشفت التحقيقات الإضافية أن دنكان قد عاد للتو من ليبيريا، إحدى الدول في خضم وباء الإيبولا الشديد. في 15 سبتمبر، أي قبل تسعة أيام من ظهوره في المستشفى في دالاس، ساعد دنكان في نقل جار مصاب بالإيبولا إلى مستشفى في ليبيريا. استمر المستشفى في علاج دنكان، لكنه توفي بعد عدة أيام من دخوله المستشفى.
يشير الجدول الزمني لحالة دنكان إلى دورة حياة فيروس إيبولا. تتراوح فترة حضانة الإيبولا من يومين إلى 21 يومًا. مرت تسعة أيام بين تعرض دنكان لعدوى الفيروس وظهور أعراضه. وهذا يتوافق جزئيًا مع فترة الكسوف في نمو أعداد الفيروس. خلال مرحلة الكسوف، لم يكن دنكان قادرًا على نقل المرض للآخرين. ومع ذلك، بمجرد أن يبدأ الشخص المصاب في إظهار الأعراض، يصبح المرض معديًا جدًا. ينتقل فيروس الإيبولا من خلال الاتصال المباشر مع قطرات سوائل الجسم مثل اللعاب والدم والقيء. كان من الممكن أن يكون دنكان قد نقل المرض إلى الآخرين في أي وقت بعد أن بدأت تظهر عليه الأعراض، وربما قبل وصوله إلى المستشفى في دالاس ببعض الوقت. بمجرد أن يدرك المستشفى أن مريضًا مثل دنكان مصاب بفيروس إيبولا، يتم وضع المريض على الفور في الحجر الصحي، ويبدأ مسؤولو الصحة العامة في إجراء تتبع خلفي لتحديد كل شخص قد يكون مريض مثل دنكان قد تفاعل معه خلال الفترة التي ظهرت فيها الأعراض.
تمكن مسؤولو الصحة العامة من تعقب 10 أفراد معرضين للخطر (أفراد عائلة دنكان) و 50 فردًا منخفض المخاطر لمراقبتهم بحثًا عن علامات العدوى. لم يصاب أي منهم بالمرض. ومع ذلك، فقد أصيبت إحدى الممرضات المكلفات برعاية دنكان. هذا، إلى جانب التشخيص الخاطئ الأولي لدنكان، أوضح أن المستشفيات الأمريكية بحاجة إلى توفير تدريب إضافي للعاملين الطبيين لمنع تفشي الإيبولا المحتمل في الولايات المتحدة.
التمارين الرياضية\(\PageIndex{7}\)
- ما أنواع التدريب التي يمكن أن تعد المهنيين الصحيين لاحتواء الأوبئة الناشئة مثل تفشي الإيبولا في عام 2014؟
- ما الفرق بين العامل الممرض المعدي والممرض المعدي؟

للحصول على معلومات إضافية حول الإيبولا، يرجى زيارة موقع CDC.
ملخص
- تستهدف العديد من الفيروسات مضيفات أو أنسجة معينة. قد يكون لدى البعض أكثر من مضيف واحد.
- تتبع العديد من الفيروسات عدة مراحل لإصابة الخلايا المضيفة. تشمل هذه المراحل التعلق والاختراق والتفكيك والتركيب الحيوي والنضج والإطلاق.
- تحتوي البكتيريا على دورة ليتية أو ليسوجينية. تؤدي الدورة اللايتية إلى موت المضيف، بينما تؤدي الدورة الليسوجينية إلى دمج العاثية في جينوم المضيف.
- تقوم البكتيريا بحقن الحمض النووي في الخلية المضيفة، بينما تدخل الفيروسات الحيوانية عن طريق إندوسيتوسيس أو الاندماج الغشائي.
- يمكن أن تخضع فيروسات الحيوانات لوقت الاستجابة، على غرار الليسوجيني في مرحلة البكتيريا.
- غالبية الفيروسات النباتية عبارة عن الحمض النووي الريبي ذو الخصلة الإيجابية ويمكن أن تخضع لعدوى الكمون أو العدوى المزمنة أو الليتية، كما لوحظ في فيروسات الحيوانات.
- منحنى نمو مجموعات البكتيريا هو منحنى ضرب من خطوة واحدة وليس منحنى سيني، مقارنة بمنحنى نمو البكتيريا.
- تنقل البكتيريا المعلومات الجينية بين المضيفين باستخدام النقل العام أو المتخصص.
الحواشي
- 1 منظمة الصحة العالمية. «بيانات وإحصاءات منظمة الصحة العالمية حول الإيبولا». 18 مارس 2005. http://apps.who.int/gho/data/view.eb...150318؟ lang=en


