14.1: الأساس التاريخي للتفاهم الحديث
- Page ID
- 196572
المهارات اللازمة للتطوير
- شرح تحويل الحمض النووي
- وصف التجارب الرئيسية التي ساعدت في تحديد أن الحمض النووي هو المادة الوراثية
- اذكر قواعد Chargaff واشرحها
تطورت التفاهمات الحديثة للحمض النووي من اكتشاف الحمض النووي إلى تطوير نموذج الحلزون المزدوج. في ستينيات القرن التاسع عشر، كان فريدريش ميشر (الشكل\(\PageIndex{1}\))، الطبيب حسب المهنة، أول شخص يعزل المواد الكيميائية الغنية بالفوسفات من خلايا الدم البيضاء أو كريات الدم البيضاء. أطلق على هذه المواد الكيميائية (التي ستعرف في النهاية باسم RNA و DNA) اسم nuclein لأنها كانت معزولة عن نوى الخلايا.

رابط إلى التعلم

لرؤية ميشر يجري تجربة خطوة بخطوة، انقر فوق هذه المراجعة لكيفية اكتشافه للدور الرئيسي للحمض النووي والبروتينات في النواة.
بعد نصف قرن، ربما كان عالم البكتيريا البريطاني فريدريك غريفيث أول شخص أظهر أن المعلومات الوراثية يمكن نقلها من خلية إلى أخرى «أفقيًا»، وليس عن طريق النسب. في عام 1928، أبلغ عن أول عرض توضيحي للتحول البكتيري، وهي عملية يتم فيها امتصاص الحمض النووي الخارجي بواسطة خلية، وبالتالي تغيير الشكل وعلم وظائف الأعضاء. كان يعمل مع المكورات العقدية الرئوية، البكتيريا التي تسبب الالتهاب الرئوي. عمل غريفيث بسلالتين، خشنة (R) وسلسة (S). تعتبر سلالة R غير مسببة للأمراض (لا تسبب المرض) وتسمى بالخشونة لأن سطحها الخارجي عبارة عن جدار خلوي ويفتقر إلى الكبسولة؛ ونتيجة لذلك، يبدو سطح الخلية غير متساوٍ تحت المجهر. تعتبر سلالة S مسببة للأمراض (مسببة للأمراض) وتحتوي على كبسولة خارج جدار الخلية. ونتيجة لذلك، تتمتع بمظهر سلس تحت المجهر. قام جريفيث بحقن سلالة R الحية في الفئران ونجوا. في تجربة أخرى، عندما قام بحقن الفئران بسلالة S القاتلة للحرارة، نجت أيضًا. في مجموعة ثالثة من التجارب، تم حقن خليط من سلالة R الحية وسلالة S القاتلة بالحرارة في الفئران، وماتت الفئران - لدهشته. عند عزل البكتيريا الحية عن الفأر الميت، تم استعادة سلالة S فقط من البكتيريا. عندما تم حقن سلالة S المعزولة هذه في الفئران الطازجة، ماتت الفئران. استنتج غريفيث أن شيئًا ما قد انتقل من سلالة S القاتلة بالحرارة إلى سلالة R الحية وحولها إلى سلالة S المسببة للأمراض، وأطلق على هذا مبدأ التحويل (الشكل\(\PageIndex{2}\)). تُعرف هذه التجارب الآن باسم تجارب التحول التي أجراها جريفيث.
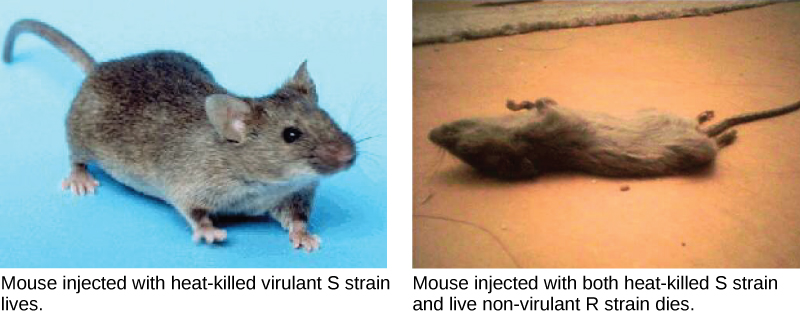
كان العلماء أوزوالد أفيري وكولين ماكلويد وماكلين مكارتي (1944) مهتمين باستكشاف مبدأ التحول هذا بشكل أكبر. لقد عزلوا سلالة S من الفئران الميتة وعزلوا البروتينات والأحماض النووية، أي RNA و DNA، حيث كانت هذه العوامل مرشحة محتملة لجزيء الوراثة. لقد أجروا دراسة منهجية للتخلص من المرض. استخدموا الإنزيمات التي أدت إلى تدهور كل مكون على وجه التحديد ثم استخدموا كل خليط على حدة لتحويل سلالة R. ووجدوا أنه عندما يتحلل الحمض النووي، لم يعد الخليط الناتج قادرًا على تحويل البكتيريا، في حين أن جميع التركيبات الأخرى كانت قادرة على تحويل البكتيريا. قادهم هذا إلى استنتاج أن الحمض النووي هو مبدأ التحويل.
الاتصال الوظيفي: علماء الطب الشرعي وتحليل الحمض النووي
تم استخدام دليل الحمض النووي لأول مرة لحل قضية الهجرة. بدأت القصة مع صبي في سن المراهقة يعود إلى لندن من غانا ليكون مع والدته. وكانت سلطات الهجرة في المطار تشك فيه، معتقدة أنه كان يسافر بجواز سفر مزور. بعد الكثير من الإقناع، سُمح له بالذهاب للعيش مع والدته، لكن سلطات الهجرة لم تسقط القضية المرفوعة ضده. تم تقديم جميع أنواع الأدلة، بما في ذلك الصور الفوتوغرافية، إلى السلطات، ولكن إجراءات الترحيل بدأت مع ذلك. في نفس الوقت تقريبًا، اخترع الدكتور أليك جيفريز من جامعة ليستر في المملكة المتحدة تقنية تعرف باسم بصمة الحمض النووي. اتصلت سلطات الهجرة بالدكتور جيفريز للحصول على المساعدة. أخذ عينات الحمض النووي من الأم وثلاثة من أطفالها، بالإضافة إلى أم غير مرتبطة، وقارن العينات بالحمض النووي للصبي. نظرًا لأن الأب البيولوجي لم يكن موجودًا في الصورة، تمت مقارنة الحمض النووي للأطفال الثلاثة بالحمض النووي للصبي. وجد تطابقًا في الحمض النووي للصبي لكل من الأم وإخوته الثلاثة. وخلص إلى أن الصبي هو بالفعل ابن الأم.
يقوم علماء الطب الشرعي بتحليل العديد من العناصر، بما في ذلك المستندات والكتابة اليدوية والأسلحة النارية والعينات البيولوجية. يقومون بتحليل محتوى الحمض النووي للشعر والسائل المنوي واللعاب والدم، ومقارنته بقاعدة بيانات ملفات تعريف الحمض النووي للمجرمين المعروفين. يشمل التحليل عزل الحمض النووي والتسلسل وتحليل التسلسل؛ تتضمن معظم تحليلات الحمض النووي الشرعي تضخيم تفاعل البوليميراز المتسلسل (PCR) لمواقع التكرار الترادفي القصير (STR) والترشيد الكهربائي لتحديد طول الجزء المضخم بـ PCR. يتم تسلسل الحمض النووي للميتوكوندريا فقط للطب الشرعي. ومن المتوقع أن يظهر علماء الطب الشرعي في جلسات المحكمة لتقديم النتائج التي توصلوا إليها. عادة ما يتم توظيفهم في مختبرات الجريمة التابعة للوكالات الحكومية بالمدينة والولاية. يعمل علماء الوراثة الذين يجربون تقنيات الحمض النووي أيضًا في المنظمات العلمية والبحثية والصناعات الدوائية ومختبرات الكليات والجامعات. يجب على الطلاب الذين يرغبون في ممارسة مهنة كعالم في الطب الشرعي أن يكونوا حاصلين على الأقل على درجة البكالوريوس في الكيمياء أو البيولوجيا أو الفيزياء، ويفضل أن يكونوا من ذوي الخبرة في العمل في المختبر.
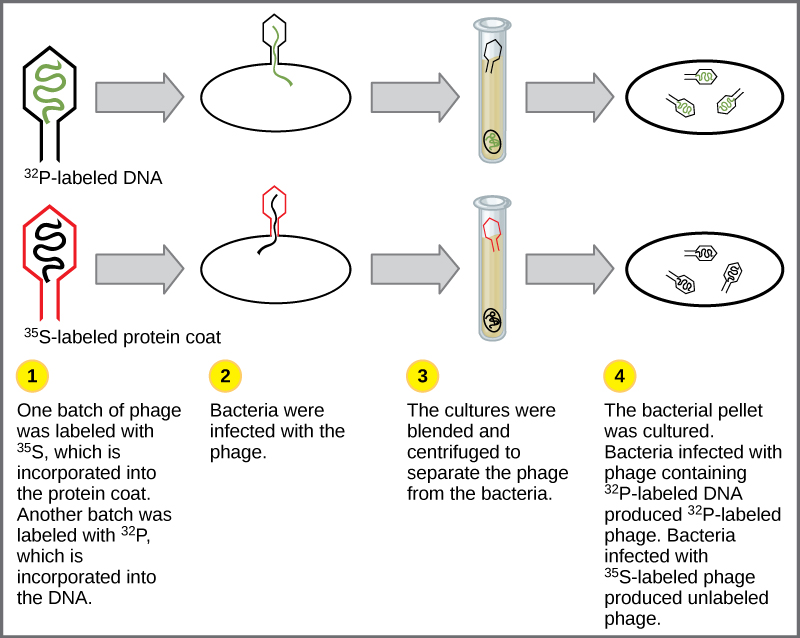
قدمت التجارب التي أجرتها مارثا تشيس وألفريد هيرشي في عام 1952 دليلًا تأكيديًا على أن الحمض النووي هو المادة الوراثية وليس البروتينات. كان تشيس وهيرشي يدرسان البكتيريا، وهو فيروس يصيب البكتيريا. عادةً ما تحتوي الفيروسات على بنية بسيطة: طبقة بروتينية تسمى القفيصة، ونواة الحمض النووي التي تحتوي على المادة الوراثية، إما DNA أو RNA. تصيب البكتيريا الخلية البكتيرية المضيفة عن طريق الالتصاق بسطحها، ثم تقوم بحقن الأحماض النووية داخل الخلية. يقوم الحمض النووي للعاثية بعمل نسخ متعددة من نفسه باستخدام الآلة المضيفة، وفي النهاية تنفجر الخلية المضيفة، مما يؤدي إلى إطلاق عدد كبير من البكتيريا. قام هيرشي وتشيس بتسمية دفعة واحدة من العاثية بالكبريت المشع، 35 S، لتسمية طبقة البروتين. تم تصنيف دفعة أخرى من العاهرات بالفوسفور المشع، 32 P. نظرًا لوجود الفوسفور في الحمض النووي، وليس البروتين، فسيتم وضع علامة على الحمض النووي وليس البروتين بالفوسفور المشع.
تم السماح لكل دفعة من العاهرات بإصابة الخلايا بشكل منفصل. بعد الإصابة، تم وضع المعلق البكتيري العاجي في الخلاط، مما تسبب في فصل طبقة العاثية عن الخلية المضيفة. تم تدوير العاثية والمعلق البكتيري في جهاز طرد مركزي. استقرت الخلايا البكتيرية الثقيلة وشكلت حبيبة، بينما بقيت جزيئات العاثية الأخف في المادة الطافية. في الأنبوب الذي يحتوي على العاثية المسمى بـ 35 S، احتوت المادة الطافية على العاثية التي تحمل علامة إشعاعية، بينما لم يتم اكتشاف أي نشاط إشعاعي في الحبيبات. في الأنبوب الذي يحتوي على العاثية المسمى بـ 32 P، تم اكتشاف النشاط الإشعاعي في الحبيبات التي تحتوي على الخلايا البكتيرية الثقيلة، ولم يتم اكتشاف أي نشاط إشعاعي في المادة الطافية. استنتج هيرشي وتشيس أن الحمض النووي للعاثية هو الذي تم حقنه في الخلية وحمل المعلومات لإنتاج المزيد من جزيئات العاثية، وبالتالي تقديم دليل على أن الحمض النووي هو المادة الوراثية وليس البروتينات (الشكل\(\PageIndex{3}\)).
في نفس الوقت تقريبًا، قام عالم الكيمياء الحيوية النمساوي Erwin Chargaff بفحص محتوى الحمض النووي في الأنواع المختلفة ووجد أن كميات الأدينين والثايمين والجوانين والسيتوزين لم يتم العثور عليها بكميات متساوية، وأنها تختلف من نوع إلى آخر، ولكن ليس بين أفراد من نفس النوع. ووجد أن كمية الأدينين تساوي كمية الثايمين، وكمية السيتوزين تساوي كمية الجوانين، أو A = T و G = C. وهذا ما يعرف أيضًا باسم قواعد Chargaff. أثبتت هذه النتيجة أنها مفيدة للغاية عندما كان واتسون وكريك يستعدان لاقتراح نموذج الحلزون المزدوج للحمض النووي.
ملخص
تم عزل الحمض النووي لأول مرة من خلايا الدم البيضاء من قبل فريدريش ميشر، الذي أطلق عليه اسم النوكلين لأنه كان معزولًا عن النواة. قدمت تجارب فريدريك غريفيث مع سلالات المكورات العقدية الرئوية أول تلميح إلى أن الحمض النووي قد يكون مبدأ التحويل. أثبت أفيري وماكلويد ومكارتي أن الحمض النووي مطلوب لتحويل البكتيريا. أثبتت التجارب اللاحقة التي أجراها هيرشي وتشيس باستخدام البكتيريا T2 أن الحمض النووي هو المادة الوراثية. وجد Chargaff أن نسبة A = T و C = G، وأن النسبة المئوية لمحتوى A و T و G و C تختلف باختلاف الأنواع.
مسرد المصطلحات
- تحول
- عملية يتم فيها امتصاص الحمض النووي الخارجي بواسطة خلية


