7.4: الفسفرة التأكسدية
- Page ID
- 196237
المهارات اللازمة للتطوير
- وصف كيفية تحرك الإلكترونات عبر سلسلة نقل الإلكترون وما يحدث لمستويات طاقتها
- اشرح كيفية إنشاء تدرج البروتون (H +) والحفاظ عليه بواسطة سلسلة نقل الإلكترون
لقد قرأت للتو عن مسارين في هدم الجلوكوز - تحلل السكر ودورة حمض الستريك - اللذان يولدان ATP. ومع ذلك، فإن معظم ATP المتولد أثناء الهدم الهوائي للجلوكوز لا يتولد مباشرة من هذه المسارات. بل إنه مشتق من عملية تبدأ بتحريك الإلكترونات من خلال سلسلة من ناقلات الإلكترون التي تخضع لتفاعلات الأكسدة والاختزال. يؤدي هذا إلى تراكم أيونات الهيدروجين داخل مساحة المصفوفة. لذلك، يتشكل تدرج التركيز الذي تنتشر فيه أيونات الهيدروجين خارج مساحة المصفوفة بالمرور عبر تركيب ATP. يعمل تيار أيونات الهيدروجين على تعزيز العمل التحفيزي لسينثاز ATP، الذي يقوم بتفسرة ADP، مما ينتج ATP.
سلسلة نقل الإلكترون
سلسلة نقل الإلكترون (الشكل\(\PageIndex{1}\)) هي المكون الأخير للتنفس الهوائي وهي الجزء الوحيد من استقلاب الجلوكوز الذي يستخدم الأكسجين الجوي. ينتشر الأكسجين باستمرار في النباتات؛ وفي الحيوانات، يدخل الجسم من خلال الجهاز التنفسي. النقل الإلكتروني عبارة عن سلسلة من تفاعلات الأكسدة والاختزال التي تشبه سباق التتابع أو لواء الجرافة حيث تنتقل الإلكترونات بسرعة من مكون إلى آخر، إلى نقطة نهاية السلسلة حيث تقلل الإلكترونات الأكسجين الجزيئي وتنتج الماء. هناك أربعة مجمعات تتكون من البروتينات، المصنفة من الأول إلى الرابع في الشكل\(\PageIndex{1}\)، ويسمى تجميع هذه المجمعات الأربعة، جنبًا إلى جنب مع حاملات الإلكترون المتنقلة والملحقات المرتبطة بها، بسلسلة نقل الإلكترون. توجد سلسلة نقل الإلكترون في نسخ متعددة في غشاء الميتوكوندريا الداخلي لحقيقيات النوى والغشاء البلازمي لبدائيات النواة.
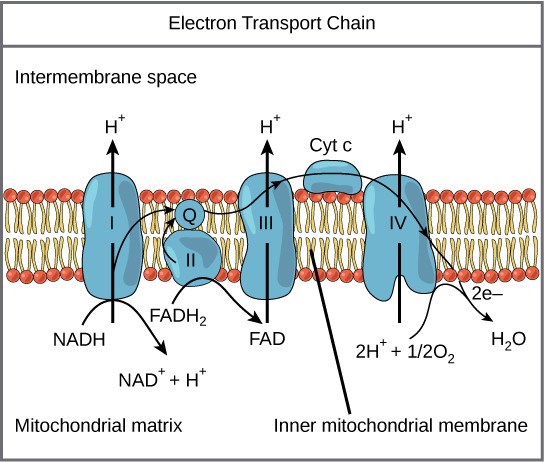
المجمع الأول
للبدء، يتم نقل إلكترونين إلى المجمع الأول على متن NADH. يتكون هذا المركب، المسمى I، من أحادي النوكليوتيد الفلافين (FMN) وبروتين يحتوي على الحديد والكبريت (Fe-S). FMN، المشتق من فيتامين B 2، المعروف أيضًا باسم الريبوفلافين، هو واحد من عدة مجموعات تعويضية أو عوامل مساعدة في سلسلة نقل الإلكترون. المجموعة التعويضية هي جزيء غير بروتيني مطلوب لنشاط البروتين. مجموعات الأطراف الاصطناعية هي جزيئات عضوية أو غير عضوية وغير ببتيد مرتبطة ببروتين يسهل وظيفته؛ وتشمل المجموعات التعويضية الإنزيمات المشتركة، وهي المجموعات التعويضية للإنزيمات. الإنزيم الموجود في المركب الأول هو نازعة هيدروجين NADH وهو بروتين كبير جدًا يحتوي على 45 سلسلة من الأحماض الأمينية. يمكن للمركب I ضخ أربعة أيونات هيدروجين عبر الغشاء من المصفوفة إلى الفضاء بين الأغشية، وبهذه الطريقة يتم إنشاء التدرج الأيوني للهيدروجين والحفاظ عليه بين الجزأين المفصولين بغشاء الميتوكوندريا الداخلي.
سؤال وجواب 2
يستقبل المجمع الثاني مباشرة FADH 2، والذي لا يمر عبر المجمع الأول. المركب الذي يربط المجمعين الأول والثاني بالثالث هو أوبيكينون (Q). جزيء Q قابل للذوبان في الدهون ويتحرك بحرية عبر النواة الكارهة للماء للغشاء. بمجرد اختزاله، (QH 2)، يقوم يوبيكوينون بتوصيل إلكتروناته إلى المجمع التالي في سلسلة نقل الإلكترون. يستقبل Q الإلكترونات المشتقة من NADH من المركب الأول والإلكترونات المشتقة من FADH 2 من المركب الثاني، بما في ذلك نازعة هيدروجين السكسينات. يشكل هذا الإنزيم و FADH 2 مركبًا صغيرًا يوصل الإلكترونات مباشرة إلى سلسلة نقل الإلكترون، متجاوزًا المركب الأول. نظرًا لأن هذه الإلكترونات تتجاوز وبالتالي لا تنشط مضخة البروتون في المجمع الأول، يتم تصنيع عدد أقل من جزيئات ATP من إلكترونات FADH 2. يتناسب عدد جزيئات ATP التي تم الحصول عليها في النهاية بشكل مباشر مع عدد البروتونات التي يتم ضخها عبر غشاء الميتوكوندريا الداخلي.
المجمع الثالث
يتكون المجمع الثالث من السيتوكروم ب، وبروتين Fe-S آخر، ومركز ريسك (مركز 2Fe-2S)، وبروتينات السيتوكروم ج؛ ويسمى هذا المركب أيضًا السيتوكروم أوكسيدوركتاز. تحتوي بروتينات السيتوكروم على مجموعة اصطناعية من الهيم. يشبه جزيء الهيم الهيم في الهيموجلوبين، لكنه يحمل الإلكترونات وليس الأكسجين. ونتيجة لذلك، ينخفض أيون الحديد في جوهره ويتأكسد أثناء مروره بالإلكترونات، ويتأرجح بين حالات الأكسدة المختلفة: Fe ++ (مخفض) و Fe +++ (مؤكسد). تتميز جزيئات الهيم في السيتوكرومات بخصائص مختلفة قليلاً بسبب تأثيرات البروتينات المختلفة التي تربطها، مما يعطي خصائص مختلفة قليلاً لكل مركب. يضخ المركب III البروتونات عبر الغشاء ويمرر إلكتروناتها إلى السيتوكروم c لنقلها إلى المركب الرابع من البروتينات والإنزيمات (السيتوكروم c هو متقبل الإلكترونات من Q؛ ومع ذلك، بينما يحمل Q أزواجًا من الإلكترونات، يمكن للسيتوكروم c قبول واحد فقط في كل مرة).
المجمع الرابع
يتكون المجمع الرابع من بروتينات السيتوكروم c و a و a 3. يحتوي هذا المجمع على مجموعتين من الهيم (واحدة في كل من السيتوكرومات، a، و a 3) وثلاثة أيونات نحاسية (زوج من Cu A وواحد Cu B في السيتوكروم a 3). تحتفظ السيتوكرومات بجزيء الأكسجين بإحكام شديد بين أيونات الحديد والنحاس حتى يتم تقليل الأكسجين تمامًا. ثم يلتقط الأكسجين المخفض اثنين من أيونات الهيدروجين من الوسط المحيط لإنتاج الماء (H 2 O). تساهم إزالة أيونات الهيدروجين من النظام في التدرج الأيوني المستخدم في عملية التناضح الكيميائي.
التناضح الكيميائي
في التناضح الكيميائي، تُستخدم الطاقة الحرة من سلسلة تفاعلات الأكسدة والاختزال الموصوفة للتو لضخ أيونات الهيدروجين (البروتونات) عبر الغشاء. يحدد التوزيع غير المتكافئ لأيونات H+ عبر الغشاء كلاً من التركيز والتدرجات الكهربائية (وبالتالي التدرج الكهروكيميائي)، بسبب الشحنة الموجبة لأيونات الهيدروجين وتجميعها على جانب واحد من الغشاء.
إذا كان الغشاء مفتوحًا للانتشار بواسطة أيونات الهيدروجين، فستميل الأيونات إلى الانتشار مرة أخرى في المصفوفة، مدفوعة بتدرجها الكهروكيميائي. تذكر أن العديد من الأيونات لا يمكن أن تنتشر عبر المناطق غير القطبية لأغشية الفوسفوليبيد دون مساعدة القنوات الأيونية. وبالمثل، لا يمكن لأيونات الهيدروجين في مساحة المصفوفة أن تمر إلا عبر غشاء الميتوكوندريا الداخلي من خلال بروتين غشائي متكامل يسمى ATP synthase (الشكل\(\PageIndex{2}\)). يعمل هذا البروتين المعقد كمولد صغير، يتم تشغيله بواسطة قوة أيونات الهيدروجين المنتشرة عبره، مما يؤدي إلى انخفاض تدرجها الكهروكيميائي. إن تقليب أجزاء من هذه الآلة الجزيئية يسهل إضافة الفوسفات إلى ADP، مما يشكل ATP، باستخدام الطاقة الكامنة لتدرج أيون الهيدروجين.
آرت كونيكشن
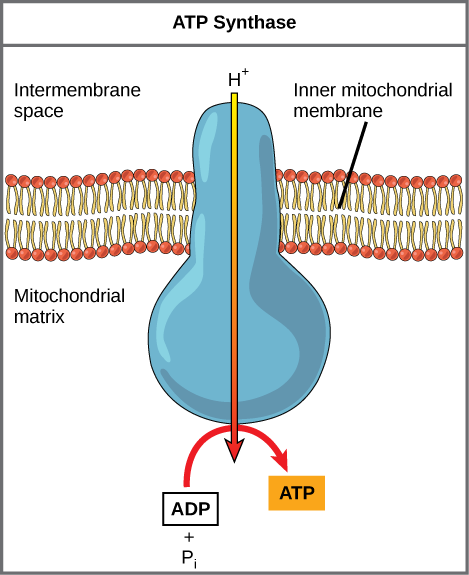
الدينيتروفينول (DNP) هو أداة فك الارتباط التي تجعل غشاء الميتوكوندريا الداخلي يتسرب إلى البروتونات. تم استخدامه حتى عام 1938 كدواء لفقدان الوزن. ما هو التأثير الذي تتوقعه من DNP على التغيير في درجة الحموضة عبر غشاء الميتوكوندريا الداخلي؟ لماذا تعتقد أن هذا الدواء قد يكون فعالًا لفقدان الوزن؟
يستخدم التناضح الكيميائي (الشكل\(\PageIndex{3}\)) لتوليد 90 في المائة من ATP الذي يتم إنتاجه أثناء تقويض الجلوكوز الهوائي؛ وهي أيضًا الطريقة المستخدمة في التفاعلات الضوئية لعملية التمثيل الضوئي لتسخير طاقة ضوء الشمس في عملية الفسفور الضوئي. تذكر أن إنتاج ATP باستخدام عملية التناضح الكيميائي في الميتوكوندريا يسمى الفسفرة التأكسدية. النتيجة الإجمالية لهذه التفاعلات هي إنتاج ATP من طاقة الإلكترونات التي تمت إزالتها من ذرات الهيدروجين. كانت هذه الذرات في الأصل جزءًا من جزيء الجلوكوز. في نهاية المسار، تُستخدم الإلكترونات لتقليل جزيء الأكسجين إلى أيونات الأكسجين. تجذب الإلكترونات الإضافية على الأكسجين أيونات الهيدروجين (البروتونات) من الوسط المحيط، ويتشكل الماء.
آرت كونيكشن
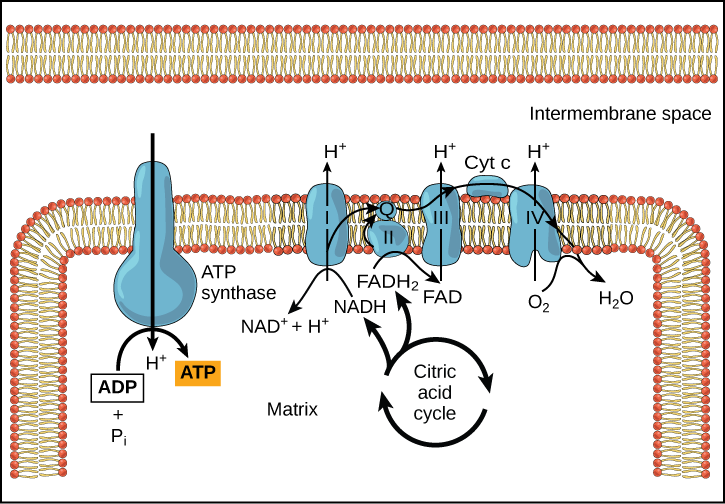
يمنع السيانيد أوكسيديز السيتوكروم سي، وهو أحد مكونات سلسلة نقل الإلكترون. في حالة حدوث تسمم بالسيانيد، هل تتوقع زيادة أو نقصان درجة الحموضة في الفضاء بين الأغشية؟ ما تأثير السيانيد على تخليق ATP؟
عائد ATP
يختلف عدد جزيئات ATP الناتجة عن تقويض الجلوكوز. على سبيل المثال، يختلف عدد أيونات الهيدروجين التي يمكن لمجمعات سلسلة نقل الإلكترون ضخها عبر الغشاء بين الأنواع. مصدر آخر للتباين ينبع من مكوك الإلكترونات عبر أغشية الميتوكوندريا. (لا يمكن لـ NADH الناتج عن تحلل السكر دخول الميتوكوندريا بسهولة.) وبالتالي، يتم التقاط الإلكترونات من داخل الميتوكوندريا إما عن طريق NAD + أو FAD +. كما تعلمت سابقًا، يمكن لجزيئات FAD + هذه نقل عدد أقل من الأيونات؛ وبالتالي، يتم إنشاء عدد أقل من جزيئات ATP عندما يعمل FAD + كحامل. يستخدم NAD+ كناقل للإلكترون في الكبد ويعمل FAD + في الدماغ.
هناك عامل آخر يؤثر على إنتاج جزيئات ATP الناتجة عن الجلوكوز وهو حقيقة أن المركبات الوسيطة في هذه المسارات تستخدم لأغراض أخرى. يرتبط هدم الجلوكوز بالمسارات التي تبني أو تكسر جميع المركبات البيوكيميائية الأخرى في الخلايا، والنتيجة أكثر فوضوية إلى حد ما من الحالات المثالية الموصوفة حتى الآن. على سبيل المثال، يتم إدخال السكريات الأخرى غير الجلوكوز في المسار الجليكوليتي لاستخراج الطاقة. علاوة على ذلك، فإن السكريات الكربونية الخمسة التي تشكل الأحماض النووية مصنوعة من المواد الوسيطة في تحلل السكر. يمكن تصنيع بعض الأحماض الأمينية غير الأساسية من المواد الوسيطة لكل من تحلل السكر ودورة حمض الستريك. تُصنع الدهون، مثل الكوليسترول والدهون الثلاثية، أيضًا من المواد الوسيطة في هذه المسارات، ويتم تكسير كل من الأحماض الأمينية والدهون الثلاثية للحصول على الطاقة من خلال هذه المسارات. بشكل عام، في الأنظمة الحية، تستخرج مسارات هدم الجلوكوز هذه حوالي 34 بالمائة من الطاقة الموجودة في الجلوكوز.
ملخص
سلسلة نقل الإلكترون هي جزء من التنفس الهوائي الذي يستخدم الأكسجين الحر كمستقبل إلكتروني نهائي للإلكترونات التي تمت إزالتها من المركبات الوسيطة في تقويض الجلوكوز. تتكون سلسلة نقل الإلكترون من أربعة مجمعات كبيرة متعددة البروتينات مدمجة في غشاء الميتوكوندريا الداخلي وحاملتين صغيرتين للإلكترون قابلتين للانتشار تنقلان الإلكترونات بينهما. يتم تمرير الإلكترونات من خلال سلسلة من تفاعلات الأكسدة والاختزال، مع استخدام كمية صغيرة من الطاقة الحرة في ثلاث نقاط لنقل أيونات الهيدروجين عبر الغشاء. تساهم هذه العملية في التدرج المستخدم في التناضح الكيميائي. تفقد الإلكترونات التي تمر عبر سلسلة نقل الإلكترون الطاقة تدريجيًا، وتكمل الإلكترونات عالية الطاقة المتبرع بها للسلسلة إما NADH أو FADH 2 السلسلة، حيث تعمل الإلكترونات منخفضة الطاقة على تقليل جزيئات الأكسجين وتشكيل الماء. ينخفض مستوى الطاقة الحرة للإلكترونات من حوالي 60 كيلو كالوري/مول في NADH أو 45 كيلو كالوري/مول في FADH 2 إلى حوالي 0 كيلو كالوري/مول في الماء. المنتجات النهائية لسلسلة نقل الإلكترون هي الماء و ATP. يمكن تحويل عدد من المركبات الوسيطة لدورة حمض الستريك إلى استقلاب الجزيئات البيوكيميائية الأخرى، مثل الأحماض الأمينية غير الأساسية والسكريات والدهون. يمكن أن تعمل هذه الجزيئات نفسها كمصادر للطاقة لمسارات الجلوكوز.
اتصالات فنية
الشكل\(\PageIndex{2}\): الدينيتروفينول (DNP) هو جهاز فك الارتباط الذي يجعل غشاء الميتوكوندريا الداخلي يتسرب إلى البروتونات. تم استخدامه حتى عام 1938 كدواء لفقدان الوزن. ما هو التأثير الذي تتوقعه من DNP على التغيير في درجة الحموضة عبر غشاء الميتوكوندريا الداخلي؟ لماذا تعتقد أن هذا الدواء قد يكون فعالًا لفقدان الوزن؟
- إجابة
-
بعد التسمم بـ DNP، لم تعد سلسلة نقل الإلكترون قادرة على تشكيل تدرج بروتوني، ولم يعد سينثاس ATP قادرًا على صنع ATP. DNP هو دواء غذائي فعال لأنه يفصل بين تخليق ATP؛ بمعنى آخر، بعد تناوله، يحصل الشخص على طاقة أقل من الطعام الذي يتناوله. ومن المثير للاهتمام أن أحد أسوأ الآثار الجانبية لهذا الدواء هو ارتفاع الحرارة أو ارتفاع درجة حرارة الجسم. نظرًا لعدم إمكانية تكوين ATP، يتم فقدان الطاقة من نقل الإلكترون كحرارة.
الشكل\(\PageIndex{3}\): يمنع السيانيد أوكسيديز السيتوكروم سي، وهو أحد مكونات سلسلة نقل الإلكترون. في حالة حدوث تسمم بالسيانيد، هل تتوقع زيادة أو نقصان درجة الحموضة في الفضاء بين الأغشية؟ ما تأثير السيانيد على تخليق ATP؟
- إجابة
-
بعد التسمم بالسيانيد، لم تعد سلسلة نقل الإلكترون قادرة على ضخ الإلكترونات في الفضاء بين الأغشية. ستزداد درجة الحموضة في الفضاء بين الأغشية، وسينخفض تدرج درجة الحموضة، وسيتوقف تخليق ATP.
مسرد المصطلحات
- سينثاز ATP
- (أيضًا، F1F0 ATP synthase) مركب بروتين مضمن في الغشاء يضيف الفوسفات إلى ADP بالطاقة من البروتونات المنتشرة عبره
- مجموعة الأطراف الاصطناعية
- جزيء (أيضًا عامل مساعد اصطناعي) مرتبط بالبروتين الذي يسهل وظيفة البروتين
- يوبيكوينون
- ناقل الإلكترون القابل للذوبان في سلسلة نقل الإلكترون التي تربط المركب الأول أو الثاني بالثالث


