10.6: תרגום פרוקריוטי
- Page ID
- 208432
ברגע שה-RNA יצא מה-RNAP ויש מספיק מקום להכיל ריבוזום, התרגום יכול להתחיל בפרוקריוטים. למעשה, עבור גנים בעלי ביטוי גבוה, זה לא יהיה יוצא דופן לראות פולימראזות RNA מרובות המתעתקות את ה- DNA ואת הריבוזומים המרובים על כל אחד מהתמלילים המתרגמים את ה- mRNA לחלבון! התהליך מתחיל ביחידת המשנה הריבוזומלית הקטנה (ורק ביחידת המשנה הקטנה - אם היא מחוברת ליחידת המשנה הגדולה, היא אינה מסוגלת לקשור את ה- mRNA), הנקשרת ל- mRNA באופן רופף ומתחילה לסרוק אותו אחר רצף זיהוי הנקרא רצף שיין-דלגרנו, על שם מגליו. ברגע שזה מזוהה על ידי תת-היחידה הריבוזומלית הקטנה rRNA, תת-היחידה הקטנה ממוקמת סביב קודון ההתחלה (AUG). תהליך זה מתאפשר על ידי גורמי חניכה כדלקמן.
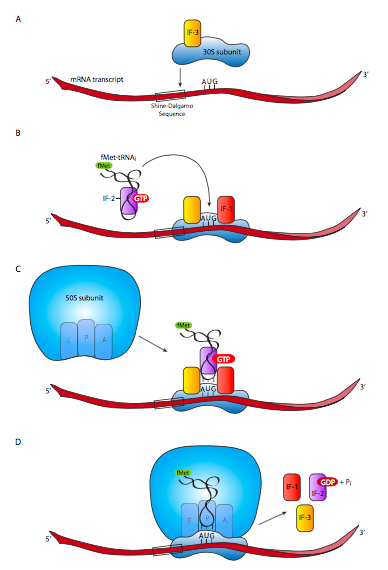
יחידת המשנה הריבוזומלית 30S מתנתקת מתת-היחידה הריבוזומלית 50S אם היא הייתה קשורה לאחת, ונקשרת לגורמי אינטיציה IF-1 ו- IF-3. IF-1 נקשר לאתר A, שם הוא מונע ממולקולות aminoacyl-tRNA חדשות להיכנס לפני הרכבת הריבוזום המלא. זה גם מקל על הרכבה וייצוב של מתחם החניכה. IF-3 נדרש כדי לאפשר ליחידת המשנה 30S להיקשר ל- mRNA. ברגע שזה קרה, IF-2-GTP מגיע למקום, נושא עמו את היוזם aminoacyl-tRNA. זה מתיישב באתר P, הממוקם כך שהאנטיקודון של ה-tRNA מתיישב מעל קודון ההתחלה AUG של ה-mRNA. יש צורך בהידרוליזה של ה- GTP המחובר ל- IF-2 ושחרור כל גורמי ההתחלה כדי לאפשר ליחידת המשנה 50S להיקשר ליחידת המשנה 30S ליצירת הריבוזום המלא והתפקודי במלואו. מכיוון שנדרשה הידרוליזה של GTP, ההצטרפות של יחידות המשנה היא בלתי הפיכה באופן ספונטני, ודורשת הוצאת אנרגיה עם סיום התרגום. ברגע שיחידת המשנה 50S מצטרפת ליחידת המשנה 30S, אתר A מוכן לקבל את ה- aminoacyl-tRNA הבא.
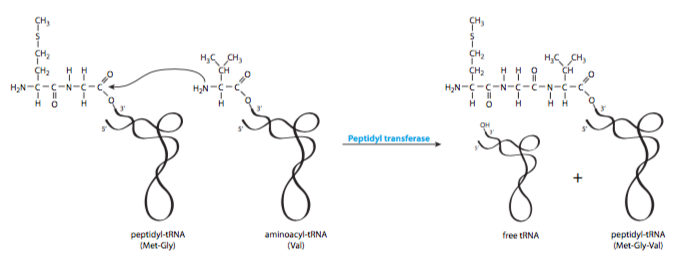
תפיסה מוטעית נפוצה ומובנת היא שחומצת האמינו החדשה המובאת לריבוזום מתווספת לשרשרת הפוליפפטיד הגדלה. למעשה, המנגנון הוא בדיוק ההפך: הפוליפפטיד מתווסף לחומצת האמינו החדשה (איור\(\PageIndex{4}\)). זה מתחיל מחומצת האמינו השנייה שמתווספת לחלבון חדש (איור\(\PageIndex{5}\)). חומצת האמינו הראשונה, מתיונין, כדאי לזכור, נכנסה יחד עם IF-2 וה-tRNA היוזם. האמינואציל-tRNA החדש מלווה על ידי EF-Tu, גורם התארכות הנושא GTP. ברגע שה-AA-tRNA נמצא במקום, EF-Tu מבצע הידרוליזה של ה-GTP ומתנתק מה-aminoacyl-tRNA והריבוזום.
במשך זמן רב, הייתה מעט מסתורין סביב העגינה בו זמנית של שתי מולקולות tRNA על קודונים סמוכים מיד של mRNA. בתנאים רגילים, לא אמור להיות מספיק מקום, מכיוון שה-tRNAs מגושמים למדי ואחד צריך לחסום את השני מלהגיע ל-mRNA כדי ליצור התאמת קודון-אנטיקודון. העניין התבהר לבסוף בשנת 2001 עם בדיקות קריסטלוגרפיות של קרני רנטגן המראות עיקול ב- mRNA בין הקודון בחריץ P לקודון בחריץ A. העיקול מציב את שני ה-tRNAs הקשורים בזוויות מעט שונות ובכך יוצר מספיק מקום לשניהם כדי לשמור על קשרי מימן בזוג בסיסים עם ה-mRNA. ראה יוסופוב ואח ', מדע 292 (5518): 883-896, 2001.
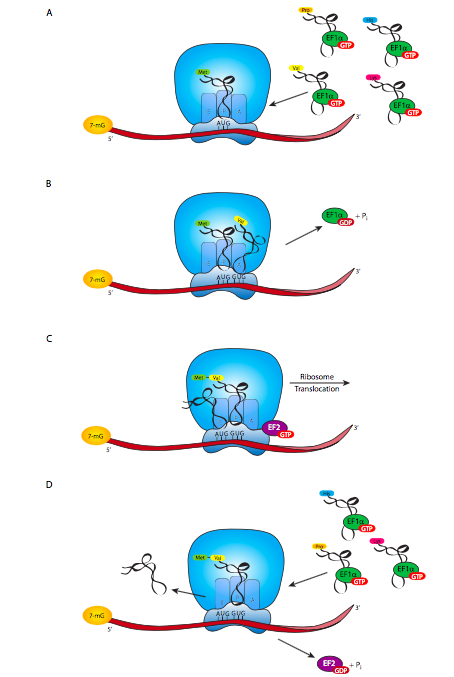
כאשר aminoacyl-tRNA חדש נופל לתוך חריץ A של הריבוזום, האנטיקודון מסודר עם הקודון של ה- mRNA. אם אין השלמה, ה-aminoacyl-tRNA בקרוב צף חזרה מהחריץ כדי להיות מוחלף על ידי מועמד אחר. עם זאת, אם יש השלמה (או משהו קרוב מספיק, נזכר ברעיון הנדנוד) אז נוצרים קשרי H בין הקודון לאנטי-קודון, ה-tRNA משנה את הקונפורמציה, מה שמעביר את הקונפורמציה של EF-Tu, וגורם להידרוליזה של GTP ל-GDP + P i, ושחרור מה-AA-tRNA. האינטראקציה של קודון-אנטיקודון יציבה מספיק זמן כדי שהפעילות הקטליטית של הריבוזום תעשה הידרוליזה של הקשר בין fMet ל-tRNAF בחריץ P, ולחבר את ה-fMet לחומצת האמינו החדשה עם קשר פפטיד בחריץ A. חומצת האמינו החדשה עדיין מחוברת ל-tRNA שלה, וככל שתהליך זה מתרחש, הריבוזום משנה את המיקום ביחס ל-mRNA ו-tRNA. זה מכניס את ה- tRNAF הריק כעת (ללא חומצת אמינו) בחריץ E, ה- tRNAaA בחריץ P, מחובר לאותו aa המחובר ל- Met, וחריץ A שוב פתוח ל- tRNA חדש להיכנס. גורם ההתארכות EF-G נקשר ליד חריץ A ברגע ש- EF-Tu עוזב, ונדרש לטרנסלוקציה ריבוזומלית, ומספק אנרגיה לתהליך על ידי הידרוליזה של GTP שהוא נושא עמו לריבוזום. מניסיון התלמידים שלי, נראה שהדרך הטובה ביותר ללמוד זאת היא ללמוד את התרשימים ולראות את תנועות המולקולות, ולמלא את הפרטים המכניסטיים במוחך. תהליך זה נמשך עד שהריבוזום מביא את חריץ A בקנה אחד עם קודון עצירה.
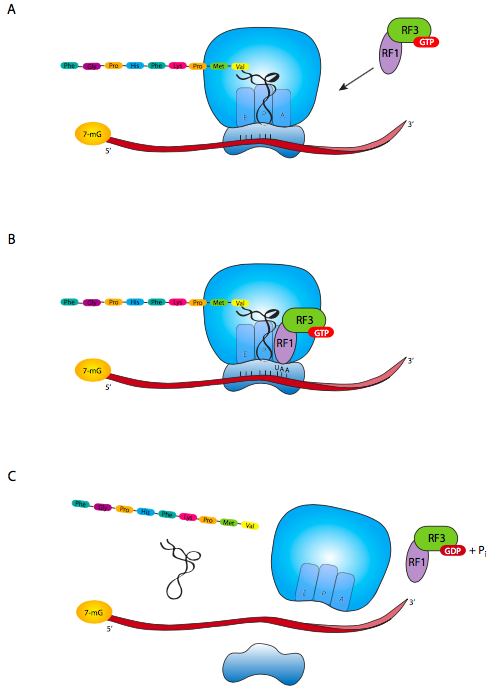
אין tRNA עם אנטיקודון לקודון העצירה. במקום זאת, יש קבוצה של גורמי שחרור שנכנסים לאתר A של הריבוזום, נקשרים לקודון העצירה ומפעילים את הריבוזום כדי לחתוך את הקשר בין שרשרת הפוליפפטיד ל-tRNA האחרון (איור). \(\PageIndex{6}\) תלוי איזה קודון עצירה קיים, RF1 (מזהה UAA או UAG) או RF2 (עבור UAA או UGA) נכנס לראשונה לחריץ A. ה- RF1 או RF2 מורכב עם RF3, המעורב בשחרור הבא של מתחם ה- RF מחריץ A. זה הכרחי מכיוון שברגע שהפוליפפטיד שוחרר מהריבוזום, יש לשחרר את ה-mRNA. גורם משחרר ריבוזום (RRF) נקשר גם בחריץ A, מה שגורם לשינוי קונפורמטיבי בריבוזום המשחרר את ה- tRNA הקודם ועכשיו הריק. לבסוף, EF-G נקשר ל- RRF, ועם הידרוליזה נלווית של GTP, גורם לדי-סוציאליזציה של הריבוזום ליחידות משנה גדולות וקטנות נפרדות. שים לב שהשילוב של EF-G/RRF הוא שגורם לדיסוציאציה; EF-G לבדו ממלא תפקיד אחר בתנועת הריבוזומים כאשר הוא אינו נמצא בקודון העצירה.


